名校
解题方法
1 . “化学——我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。根据所学知识,回答下列问题:
(1)沾有水的铁锅在高温火焰上灼烧会发黑,该反应的化学方程式为___________ 。
(2)食用加碘食盐能消除碘缺乏病的困扰,碘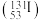 的质量数是
的质量数是___________ 。
(3)臭氧、“84”消毒液、二氧化氯、高铁酸钠等都是生活中常见的消毒剂。
①臭氧和氧气互为___________ (填“同位素”或“同素异形体”)。
②生活中“84”消毒液和洁厕灵(主要成分是稀盐酸)不能混合使用,原因是___________ 。
③ 是一种新型含氯消毒剂,在自来水消毒领域已经开始使用。实验室可通过反应
是一种新型含氯消毒剂,在自来水消毒领域已经开始使用。实验室可通过反应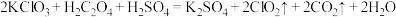 制得
制得 。该反应中产生
。该反应中产生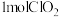 时,转移的电子的物质的量为
时,转移的电子的物质的量为___________ 。
④高铁酸钠 还是一种新型的净水剂。其净水过程中所发生的化学反应主要为
还是一种新型的净水剂。其净水过程中所发生的化学反应主要为 (胶体)
(胶体)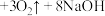 ,证明有
,证明有 胶体生成的实验操作为
胶体生成的实验操作为___________ 。
(4)汽车安全气囊弹出时发生反应: ,该反应中被氧化的N与被还原的N的物质的量之比为
,该反应中被氧化的N与被还原的N的物质的量之比为___________ 。
(5)铝制器具不宜盛放碱性食物,请写出铝与 溶液反应的离子方程式:
溶液反应的离子方程式:___________ 。
(1)沾有水的铁锅在高温火焰上灼烧会发黑,该反应的化学方程式为
(2)食用加碘食盐能消除碘缺乏病的困扰,碘
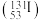 的质量数是
的质量数是(3)臭氧、“84”消毒液、二氧化氯、高铁酸钠等都是生活中常见的消毒剂。
①臭氧和氧气互为
②生活中“84”消毒液和洁厕灵(主要成分是稀盐酸)不能混合使用,原因是
③
 是一种新型含氯消毒剂,在自来水消毒领域已经开始使用。实验室可通过反应
是一种新型含氯消毒剂,在自来水消毒领域已经开始使用。实验室可通过反应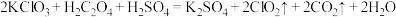 制得
制得 。该反应中产生
。该反应中产生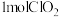 时,转移的电子的物质的量为
时,转移的电子的物质的量为④高铁酸钠
 还是一种新型的净水剂。其净水过程中所发生的化学反应主要为
还是一种新型的净水剂。其净水过程中所发生的化学反应主要为 (胶体)
(胶体)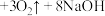 ,证明有
,证明有 胶体生成的实验操作为
胶体生成的实验操作为(4)汽车安全气囊弹出时发生反应:
 ,该反应中被氧化的N与被还原的N的物质的量之比为
,该反应中被氧化的N与被还原的N的物质的量之比为(5)铝制器具不宜盛放碱性食物,请写出铝与
 溶液反应的离子方程式:
溶液反应的离子方程式:
您最近一年使用:0次
2 . 将24.4gNaOH固体溶于水配成100mL溶液
(1)该溶液中NaOH的物质的量浓度为_____ ,OH-的浓度为_____ 。
(2)从该溶液中取出10mL,含NaOH的质量为_____ ,含NaOH的物质的量为_____ 。
(3)将取出的10mL溶液加水稀释到100mL,稀释后溶液中NaOH的物质的量浓度为_____ 。
(1)该溶液中NaOH的物质的量浓度为
(2)从该溶液中取出10mL,含NaOH的质量为
(3)将取出的10mL溶液加水稀释到100mL,稀释后溶液中NaOH的物质的量浓度为
您最近一年使用:0次
3 . 如图是有关钠与水反应及产物检验的实验装置。实验开始时先向管内加入滴有酚酞的水,使水位达到B端管口,然后迅速塞紧橡胶塞并拔掉大头针,此时Na掉入水中。

回答下列问题:
(1)钠与水反应的化学方程式为_______ 。
(2)钠与水反应的现象很多,不同的现象证明不同的性质。
①能证明钠的密度比水小的现象是_______ 。
②能证明钠的熔点低的现象是_______ 。
③能证明有氢氧化钠生成的现象是_______ 。
④能证明有气体产生的现象是A端液面_______ B端液面(填“高于”、或“低于”)

回答下列问题:
(1)钠与水反应的化学方程式为
(2)钠与水反应的现象很多,不同的现象证明不同的性质。
①能证明钠的密度比水小的现象是
②能证明钠的熔点低的现象是
③能证明有氢氧化钠生成的现象是
④能证明有气体产生的现象是A端液面
您最近一年使用:0次
解题方法
4 . 有下列物质:①熔融氯化钠 ②Al2(SO4)3 ③液态HCl ④稀硫酸 ⑤二氧化碳 ⑥铁 ⑦蔗糖
请回答下列问题:
(1)可以导电的有_______ (填序号,下同)。
(2)属于电解质的有_______ 。
(3)属于非电解质的有_______ 。
(4)②在水中的电离方程式为_______ 。
(5)请写出④与⑥反应的离子方程式_______ 。
请回答下列问题:
(1)可以导电的有
(2)属于电解质的有
(3)属于非电解质的有
(4)②在水中的电离方程式为
(5)请写出④与⑥反应的离子方程式
您最近一年使用:0次
名校
5 . Ⅰ.物质的量是高中化学常用的物理量,请完成以下有关计算:
(1)2 mol H2SO4中含___________ mol H,所含氧原子跟___________ mol H2O所含氧原子个数相等。
(2)2 mol O3和3 mol O2的质量之比为___________ ,同温同压下的体积之比为___________ 。
Ⅱ.用Na2CO3固体配制1mol/L的Na2CO3溶液100mL。
(3)供选用的仪器有:①玻璃棒;②50mL烧杯;③100mL量筒;④100mL容量瓶;⑤250mL量筒;⑥天平;应选用的仪器有___________ (填编号)。还缺少的实验仪器是___________ 。
(4)应称取Na2CO3的质量为___________ 。
(5)配制过程中,下列操作会使配制的Na2CO3溶液浓度偏高的是___________ 。(填序号)
①容量瓶使用时未干燥 ②定容时俯视刻度线 ③定容时不小心有少量蒸馏水滴到瓶外
④定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线。
(1)2 mol H2SO4中含
(2)2 mol O3和3 mol O2的质量之比为
Ⅱ.用Na2CO3固体配制1mol/L的Na2CO3溶液100mL。
(3)供选用的仪器有:①玻璃棒;②50mL烧杯;③100mL量筒;④100mL容量瓶;⑤250mL量筒;⑥天平;应选用的仪器有
(4)应称取Na2CO3的质量为
(5)配制过程中,下列操作会使配制的Na2CO3溶液浓度偏高的是
①容量瓶使用时未干燥 ②定容时俯视刻度线 ③定容时不小心有少量蒸馏水滴到瓶外
④定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线。
您最近一年使用:0次
名校
6 . 完成下列填空
(1)用双线桥 法标明下列反应的电子转移的方向和数目:__________

(2)写出下列反应的离子 方程式。
①CuSO4 溶液与Ba(OH)2溶液混合:___________
②Fe2O3与稀盐酸混合:___________
(3)写出铁与水蒸气反应的化学方程式 :___________
(4)写出H2SO4的电离 方程式:___________
(1)用

(2)写出下列反应的
①CuSO4 溶液与Ba(OH)2溶液混合:
②Fe2O3与稀盐酸混合:
(3)写出铁与水蒸气反应的
(4)写出H2SO4的
您最近一年使用:0次
名校
7 . 按要求回答问题:
(1)写出氯化铁的电离方程式:___________
(2)写出氢氧化铜与盐酸反应的离子方程式:___________
(3)写出过氧化钠与二氧化碳反应化学方程式:___________
(4)53克Na2CO3的物质的量是___________ ,其中含有Na+的个数为___________
(1)写出氯化铁的电离方程式:
(2)写出氢氧化铜与盐酸反应的离子方程式:
(3)写出过氧化钠与二氧化碳反应化学方程式:
(4)53克Na2CO3的物质的量是
您最近一年使用:0次
名校
解题方法
8 . 现有下列9种物质:①蔗糖,②熔融NaCl,③石墨,④铜丝,⑤NaOH固体,⑥SO2,⑦NaHSO4固体,⑧液态H2SO4,⑨饱和FeCl3溶液。
上述物质中可导电的是___________ (填序号,下同);上述物质中属于电解质的是___________ 。属于非电解质的是___________ 。
上述物质中可导电的是
您最近一年使用:0次
9 . 室温下,用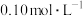
 溶液滴定
溶液滴定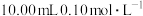
 (二元弱酸)溶液所得滴定曲线如图,请回答下列问题:
(二元弱酸)溶液所得滴定曲线如图,请回答下列问题:

(1)用电离方程式表示草酸溶液显酸性的原因_______ 。
(2)带你⑤所示溶液中,
_______  (填“>”“<”“=”)。
(填“>”“<”“=”)。
(3)已知: 、
、 在酸性条件下均能将草酸钠(
在酸性条件下均能将草酸钠( )氧化成
)氧化成 ,测定软锰矿中
,测定软锰矿中 质量分数的方法是:称取
质量分数的方法是:称取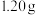 软锰矿样品,加入
软锰矿样品,加入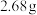 草酸钠固体,再加入足量的稀硫酸并加热(杂质不参加反应),充分反应后冷却,滤去杂质,将所得滤液转移到250 mL容量瓶中并定容,从中取出
草酸钠固体,再加入足量的稀硫酸并加热(杂质不参加反应),充分反应后冷却,滤去杂质,将所得滤液转移到250 mL容量瓶中并定容,从中取出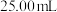 待测液放入锥形瓶中,再用
待测液放入锥形瓶中,再用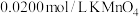 标准溶液进行滴定,反应的离子方程式为:
标准溶液进行滴定,反应的离子方程式为: ,当滴入
,当滴入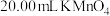 溶液时恰好完全反应。
溶液时恰好完全反应。

①在酸性条件下, 将
将 氧化的离子方程式为
氧化的离子方程式为_______ 。
②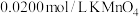 标准溶液应选用下图中的
标准溶液应选用下图中的_______ (填“甲”或“乙”)盛装;
③将锥形瓶置于滴定管下方进行滴定时,眼睛注视_______ 直至滴定终点;判断到达滴定终点的现象是_______ 。
④软锰矿中 的质量分数为
的质量分数为_______ 。
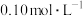
 溶液滴定
溶液滴定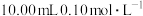
 (二元弱酸)溶液所得滴定曲线如图,请回答下列问题:
(二元弱酸)溶液所得滴定曲线如图,请回答下列问题:
(1)用电离方程式表示草酸溶液显酸性的原因
(2)带你⑤所示溶液中,

 (填“>”“<”“=”)。
(填“>”“<”“=”)。(3)已知:
 、
、 在酸性条件下均能将草酸钠(
在酸性条件下均能将草酸钠( )氧化成
)氧化成 ,测定软锰矿中
,测定软锰矿中 质量分数的方法是:称取
质量分数的方法是:称取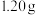 软锰矿样品,加入
软锰矿样品,加入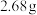 草酸钠固体,再加入足量的稀硫酸并加热(杂质不参加反应),充分反应后冷却,滤去杂质,将所得滤液转移到250 mL容量瓶中并定容,从中取出
草酸钠固体,再加入足量的稀硫酸并加热(杂质不参加反应),充分反应后冷却,滤去杂质,将所得滤液转移到250 mL容量瓶中并定容,从中取出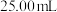 待测液放入锥形瓶中,再用
待测液放入锥形瓶中,再用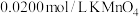 标准溶液进行滴定,反应的离子方程式为:
标准溶液进行滴定,反应的离子方程式为: ,当滴入
,当滴入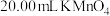 溶液时恰好完全反应。
溶液时恰好完全反应。
①在酸性条件下,
 将
将 氧化的离子方程式为
氧化的离子方程式为②
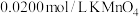 标准溶液应选用下图中的
标准溶液应选用下图中的③将锥形瓶置于滴定管下方进行滴定时,眼睛注视
④软锰矿中
 的质量分数为
的质量分数为
您最近一年使用:0次
2021-01-30更新
|
310次组卷
|
3卷引用:广东省阳江市高新区2022-2023学年高二上学期1月期末考试化学试题
名校
解题方法
10 . (1)已知稀溶液中,1molH2SO4与2molNaOH恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应的中和反应反应热的热化学方程式:_____________ 。
(2)碳的燃烧热为393.5kJ·mol-1,写出表示碳的燃烧热的热化学方程式:________ 。
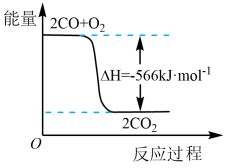
(3)已知CO(g)转化成CO2(g)的能量变化如图所示。写出该反应的热化学方程式:____________ 。
(4)25℃、10lkPa条件下充分燃烧一定量的丁烷气体,放出的热量为QkJ,经测定,将生成的CO2通入足量澄清石灰水中产生25g白色沉淀,写出表示丁烷燃烧热的热化学方程式:__________________ 。
(5)已知下列热化学方程式:
①CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H1=-870.3kJ/mol
②C(s)+O2(g)═CO2(g)△H2=-393.5kJ/mol
③H2(g)+ O2(g)═H2O(l)△H3=-285.8kJ/mol写出由C(s)、H2(g)和O2(g)化合生成CH3COOH(l)的热化学方程式:
O2(g)═H2O(l)△H3=-285.8kJ/mol写出由C(s)、H2(g)和O2(g)化合生成CH3COOH(l)的热化学方程式:_______________ 。
(2)碳的燃烧热为393.5kJ·mol-1,写出表示碳的燃烧热的热化学方程式:
(3)已知CO(g)转化成CO2(g)的能量变化如图所示。写出该反应的热化学方程式:

(4)25℃、10lkPa条件下充分燃烧一定量的丁烷气体,放出的热量为QkJ,经测定,将生成的CO2通入足量澄清石灰水中产生25g白色沉淀,写出表示丁烷燃烧热的热化学方程式:
(5)已知下列热化学方程式:
①CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H1=-870.3kJ/mol
②C(s)+O2(g)═CO2(g)△H2=-393.5kJ/mol
③H2(g)+
 O2(g)═H2O(l)△H3=-285.8kJ/mol写出由C(s)、H2(g)和O2(g)化合生成CH3COOH(l)的热化学方程式:
O2(g)═H2O(l)△H3=-285.8kJ/mol写出由C(s)、H2(g)和O2(g)化合生成CH3COOH(l)的热化学方程式:
您最近一年使用:0次
2020-11-23更新
|
725次组卷
|
8卷引用:广东省阳东广雅学校2017-2018学年高二11月月考化学试题



