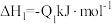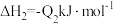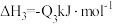(1)已知稀溶液中,1molH2SO4与2molNaOH恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应的中和反应反应热的热化学方程式:_____________ 。
(2)碳的燃烧热为393.5kJ·mol-1,写出表示碳的燃烧热的热化学方程式:________ 。
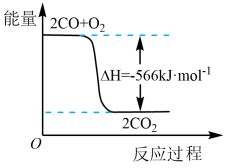
(3)已知CO(g)转化成CO2(g)的能量变化如图所示。写出该反应的热化学方程式:____________ 。
(4)25℃、10lkPa条件下充分燃烧一定量的丁烷气体,放出的热量为QkJ,经测定,将生成的CO2通入足量澄清石灰水中产生25g白色沉淀,写出表示丁烷燃烧热的热化学方程式:__________________ 。
(5)已知下列热化学方程式:
①CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H1=-870.3kJ/mol
②C(s)+O2(g)═CO2(g)△H2=-393.5kJ/mol
③H2(g)+ O2(g)═H2O(l)△H3=-285.8kJ/mol写出由C(s)、H2(g)和O2(g)化合生成CH3COOH(l)的热化学方程式:
O2(g)═H2O(l)△H3=-285.8kJ/mol写出由C(s)、H2(g)和O2(g)化合生成CH3COOH(l)的热化学方程式:_______________ 。
(2)碳的燃烧热为393.5kJ·mol-1,写出表示碳的燃烧热的热化学方程式:
(3)已知CO(g)转化成CO2(g)的能量变化如图所示。写出该反应的热化学方程式:

(4)25℃、10lkPa条件下充分燃烧一定量的丁烷气体,放出的热量为QkJ,经测定,将生成的CO2通入足量澄清石灰水中产生25g白色沉淀,写出表示丁烷燃烧热的热化学方程式:
(5)已知下列热化学方程式:
①CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H1=-870.3kJ/mol
②C(s)+O2(g)═CO2(g)△H2=-393.5kJ/mol
③H2(g)+
 O2(g)═H2O(l)△H3=-285.8kJ/mol写出由C(s)、H2(g)和O2(g)化合生成CH3COOH(l)的热化学方程式:
O2(g)═H2O(l)△H3=-285.8kJ/mol写出由C(s)、H2(g)和O2(g)化合生成CH3COOH(l)的热化学方程式:
17-18高二上·广东阳江·阶段练习 查看更多[8]
更新时间:2020-11-23 12:37:14
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】(1甲醛是一种重要的化工产品,可利用甲醇催化脱氢制备。甲醛与气态甲醇转化的能量关系如图所示。
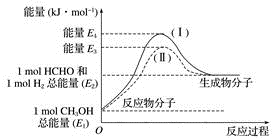
①甲醇催化脱氢转化为甲醛的反应是___________  填“吸热”或“放热”
填“吸热”或“放热” 反应。
反应。
②过程Ⅰ与过程Ⅱ的反应热是否相同?___________ ,原因是___________ 。
(2)在 、101kPa下,1g甲醇
、101kPa下,1g甲醇 燃烧生成
燃烧生成 和液态水时放热
和液态水时放热 。则表示甲醇燃烧热的热化学方程式为:
。则表示甲醇燃烧热的热化学方程式为:___________ 。
(3)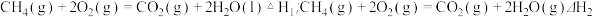 △H1
△H1___________ △H2(填“>”、“﹤”或“=”)
(4)已知拆开 键、
键、 键、
键、 键分别需要的能量是
键分别需要的能量是 、
、 、
、 ,则
,则 与
与 反应生成
反应生成 的热化学方程式为:
的热化学方程式为:___________
(5)白磷与氧可发生如下反应: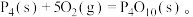 已知断裂下列化学键需要吸收的能量分别为如下
已知断裂下列化学键需要吸收的能量分别为如下
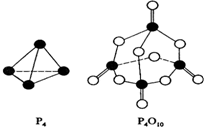
根据图示的分子结构和有关数据估算该反应的
___________ ;
(6)肼可作为火箭发动机的燃料,与氧化剂 反应生成
反应生成 和水蒸气。
和水蒸气。
已知:①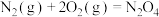
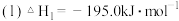
②
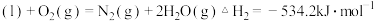
写出肼和 反应的热化学方程式
反应的热化学方程式___________ 。

①甲醇催化脱氢转化为甲醛的反应是
 填“吸热”或“放热”
填“吸热”或“放热” 反应。
反应。②过程Ⅰ与过程Ⅱ的反应热是否相同?
(2)在
 、101kPa下,1g甲醇
、101kPa下,1g甲醇 燃烧生成
燃烧生成 和液态水时放热
和液态水时放热 。则表示甲醇燃烧热的热化学方程式为:
。则表示甲醇燃烧热的热化学方程式为:(3)
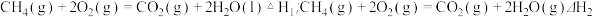 △H1
△H1(4)已知拆开
 键、
键、 键、
键、 键分别需要的能量是
键分别需要的能量是 、
、 、
、 ,则
,则 与
与 反应生成
反应生成 的热化学方程式为:
的热化学方程式为:(5)白磷与氧可发生如下反应:
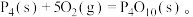 已知断裂下列化学键需要吸收的能量分别为如下
已知断裂下列化学键需要吸收的能量分别为如下| 化学键 |  |  | 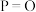 |  |  |
键能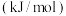 | a | b | c | d | e |

根据图示的分子结构和有关数据估算该反应的

(6)肼可作为火箭发动机的燃料,与氧化剂
 反应生成
反应生成 和水蒸气。
和水蒸气。已知:①
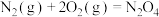
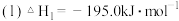
②

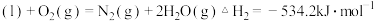
写出肼和
 反应的热化学方程式
反应的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】参考下列图表和有关要求回答问题:
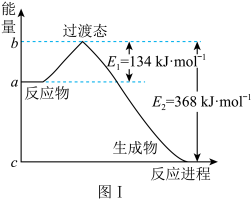
(1)图Ⅰ是 1mol NO2(g)和 1 mol CO(g)反应生成 CO2和NO 过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是_____ (填“增大”“减小”或“不变”,下同),ΔH 的变化是_____ 。请写出 NO2和 CO反应的热化学方程式:_____ 。
(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)ΔH=+49.0 kJ·mol-1
②CH3OH(g)+ O2(g)=CO2(g)+2H2(g)ΔH=-192.9 kJ·mol-1
O2(g)=CO2(g)+2H2(g)ΔH=-192.9 kJ·mol-1
又知③H2O(g)=H2O(l) ΔH=-44 kJ·mol-1则甲醇燃烧生成液态水的热化学方程式:_____ 。
(3)下表是部分化学键的键能数据:
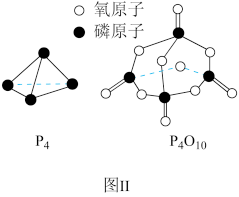
已知 1 mol 白磷(P4)完全燃烧放热为 dkJ,白磷及其完全燃烧的产物结构如图Ⅱ所示,则表中 x=_____ kJ·mol-1(用含有 a、b、c、d 的代数式表示)。


(1)图Ⅰ是 1mol NO2(g)和 1 mol CO(g)反应生成 CO2和NO 过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是
(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)ΔH=+49.0 kJ·mol-1
②CH3OH(g)+
 O2(g)=CO2(g)+2H2(g)ΔH=-192.9 kJ·mol-1
O2(g)=CO2(g)+2H2(g)ΔH=-192.9 kJ·mol-1又知③H2O(g)=H2O(l) ΔH=-44 kJ·mol-1则甲醇燃烧生成液态水的热化学方程式:
(3)下表是部分化学键的键能数据:
| 化学键 | P—P | P—O | O=O | P=O |
| 键能/kJ·mol-1 | a | b | c | x |
已知 1 mol 白磷(P4)完全燃烧放热为 dkJ,白磷及其完全燃烧的产物结构如图Ⅱ所示,则表中 x=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】化学反应都会伴随能量变化,还可以进行化学能与热能、电能、光能等各种形式能量之间的转化。
(1)化学家借助太阳能产生的电能和热能,使空气和水成功地合成了氨气。下列说法正确的是________ 。
A.该过程中有电能转化为化学能的过程
B.该过程属于氮的固定
C.太阳能为新能源
D.断裂 键会释放出能量
键会释放出能量
E.上面涉及到的化学反应均为放热反应
F.Ba(OH)2·8H2O与NH4Cl反应生成NH3的过程放热
(2)利用如图所示装置测定盐酸与氢氧化钠溶液中和反应的反应热
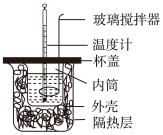
①下列说法错误的是_________________ 。
A.向盐酸中加入氢氧化钠溶液时沿玻璃棒缓慢倒入
B.用测完酸初始温度的温度计,直接测碱的初始温度,测得△H偏小
C.用铜丝搅拌器代替玻璃搅拌器,不影响实验结果
D.改用等浓度的氨水代替氢氧化钠溶液测出的△H偏大
②向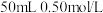 的
的 溶液中分别加入稍过量等浓度等体积的稀醋酸、稀盐酸、浓硫酸,则完全反应时的放出热量
溶液中分别加入稍过量等浓度等体积的稀醋酸、稀盐酸、浓硫酸,则完全反应时的放出热量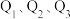 从大到小的排序是
从大到小的排序是______________________________ 。
(3)氮是动植物生长不可缺少的元素,合成氨的反应对人类解决粮食问题贡献巨大,反应如下: 。
。
①一定温度下向2L恒容密闭的容器中通入0.6mol N2和1 mol H2 ,2min时测得NH3为0.4mol,前2min内以H2表示的平均反应速率为___________________ ,H2的转化率为__________ (转化率为已被转化的反应物的物质的量与其初始的物质的之比)
②温度一定的条件下,将一定量的N2和H2的混合气体充入某体积不变的密闭容器中,一段时间后,下列叙述能说明该反应达到平衡状态的是_____________________ (填字母)。
a.密闭容器中混合气体的密度不变 b.N2、H2、NH3的物质的量之比为1∶3∶2
c.容器中的压强不随时间变化 d.密闭容器中氨的体积分数不变
e. 生成1mol N2 的同时生成2mol NH3 f. υ正(N2)= 3υ逆(H2)
(4)理论上,任何自发的氧化还原反应都可以设计成原电池。利用反应 设计一种化学电池,回答下列问题:
设计一种化学电池,回答下列问题:
正极上发生的电极反应式为________________ ,若导线上转移的电子为1mol,则消耗金属铜的质量为_____________ 。
(1)化学家借助太阳能产生的电能和热能,使空气和水成功地合成了氨气。下列说法正确的是
A.该过程中有电能转化为化学能的过程
B.该过程属于氮的固定
C.太阳能为新能源
D.断裂
 键会释放出能量
键会释放出能量E.上面涉及到的化学反应均为放热反应
F.Ba(OH)2·8H2O与NH4Cl反应生成NH3的过程放热
(2)利用如图所示装置测定盐酸与氢氧化钠溶液中和反应的反应热

①下列说法错误的是
A.向盐酸中加入氢氧化钠溶液时沿玻璃棒缓慢倒入
B.用测完酸初始温度的温度计,直接测碱的初始温度,测得△H偏小
C.用铜丝搅拌器代替玻璃搅拌器,不影响实验结果
D.改用等浓度的氨水代替氢氧化钠溶液测出的△H偏大
②向
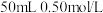 的
的 溶液中分别加入稍过量等浓度等体积的稀醋酸、稀盐酸、浓硫酸,则完全反应时的放出热量
溶液中分别加入稍过量等浓度等体积的稀醋酸、稀盐酸、浓硫酸,则完全反应时的放出热量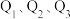 从大到小的排序是
从大到小的排序是(3)氮是动植物生长不可缺少的元素,合成氨的反应对人类解决粮食问题贡献巨大,反应如下:
 。
。①一定温度下向2L恒容密闭的容器中通入0.6mol N2和1 mol H2 ,2min时测得NH3为0.4mol,前2min内以H2表示的平均反应速率为
②温度一定的条件下,将一定量的N2和H2的混合气体充入某体积不变的密闭容器中,一段时间后,下列叙述能说明该反应达到平衡状态的是
a.密闭容器中混合气体的密度不变 b.N2、H2、NH3的物质的量之比为1∶3∶2
c.容器中的压强不随时间变化 d.密闭容器中氨的体积分数不变
e. 生成1mol N2 的同时生成2mol NH3 f. υ正(N2)= 3υ逆(H2)
(4)理论上,任何自发的氧化还原反应都可以设计成原电池。利用反应
 设计一种化学电池,回答下列问题:
设计一种化学电池,回答下列问题:正极上发生的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】根据要求回答下列问题:
(1)下列过程不一定释放能量的是________ 。
A. 化合反应 B. 分解反应 C. 形成化学键 D. 燃料燃烧 E. 酸碱中和 F. 炸药爆炸
(2)等质量的下列物质分别完全燃烧生成 ,放出热量较多的是
,放出热量较多的是________ 。
A. 硫蒸气 B. 硫固体
(3)已知:通常条件下,强酸强碱稀溶液中和生成 水放出的热量为中和热。稀溶液中
水放出的热量为中和热。稀溶液中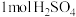 和
和 恰好完全反应时放出
恰好完全反应时放出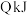 热量,则其中和热为
热量,则其中和热为________  。
。
(4)已知 和
和 反应生成
反应生成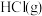 是放热反应,且断开
是放热反应,且断开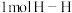 键、
键、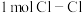 键、
键、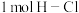 键需吸收的能量分别为
键需吸收的能量分别为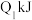 、
、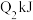 、
、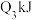 。由此可以推知下列关系正确的是
。由此可以推知下列关系正确的是________ (填序号)。
A.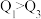 B.
B. 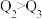 C.
C. 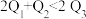
D.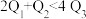 E.
E. 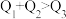 F.
F. 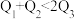
(1)下列过程不一定释放能量的是
A. 化合反应 B. 分解反应 C. 形成化学键 D. 燃料燃烧 E. 酸碱中和 F. 炸药爆炸
(2)等质量的下列物质分别完全燃烧生成
 ,放出热量较多的是
,放出热量较多的是A. 硫蒸气 B. 硫固体
(3)已知:通常条件下,强酸强碱稀溶液中和生成
 水放出的热量为中和热。稀溶液中
水放出的热量为中和热。稀溶液中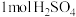 和
和 恰好完全反应时放出
恰好完全反应时放出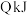 热量,则其中和热为
热量,则其中和热为 。
。(4)已知
 和
和 反应生成
反应生成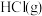 是放热反应,且断开
是放热反应,且断开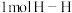 键、
键、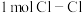 键、
键、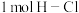 键需吸收的能量分别为
键需吸收的能量分别为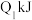 、
、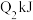 、
、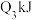 。由此可以推知下列关系正确的是
。由此可以推知下列关系正确的是A.
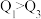 B.
B. 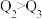 C.
C. 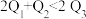
D.
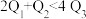 E.
E. 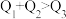 F.
F. 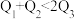
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题
(1)用做消化系统X射线检查的内服药剂“钡餐”的化学式为___________ 。
(2)酸雨的
___________ 5.6(填“>”、“<”、“=”)。
(3) 的电子式
的电子式___________ 。
(4)工业上用焦炭还原石英砂可以制得含有少量杂质的粗硅,化学方程式为___________ 。
(5)己知:①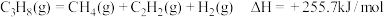
②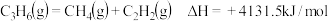
则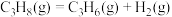 的
的
___________ 。
(1)用做消化系统X射线检查的内服药剂“钡餐”的化学式为
(2)酸雨的

(3)
 的电子式
的电子式(4)工业上用焦炭还原石英砂可以制得含有少量杂质的粗硅,化学方程式为
(5)己知:①
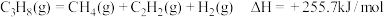
②
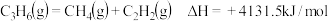
则
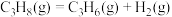 的
的
您最近一年使用:0次
【推荐2】我国要在2030年前实现碳达峰、2060年前实现碳中和的目标,CO2的捕集与转化是研究的重要课题。
(1)CO2和CH4重整可制合成气CO和H2,其热化学反应方程式为CO2(g)+CH4(g)=2CO(g)+2H2(g) ΔH=+247 kJ·mol-1。
已知下列热化学反应方程式:
反应1:C(s)+2H2(g)=CH4(g) ΔH1
反应2:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2=-40.0 kJ·mol-1
反应3:C(s)+H2O(g)=CO(g)+H2(g) ΔH3=+132.0 kJ·mol-1
则ΔH1=___________ kJ·mol-1。
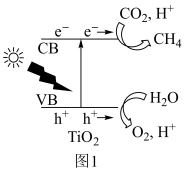
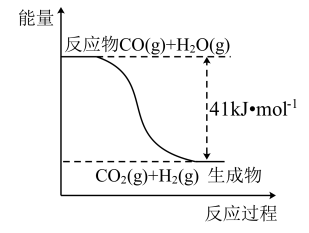
(2)光催化还原法实现CO2甲烷化可能的反应机理如图1所示。该过程可描述为:光照条件下,催化剂TiO2的价带(VB)中的电子激发至导带(CB)中,价带中形成电子空穴(h+),___________ 。
(3)一种电化学法将CO2转化为乙烯的原理如图2所示。
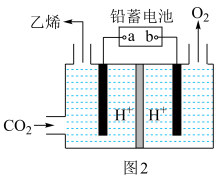
①阴极上的电极反应式为___________ 。
②以铅蓄电池为电源,每生成0.5 mol乙烯,理论上产生O2的物质的量为___________ 。
(1)CO2和CH4重整可制合成气CO和H2,其热化学反应方程式为CO2(g)+CH4(g)=2CO(g)+2H2(g) ΔH=+247 kJ·mol-1。
已知下列热化学反应方程式:
反应1:C(s)+2H2(g)=CH4(g) ΔH1
反应2:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2=-40.0 kJ·mol-1
反应3:C(s)+H2O(g)=CO(g)+H2(g) ΔH3=+132.0 kJ·mol-1
则ΔH1=
(2)光催化还原法实现CO2甲烷化可能的反应机理如图1所示。该过程可描述为:光照条件下,催化剂TiO2的价带(VB)中的电子激发至导带(CB)中,价带中形成电子空穴(h+),

(3)一种电化学法将CO2转化为乙烯的原理如图2所示。

①阴极上的电极反应式为
②以铅蓄电池为电源,每生成0.5 mol乙烯,理论上产生O2的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】 年北京冬奥会首次使用氢能代替丙烷,体现了“绿色环保”办奥理念。丙烷脱氢制丙烯具有显著的经济价值和社会意义,丙烷无氧脱氢还可能生成甲烷、丙炔等副产物。回答下列问题:
年北京冬奥会首次使用氢能代替丙烷,体现了“绿色环保”办奥理念。丙烷脱氢制丙烯具有显著的经济价值和社会意义,丙烷无氧脱氢还可能生成甲烷、丙炔等副产物。回答下列问题:
(1)已知:I. ;
;
II.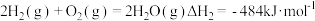 。
。
在一定催化剂下,丙烷无氧脱氢制丙烯的热化学方程式 ∆H=
∆H= ___________ kJ∙mol-1。
(2) 时,将
时,将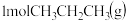 充入某恒容刚性密闭容器中,在催化剂作用下发生反应:
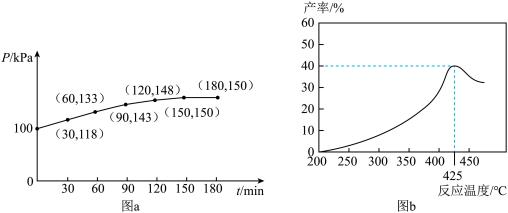
充入某恒容刚性密闭容器中,在催化剂作用下发生反应: 。用压强传感器测出容器内体系压强随时间的变化关系如图
。用压强传感器测出容器内体系压强随时间的变化关系如图 所示:
所示:
①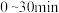 内,用
内,用 的分压变化表示上述脱氢反应的平均反应速率为
的分压变化表示上述脱氢反应的平均反应速率为___________ 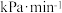 。
。
②保持相同反应时间,在不同温度下,丙烯产率如图 所示,丙烯产率在425℃之前随温度升高而增大的原因可能是
所示,丙烯产率在425℃之前随温度升高而增大的原因可能是___________ 或___________ 。425℃之后,丙烯产率快速降低的主要原因可能是___________ (任写一点)。
 年北京冬奥会首次使用氢能代替丙烷,体现了“绿色环保”办奥理念。丙烷脱氢制丙烯具有显著的经济价值和社会意义,丙烷无氧脱氢还可能生成甲烷、丙炔等副产物。回答下列问题:
年北京冬奥会首次使用氢能代替丙烷,体现了“绿色环保”办奥理念。丙烷脱氢制丙烯具有显著的经济价值和社会意义,丙烷无氧脱氢还可能生成甲烷、丙炔等副产物。回答下列问题:(1)已知:I.
 ;
;II.
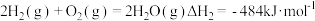 。
。在一定催化剂下,丙烷无氧脱氢制丙烯的热化学方程式
 ∆H=
∆H= (2)
 时,将
时,将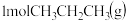 充入某恒容刚性密闭容器中,在催化剂作用下发生反应:
充入某恒容刚性密闭容器中,在催化剂作用下发生反应: 。用压强传感器测出容器内体系压强随时间的变化关系如图
。用压强传感器测出容器内体系压强随时间的变化关系如图 所示:
所示:
①
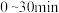 内,用
内,用 的分压变化表示上述脱氢反应的平均反应速率为
的分压变化表示上述脱氢反应的平均反应速率为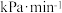 。
。②保持相同反应时间,在不同温度下,丙烯产率如图
 所示,丙烯产率在425℃之前随温度升高而增大的原因可能是
所示,丙烯产率在425℃之前随温度升高而增大的原因可能是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)已知乙醇的燃烧热为-1366.8kJ/mol,写出相应的热化学方程式__ 。
(2)已知强酸强碱的中和热为-57.3kJ/mol,写出稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式:__ 。
(3)已知16g硫固体完全燃烧时放出148.4kJ的热量,则硫的燃烧热的热化学方程式:__ 。
(4)已知:101kPa时,2C(s)+O2(g)=2CO(g)ΔH=-221kJ/mol,则碳的燃烧热数值___ 110.5kJ/mol(填>,<,=)。
(5)已知:稀溶液中,H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3kJ/mol,则浓硫酸与稀NaOH溶液反应生成1mol水,放出的热量___ 57.3kJ(填>,<,=)。
(6)已知一定条件下合成氨反应:N2(g)+3H2(g) 2NH3(g)ΔH=-92.0kJ·mol-1,相同条件下将1molN2和3molH2放在一密闭容器中充分反应,测得反应放出的热量
2NH3(g)ΔH=-92.0kJ·mol-1,相同条件下将1molN2和3molH2放在一密闭容器中充分反应,测得反应放出的热量___ (假定热量无损失)92.0kJ(填>,<,=)。
(7)相同条件下2mol氢原子所具有的能量___ 1mol氢分子所具有的能量(填>,<,=)
(2)已知强酸强碱的中和热为-57.3kJ/mol,写出稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式:
(3)已知16g硫固体完全燃烧时放出148.4kJ的热量,则硫的燃烧热的热化学方程式:
(4)已知:101kPa时,2C(s)+O2(g)=2CO(g)ΔH=-221kJ/mol,则碳的燃烧热数值
(5)已知:稀溶液中,H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3kJ/mol,则浓硫酸与稀NaOH溶液反应生成1mol水,放出的热量
(6)已知一定条件下合成氨反应:N2(g)+3H2(g)
 2NH3(g)ΔH=-92.0kJ·mol-1,相同条件下将1molN2和3molH2放在一密闭容器中充分反应,测得反应放出的热量
2NH3(g)ΔH=-92.0kJ·mol-1,相同条件下将1molN2和3molH2放在一密闭容器中充分反应,测得反应放出的热量(7)相同条件下2mol氢原子所具有的能量
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】金刚石和石墨燃烧,氧气不足时生成一氧化碳,充分燃烧生成二氧化碳,反应中放出的热量如图所示。
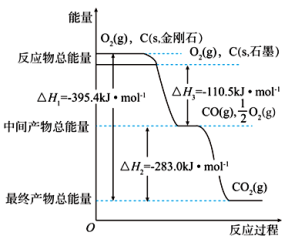
(1)在通常状况下,金刚石和石墨中___________ (填“金刚石”或“石墨”)更稳定,石墨的燃烧热ΔH为___________ 。
(2)当10g丁烷完全燃烧生成CO2和液态水时,放出热量为500kJ,写出表示丁烷燃烧热的热化学方程式:___________ 。
(3)已知:N2、O2分子中化学键的键能分别是946kJ·mol-1、497kJ·mol-1;N2(g)+O2(g)=2NO(g) ΔH=+180.0kJ·mol-1。NO分子中化学键的键能为___________ kJ·mol-1。
(4)由盖斯定律结合下述反应方程式,回答问题:
已知:①C(s)+O2(g)=CO2(g) ΔH1; ②2CO(g)+O2(g)=2CO2(g) ΔH2;③TiO2(g)+2Cl2(g)=TiCl4(s)+O2(g) ΔH3;则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=___________ 。(列出关于ΔH1、ΔH2、ΔH3的表达式)

(1)在通常状况下,金刚石和石墨中
(2)当10g丁烷完全燃烧生成CO2和液态水时,放出热量为500kJ,写出表示丁烷燃烧热的热化学方程式:
(3)已知:N2、O2分子中化学键的键能分别是946kJ·mol-1、497kJ·mol-1;N2(g)+O2(g)=2NO(g) ΔH=+180.0kJ·mol-1。NO分子中化学键的键能为
(4)由盖斯定律结合下述反应方程式,回答问题:
已知:①C(s)+O2(g)=CO2(g) ΔH1; ②2CO(g)+O2(g)=2CO2(g) ΔH2;③TiO2(g)+2Cl2(g)=TiCl4(s)+O2(g) ΔH3;则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的ΔH=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氨是重要的化工原料,已知 在纯氧中燃烧的能量变化如图。
在纯氧中燃烧的能量变化如图。
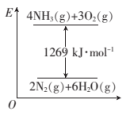
(1)已知:
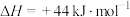 ,则
,则 的燃烧热的热化学方程式为
的燃烧热的热化学方程式为_______ 。
(2) 的燃烧反应可设计成燃料电池,工作原理如图甲所示。电极b为
的燃烧反应可设计成燃料电池,工作原理如图甲所示。电极b为_______ (填“正极”或“负极”);电极a上的电极反应为_______ 。当共消耗1.568 L(标准状况)气体时,通过负载的电子的物质的量为_______ mol。
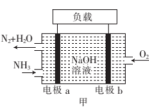
(3)一种肼( )燃料电池的工作原理如图乙所示。
)燃料电池的工作原理如图乙所示。
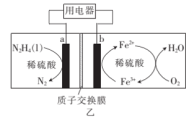
①a极的电极反应式为_______ ;电池中 的离子方程式为
的离子方程式为_______ 。
②若利用该电池给铅酸蓄电池充电,当消耗3.2 g 时,
时, 电极质量
电极质量_______ (填“增加”或“减少”)_______ g。
 在纯氧中燃烧的能量变化如图。
在纯氧中燃烧的能量变化如图。
(1)已知:

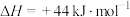 ,则
,则 的燃烧热的热化学方程式为
的燃烧热的热化学方程式为(2)
 的燃烧反应可设计成燃料电池,工作原理如图甲所示。电极b为
的燃烧反应可设计成燃料电池,工作原理如图甲所示。电极b为
(3)一种肼(
 )燃料电池的工作原理如图乙所示。
)燃料电池的工作原理如图乙所示。
①a极的电极反应式为
 的离子方程式为
的离子方程式为②若利用该电池给铅酸蓄电池充电,当消耗3.2 g
 时,
时, 电极质量
电极质量
您最近一年使用:0次

 氢氧化钠溶液与适量稀硫酸完全反应放出5.73kJ的热量,表示中和热的热化学方程式为
氢氧化钠溶液与适量稀硫酸完全反应放出5.73kJ的热量,表示中和热的热化学方程式为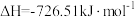 ,表示甲醇燃烧热的热化学方程式为
,表示甲醇燃烧热的热化学方程式为