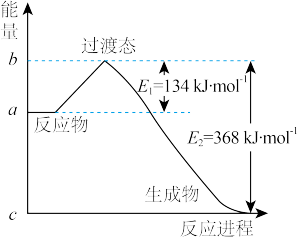
(1甲醛是一种重要的化工产品,可利用甲醇催化脱氢制备。甲醛与气态甲醇转化的能量关系如图所示。
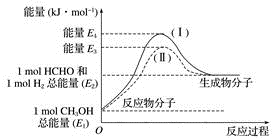
①甲醇催化脱氢转化为甲醛的反应是___________  填“吸热”或“放热”
填“吸热”或“放热” 反应。
反应。
②过程Ⅰ与过程Ⅱ的反应热是否相同?___________ ,原因是___________ 。
(2)在 、101kPa下,1g甲醇
、101kPa下,1g甲醇 燃烧生成
燃烧生成 和液态水时放热
和液态水时放热 。则表示甲醇燃烧热的热化学方程式为:
。则表示甲醇燃烧热的热化学方程式为:___________ 。
(3)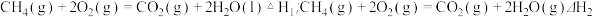 △H1
△H1___________ △H2(填“>”、“﹤”或“=”)
(4)已知拆开 键、
键、 键、
键、 键分别需要的能量是
键分别需要的能量是 、
、 、
、 ,则
,则 与
与 反应生成
反应生成 的热化学方程式为:
的热化学方程式为:___________
(5)白磷与氧可发生如下反应: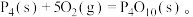 已知断裂下列化学键需要吸收的能量分别为如下
已知断裂下列化学键需要吸收的能量分别为如下
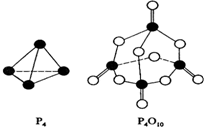
根据图示的分子结构和有关数据估算该反应的
___________ ;
(6)肼可作为火箭发动机的燃料,与氧化剂 反应生成
反应生成 和水蒸气。
和水蒸气。
已知:①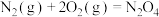
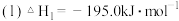
②
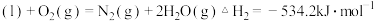
写出肼和 反应的热化学方程式
反应的热化学方程式___________ 。

①甲醇催化脱氢转化为甲醛的反应是
 填“吸热”或“放热”
填“吸热”或“放热” 反应。
反应。②过程Ⅰ与过程Ⅱ的反应热是否相同?
(2)在
 、101kPa下,1g甲醇
、101kPa下,1g甲醇 燃烧生成
燃烧生成 和液态水时放热
和液态水时放热 。则表示甲醇燃烧热的热化学方程式为:
。则表示甲醇燃烧热的热化学方程式为:(3)
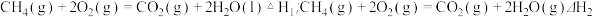 △H1
△H1(4)已知拆开
 键、
键、 键、
键、 键分别需要的能量是
键分别需要的能量是 、
、 、
、 ,则
,则 与
与 反应生成
反应生成 的热化学方程式为:
的热化学方程式为:(5)白磷与氧可发生如下反应:
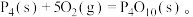 已知断裂下列化学键需要吸收的能量分别为如下
已知断裂下列化学键需要吸收的能量分别为如下| 化学键 |  |  | 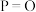 |  |  |
键能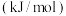 | a | b | c | d | e |

根据图示的分子结构和有关数据估算该反应的

(6)肼可作为火箭发动机的燃料,与氧化剂
 反应生成
反应生成 和水蒸气。
和水蒸气。已知:①
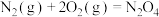
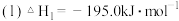
②

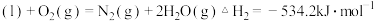
写出肼和
 反应的热化学方程式
反应的热化学方程式
20-21高二上·江西宜春·阶段练习 查看更多[3]
广西钦州市第四中学2023-2024学年高二上学期9月考试化学试卷(已下线)第04讲 第一章《化学反应的热效应》单元测试(基础巩固)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)江西宜春市第九中学2020-2021学年高二上学期第一次月考化学试题
更新时间:2021-01-06 09:40:20
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】填空
I.CO2和CH4在一定条件下合成乙酸: 完成下列填空:
完成下列填空:
(1)写出碳原子最外电子层的轨道表示式______ 。碳元素在周期表中位置:______ 。
(2)钛(Ti)是22号元素,它是______ (选填编号)。
a.主族元素 b.副族元素 c.短周期元素 d.长周期元素
(3)CO2分子的电子式为______ ;其熔沸点比CS2低,原因是______ 。
Ⅱ.依据事实,写出下列反应的热化学方程式。
(4)13gC2H2(g)完全燃烧生成CO2和H2O(l)时,放出659kJ的热量,该反应的热化学方程式为______ 。
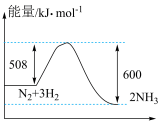
(5)根据如图写出热化学方程式______ ;
(6)已知:
且硅晶体中每个 硅原子和其他4个硅原子形成4 个共价键,工业上制取高纯硅的反应方程式为:SiCl4(g)+2H2(g) Si(s)+4HCl(g),该反应的反应热为ΔH=
Si(s)+4HCl(g),该反应的反应热为ΔH=______ 。
Ⅲ.
(7)工业上常用A(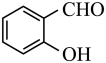 )与B(
)与B(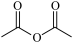 )在催化剂存在下加热反应制得香豆素(
)在催化剂存在下加热反应制得香豆素(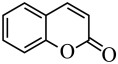 )。该反应涉及的反应类型有加成反应、
)。该反应涉及的反应类型有加成反应、______ 、______ 。
(8)写出香豆素在NaOH水溶液、加热条件下发生水解反应与化学方程式:______ 。
I.CO2和CH4在一定条件下合成乙酸:
 完成下列填空:
完成下列填空:(1)写出碳原子最外电子层的轨道表示式
(2)钛(Ti)是22号元素,它是
a.主族元素 b.副族元素 c.短周期元素 d.长周期元素
(3)CO2分子的电子式为
Ⅱ.依据事实,写出下列反应的热化学方程式。
(4)13gC2H2(g)完全燃烧生成CO2和H2O(l)时,放出659kJ的热量,该反应的热化学方程式为
(5)根据如图写出热化学方程式

(6)已知:
| 化学键 | Si-Cl | H-H | H-Cl | Si-Si |
| 键能/kJ·mol-1 | 360 | 436 | 431 | 176 |
 Si(s)+4HCl(g),该反应的反应热为ΔH=
Si(s)+4HCl(g),该反应的反应热为ΔH=Ⅲ.
(7)工业上常用A(
 )与B(
)与B( )在催化剂存在下加热反应制得香豆素(
)在催化剂存在下加热反应制得香豆素( )。该反应涉及的反应类型有加成反应、
)。该反应涉及的反应类型有加成反应、(8)写出香豆素在NaOH水溶液、加热条件下发生水解反应与化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101 kPa下,已知该反应每消耗1 mol CuCl(s),放热44.4 kJ,该反应的热化学方程式是___________ 。
(2)已知:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
CO(g)+ O2(g)=CO2(g) ΔH=-283 kJ·mol-1
O2(g)=CO2(g) ΔH=-283 kJ·mol-1
某H2和CO的混合气体完全燃烧时放出113.76 kJ热量,同时生成3.6 g液态水,则原混合气体中H2和CO的物质的量分别为___________ 。
(1)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101 kPa下,已知该反应每消耗1 mol CuCl(s),放热44.4 kJ,该反应的热化学方程式是
(2)已知:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
CO(g)+
 O2(g)=CO2(g) ΔH=-283 kJ·mol-1
O2(g)=CO2(g) ΔH=-283 kJ·mol-1某H2和CO的混合气体完全燃烧时放出113.76 kJ热量,同时生成3.6 g液态水,则原混合气体中H2和CO的物质的量分别为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】依据事实,写出下列反应的热化学方程式:
(1)1mol的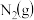 与适量的
与适量的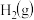 反应生成
反应生成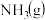 ,放出92.2kJ热量。
,放出92.2kJ热量。_______ 。
(2)其他相关数据如下表:
写出1mol 和1mol
和1mol 化合时的热化学方程式:
化合时的热化学方程式:_______ 。
(3)已知ag乙烯气体充分燃烧时生成1mol 和液态水,放出bkJ的热量,则表示乙烯燃烧热的热化学方程式为:
和液态水,放出bkJ的热量,则表示乙烯燃烧热的热化学方程式为:_______ 。
(4)已知CO(g)和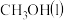 的燃烧热分别为283.0kJ/mol和726.5kJ/mol。请写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
的燃烧热分别为283.0kJ/mol和726.5kJ/mol。请写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:_______ 。
(1)1mol的
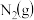 与适量的
与适量的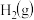 反应生成
反应生成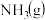 ,放出92.2kJ热量。
,放出92.2kJ热量。(2)其他相关数据如下表:
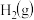 | 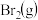 | 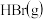 | |
| 1mol分子中的化学键断裂时需要吸收的能量 | 436 | 230 | 369 |
 和1mol
和1mol 化合时的热化学方程式:
化合时的热化学方程式:(3)已知ag乙烯气体充分燃烧时生成1mol
 和液态水,放出bkJ的热量,则表示乙烯燃烧热的热化学方程式为:
和液态水,放出bkJ的热量,则表示乙烯燃烧热的热化学方程式为:(4)已知CO(g)和
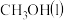 的燃烧热分别为283.0kJ/mol和726.5kJ/mol。请写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
的燃烧热分别为283.0kJ/mol和726.5kJ/mol。请写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。请回答下列问题:
(1)已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H=+49.0kJ/mol
②CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) △H=-192.9kJ/mol
由上述方程式可知,CH3OH(g)的燃烧热__________ (填“大于”、“等于”或小于”)192.9kJ/mol。已知水的汽化热为44 kJ/mol,则表示氢气燃烧热的热化学方程式为__________________________ 。
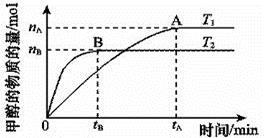
(2)在容积为2 L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的情况下实验结果如下图所示(注:T1、T2均大于300 ℃),该反应为_________ 反应(填“放热”或“吸热”);在T1温度时,将1 mol CO2和3 mol H2充入一密闭恒容容器中,充分反应达到平衡后,若CO2转化率为a,则容器内的压强与起始压强之比为______________ 。
(1)已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H=+49.0kJ/mol
②CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) △H=-192.9kJ/mol
由上述方程式可知,CH3OH(g)的燃烧热
(2)在容积为2 L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的情况下实验结果如下图所示(注:T1、T2均大于300 ℃),该反应为

您最近一年使用:0次
【推荐2】能源是人类生活和社会发展的物质基础,研究化学反应中的能量变化,有助于更好地利用化学反应为人们的生产和生活服务。请回答下列问题:
(1)从能量的角度看:断开化学键要________ 能量;形成化学键要________ 能量。
(2)已知强酸与强碱的稀溶液发生的中和反应可表示为 △H=-57.3 kJ/mol。中和热测定实验中,用到的玻璃仪器有烧杯、量筒、
△H=-57.3 kJ/mol。中和热测定实验中,用到的玻璃仪器有烧杯、量筒、________ 、________ 。若用20 g NaOH配成的稀溶液与足量稀盐酸反应,则能放出________ kJ的热量。
(3)0.2 mol液态高能燃料联氨(分子式为N2H4)在氧气中燃烧会生成氮气和液态水,并放出124.25 kJ的热量,则其热化学方程式为_________________________ 。
(4)已知: △H=-44 kJ/mol;
△H=-44 kJ/mol;
 △H=-1228 kJ/mol。
△H=-1228 kJ/mol。
写出液态酒精完全燃烧后温度恢复到室温时反应的热化学方程式:_______________________ 。
(1)从能量的角度看:断开化学键要
(2)已知强酸与强碱的稀溶液发生的中和反应可表示为
 △H=-57.3 kJ/mol。中和热测定实验中,用到的玻璃仪器有烧杯、量筒、
△H=-57.3 kJ/mol。中和热测定实验中,用到的玻璃仪器有烧杯、量筒、(3)0.2 mol液态高能燃料联氨(分子式为N2H4)在氧气中燃烧会生成氮气和液态水,并放出124.25 kJ的热量,则其热化学方程式为
(4)已知:
 △H=-44 kJ/mol;
△H=-44 kJ/mol; △H=-1228 kJ/mol。
△H=-1228 kJ/mol。写出液态酒精完全燃烧后温度恢复到室温时反应的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】磷存在于人体所有细胞中,是维持骨骼和牙齿的必要物质,几乎参与所有生理上的化学反应。磷还能让心脏有规律地跳动、维持肾脏正常机能和传达神经刺激的重要物质。许多磷的化合物是工业上的重要原料。请完成下列填空:
P(s,红磷)+ O2(g)=
O2(g)= P4O10(s)+738.5 kJ
P4O10(s)+738.5 kJ
P4(s,白磷)+ 5O2(g)=P4O10(s)+2983.2 kJ
(1)则白磷转化为红磷的热化学方程式_____________________ 。
(2)红磷在KOH溶液的悬浊液中和KOCl作用,可以生成K6P6O12的钾盐和KCl等产物。请写出该反应的化学方程式,并标出电子转移方向和数目。____
(3)制备MgNH4PO4时通常在镁盐(如氯化镁)溶液中加Na2HPO4 、氨水和铵盐溶液(如氯化铵),反应式为MgCl2+Na2HPO4+NH3=2NaCl+MgNH4PO4↓。在此反应中,如果不加铵盐,在碱性溶液中,Mg2+将会被氨水沉淀,其离子方程式为____________________ ;加入铵盐之后,可防止产生Mg(OH)2沉淀。请用电离平衡原理解释原因:_________
(4)H3PO3与碘水反应,碘水的棕黄色褪去,生成磷酸,向上述反应后的溶液中加入过量的AgNO3溶液,生成黄色沉淀。则H3PO3与碘水反应的化学方程式为___________ ;黄色沉淀是_________ ,可用作于_____________________ (写出任意一种用途即可)。
P(s,红磷)+
 O2(g)=
O2(g)= P4O10(s)+738.5 kJ
P4O10(s)+738.5 kJ P4(s,白磷)+ 5O2(g)=P4O10(s)+2983.2 kJ
(1)则白磷转化为红磷的热化学方程式
(2)红磷在KOH溶液的悬浊液中和KOCl作用,可以生成K6P6O12的钾盐和KCl等产物。请写出该反应的化学方程式,并标出电子转移方向和数目。
(3)制备MgNH4PO4时通常在镁盐(如氯化镁)溶液中加Na2HPO4 、氨水和铵盐溶液(如氯化铵),反应式为MgCl2+Na2HPO4+NH3=2NaCl+MgNH4PO4↓。在此反应中,如果不加铵盐,在碱性溶液中,Mg2+将会被氨水沉淀,其离子方程式为
(4)H3PO3与碘水反应,碘水的棕黄色褪去,生成磷酸,向上述反应后的溶液中加入过量的AgNO3溶液,生成黄色沉淀。则H3PO3与碘水反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】请运用反应热的知识填写下列空白:
(1)已知: (s,白磷)=
(s,白磷)= (s,黑磷)
(s,黑磷) 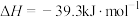 ;
;
 (s,白磷)=
(s,白磷)= (s,红磷)
(s,红磷) 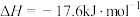 ;
;
由此推知,其中最稳定的磷单质是___________ 。
(2)①硅粉与HCl在300℃时反应生成1 mol SiHCl3气体和H2,放出225 kJ热量,该反应的热化学方程式为___________ 。
②在 25℃ 和 101kPa时,4 g硫粉在O2中完全燃烧生成SO2气体,放出37 kJ的热量,写出表示S燃烧热的热化学方程式:___________ 。
(3)已知上述反应中相关的化学键键能数据如下:
则该反应的 ΔH = ___________ 。
(4)将 氢化为
氢化为 有三种方法,对应的反应依次为:
有三种方法,对应的反应依次为:
①

②

③

反应③的 ΔH3 =___________ (用ΔH1,ΔH2表示)
(5)①2Cu2O(s) + O2(g) =4CuO(s) ΔH1=-277kJ·mol-1
②8CuO(s) + CH4(g)=4Cu2O(s) + CO2(g)+2H2O(g) ΔH2=-348kJ·mol-1
反应CH4(g) +2O2(g)=CO2(g)+2H2O(g) ΔH=___________ kJ·mol-1
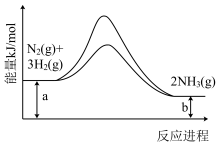
(6)合成氨反应常使用铁触媒提高反应速率。如图为有、无铁触媒时,反应的能量变化示意图。写出该反应的热化学方程式___________ 。
(1)已知:
 (s,白磷)=
(s,白磷)= (s,黑磷)
(s,黑磷) 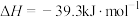 ;
; (s,白磷)=
(s,白磷)= (s,红磷)
(s,红磷) 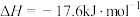 ;
;由此推知,其中最稳定的磷单质是
(2)①硅粉与HCl在300℃时反应生成1 mol SiHCl3气体和H2,放出225 kJ热量,该反应的热化学方程式为
②在 25℃ 和 101kPa时,4 g硫粉在O2中完全燃烧生成SO2气体,放出37 kJ的热量,写出表示S燃烧热的热化学方程式:
(3)已知上述反应中相关的化学键键能数据如下:
| 化学键 | C-H | C=O | H-H | C O(CO) O(CO) |
| 键能/kJ·mol−1 | 413 | 745 | 436 | 1075 |
(4)将
 氢化为
氢化为 有三种方法,对应的反应依次为:
有三种方法,对应的反应依次为:①


②


③


反应③的 ΔH3 =
(5)①2Cu2O(s) + O2(g) =4CuO(s) ΔH1=-277kJ·mol-1
②8CuO(s) + CH4(g)=4Cu2O(s) + CO2(g)+2H2O(g) ΔH2=-348kJ·mol-1
反应CH4(g) +2O2(g)=CO2(g)+2H2O(g) ΔH=
(6)合成氨反应常使用铁触媒提高反应速率。如图为有、无铁触媒时,反应的能量变化示意图。写出该反应的热化学方程式

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据所学知识,回答下列问题。
(1)实验室中和热的测定过程中,玻璃搅拌器的正确操作是_______ (填字母)
A.顺时针搅拌 B.逆时针搅拌 C.上下移动
(2)中和热的测定,倒入NaOH溶液的正确操作是_______ (填字母)
a.沿玻璃棒缓慢倒入 b.分三次倒入 c.一次迅速倒入
(3)若中和热的测定实验过程中,内筒未加杯盖,求得的中和反应反应热
_______ (填“偏大“偏小”或“无影响”)。
(4)向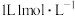 的
的 溶液中分别加入下列物质:①浓硫酸;②稀硝酸;③稀醋酸。反应恰好完全,生成1mol水时的热效应分别为
溶液中分别加入下列物质:①浓硫酸;②稀硝酸;③稀醋酸。反应恰好完全,生成1mol水时的热效应分别为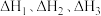 ,则三者由大到小的顺序为
,则三者由大到小的顺序为_______ 。
(5)已知:①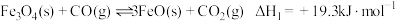
②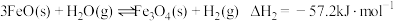
③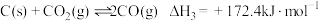
碳与水蒸气反应制氢气的总反应热化学方程式是_______ 。
(6)图Ⅰ是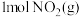 和
和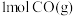 反应生成
反应生成 和
和 过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大,
过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大, 的变化是
的变化是_______ ,(填“增大”、“减小”、“不变”,下同)。 的变化是
的变化是_______ 。
(1)实验室中和热的测定过程中,玻璃搅拌器的正确操作是
A.顺时针搅拌 B.逆时针搅拌 C.上下移动
(2)中和热的测定,倒入NaOH溶液的正确操作是
a.沿玻璃棒缓慢倒入 b.分三次倒入 c.一次迅速倒入
(3)若中和热的测定实验过程中,内筒未加杯盖,求得的中和反应反应热

(4)向
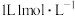 的
的 溶液中分别加入下列物质:①浓硫酸;②稀硝酸;③稀醋酸。反应恰好完全,生成1mol水时的热效应分别为
溶液中分别加入下列物质:①浓硫酸;②稀硝酸;③稀醋酸。反应恰好完全,生成1mol水时的热效应分别为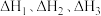 ,则三者由大到小的顺序为
,则三者由大到小的顺序为(5)已知:①
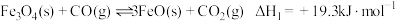
②
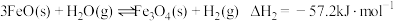
③
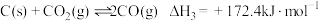
碳与水蒸气反应制氢气的总反应热化学方程式是
(6)图Ⅰ是
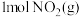 和
和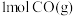 反应生成
反应生成 和
和 过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大,
过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大, 的变化是
的变化是 的变化是
的变化是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】为解决能源短缺问题,工业生产中应合理利用化学能。
(1)实验室用50mL 0.5mol/L的盐酸和50mL 0.55mol/L的NaOH(密度均为1g/cm3)测定中和热。反应前两溶液的温度均为25.2℃,混合后混合溶液的最高温度为28.2℃,反应溶液的比热容为C=4.18J/(g·℃),请写出该反应的热化学方程式_______ 。
(2)25℃,1.01×105Pa时,实验测得,4g氢气在O2中完全燃烧生成液态水放出572kJ的热量,则H2的燃烧热 的热化学方程式为_______ 。
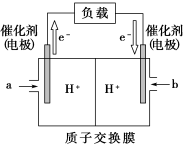
(3)下图是某笔记本电脑使用的甲醇燃料电池的结构示意图。放电时甲醇应从_______ 处通入(填“a”或“b”),电池内部H+向_______ (填“左”或“右”)移动。写出电池负极的电极反应式_______ 。
(4)从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。
已知:N2(g)+3H2(g)=2NH3(g) ΔH=-93kJ·mol-1.试根据表中所列键能数据计算a的数值_______ 。
(5)已知:C(s,石墨)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1①
2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6kJ·mol-1②
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2599kJ·mol-1③
根据盖斯定律,计算反应2C(s,石墨)+H2(g)=C2H2(g)的ΔH=_______ 。
(1)实验室用50mL 0.5mol/L的盐酸和50mL 0.55mol/L的NaOH(密度均为1g/cm3)测定中和热。反应前两溶液的温度均为25.2℃,混合后混合溶液的最高温度为28.2℃,反应溶液的比热容为C=4.18J/(g·℃),请写出该反应的热化学方程式
(2)25℃,1.01×105Pa时,实验测得,4g氢气在O2中完全燃烧生成液态水放出572kJ的热量,则H2的
(3)下图是某笔记本电脑使用的甲醇燃料电池的结构示意图。放电时甲醇应从

(4)从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。
| 化学键 | H—H | N—H | N≡N |
| 键能/kJ·mol-1 | 436 | a | 945 |
已知:N2(g)+3H2(g)=2NH3(g) ΔH=-93kJ·mol-1.试根据表中所列键能数据计算a的数值
(5)已知:C(s,石墨)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1①
2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6kJ·mol-1②
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2599kJ·mol-1③
根据盖斯定律,计算反应2C(s,石墨)+H2(g)=C2H2(g)的ΔH=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】反应热产生的原因:以H2(g)+Cl2(g)=2HCl(g)为例说明_______ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)键能是表征化学键强度的物理量,可以用键断裂时所需能量的大小来衡量。从断键和成键的角度分析反应2H2(g)+O2(g)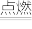 2H2O(g)中能量的变化,化学键的键能如表所示:
2H2O(g)中能量的变化,化学键的键能如表所示:
则生成1molH2O(g)可以放出____ kJ热量。
(2)下列反应中,属于放热反应的是____ (填字母,下同),属于吸热反应的是____ 。
a.盐酸与烧碱溶液反应
b.Ba(OH)2•8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氢气在氧气中燃烧生成水
d.高温煅烧石灰石使其分解
e.铝和盐酸反应
f.葡萄糖在人体内氧化分解
(3)A、B、C、D四种金属按下表中装置进行实验。
根据实验现象回答下列问题:
①装置甲溶液中的阴离子移向____ (填“A”或“B”)极。
②装置乙中正极的电极反应式为____ 。
③四种金属活动性由强到弱的顺序是____ 。
(1)键能是表征化学键强度的物理量,可以用键断裂时所需能量的大小来衡量。从断键和成键的角度分析反应2H2(g)+O2(g)
 2H2O(g)中能量的变化,化学键的键能如表所示:
2H2O(g)中能量的变化,化学键的键能如表所示:| 化学键 | H—H | O=O | H—O |
| 键能(kJ·mol-1) | 436 | 496 | 463 |
则生成1molH2O(g)可以放出
(2)下列反应中,属于放热反应的是
a.盐酸与烧碱溶液反应
b.Ba(OH)2•8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氢气在氧气中燃烧生成水
d.高温煅烧石灰石使其分解
e.铝和盐酸反应
f.葡萄糖在人体内氧化分解
(3)A、B、C、D四种金属按下表中装置进行实验。
| 装置 | 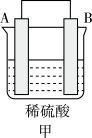 |  | 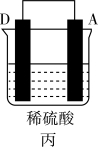 |
| 现象 | 金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
①装置甲溶液中的阴离子移向
②装置乙中正极的电极反应式为
③四种金属活动性由强到弱的顺序是
您最近一年使用:0次




