能源是人类生活和社会发展的物质基础,研究化学反应中的能量变化,有助于更好地利用化学反应为人们的生产和生活服务。请回答下列问题:
(1)从能量的角度看:断开化学键要________ 能量;形成化学键要________ 能量。
(2)已知强酸与强碱的稀溶液发生的中和反应可表示为 △H=-57.3 kJ/mol。中和热测定实验中,用到的玻璃仪器有烧杯、量筒、
△H=-57.3 kJ/mol。中和热测定实验中,用到的玻璃仪器有烧杯、量筒、________ 、________ 。若用20 g NaOH配成的稀溶液与足量稀盐酸反应,则能放出________ kJ的热量。
(3)0.2 mol液态高能燃料联氨(分子式为N2H4)在氧气中燃烧会生成氮气和液态水,并放出124.25 kJ的热量,则其热化学方程式为_________________________ 。
(4)已知: △H=-44 kJ/mol;
△H=-44 kJ/mol;
 △H=-1228 kJ/mol。
△H=-1228 kJ/mol。
写出液态酒精完全燃烧后温度恢复到室温时反应的热化学方程式:_______________________ 。
(1)从能量的角度看:断开化学键要
(2)已知强酸与强碱的稀溶液发生的中和反应可表示为
 △H=-57.3 kJ/mol。中和热测定实验中,用到的玻璃仪器有烧杯、量筒、
△H=-57.3 kJ/mol。中和热测定实验中,用到的玻璃仪器有烧杯、量筒、(3)0.2 mol液态高能燃料联氨(分子式为N2H4)在氧气中燃烧会生成氮气和液态水,并放出124.25 kJ的热量,则其热化学方程式为
(4)已知:
 △H=-44 kJ/mol;
△H=-44 kJ/mol; △H=-1228 kJ/mol。
△H=-1228 kJ/mol。写出液态酒精完全燃烧后温度恢复到室温时反应的热化学方程式:
更新时间:2021-01-09 11:53:20
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活所需的主要能源物质。
(1)有机物 、
、 可以相互转化:
可以相互转化:


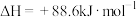 ;
; 、
、 相比,较不稳定的是
相比,较不稳定的是___________ 。
(2)使 和
和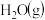 通过灼热的炭层,生成
通过灼热的炭层,生成 和
和 ,当消耗
,当消耗
 时释放出
时释放出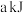 热量,写出该反应的热化学方程式
热量,写出该反应的热化学方程式___________ 。
(3)工业上可采用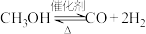 的方法来制取高纯度的
的方法来制取高纯度的 和
和 。我国研究人员采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用*标注。下图为计算机模拟的各步反应的能量变化示意图:
。我国研究人员采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用*标注。下图为计算机模拟的各步反应的能量变化示意图:

该历程中最大能垒(活化能)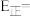
___________  ,该历程中,放热最多的步骤的化学方程式为
,该历程中,放热最多的步骤的化学方程式为___________ 。
(1)有机物
 、
、 可以相互转化:
可以相互转化:


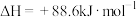 ;
; 、
、 相比,较不稳定的是
相比,较不稳定的是(2)使
 和
和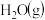 通过灼热的炭层,生成
通过灼热的炭层,生成 和
和 ,当消耗
,当消耗
 时释放出
时释放出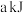 热量,写出该反应的热化学方程式
热量,写出该反应的热化学方程式(3)工业上可采用
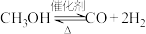 的方法来制取高纯度的
的方法来制取高纯度的 和
和 。我国研究人员采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用*标注。下图为计算机模拟的各步反应的能量变化示意图:
。我国研究人员采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用*标注。下图为计算机模拟的各步反应的能量变化示意图:
该历程中最大能垒(活化能)
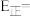
 ,该历程中,放热最多的步骤的化学方程式为
,该历程中,放热最多的步骤的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)氮是动植物生长不可缺少的元素,合成氨的反应对人类解决粮食问题贡献巨大,反应如下:N2(g)+3H2(g) 2NH3(g)。
2NH3(g)。
①合成氨的反应中的能量变化如图所示。该反应是___ 反应(填“吸热”或“放热”),其原因是反应物化学键断裂吸收的总能量___ (填“大于”或“小于”)生成物化学键形成放出的总能量。

②在一定条件下,将一定量的N2和H2的混合气体充入某密闭容器中,一段时间后,下列叙述能说明该反应达到平衡状态的是___ (填序号)。
A.容器中气体密度不变
B.N2、H2、NH3的物质的量之比为1:3:2
C.容器中的压强不随时间变化
D.单位时间内每断裂6 mol N—H键的同时断裂3 mol H﹣H键
(2)某温度时,在一个容积为2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。2分钟时达到平衡状态,根据图中数据,试填写下列空白:

①该反应的化学方程式为___ 。
②反应开始到平衡建立,用气体Z表示的反应速率为___ ;若反应容器体积可变,则充入氮气会使反应速率___ (填”变快”、”变慢”或”不变”)
 2NH3(g)。
2NH3(g)。①合成氨的反应中的能量变化如图所示。该反应是

②在一定条件下,将一定量的N2和H2的混合气体充入某密闭容器中,一段时间后,下列叙述能说明该反应达到平衡状态的是
A.容器中气体密度不变
B.N2、H2、NH3的物质的量之比为1:3:2
C.容器中的压强不随时间变化
D.单位时间内每断裂6 mol N—H键的同时断裂3 mol H﹣H键
(2)某温度时,在一个容积为2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。2分钟时达到平衡状态,根据图中数据,试填写下列空白:

①该反应的化学方程式为
②反应开始到平衡建立,用气体Z表示的反应速率为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)稀溶液中, 与
与 完全反应时,放出
完全反应时,放出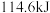 热量,写出表示中和热的热化学方程式
热量,写出表示中和热的热化学方程式___________ 。
(2) 燃烧热为
燃烧热为 ,写出表示燃烧热的热化学方程式为:
,写出表示燃烧热的热化学方程式为:______________ 。
(3) ,拆开
,拆开 键、
键、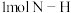 键、
键、 键分别篇要的能量是
键分别篇要的能量是 、
、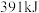 、
、 ,则
,则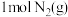 生成
生成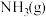 的反应热
的反应热 为
为_____________ 。
(1)稀溶液中,
 与
与 完全反应时,放出
完全反应时,放出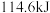 热量,写出表示中和热的热化学方程式
热量,写出表示中和热的热化学方程式(2)
 燃烧热为
燃烧热为 ,写出表示燃烧热的热化学方程式为:
,写出表示燃烧热的热化学方程式为:(3)
 ,拆开
,拆开 键、
键、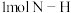 键、
键、 键分别篇要的能量是
键分别篇要的能量是 、
、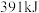 、
、 ,则
,则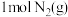 生成
生成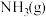 的反应热
的反应热 为
为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】I.化学反应伴随能量变化,获取反应能量变化有多条途径。回答下列问题:
(1)理论研究表明,在101kPa和298K下,HCN(g)=HNC(g)异构化反应过程的能量变化如图所示,HCN与HNC稳定性较弱的是___________ 。

(2)已知:
计算可得:HNC(g)=HCN(g) △H=___________ kJ/mol|(用含a、b的式子表示)。
(3)神舟系列火箭用偏二甲肼C2H8N2作燃料,N2O4作氧化剂,反应后产物无污染。
已知:反应1:N2(g)+2O2(g)=N2O4(g) △H=xkJ∙mol-1
反应2:C2H8N2(1)+4O2(g)=N2(g)+2CO2(g)+4H2O(g) △H2=ykJ∙mol-1
写出C2H8N2(1)和N2O4(g)反应生成N2(g)、CO2(g)、H2O(g)的热化学方程式:___________ 。
II.某学生通过测定反应过程中所放出的热量来计算中和反应的反应热。将50mL0.50mol/L的盐酸与50mL0.55mol/L的NaOH溶液加入如图所示的装置中,进行中和反应。请回答下列问题:

(4)从实验装置上看,图中缺少的一种玻璃仪器是___________ (填仪器名称)。
(5)该同学做实验时有些操作不规范,造成测得中和反应反应热△H偏低,请你分析可能的原因是___________。
(1)理论研究表明,在101kPa和298K下,HCN(g)=HNC(g)异构化反应过程的能量变化如图所示,HCN与HNC稳定性较弱的是

(2)已知:
| 化学键种类 | C-H | N-H | C≡N |
| 键能(kJ/mol) | a | b | c |
(3)神舟系列火箭用偏二甲肼C2H8N2作燃料,N2O4作氧化剂,反应后产物无污染。
已知:反应1:N2(g)+2O2(g)=N2O4(g) △H=xkJ∙mol-1
反应2:C2H8N2(1)+4O2(g)=N2(g)+2CO2(g)+4H2O(g) △H2=ykJ∙mol-1
写出C2H8N2(1)和N2O4(g)反应生成N2(g)、CO2(g)、H2O(g)的热化学方程式:
II.某学生通过测定反应过程中所放出的热量来计算中和反应的反应热。将50mL0.50mol/L的盐酸与50mL0.55mol/L的NaOH溶液加入如图所示的装置中,进行中和反应。请回答下列问题:

(4)从实验装置上看,图中缺少的一种玻璃仪器是
(5)该同学做实验时有些操作不规范,造成测得中和反应反应热△H偏低,请你分析可能的原因是___________。
| A.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓 |
| B.在量取盐酸时仰视读数 |
| C.测量盐酸的温度后,温度计没有用水冲洗干净 |
| D.用Ba(OH)2溶液和硫酸代替上述试剂 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氮元素在工业应用上有重要地位,回答下列问题:
(1)理论研究表明,在 和
和 下,
下, 异构化反应的能量变化如图。
异构化反应的能量变化如图。
___________ 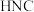 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
②该异构化反应的
___________ 
(2)“长征 ”运载火箭使用
”运载火箭使用 和
和 (偏二甲册)作推进剂。
(偏二甲册)作推进剂。 液态
液态 在液态
在液态 中燃烧生成
中燃烧生成 、
、 、
、 三种气体,放出
三种气体,放出 热量。该反应的热化学方程式为
热量。该反应的热化学方程式为________ 。
(3)科学家用氮气和氢气制备肼,过程如下:

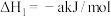

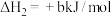
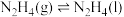
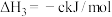
则

___________  (用含a、b、c的计算式表示)。
(用含a、b、c的计算式表示)。
(4)化学反应常伴随热效应。某些反应(如中和反应)的热量变化,其数值Q可通过量热装置测量反应前后体系温度变化,用公式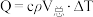 计算获得。
计算获得。
①热量的测定:取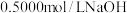 溶液和
溶液和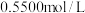 盐酸各
盐酸各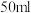 进行反应,测得反应前后体系的温度值(℃)分别为
进行反应,测得反应前后体系的温度值(℃)分别为 、
、 ,则该过程放出的热量为
,则该过程放出的热量为___________ J(c和 分别取
分别取 和
和 ,忽略水以外各物质吸收的热量,后同),则该实验测得中和热
,忽略水以外各物质吸收的热量,后同),则该实验测得中和热
________  。
。
②下列操作会使所测得的焓变 偏小的是
偏小的是___________
a.用等物质的量浓度的醋酸代替盐酸实验
b.量热装置绝热效果欠佳
c. 溶液量多了
溶液量多了
(1)理论研究表明,在
 和
和 下,
下, 异构化反应的能量变化如图。
异构化反应的能量变化如图。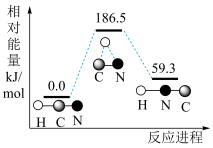

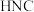 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。②该异构化反应的


(2)“长征
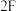 ”运载火箭使用
”运载火箭使用 和
和 (偏二甲册)作推进剂。
(偏二甲册)作推进剂。 液态
液态 在液态
在液态 中燃烧生成
中燃烧生成 、
、 、
、 三种气体,放出
三种气体,放出 热量。该反应的热化学方程式为
热量。该反应的热化学方程式为(3)科学家用氮气和氢气制备肼,过程如下:

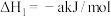

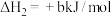
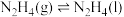
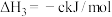
则


 (用含a、b、c的计算式表示)。
(用含a、b、c的计算式表示)。(4)化学反应常伴随热效应。某些反应(如中和反应)的热量变化,其数值Q可通过量热装置测量反应前后体系温度变化,用公式
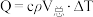 计算获得。
计算获得。①热量的测定:取
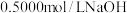 溶液和
溶液和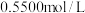 盐酸各
盐酸各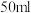 进行反应,测得反应前后体系的温度值(℃)分别为
进行反应,测得反应前后体系的温度值(℃)分别为 、
、 ,则该过程放出的热量为
,则该过程放出的热量为 分别取
分别取 和
和 ,忽略水以外各物质吸收的热量,后同),则该实验测得中和热
,忽略水以外各物质吸收的热量,后同),则该实验测得中和热
 。
。②下列操作会使所测得的焓变
 偏小的是
偏小的是a.用等物质的量浓度的醋酸代替盐酸实验
b.量热装置绝热效果欠佳
c.
 溶液量多了
溶液量多了
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】根据所学知识,完成下列问题。
(1)下列反应中,属于吸热反应的是___________ (填序号)。
a.灼热的炭与CO2反应 b.煅烧石灰石 c.铝与盐酸反应 d.盐酸与氢氧化钠反应
(2)已知CH4、CH3OH(l)的燃烧热分别为890.3kJ/mol,726.5kJ/mol,
①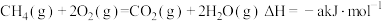 ,则a
,则a___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
②写出表示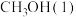 燃烧热的热化学方程式
燃烧热的热化学方程式___________ ;
(3)盐碱地(含较多Na2CO3、NaCl)不利于植物生长,盐碱地呈碱性的原因:___________ (用离子方程式说明);
(4)水溶液是中学化学的重点研究对象、水是极弱的电解质,也是最重要的溶剂。常温下某电解质溶解在水中后,溶液中水电离产生的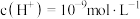 ,则该电解质可能是
,则该电解质可能是___________ (填序号)。
A. B.HCl C.
B.HCl C. D.
D. E.
E.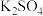
(5)联氨(N2H4)是一种应用广泛的化工原料,可用作火箭燃料。N2H4性质与NH3类似,在水中,N2H4是一种二元弱碱,请写出等物质的量N2H4与硫酸反应生成的盐的化学式为___________ 。
(1)下列反应中,属于吸热反应的是
a.灼热的炭与CO2反应 b.煅烧石灰石 c.铝与盐酸反应 d.盐酸与氢氧化钠反应
(2)已知CH4、CH3OH(l)的燃烧热分别为890.3kJ/mol,726.5kJ/mol,
①
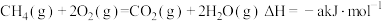 ,则a
,则a (填“>”“<”或“=”)。
(填“>”“<”或“=”)。②写出表示
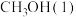 燃烧热的热化学方程式
燃烧热的热化学方程式(3)盐碱地(含较多Na2CO3、NaCl)不利于植物生长,盐碱地呈碱性的原因:
(4)水溶液是中学化学的重点研究对象、水是极弱的电解质,也是最重要的溶剂。常温下某电解质溶解在水中后,溶液中水电离产生的
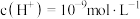 ,则该电解质可能是
,则该电解质可能是A.
 B.HCl C.
B.HCl C. D.
D. E.
E.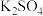
(5)联氨(N2H4)是一种应用广泛的化工原料,可用作火箭燃料。N2H4性质与NH3类似,在水中,N2H4是一种二元弱碱,请写出等物质的量N2H4与硫酸反应生成的盐的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】短周期的元素在自然界中比较常见,尤其是非金属元素及其化合物在社会生活中有着很重要的作用。
(1)红酒中添加一定量的SO2可以防止酒液氧化,这利用了SO2的______ 性。自来水中含硫量约70mg/L,它只能以_____ (填微粒符号)形式存在。
(2)实验室可用浓氨水与氢氧化钠固体作用制取氨气,试用平衡原理分析氢氧化钠的作用:_____ 。
(3)如图是向5mL0.1mol·L-1氨水中逐滴滴加0.1mol·L-1醋酸,测量其导电性的数字化实验曲线图,请你解释曲线变化的原因_____ 。

甲硫醇(CH3SH)是一种重要的有机合成原料,用于合成染料、医药、农药等。工业上可用甲醇和硫化氢气体制取:CH3OH+H2S CH3SH+H2O。
CH3SH+H2O。
完成下列填空:
(4)写出该反应的化学平衡常数表达式_____ 。该反应的温度为280~450℃,选该反应温度可能的原因是:①加快反应速率;②_____ 。
(5)已知在2L密闭容器中,只加入反应物,进行到10分钟时达到平衡,测得水的质量为5.4g,则v(CH3SH)=_____ mol/(L•min)。
(6)常温常压下,2.4g甲硫醇完全燃烧生成二氧化硫和其他稳定产物,并同时放出52.42kJ的热量,则甲硫醇燃烧的热化学方程式为______ 。
(1)红酒中添加一定量的SO2可以防止酒液氧化,这利用了SO2的
(2)实验室可用浓氨水与氢氧化钠固体作用制取氨气,试用平衡原理分析氢氧化钠的作用:
(3)如图是向5mL0.1mol·L-1氨水中逐滴滴加0.1mol·L-1醋酸,测量其导电性的数字化实验曲线图,请你解释曲线变化的原因

甲硫醇(CH3SH)是一种重要的有机合成原料,用于合成染料、医药、农药等。工业上可用甲醇和硫化氢气体制取:CH3OH+H2S
 CH3SH+H2O。
CH3SH+H2O。| 熔点(℃) | 沸点(℃) | |
| 甲醇 | -97 | 64.7 |
| 甲硫醇 | -123 | 7.6 |
完成下列填空:
(4)写出该反应的化学平衡常数表达式
(5)已知在2L密闭容器中,只加入反应物,进行到10分钟时达到平衡,测得水的质量为5.4g,则v(CH3SH)=
(6)常温常压下,2.4g甲硫醇完全燃烧生成二氧化硫和其他稳定产物,并同时放出52.42kJ的热量,则甲硫醇燃烧的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】根据已知条件,写出对应的热化学方程式。
(1)已知100ml lmol/L的氢氧化钠溶液与适量硫酸溶液完全反应放出5.73kJ的热量,请写出表示中和热的热化学方程式______________________________ 。
(2)1mol C2H4(g)与适量O2(g)反应,生成CO2(g)和H2O(l),放出1141kJ热量______________________________ 。
(3)1mol C2H5OH(l)与适量O2(g)反应,生成CO2(g)和H2O(l),放出1366.8kJ热量______________________________ 。
(4)2mol Al(s)与适量O2(g)发生反应,生成Al2O3(s),放出1669.8kJ热量______________________________ 。
(5)已知金刚石的燃烧热△H=-395.0kJ/mol,写出金刚石燃烧的热化学方程式______________________________ 。
(1)已知100ml lmol/L的氢氧化钠溶液与适量硫酸溶液完全反应放出5.73kJ的热量,请写出表示中和热的热化学方程式
(2)1mol C2H4(g)与适量O2(g)反应,生成CO2(g)和H2O(l),放出1141kJ热量
(3)1mol C2H5OH(l)与适量O2(g)反应,生成CO2(g)和H2O(l),放出1366.8kJ热量
(4)2mol Al(s)与适量O2(g)发生反应,生成Al2O3(s),放出1669.8kJ热量
(5)已知金刚石的燃烧热△H=-395.0kJ/mol,写出金刚石燃烧的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】水煤气变换反应是工业上的重要反应,可用于制氢。
水煤气变换反应:H2O(g)+CO(g) CO2(g)+H2(g) ΔH=-41.2kJ·mol-1
CO2(g)+H2(g) ΔH=-41.2kJ·mol-1
该反应分两步完成:
3Fe2O3(s)+CO(g) 2Fe3O4(s)+CO2(g) ΔH1=-47.2kJ·mol-1
2Fe3O4(s)+CO2(g) ΔH1=-47.2kJ·mol-1
2Fe3O4(s)+H2O(g) 3Fe2O3(s)+H2(g) ΔH2
3Fe2O3(s)+H2(g) ΔH2
ΔH2=_____ kJ·mol-1.
水煤气变换反应:H2O(g)+CO(g)
 CO2(g)+H2(g) ΔH=-41.2kJ·mol-1
CO2(g)+H2(g) ΔH=-41.2kJ·mol-1该反应分两步完成:
3Fe2O3(s)+CO(g)
 2Fe3O4(s)+CO2(g) ΔH1=-47.2kJ·mol-1
2Fe3O4(s)+CO2(g) ΔH1=-47.2kJ·mol-12Fe3O4(s)+H2O(g)
 3Fe2O3(s)+H2(g) ΔH2
3Fe2O3(s)+H2(g) ΔH2ΔH2=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
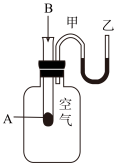
(1)为了研究化学反应A+B=C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。试回答下列问题:
①该反应为____ 反应(填“放热”或“吸热”)。
②A和B的总能量比C和D的总能量____ (填“高”或“低”)。
③反应物化学键断裂吸收的能量____ (填“大”或“小”)于生成物化学键形成放出的能量。
(2)已知拆开1molH-H键、1molN-H键、1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为____ 。
(3)向1L1mol/L的NaOH溶液中加入下列物质:①浓H2SO4;②稀硝酸;③稀醋酸,恰好完全反应的热效应为△H1、△H2、△H3,则三者由小到大顺序为____ 。
(4)丙烷燃烧可以通过以下两种途径:
途径I:C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ΔH=-akJ/mol
途径II:C3H8(g)=C3H6(g)+H2(g) ΔH=+bkJ/mol
2C3H6(g)+9O2(g)=6CO2(g)+6H2O(l) ΔH=-ckJ/mol
2H2(g)+O2(g)=2H2O(l) ΔH=-dkJ/mol(a、b、c、d均为正值)
判断等量的丙烷通过两种途径放出的热量,途径I放出的热量____ (填“大于”、“等于”或“小于”)途径II放出的热量。
(1)为了研究化学反应A+B=C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。试回答下列问题:

①该反应为
②A和B的总能量比C和D的总能量
③反应物化学键断裂吸收的能量
(2)已知拆开1molH-H键、1molN-H键、1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为
(3)向1L1mol/L的NaOH溶液中加入下列物质:①浓H2SO4;②稀硝酸;③稀醋酸,恰好完全反应的热效应为△H1、△H2、△H3,则三者由小到大顺序为
(4)丙烷燃烧可以通过以下两种途径:
途径I:C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ΔH=-akJ/mol
途径II:C3H8(g)=C3H6(g)+H2(g) ΔH=+bkJ/mol
2C3H6(g)+9O2(g)=6CO2(g)+6H2O(l) ΔH=-ckJ/mol
2H2(g)+O2(g)=2H2O(l) ΔH=-dkJ/mol(a、b、c、d均为正值)
判断等量的丙烷通过两种途径放出的热量,途径I放出的热量
您最近一年使用:0次
【推荐3】已知氢气的燃烧热为285 kJ·mol−1,氨气在氧气中燃烧的热化学方程式为:4NH3(g) + 3O2(g)  2N2(g) + 6H2O(l) ΔH = -1526 kJ·mol−1
2N2(g) + 6H2O(l) ΔH = -1526 kJ·mol−1
回答下列问题:
(1)写出表示氢气燃烧热的热化学方程式_______ ,氢气作为未来理想燃料的优点是_______ 。
(2)根据上述信息可知:N2(g) + 3H2(g) 2NH3(g) ΔH =
2NH3(g) ΔH =_______ ,若H-H的键能为436 kJ·mol−1,N-H的键能为400 kJ·mol−1,则N≡N的键能为_______ kJ·mol−1。
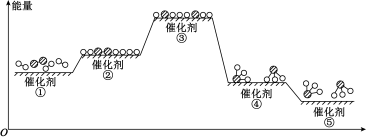
(3)工业上,合成氨反应在催化剂表面的变化如图所示,下列说法错误的是_______(填标号)。
 2N2(g) + 6H2O(l) ΔH = -1526 kJ·mol−1
2N2(g) + 6H2O(l) ΔH = -1526 kJ·mol−1回答下列问题:
(1)写出表示氢气燃烧热的热化学方程式
(2)根据上述信息可知:N2(g) + 3H2(g)
 2NH3(g) ΔH =
2NH3(g) ΔH =(3)工业上,合成氨反应在催化剂表面的变化如图所示,下列说法错误的是_______(填标号)。

| A.①→②表示催化剂的吸附过程,该过程吸收能量 |
| B.②→③→④的过程中有非极性键的断裂和形成 |
| C.合成氨反应正反应的活化能小于逆反应的活化能 |
| D.过程⑤中有化学键的断裂 |
您最近一年使用:0次



