运动会中的火炬一般采用丙烷(C3H8)为燃料。丙烷热值较高,污染较小,是一种优良的燃料。试回答下列问题:

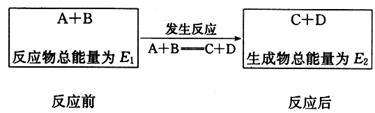
(1)如图是一定量丙烷完全燃烧生成CO2和1 mol H2O(l)过程中的能量变化图,请在图中的括号内填入“+”或“-”______ 。
(2)写出表示丙烷标准燃烧热的热化学方程式:___________ 。

(1)如图是一定量丙烷完全燃烧生成CO2和1 mol H2O(l)过程中的能量变化图,请在图中的括号内填入“+”或“-”
(2)写出表示丙烷标准燃烧热的热化学方程式:
更新时间:2021-05-25 14:33:51
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】写出下列反应的热化学方程式:1mol液态肼(N2H4)在氧气中充分燃烧,生成N2(g)和液态水,放出622KJ的热量。___
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】填空
(1)写出漂白粉有效成分的化学式_____ 。
(2)写出1,2-二溴乙烷的结构简式_____ 。
(3)任写一个能得到SO2的化学反应方程式_____ 。
(4)已知25℃和101KPa时,液态甲醇(CH₃OH)的燃烧热/ 请写出表示甲醇燃烧热的热化学方程式
请写出表示甲醇燃烧热的热化学方程式_____ 。
(5)根据甲醇在酸性电解质中与氧气作用生成二氧化碳和水的反应,设计一种燃料电池。该燃料电池工作时,负极的电极反应式是_____ 。
(6)以丙烯为原料来生产聚丙烯,请写出该反应的化学方程式为_____ 。
(7)SOCl2是一种液态化合物。向盛有10ml水的锥形瓶中,小心滴加8~10滴SOCl2,可观察到剧烈反应,液面上有白雾形成,并有带刺激性气味的气体逸出。请写出SOCl2与水反应的化学方程式:_____ 。
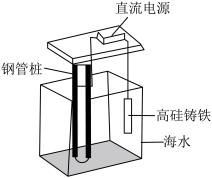
(8)海港、码头的钢管桩会受到海水的长期侵蚀,常用外加电流法对其进行保护,工作原理如图所示。钢管桩上主要发生的电极反应式为:_____ (假设海水为氯化钠溶液,下同)。也可以在钢管桩上焊接锌块进行保护,钢管桩中的铁上主要发生的电极反应式为:_____
(1)写出漂白粉有效成分的化学式
(2)写出1,2-二溴乙烷的结构简式
(3)任写一个能得到SO2的化学反应方程式
(4)已知25℃和101KPa时,液态甲醇(CH₃OH)的燃烧热/
 请写出表示甲醇燃烧热的热化学方程式
请写出表示甲醇燃烧热的热化学方程式(5)根据甲醇在酸性电解质中与氧气作用生成二氧化碳和水的反应,设计一种燃料电池。该燃料电池工作时,负极的电极反应式是
(6)以丙烯为原料来生产聚丙烯,请写出该反应的化学方程式为
(7)SOCl2是一种液态化合物。向盛有10ml水的锥形瓶中,小心滴加8~10滴SOCl2,可观察到剧烈反应,液面上有白雾形成,并有带刺激性气味的气体逸出。请写出SOCl2与水反应的化学方程式:
(8)海港、码头的钢管桩会受到海水的长期侵蚀,常用外加电流法对其进行保护,工作原理如图所示。钢管桩上主要发生的电极反应式为:

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】依据事实,写出下列反应的热化学方程式。
(1)在101 kPa时,H2在1.00 mol O2中完全燃烧生成2.00 mol液态H2O,放出571.6 kJ的热量,表示H2燃烧热的热化学方程式为___________________ 。
(2)卫星发射时可用肼(N2H4)为燃料,3.2 g N2H4(气态)在O2(气态)中燃烧,生成N2(气态)和H2O(气态),放出53.4 kJ的热量___________________ 。
(3)已知CO(g)和CH3OH(l)的燃烧热ΔH分别为-283.0kJ·mol-1和-726.5kJ·mol-1。写出CH3OH(l)不完全燃烧生成CO和液态水的热化学方程式___________________ 。
(4)已知稀溶液中,1mol H2SO4与NaOH溶液恰好完全反应时,放出114.6kJ的热量,表示其中和热的热化学方程式___________________ 。
(5)已知:C(s)+O2(g)=CO2(g) ΔH=-437.3 kJ·mol-1
H2(g)+ O2(g)=H2O(g) ΔH=-285.8 kJ·mol-1
O2(g)=H2O(g) ΔH=-285.8 kJ·mol-1
CO(g)+ O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
则碳和水蒸气反应生成一氧化碳和氢气)的热化学方程式是___________________ 。
(6)NaBH4(s)与H2O(l)反应生成NaBO2(s)和H2(g)。在25 ℃、101 kPa下,已知每消耗3.8 g NaBH4(s)放热21.6 kJ,该反应的热化学方程式是___________________ 。
(1)在101 kPa时,H2在1.00 mol O2中完全燃烧生成2.00 mol液态H2O,放出571.6 kJ的热量,表示H2燃烧热的热化学方程式为
(2)卫星发射时可用肼(N2H4)为燃料,3.2 g N2H4(气态)在O2(气态)中燃烧,生成N2(气态)和H2O(气态),放出53.4 kJ的热量
(3)已知CO(g)和CH3OH(l)的燃烧热ΔH分别为-283.0kJ·mol-1和-726.5kJ·mol-1。写出CH3OH(l)不完全燃烧生成CO和液态水的热化学方程式
(4)已知稀溶液中,1mol H2SO4与NaOH溶液恰好完全反应时,放出114.6kJ的热量,表示其中和热的热化学方程式
(5)已知:C(s)+O2(g)=CO2(g) ΔH=-437.3 kJ·mol-1
H2(g)+
 O2(g)=H2O(g) ΔH=-285.8 kJ·mol-1
O2(g)=H2O(g) ΔH=-285.8 kJ·mol-1CO(g)+
 O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1则碳和水蒸气反应生成一氧化碳和氢气)的热化学方程式是
(6)NaBH4(s)与H2O(l)反应生成NaBO2(s)和H2(g)。在25 ℃、101 kPa下,已知每消耗3.8 g NaBH4(s)放热21.6 kJ,该反应的热化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氢能是一种极具发展潜力的清洁能源。3月29日,长城汽车氢能战略全球发布会推出氢能技术,并计划今年推出全球首款C级氢燃料电池SUV。关于氢能,根据要求回答问题:
I.制备氢气
制备氢气常采用以下方法:①电解水法:2H2O 2H2↑+O2↑
2H2↑+O2↑
②水煤气法:C+H2O(g) CO+H2,CO+H2O
CO+H2,CO+H2O CO2+H2
CO2+H2
③太阳能光催化分解水法:2H2O 2H2↑+O2↑
2H2↑+O2↑
(1)三种方法中最节能的是____ (填标号)。
(2)已知拆开1molH-H、1molO=O和1molH-O分别需要的能量依次为436kJ、498kJ、和463kJ,则理论上每3.6gH2O(g)完全分解,需____ (填“放出”或“吸收”)能量___ kJ。下列能正确表示该过程的能量变化示意图的是____ (填标号)。
A. B.
B. C.
C. D.
D.
II.氢燃料电池
(3)氢燃料电池具有清洁高效等优点,其简易装置如图所示。该电池正极反应式为____ ;在标准状况下,当有1mol电子通过外电路时,消耗氢气的体积至少为:____ 。

I.制备氢气
制备氢气常采用以下方法:①电解水法:2H2O
 2H2↑+O2↑
2H2↑+O2↑②水煤气法:C+H2O(g)
 CO+H2,CO+H2O
CO+H2,CO+H2O CO2+H2
CO2+H2③太阳能光催化分解水法:2H2O
 2H2↑+O2↑
2H2↑+O2↑(1)三种方法中最节能的是
(2)已知拆开1molH-H、1molO=O和1molH-O分别需要的能量依次为436kJ、498kJ、和463kJ,则理论上每3.6gH2O(g)完全分解,需
A.
 B.
B. C.
C. D.
D.
II.氢燃料电池
(3)氢燃料电池具有清洁高效等优点,其简易装置如图所示。该电池正极反应式为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)已知充分燃烧a g乙炔(C2H2)气体时生成1 mol二氧化碳气体和液态水,并放出热量b kJ,表示乙炔燃烧热的热化学方程式为______ 。
(2)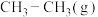 →
→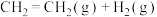
 ,有关化学键的键能如下表:
,有关化学键的键能如下表:
则该反应的反应热
_____ 。
(3)碳(s)在氧气供应不充足时,生成CO同时还部分生成 。因此无法通过实验直接测得反应:
。因此无法通过实验直接测得反应: 的
的 。但可设计实验利用盖斯定律计算出该反应的
。但可设计实验利用盖斯定律计算出该反应的 ,计算时需要测得的实验数据有
,计算时需要测得的实验数据有______ 。
(4)硝酸厂的尾气直接排放将污染空气,目前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为
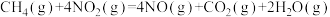
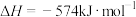
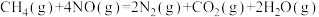
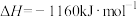
则甲烷直接将NO2还原为N2的热化学方程式为_____ 。
(5)CO、H2可用于合成甲醇和甲醚其反应为(m、n均大于0):
反应①:
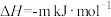
反应②:
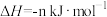
反应③: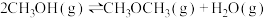
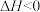
则m与n的关系为______ 。
(1)已知充分燃烧a g乙炔(C2H2)气体时生成1 mol二氧化碳气体和液态水,并放出热量b kJ,表示乙炔燃烧热的热化学方程式为
(2)
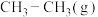 →
→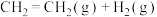
 ,有关化学键的键能如下表:
,有关化学键的键能如下表:| 化学键 |  |  |  |  |
键能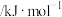 | 414 | 615 | 347 | 435 |
则该反应的反应热

(3)碳(s)在氧气供应不充足时,生成CO同时还部分生成
 。因此无法通过实验直接测得反应:
。因此无法通过实验直接测得反应: 的
的 。但可设计实验利用盖斯定律计算出该反应的
。但可设计实验利用盖斯定律计算出该反应的 ,计算时需要测得的实验数据有
,计算时需要测得的实验数据有(4)硝酸厂的尾气直接排放将污染空气,目前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为
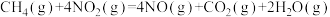
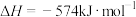
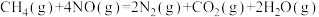
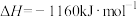
则甲烷直接将NO2还原为N2的热化学方程式为
(5)CO、H2可用于合成甲醇和甲醚其反应为(m、n均大于0):
反应①:

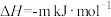
反应②:

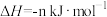
反应③:
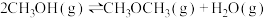
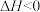
则m与n的关系为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】依据事实,回答下列问题。
(1)在25℃、101kPa时,1.0gC8H18(l,辛烷)燃烧生成CO2(g)和H2O(l),放出48.40kJ的热量,则C8H18(l)的燃烧热为___ kJ/mol。
(2)已知N2(g)+2O2(g)=2NO2(g);ΔH=+67.7kJ/mol,N2H4(g)+O2(g)=N2(g)+2H2O(g);ΔH=-534kJ/mol,根据盖斯定律写出肼(N2H4)与NO2完全反应生成氮气和气态水的热化学方程式____ 。
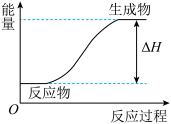
(3)某反应过程中的能量变化如图所示,则该反应是____ (填“放热”或“吸热”)反应,判断依据是____ 。
(4)已知:2NH3(g)+3Cl2(g)=N2(g)+6HCl(g) ΔH=–462kJ•mol-1
 ,
,
则断开1molH–N键与断开1molH–Cl键所需能量相差约为_____ kJ。
(1)在25℃、101kPa时,1.0gC8H18(l,辛烷)燃烧生成CO2(g)和H2O(l),放出48.40kJ的热量,则C8H18(l)的燃烧热为
(2)已知N2(g)+2O2(g)=2NO2(g);ΔH=+67.7kJ/mol,N2H4(g)+O2(g)=N2(g)+2H2O(g);ΔH=-534kJ/mol,根据盖斯定律写出肼(N2H4)与NO2完全反应生成氮气和气态水的热化学方程式
(3)某反应过程中的能量变化如图所示,则该反应是

(4)已知:2NH3(g)+3Cl2(g)=N2(g)+6HCl(g) ΔH=–462kJ•mol-1
 ,
,
则断开1molH–N键与断开1molH–Cl键所需能量相差约为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】乙烯是重要的有机化学原料,工业上可利用乙烷脱氢制备乙烯。
(1)乙烷裂解为乙烯为自由基反应,其可能的引发反应及对应化学键的解离能如下:
根据表格信息,乙烷裂解引发的反应主要为___________ 。
(2)经过引发的后续反应历程为(已略去链终止过程):
……
 ΔH1
ΔH1
 ΔH2
ΔH2
①C2H4(g)+H2(g)→C2H6(g)的ΔH=___________ (用含ΔH1和ΔH2的式子表示)。
②上述历程中“……”所代表的反应为___________ 。
(3)①丙烯与HCl发生加成反应,生成CH3CHClCH3和CH3CH2CH2Cl两种产物,其能量与反应历程如图所示,其中正确的说法是___________ 。

A.若反应的时间足够长,产物应该以CH3CH2CH2Cl为主
B.合成CH3CHClCH3的反应中,第I步反应为整个反应的决速步骤
C.总反应CH2=CHCH3(g)+HCl(g)=CH3CH2CH2Cl(g)的ΔH=ΔE3—ΔE4
②工业生产中,保持其他条件不变,若要提高产物中CH3CH2CH2Cl的比例,可采用的措施有___________ 、___________ 。
(1)乙烷裂解为乙烯为自由基反应,其可能的引发反应及对应化学键的解离能如下:
| 可能的引发反应 | 有关键的解离能(kJ/mol) |
| C2H6(g)→C2H5·(g)+H·(g) | 410 |
| C2H6(g)→2CH3·(g) | 368 |
根据表格信息,乙烷裂解引发的反应主要为
(2)经过引发的后续反应历程为(已略去链终止过程):
……
 ΔH1
ΔH1 ΔH2
ΔH2①C2H4(g)+H2(g)→C2H6(g)的ΔH=
②上述历程中“……”所代表的反应为
(3)①丙烯与HCl发生加成反应,生成CH3CHClCH3和CH3CH2CH2Cl两种产物,其能量与反应历程如图所示,其中正确的说法是

A.若反应的时间足够长,产物应该以CH3CH2CH2Cl为主
B.合成CH3CHClCH3的反应中,第I步反应为整个反应的决速步骤
C.总反应CH2=CHCH3(g)+HCl(g)=CH3CH2CH2Cl(g)的ΔH=ΔE3—ΔE4
②工业生产中,保持其他条件不变,若要提高产物中CH3CH2CH2Cl的比例,可采用的措施有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】断开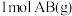 分子中的化学键使其分别生成气态A原子和气态B原子所吸收的能量称为
分子中的化学键使其分别生成气态A原子和气态B原子所吸收的能量称为 键的键能。下表列出了一些化学键的键能E:
键的键能。下表列出了一些化学键的键能E:
请回答下列问题:
(1)如图表示某反应的能量变化关系,则此反应为_____________ (填“吸热”或“放热”)反应,其中
_____________ (用含有a、b的关系式表示)。
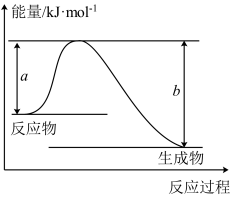
(2)若图示中表示反应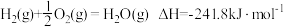 ,
,
①则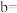
_____________  ,x=
,x=_____________ .
②此热化学方程式的意义是__________________________ 。
③画出此热化学方程式对应的焓变示意图______________ 。

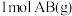 分子中的化学键使其分别生成气态A原子和气态B原子所吸收的能量称为
分子中的化学键使其分别生成气态A原子和气态B原子所吸收的能量称为 键的键能。下表列出了一些化学键的键能E:
键的键能。下表列出了一些化学键的键能E:化学键 |
|
|
|
|
|
|
|
| 436 | 247 | x | 330 | 413 | 463 | 431 |
请回答下列问题:
(1)如图表示某反应的能量变化关系,则此反应为


(2)若图示中表示反应
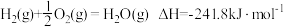 ,
,①则
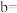
 ,x=
,x=②此热化学方程式的意义是
③画出此热化学方程式对应的焓变示意图

您最近一年使用:0次


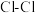

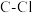



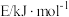
 C+D的说法正确的是
C+D的说法正确的是

