写出下列反应的热化学方程式:1mol液态肼(N2H4)在氧气中充分燃烧,生成N2(g)和液态水,放出622KJ的热量。___
更新时间:2019-11-27 19:14:17
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1)在25℃、1.01×105Pa时,16g S粉在足量的氧气中充分燃烧生成二氧化硫气体,放出148.5kJ的热量,则S的燃烧热的热化学方程式为:___ 。
(2)1L1mol/L稀盐酸跟1L1mol/LNaOH溶液起中和反应放出57.3kJ热量,其热化学方程式为:___ 。
(3)已知如图所示的可逆反应:
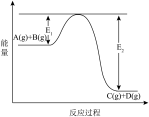
①A(g)+B(g) 2C(g) +D(g);ΔH=QkJ/mol则Q
2C(g) +D(g);ΔH=QkJ/mol则Q___ 0(填“>”、“<”或“=”)
②反应体系中加入催化剂,反应速率增大,则E1的变化是:E1___ ,ΔH的变化是:ΔH___ (填“增大”“减小”“不变”)。
(4)发射卫星用N2H4作燃料,NO2作氧化剂,两者反应生成N2和水蒸气,
已知:N2(g)+2O2(g)=2NO2(g) △H1=+67.7kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H2=-534kJ/mol
则1mol气体肼和NO2完全反应时的反应热△H=___ kJ/mol。
(5)已知反应A放出热量Q1kJ,焓变为△H1,反应B放出热量Q2kJ,焓变为△H2,若Q1>Q2,则△H1___ △H2
(6)1molC与1molH2O(g)反应生成1molCO(g)和1molH2(g),需吸收131.5kJ的热量,该反应的反应热为△H=___ kJ/mol;
(7)反应A+3B=2C+2D在四种不同情况下的反应速率分别为:
①v(A)=0.15mol/(L・s) ②v(B)=0.6mol/(L・s)
③v(C)=0.4mol/(L・s) ④v(D)=0.45mol(L・s)
则该反应进行最快的为___ (填序号)
(2)1L1mol/L稀盐酸跟1L1mol/LNaOH溶液起中和反应放出57.3kJ热量,其热化学方程式为:
(3)已知如图所示的可逆反应:

①A(g)+B(g)
 2C(g) +D(g);ΔH=QkJ/mol则Q
2C(g) +D(g);ΔH=QkJ/mol则Q②反应体系中加入催化剂,反应速率增大,则E1的变化是:E1
(4)发射卫星用N2H4作燃料,NO2作氧化剂,两者反应生成N2和水蒸气,
已知:N2(g)+2O2(g)=2NO2(g) △H1=+67.7kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H2=-534kJ/mol
则1mol气体肼和NO2完全反应时的反应热△H=
(5)已知反应A放出热量Q1kJ,焓变为△H1,反应B放出热量Q2kJ,焓变为△H2,若Q1>Q2,则△H1
(6)1molC与1molH2O(g)反应生成1molCO(g)和1molH2(g),需吸收131.5kJ的热量,该反应的反应热为△H=
(7)反应A+3B=2C+2D在四种不同情况下的反应速率分别为:
①v(A)=0.15mol/(L・s) ②v(B)=0.6mol/(L・s)
③v(C)=0.4mol/(L・s) ④v(D)=0.45mol(L・s)
则该反应进行最快的为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题
(1)已知热化学方程式:SO2(g)+ O2(g)
O2(g) SO3(g)ΔH=-98.32kJ·mol-1,在容器中充入2molSO2和1molO2充分反应,最终放出的热量可能为___________。
SO3(g)ΔH=-98.32kJ·mol-1,在容器中充入2molSO2和1molO2充分反应,最终放出的热量可能为___________。
(2)已知H2(g)+Br2(l)=2HBr(g) ΔH=-72kJ·mol-1,蒸发1molBr2(l)需要吸收的能量为30kJ,其他相关数据如下表:
则表中a=___________ 。
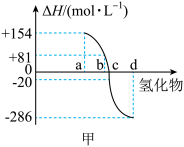
(3)热力学标准态(298.15K、101kPa)下,由稳定单质发生反应生成1mol化合物的反应热叫作该化合物的生成热(ΔH)。图甲为氧族元素中的氧、硫、硒(Se)、碲在生成1mol气态氢化物时的焓变数据,根据焓变数据可确定a、b、c、d分别代表那种元素,试写出硒化氢在上述条件下发生分解反应的热化学方程式为___________ 。
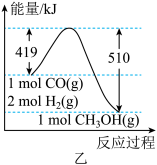
(4)图乙表示CO和H2反应生成CH3OH过程中能量变化示意图,请写出CO和H2反应的热化学方程式:___________ 。
(5)采用真空封管法制备磷化硼纳米颗粒,在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示。
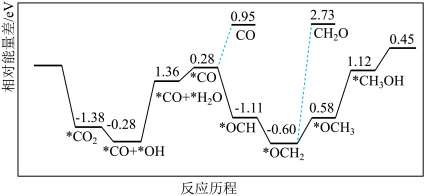
容易得到的副产物有CO和CH2O,其中相对较多的副产物为___________ ;上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中___________ (填字母)的能量变化。
A.*CO+*OH→*CO+*H2O
B.*CO→*OCH
C.*OCH2→*OCH3
D.*OCH3→*CH3OH
(1)已知热化学方程式:SO2(g)+
 O2(g)
O2(g) SO3(g)ΔH=-98.32kJ·mol-1,在容器中充入2molSO2和1molO2充分反应,最终放出的热量可能为___________。
SO3(g)ΔH=-98.32kJ·mol-1,在容器中充入2molSO2和1molO2充分反应,最终放出的热量可能为___________。| A.等于196.64kJ | B.小于98.32kJ | C.小于196.64kJ | D.大于196.64kJ |
| 物质 | H2(g) | Br2(g) | HBr(g) |
| 1mol分子中的化学键断裂时需要吸收的能量/kJ | 436 | 200 | a |
(3)热力学标准态(298.15K、101kPa)下,由稳定单质发生反应生成1mol化合物的反应热叫作该化合物的生成热(ΔH)。图甲为氧族元素中的氧、硫、硒(Se)、碲在生成1mol气态氢化物时的焓变数据,根据焓变数据可确定a、b、c、d分别代表那种元素,试写出硒化氢在上述条件下发生分解反应的热化学方程式为

(4)图乙表示CO和H2反应生成CH3OH过程中能量变化示意图,请写出CO和H2反应的热化学方程式:

(5)采用真空封管法制备磷化硼纳米颗粒,在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示。

容易得到的副产物有CO和CH2O,其中相对较多的副产物为
A.*CO+*OH→*CO+*H2O
B.*CO→*OCH
C.*OCH2→*OCH3
D.*OCH3→*CH3OH
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
(1)如图是N2(g)和H2(g)反应生成1 mol NH3(g)过程中能量的变化示意图,请写出N2和H2反应的热化学方程式:_______ 。
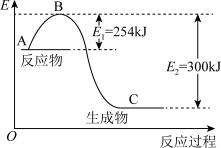
(2)若已知下列数据:
试根据表中及图中数据计算N—H的键能:___ kJ·mol-1。
(3)捕碳技术(主要指捕获CO2在降低温室气体排放中具有重要的作用。目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下反应:
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)=(NH4)2CO3(aq) ΔH1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g)=NH4HCO3(aq) ΔH2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)=2NH4HCO3(aq) ΔH3
请回答下列问题:
ΔH3与ΔH1、ΔH2之间的关系是ΔH3=___ 。
(4)试比较下列两组△H的大小(填“>”、“<”或“=”)
①H2(g)+ O2(g)=H2O(g) △H1 H2(g)+
O2(g)=H2O(g) △H1 H2(g)+ O2(g)=H2O(l) △H2
O2(g)=H2O(l) △H2
则△H1____ △H2
②S(s)+O2(g)=SO2(g) △H3
Ba(OH)2·8H2O(s)+2NH4Cl(s)=BaCl2(s)+10H2O(l)+2NH3(g) △H4
则△H3______ △H4
(1)如图是N2(g)和H2(g)反应生成1 mol NH3(g)过程中能量的变化示意图,请写出N2和H2反应的热化学方程式:

(2)若已知下列数据:
| 化学键 | H—H | N≡N |
| 键能/kJ·mol-1 | 435 | 943 |
试根据表中及图中数据计算N—H的键能:
(3)捕碳技术(主要指捕获CO2在降低温室气体排放中具有重要的作用。目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下反应:
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)=(NH4)2CO3(aq) ΔH1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g)=NH4HCO3(aq) ΔH2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)=2NH4HCO3(aq) ΔH3
请回答下列问题:
ΔH3与ΔH1、ΔH2之间的关系是ΔH3=
(4)试比较下列两组△H的大小(填“>”、“<”或“=”)
①H2(g)+
 O2(g)=H2O(g) △H1 H2(g)+
O2(g)=H2O(g) △H1 H2(g)+ O2(g)=H2O(l) △H2
O2(g)=H2O(l) △H2则△H1
②S(s)+O2(g)=SO2(g) △H3
Ba(OH)2·8H2O(s)+2NH4Cl(s)=BaCl2(s)+10H2O(l)+2NH3(g) △H4
则△H3
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】化学反应中伴随能量变化,研究化学反应中的能量变化,可以帮助我们深刻地认识化学反应,更好地为生产和生活服务,请根据所学知识回答下面问题:
(1)化学反应中断裂化学键需要___________ 能量(填“吸收”或“释放”,下同),形成化学键需要___________ 能量。
(2)①铝片与稀盐酸的反应;② 晶体与
晶体与 晶体的反应;③碳酸钙分解;④过氧化钠和二氧化碳反应;⑤
晶体的反应;③碳酸钙分解;④过氧化钠和二氧化碳反应;⑤ ;⑥碘升华。属于吸热反应的是
;⑥碘升华。属于吸热反应的是___________ (填序号),属于放热反应的是___________ (填序号)。
(3)反应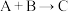 (放热)分两步进行①
(放热)分两步进行①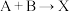 (吸热);②
(吸热);② (放热)。下列示意图中,能正确表示总反应过程中能量变化的是___________(填字母)。
(放热)。下列示意图中,能正确表示总反应过程中能量变化的是___________(填字母)。
(4)下列反应通过原电池装置,可实现化学能直接转化为电能的是___________ (填序号)。
①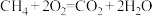
②
③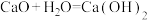
(5) 是一种优良的绝缘气体,分子结构中只存在
是一种优良的绝缘气体,分子结构中只存在 键。已知:
键。已知: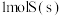 转化为气态硫原子吸收能量280kJ,断裂
转化为气态硫原子吸收能量280kJ,断裂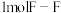 ,
, 键需要吸收的能量分别为160kJ、330kJ。则
键需要吸收的能量分别为160kJ、330kJ。则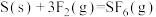 的反应热
的反应热 为
为___________ 。
(6)实验测得:101kPa时, 完全燃烧生成液态水和
完全燃烧生成液态水和 气体,放出890.3kJ的热量。写出该反应的热化学方程式:
气体,放出890.3kJ的热量。写出该反应的热化学方程式:___________ 。
(1)化学反应中断裂化学键需要
(2)①铝片与稀盐酸的反应;②
 晶体与
晶体与 晶体的反应;③碳酸钙分解;④过氧化钠和二氧化碳反应;⑤
晶体的反应;③碳酸钙分解;④过氧化钠和二氧化碳反应;⑤ ;⑥碘升华。属于吸热反应的是
;⑥碘升华。属于吸热反应的是(3)反应
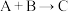 (放热)分两步进行①
(放热)分两步进行①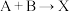 (吸热);②
(吸热);② (放热)。下列示意图中,能正确表示总反应过程中能量变化的是___________(填字母)。
(放热)。下列示意图中,能正确表示总反应过程中能量变化的是___________(填字母)。A.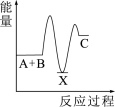 | B.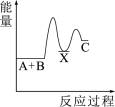 |
C.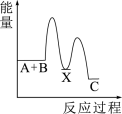 | D.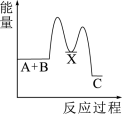 |
(4)下列反应通过原电池装置,可实现化学能直接转化为电能的是
①
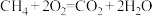
②

③
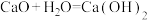
(5)
 是一种优良的绝缘气体,分子结构中只存在
是一种优良的绝缘气体,分子结构中只存在 键。已知:
键。已知: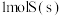 转化为气态硫原子吸收能量280kJ,断裂
转化为气态硫原子吸收能量280kJ,断裂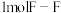 ,
, 键需要吸收的能量分别为160kJ、330kJ。则
键需要吸收的能量分别为160kJ、330kJ。则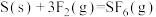 的反应热
的反应热 为
为(6)实验测得:101kPa时,
 完全燃烧生成液态水和
完全燃烧生成液态水和 气体,放出890.3kJ的热量。写出该反应的热化学方程式:
气体,放出890.3kJ的热量。写出该反应的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
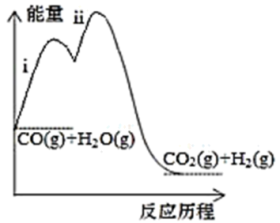
【推荐2】水煤气变换[CO(g)+H2O(g)⇌CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域。反应历程如图所示。
已知:①H2(g)+ O2=H2O(g) △H =-241.8kJ/mol
O2=H2O(g) △H =-241.8kJ/mol
②CO(g)+ O2(g)=CO2(g) △H =-283.0kJ/mol
O2(g)=CO2(g) △H =-283.0kJ/mol
回答下列问题:
(1)该反应是______ (填“吸热”或“放热”) 反应,反应的△H = ______ kJ/mol。
(2)若加入催化剂,下列说法正确的是______ 。
a.降低了反应的ΔH b.反应i和ⅱ活化能都有可能降低
c.反应速率加快 d.反应物转化率会升高
(3)天然气是重要的化石燃料,主要成分是甲烷。在25℃、101kPa时,甲烷燃烧生成气态水放出的热量为890.31kJ/mol,请写出该条件下甲烷燃烧的热化学方程式:______ 。

已知:①H2(g)+
 O2=H2O(g) △H =-241.8kJ/mol
O2=H2O(g) △H =-241.8kJ/mol②CO(g)+
 O2(g)=CO2(g) △H =-283.0kJ/mol
O2(g)=CO2(g) △H =-283.0kJ/mol回答下列问题:
(1)该反应是
(2)若加入催化剂,下列说法正确的是
a.降低了反应的ΔH b.反应i和ⅱ活化能都有可能降低
c.反应速率加快 d.反应物转化率会升高
(3)天然气是重要的化石燃料,主要成分是甲烷。在25℃、101kPa时,甲烷燃烧生成气态水放出的热量为890.31kJ/mol,请写出该条件下甲烷燃烧的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)化学反应中伴随着能量变化。下列属于吸热反应的是___________ (填序号)。
a.燃烧Co b. 晶体和
晶体和 晶体反应 c.铝和稀盐酸反应
晶体反应 c.铝和稀盐酸反应
d.NaOH溶液和稀盐酸反应 e.液态水变为水蒸气 f.水蒸气冷凝为液态水 g.碳酸氢钠与稀硫酸反应
(2)已知拆开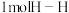 键、
键、 键、
键、 键分别需要的能量是436KJ、391KJ、946KJ,则
键分别需要的能量是436KJ、391KJ、946KJ,则 与
与 反应生成
反应生成 的热化学方程式为
的热化学方程式为___________ 。
(3)向1L1mol/L的NaOH溶液中加入下列物质:①浓 ;②稀硝酸;③稀醋酸,恰好完全反应的热效应为
;②稀硝酸;③稀醋酸,恰好完全反应的热效应为 、
、 、
、 ,则三者由小到大顺序为
,则三者由小到大顺序为___________ 。
(4)t℃时,关于 、
、 的两个反应的信息如下表所示:
的两个反应的信息如下表所示:
请写出t℃时 被NO氧化生成无毒气体的热化学方程式
被NO氧化生成无毒气体的热化学方程式___________ (反应热用a、b、c、d代数式表示)。t℃该反应的平衡常数为_________ (用 和
和 表示)。
表示)。
(1)化学反应中伴随着能量变化。下列属于吸热反应的是
a.燃烧Co b.
 晶体和
晶体和 晶体反应 c.铝和稀盐酸反应
晶体反应 c.铝和稀盐酸反应d.NaOH溶液和稀盐酸反应 e.液态水变为水蒸气 f.水蒸气冷凝为液态水 g.碳酸氢钠与稀硫酸反应
(2)已知拆开
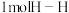 键、
键、 键、
键、 键分别需要的能量是436KJ、391KJ、946KJ,则
键分别需要的能量是436KJ、391KJ、946KJ,则 与
与 反应生成
反应生成 的热化学方程式为
的热化学方程式为(3)向1L1mol/L的NaOH溶液中加入下列物质:①浓
 ;②稀硝酸;③稀醋酸,恰好完全反应的热效应为
;②稀硝酸;③稀醋酸,恰好完全反应的热效应为 、
、 、
、 ,则三者由小到大顺序为
,则三者由小到大顺序为(4)t℃时,关于
 、
、 的两个反应的信息如下表所示:
的两个反应的信息如下表所示:| 化学反应 | 正反应活化能 | 逆反应活化能 | t℃时平衡常数 |
  |  |  |  |
 | 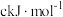 |  |  |
请写出t℃时
 被NO氧化生成无毒气体的热化学方程式
被NO氧化生成无毒气体的热化学方程式 和
和 表示)。
表示)。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】简答题,依据事实,写出下列反应的热化学方程式。
(1)1molN2(g)与适量H2(g)反应生成NH3(g)放出92.4kJ热量,写出该反应的热化学方程式:_______________________
(2)1molC(s)与适量H2O(g)反应生成CO(g)和H2(g),吸收131.5kJ热量,写出该反应的热化学方程式:____________________
(3)常温常压下,乙烯(C2H4)燃烧热△H=—1411.0kJ·mol-1,则表示乙烯燃烧热的热化学方程式_______________
(4)常温常压下,乙醇【C2H5OH】(l)的燃烧热△H=—1366.8kJ·mol-1,则表示乙醇燃烧热的热化学方程式____________________
(5)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成固体SiO2和液态H2O。已知室温下,2gSiH4自燃放出89.2kJ热量,写出该反应的热化学方程式______________________
(1)1molN2(g)与适量H2(g)反应生成NH3(g)放出92.4kJ热量,写出该反应的热化学方程式:
(2)1molC(s)与适量H2O(g)反应生成CO(g)和H2(g),吸收131.5kJ热量,写出该反应的热化学方程式:
(3)常温常压下,乙烯(C2H4)燃烧热△H=—1411.0kJ·mol-1,则表示乙烯燃烧热的热化学方程式
(4)常温常压下,乙醇【C2H5OH】(l)的燃烧热△H=—1366.8kJ·mol-1,则表示乙醇燃烧热的热化学方程式
(5)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成固体SiO2和液态H2O。已知室温下,2gSiH4自燃放出89.2kJ热量,写出该反应的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】
(1)在25℃、101kPa下, 1g甲烷完全燃烧生成CO2和液态H2O,放出55 kJ的热量,写出表示甲烷燃烧热的热化学方程式:_______ 。
(2)2Zn(s)+O2(g)=2ZnO(s) ΔH1 =-702kJ/mol
2Hg(l)+O2(g)=2HgO(s) ΔH2 =-182kJ/mol
由此可知ZnO(s)+Hg(l)= Zn(s)+HgO(s) ΔH3=_______ 。
(3)已知 2SO2(g)+O2(g) 2SO3(g)反应过程的能量变化如图所示,已知1mol SO2(g)氧化为1mol SO3的 ΔH=-99kJ·mol-1,请回答下列问题:
2SO3(g)反应过程的能量变化如图所示,已知1mol SO2(g)氧化为1mol SO3的 ΔH=-99kJ·mol-1,请回答下列问题:
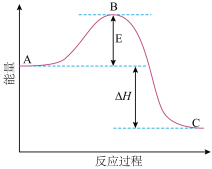
①图中A、C分别表示_______ 、_______ 。
②E的大小对该反应的反应热有无影响?_______ ,该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?_______ ,理由是_______ 。
③图中ΔH=_______ kJ/mol。
(1)在25℃、101kPa下, 1g甲烷完全燃烧生成CO2和液态H2O,放出55 kJ的热量,写出表示甲烷燃烧热的热化学方程式:
(2)2Zn(s)+O2(g)=2ZnO(s) ΔH1 =-702kJ/mol
2Hg(l)+O2(g)=2HgO(s) ΔH2 =-182kJ/mol
由此可知ZnO(s)+Hg(l)= Zn(s)+HgO(s) ΔH3=
(3)已知 2SO2(g)+O2(g)
 2SO3(g)反应过程的能量变化如图所示,已知1mol SO2(g)氧化为1mol SO3的 ΔH=-99kJ·mol-1,请回答下列问题:
2SO3(g)反应过程的能量变化如图所示,已知1mol SO2(g)氧化为1mol SO3的 ΔH=-99kJ·mol-1,请回答下列问题:
①图中A、C分别表示
②E的大小对该反应的反应热有无影响?
③图中ΔH=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)4g氢气完全燃烧生成液态水时可放出572KJ的热量,氢气的燃烧热化学方程式: ___________ 。
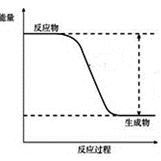
(2)下图中该反应过程ΔH_____________ 0(填<或=或>);
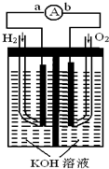
(3)下图装置是由___________ 能转化为_____________ 能,负极电极反应式为:__________________ ,正极电极反应式为:_________________________________ 。
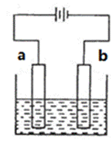
(4)如图用惰性电极电解100 mL 0.5 mol·L-1CuSO4溶液,a电极上的电极反应式为____________ ,若a电极产生56 mL气体(标况),则溶液中c(H+)=_____________ (忽略溶液体积变化),若要使电解质溶液恢复到电解前的状态,可加入__________________ (填字母)。
A.CuO B.Cu(OH)2 C.CuCO3 D.Cu2(OH)2CO3
(2)下图中该反应过程ΔH

(3)下图装置是由

(4)如图用惰性电极电解100 mL 0.5 mol·L-1CuSO4溶液,a电极上的电极反应式为
A.CuO B.Cu(OH)2 C.CuCO3 D.Cu2(OH)2CO3

您最近一年使用:0次



