名校
解题方法
1 . 某油脂常温下呈液态,其中一种成分的结构简式为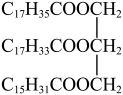 。
。
| A.加浓硫酸并加热 | B.加稀硫酸并加热 |
| C.加热 | D.加入NaOH溶液并加热 |
(2)1mol该油脂与
 加成最多消耗
加成最多消耗
(3)写出淀粉在催化剂作用下水解生成葡萄糖的反应方程式
(4)顺式聚异戊二烯的结构简式为
(5)新型合成材料的单体的结构简式如下:
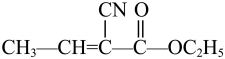
(6)外科缝合手术材料的结构片段
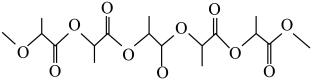 ,写出合成该聚合物所需的单体的结构简式
,写出合成该聚合物所需的单体的结构简式
您最近一年使用:0次
名校
2 . 工业制硫酸的反应之一为:2SO2(g)+O2(g) 2SO3(g),在2L恒容绝热密闭容器中投入2molSO2和适当过量的O2,在一定条件下充分反应,如图是SO2和SO3随时间的变化曲线。
2SO3(g),在2L恒容绝热密闭容器中投入2molSO2和适当过量的O2,在一定条件下充分反应,如图是SO2和SO3随时间的变化曲线。_______ (填“是”或“否”),25min时,v(正)_______ v(逆)(填“>”、“<”或“=”)。
(2)10min内,O2的反应速率为_______ ;平衡时SO2的转化率为_______ 。
(3)下列叙述不能 判断该反应达到平衡状态的是_______;
(4)在密闭容器里,通入amolSO2(g)、bmolO2(g)、cmolSO3(g),发生上述反应,当改变某种条件时,反应速率会减小的是_______(填字母)。
 2SO3(g),在2L恒容绝热密闭容器中投入2molSO2和适当过量的O2,在一定条件下充分反应,如图是SO2和SO3随时间的变化曲线。
2SO3(g),在2L恒容绝热密闭容器中投入2molSO2和适当过量的O2,在一定条件下充分反应,如图是SO2和SO3随时间的变化曲线。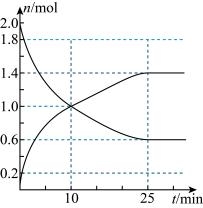
(2)10min内,O2的反应速率为
(3)下列叙述
| A.容器中压强不再改变 | B.容器中气体密度不再改变 |
| C.O2的物质的量浓度不再改变 | D.2V正(SO2)=V逆(O2) |
| A.降低温度 | B.加入催化剂 | C.缩小容器体积 | D.恒容下,充入He |
您最近一年使用:0次
名校
解题方法
3 . Ⅰ.能源是人类物质文明发展的基石,太阳能是一种清洁、绿色的能量,基于太阳能广泛应用的太阳能电池主要类型有硅太阳能电池、薄膜太阳能电池、钙钛矿太阳能电池。
(1)下列关于太阳能电池的说法正确的是_______(填选项字母,下同)。
(2)硅是构成硅太阳能电池的主要材料,下列关于硅的说法错误的是_______。
(3)晶体硅的晶胞结构如图所示:_______ 个硅原子,晶胞中最近的两个硅原子的距离为_______  ,晶体硅的密度是
,晶体硅的密度是_______  。
。
Ⅱ.工业上高纯晶体硅的制备流程如下: 中元素的电负性由大到小的顺序是
中元素的电负性由大到小的顺序是_______ (填元素符号), 分子属于
分子属于_______ 分子(填“极性”或“非极性”)。
(1)下列关于太阳能电池的说法正确的是_______(填选项字母,下同)。
| A.太阳能电池能将太阳能百分之百地转化为电能 |
| B.太阳能电池与锂电池一样可以反复充电 |
| C.漆黑的夜晚太阳能电池也能实现太阳能向电能的转化 |
| D.戈壁、沙漠等日照充足、干旱少雨的地区适合大规模安装太阳能电池 |
(2)硅是构成硅太阳能电池的主要材料,下列关于硅的说法错误的是_______。
A.硅原子的价层电子排布式为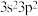 | B.硅原子核外有5种不同的空间运动状态 |
| C.硅原子核外有14种不同的电子运动状态 | D.硅元素属于s区元素 |
(3)晶体硅的晶胞结构如图所示:

 ,晶体硅的密度是
,晶体硅的密度是 。
。Ⅱ.工业上高纯晶体硅的制备流程如下:

 中元素的电负性由大到小的顺序是
中元素的电负性由大到小的顺序是 分子属于
分子属于
您最近一年使用:0次
名校
4 . 某温度时,在一个容积为2L的密闭容器中,X、Y、Z(Z为气体)三种物质的物质的量随时间的变化曲线如图所示:_______ 。
(2)反应开始至2min时,气体Z的平均反应速率为_______ 。
(3)若X、Y均为气体。
①反应达到平衡时压强是开始时的_______ 倍。
②反应达到平衡后,若将容器的体积缩小为原来的 ,重新达到平衡时,容器内温度升高(容器不与外界进行热交换),则该反应的正反应为
,重新达到平衡时,容器内温度升高(容器不与外界进行热交换),则该反应的正反应为_______ (填“放热”或“吸热”)反应。
(4)25℃时,取 的盐酸和醋酸各1mL,分别加水稀释,测得pH随溶液体积变化的曲线如图所示:
的盐酸和醋酸各1mL,分别加水稀释,测得pH随溶液体积变化的曲线如图所示:_______ 曲线(填“Ⅰ”或“Ⅱ”)代表盐酸的稀释过程。
②a点的导电性比c点的导电性_______ (填“强”或“弱”)。
③若将a、b两点的溶液加热至30℃,则 的值将
的值将_______ (填“变大”、“变小”或“不变”)。

(2)反应开始至2min时,气体Z的平均反应速率为
(3)若X、Y均为气体。
①反应达到平衡时压强是开始时的
②反应达到平衡后,若将容器的体积缩小为原来的
 ,重新达到平衡时,容器内温度升高(容器不与外界进行热交换),则该反应的正反应为
,重新达到平衡时,容器内温度升高(容器不与外界进行热交换),则该反应的正反应为(4)25℃时,取
 的盐酸和醋酸各1mL,分别加水稀释,测得pH随溶液体积变化的曲线如图所示:
的盐酸和醋酸各1mL,分别加水稀释,测得pH随溶液体积变化的曲线如图所示: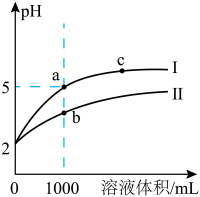
②a点的导电性比c点的导电性
③若将a、b两点的溶液加热至30℃,则
 的值将
的值将
您最近一年使用:0次
5 . 常温下,几种物质的溶度积常数如表所示:
回答下列问题:
(1)常温下,某酸性 溶液中含少量的
溶液中含少量的 ,为制得纯净
,为制得纯净 溶液,宜加入
溶液,宜加入 调至溶液
调至溶液 ,使
,使 转化为
转化为 沉淀,此时溶液中
沉淀,此时溶液中
_______ 。
(2)过滤后,将所得滤液经过_______ 、过滤、洗涤、干燥,可得到 晶体。
晶体。
(3)由 晶体得到纯的无水
晶体得到纯的无水 ,需要进行的操作是
,需要进行的操作是_______ 。
(4)某学习小组用“间接碘量法”测定含有 晶体试样(不含能与
晶体试样(不含能与 发生反应的氧化性杂质)的纯度,过程如下:取
发生反应的氧化性杂质)的纯度,过程如下:取 试样溶于水,加入过量KI固体充分反应,生成白色沉淀CuI,向溶液中加少量淀粉溶液,用
试样溶于水,加入过量KI固体充分反应,生成白色沉淀CuI,向溶液中加少量淀粉溶液,用 标准溶液滴定,达到滴定终点时,消耗
标准溶液滴定,达到滴定终点时,消耗 标准溶液
标准溶液 (已知:
(已知: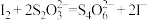 )。
)。
①达到滴定终点的现象是_______ 。
② 溶液与
溶液与 反应的离子方程式为
反应的离子方程式为_______ 。
③该试样中 的质量分数为
的质量分数为_______ 。
| 物质 |  |  |  |  |
 | 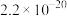 |  |  |  |
(1)常温下,某酸性
 溶液中含少量的
溶液中含少量的 ,为制得纯净
,为制得纯净 溶液,宜加入
溶液,宜加入 调至溶液
调至溶液 ,使
,使 转化为
转化为 沉淀,此时溶液中
沉淀,此时溶液中
(2)过滤后,将所得滤液经过
 晶体。
晶体。(3)由
 晶体得到纯的无水
晶体得到纯的无水 ,需要进行的操作是
,需要进行的操作是(4)某学习小组用“间接碘量法”测定含有
 晶体试样(不含能与
晶体试样(不含能与 发生反应的氧化性杂质)的纯度,过程如下:取
发生反应的氧化性杂质)的纯度,过程如下:取 试样溶于水,加入过量KI固体充分反应,生成白色沉淀CuI,向溶液中加少量淀粉溶液,用
试样溶于水,加入过量KI固体充分反应,生成白色沉淀CuI,向溶液中加少量淀粉溶液,用 标准溶液滴定,达到滴定终点时,消耗
标准溶液滴定,达到滴定终点时,消耗 标准溶液
标准溶液 (已知:
(已知: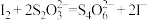 )。
)。①达到滴定终点的现象是
②
 溶液与
溶液与 反应的离子方程式为
反应的离子方程式为③该试样中
 的质量分数为
的质量分数为
您最近一年使用:0次
6 . N、S元素化合物知识在高中化学体系中占有重要地位,请根据题意回答下列问题。
(1)工业制硝酸中NH3的催化氧化化学方程式_______ 。
(2)检验溶液中含有NH4+的离子方程式_______ ,实验室一般使用_______ 检验该反应有氨气生成。
(3)向蔗糖中滴加浓硫酸,蔗糖变黑并膨胀,散发刺激性气味,说明浓硫酸具有_______ 和_______ 。(填浓硫酸的性质)
(4)铜与浓硫酸的化学反应方程式为_______ 。
(5)请用方程式解释实验室盛放碱液的试剂瓶不用玻璃塞的原因_______ 。
(1)工业制硝酸中NH3的催化氧化化学方程式
(2)检验溶液中含有NH4+的离子方程式
(3)向蔗糖中滴加浓硫酸,蔗糖变黑并膨胀,散发刺激性气味,说明浓硫酸具有
(4)铜与浓硫酸的化学反应方程式为
(5)请用方程式解释实验室盛放碱液的试剂瓶不用玻璃塞的原因
您最近一年使用:0次
名校
解题方法
7 . I.某有机物M分子的结构式如图所示:
(1)写出M的结构简式和键线式:___________ 、___________ 。
(2)下列给出了四种有机物的结构简式:A.HOCH2CH2CH=CH2;B.CH3OCH2CH=CH2;C.CH3CH2CH2CHO;D.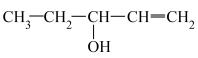 ;E.
;E. ;
;
与M属于同系物的是___________ (填选项字母,下同),互为同分异构体且官能团种类不同的是___________ ,互为同分异构体且官能团种类相同的是___________ 。
Ⅱ.利用核磁共振技术测定有机物分子三维结构的研究获得了2002年诺贝尔化学奖。某研究小组为测定某有机化合物A的结构,进行如下实验:
(3)①将有机物A置于氧气流中充分燃烧,实验测得:生成18.0gH2O和44.0gCO2,消耗氧气28.0L(标准状况),则该物质的实验式是___________ 。
②使用现代分析仪器对有机化合物A的分子结构进行测定,相关结果如图所示:___________ ,根据图2、图3(只有一组吸收峰)推测:A的结构简式为___________ (分子中有1个六元环)。
③写出化合物A属于酯类的同分异构体的结构简式:___________ (任写一种即可)。

(1)写出M的结构简式和键线式:
(2)下列给出了四种有机物的结构简式:A.HOCH2CH2CH=CH2;B.CH3OCH2CH=CH2;C.CH3CH2CH2CHO;D.
 ;E.
;E. ;
;与M属于同系物的是
Ⅱ.利用核磁共振技术测定有机物分子三维结构的研究获得了2002年诺贝尔化学奖。某研究小组为测定某有机化合物A的结构,进行如下实验:
(3)①将有机物A置于氧气流中充分燃烧,实验测得:生成18.0gH2O和44.0gCO2,消耗氧气28.0L(标准状况),则该物质的实验式是
②使用现代分析仪器对有机化合物A的分子结构进行测定,相关结果如图所示:
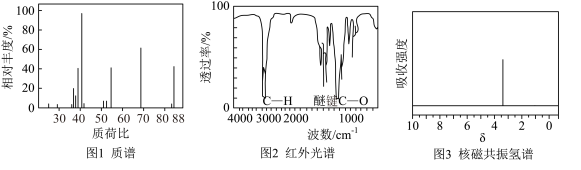
③写出化合物A属于酯类的同分异构体的结构简式:
您最近一年使用:0次
名校
8 . 化学电池的发明,是贮能和供能技术的巨大进步。
(1)生活中利用原电池原理生产了各种各样的电池,下列有关电池的叙述正确的是___________ (填字母)。
A.锌锰电池工作一段时间后碳棒会变细
B.氢氧燃料电池可将化学能直接转变为电能
C.铅蓄电池负极是PbO2,正极是Pb
(2)将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。___________ (填“A”或“B”)电极入口通甲烷,其电极反应式为___________ 。工作一段时间后,电解质溶液的pH将___________ (填“变大”、“变小”或“不变”)。
(3)有人设想利用电化学原理除去SO2,并将化学能转化为电能。装置图如下。___________ 。(填“a”或“b”)
②写出a电极的电极反应___________ 。
(4)某同学欲把反应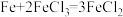 设计成原电池,请画出简易的原电池装置图
设计成原电池,请画出简易的原电池装置图________ 。
(1)生活中利用原电池原理生产了各种各样的电池,下列有关电池的叙述正确的是
A.锌锰电池工作一段时间后碳棒会变细
B.氢氧燃料电池可将化学能直接转变为电能
C.铅蓄电池负极是PbO2,正极是Pb
(2)将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。
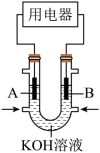
(3)有人设想利用电化学原理除去SO2,并将化学能转化为电能。装置图如下。

②写出a电极的电极反应
(4)某同学欲把反应
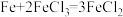 设计成原电池,请画出简易的原电池装置图
设计成原电池,请画出简易的原电池装置图
您最近一年使用:0次
名校
9 . 根据已学知识,请回答下列问题
(1)物质A的结构简式为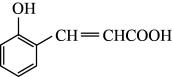 ,写出A中的含氧官能团名称
,写出A中的含氧官能团名称_____________________________ 。
(2)有机化合物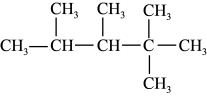 的名称是
的名称是_________________ ,其在核磁共振氢谱上有_________ 组峰。
(3)键线式 表示的有机物的分子式为
表示的有机物的分子式为 _________ ,其中等效氢个数比为_________________ 。
(4)写出1,3一丁二烯与 发生1,4-加成的反应方程式:
发生1,4-加成的反应方程式:_________________________________________________ 。
(5)与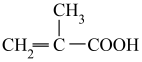 具有相同官能团的一种同分异构体的结构简式为
具有相同官能团的一种同分异构体的结构简式为_____________________ 。
(1)物质A的结构简式为
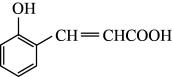 ,写出A中的含氧官能团名称
,写出A中的含氧官能团名称(2)有机化合物
 的名称是
的名称是(3)键线式
 表示的有机物的分子式为
表示的有机物的分子式为 (4)写出1,3一丁二烯与
 发生1,4-加成的反应方程式:
发生1,4-加成的反应方程式:(5)与
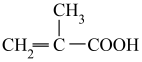 具有相同官能团的一种同分异构体的结构简式为
具有相同官能团的一种同分异构体的结构简式为
您最近一年使用:0次
名校
解题方法
10 . 到目前为止,由化学能转变的热能或电能仍然是人类使用的主要能源。现有反应①Ba(OH)2·8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑②Zn+H2SO4=ZnSO4+H2↑。试回答下列问题:
(1)两反应中属于吸热反应的是_______ (填序号,下同),能设计成原电池的是_______ 。
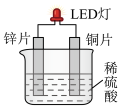
(2)化学课外活动小组设计的用铜-锌-稀硫酸原电池使LED灯发光的装置示意图。_______ (填“锌”或“铜”)电极方向移动。
②正极的电极方程式为_______ 。
③若反应过程中有0.2 mol电子的转移,则生成的氢气在标准状况下的体积为_______ L。
(3)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:_______ 。(填“正极”或“负极”)
②电极b的电极反应式为_______ 。
(1)两反应中属于吸热反应的是
(2)化学课外活动小组设计的用铜-锌-稀硫酸原电池使LED灯发光的装置示意图。
②正极的电极方程式为
③若反应过程中有0.2 mol电子的转移,则生成的氢气在标准状况下的体积为
(3)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:
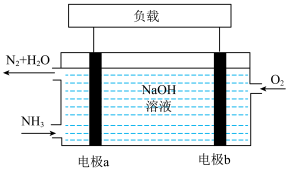
②电极b的电极反应式为
您最近一年使用:0次



