名校
1 . Ⅰ.有如图所示各步变化(部分产物未写出),A为金属单质,B为淡黄色固体,物质A~E均含有钠元素。___________ ,D.___________ 。
(2)写出A→E的化学方程式并用双线桥标出电子转移的方向和数目:___________ 。
Ⅱ.完成下列问题
(3)+2价的亚铁离子是血红蛋白(用于运输氧气)的重要组成成分。亚铁离子极不稳定,二价铁易被空气或Cl2___________ (填“氧化”或“还原”)成三价铁,请写出亚铁离子与Cl2反应的离子方程式:___________ 。
(4)某实验小组用“套管实验”来探究Na2CO3和NaHCO3的性质。___________ 。
②该实验可证明NaHCO3的热稳定性___________ (填“强于”“弱于”或“等于”)Na2CO3;___________ (填“能”或“不能”)将NaHCO3、Na2CO3的位置互换。
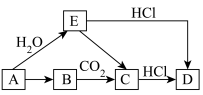
(2)写出A→E的化学方程式并用双线桥标出电子转移的方向和数目:
Ⅱ.完成下列问题
(3)+2价的亚铁离子是血红蛋白(用于运输氧气)的重要组成成分。亚铁离子极不稳定,二价铁易被空气或Cl2
(4)某实验小组用“套管实验”来探究Na2CO3和NaHCO3的性质。
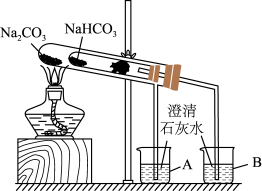
②该实验可证明NaHCO3的热稳定性
您最近一年使用:0次
名校
2 . 图所示为利用分类法对一组物质进行的分类。回答下列问题  属于
属于___________  填“酸性”或“碱性”
填“酸性”或“碱性” 氧化物,书写
氧化物,书写 与
与 反应的化学方程式
反应的化学方程式___________ ,依据该反应,可以说明
___________  填“属于”或“不属于”
填“属于”或“不属于” 碱性氧化物。
碱性氧化物。
(2)上述物质中属于电解质的是___________ 。
(3)某学生完成钠与水反应的实验,实验过程如图 、
、 、
、 所示,下列有关实验现象及结论的叙述
所示,下列有关实验现象及结论的叙述不正确 的是___________。 填序号
填序号
(4)工业上常用 与
与 溶液反应制取消毒液,该反应的化学方程式为
溶液反应制取消毒液,该反应的化学方程式为___________ 。
(5)向 溶液中加入NaOH溶液,对应的离子方程式为
溶液中加入NaOH溶液,对应的离子方程式为___________ 。
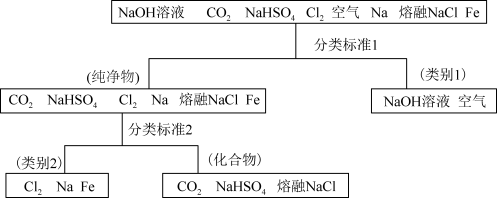
 属于
属于 填“酸性”或“碱性”
填“酸性”或“碱性” 氧化物,书写
氧化物,书写 与
与 反应的化学方程式
反应的化学方程式
 填“属于”或“不属于”
填“属于”或“不属于” 碱性氧化物。
碱性氧化物。(2)上述物质中属于电解质的是
(3)某学生完成钠与水反应的实验,实验过程如图
 、
、 、
、 所示,下列有关实验现象及结论的叙述
所示,下列有关实验现象及结论的叙述 填序号
填序号
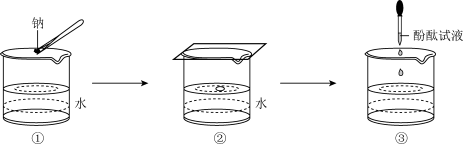
A.图 中钠熔成小球,说明钠与水反应放热且钠的熔点低 中钠熔成小球,说明钠与水反应放热且钠的熔点低 |
B.图 中钠四处游动并嘶嘶作响,说明反应产生了气体 中钠四处游动并嘶嘶作响,说明反应产生了气体 |
C.图 中滴加酚酞试液后溶液变红,说明有碱性物质生成 中滴加酚酞试液后溶液变红,说明有碱性物质生成 |
D.钠与水反应的离子方程式是: 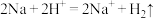 |
(4)工业上常用
 与
与 溶液反应制取消毒液,该反应的化学方程式为
溶液反应制取消毒液,该反应的化学方程式为(5)向
 溶液中加入NaOH溶液,对应的离子方程式为
溶液中加入NaOH溶液,对应的离子方程式为
您最近一年使用:0次
名校
3 . 氯气是现代工业和生活中常用的杀菌消毒剂。回答下列问题:
(1)实验室常用 固体和浓盐酸在加热条件下制取
固体和浓盐酸在加热条件下制取 ,反应的离子方程式为
,反应的离子方程式为___________ 。实验室还可用 固体和浓盐酸在室温条件下制取少量氯气(同时生成
固体和浓盐酸在室温条件下制取少量氯气(同时生成 和
和 ),可选用图中的
),可选用图中的___________ (选填“A”或“B”)作为发生装置,反应的离子方程式为___________ 。
(说明:试管中溶液均为 ,均滴入氯水5滴;淀粉遇
,均滴入氯水5滴;淀粉遇 变蓝)
变蓝)
①实验I中反应方程式为___________ ,由此推断氧化性:
___________  (填“
(填“ ”或“
”或“ ”)。
”)。
②实验Ⅱ中溶液变红是由于溶液中含有___________ (填微粒符号,下同);使溶液褪色的微粒是___________ 。
(1)实验室常用
 固体和浓盐酸在加热条件下制取
固体和浓盐酸在加热条件下制取 ,反应的离子方程式为
,反应的离子方程式为 固体和浓盐酸在室温条件下制取少量氯气(同时生成
固体和浓盐酸在室温条件下制取少量氯气(同时生成 和
和 ),可选用图中的
),可选用图中的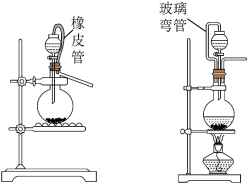
| 实验Ⅰ | 实验Ⅱ | |
| 实验操作 |
|
|
| 实验现象 | 溶液变蓝 | 石蕊溶液先变红,后褪色 |
 ,均滴入氯水5滴;淀粉遇
,均滴入氯水5滴;淀粉遇 变蓝)
变蓝)①实验I中反应方程式为

 (填“
(填“ ”或“
”或“ ”)。
”)。②实验Ⅱ中溶液变红是由于溶液中含有
您最近一年使用:0次
4 . 回答下列问题
(1)0.5molCO2的质量是___________ g;分子数为___________ 。在标准状况下,体积为___________ 。
(2)0.5molNa2SO4含有___________ molSO ,含
,含___________ molO,含___________ 个O,Na2SO4摩尔质量为___________ 。
(1)0.5molCO2的质量是
(2)0.5molNa2SO4含有
 ,含
,含
您最近一年使用:0次
5 . 科学家开发了“氧化裂解技术”,将废弃物中的聚苯乙烯(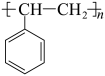 )转变为有用的苯甲酸(
)转变为有用的苯甲酸(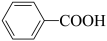 ),变废为宝。转变反应如下:
),变废为宝。转变反应如下: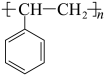
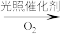
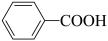 。结合上述材料,回答下列问题:
。结合上述材料,回答下列问题:
| A.属于氧化反应 | B.属于加聚反应 |
| C.发生了碳碳键的断裂 | D.反应物和产物都含有苯分子 |
(2)关于聚苯乙烯的说法正确的是___________。
| A.其单体是乙烯 | B.难溶于水 |
| C.可以制成泡沫包装材料 | D.难以自然降解,应回收处理 |
(3)苯乙烯的一些性质类似于乙烯。苯乙烯___________。
| A.属于烷烃 | B.属于不饱和烃 |
C.不能使溴的 溶液褪色 溶液褪色 | D.能使酸性 溶液褪色 溶液褪色 |
(4)苯甲酸的一些性质类似于乙酸。苯甲酸___________。
| A.可与Na反应 | B.可与NaOH反应 |
| C.一定条件下可与乙醇反应 | D.是一种常见的食品防腐剂 |
(5)一些苯环上有取代基的聚苯乙烯类高分子,也能利用上述的“氧化裂解技术”发生类似的反应。已知一种高分子R的结构如图。下列有关R的说法正确的是___________。
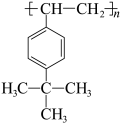
| A.能发生取代反应 | B.能在空气中燃烧 |
C.分子式为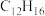 | D.能氧化裂解生成含羧基的物质 |
您最近一年使用:0次
6 . “民以食为天”,对元素周期表中有关元素的认识可使我们更好地了解食品的营养和安全。
结合上述材料,回答下列问题:
(1)仅含a、b、d三种元素的营养物质有___________。
(2)成熟水果会释放出由a和b按原子数目比 组成的气体。该气体分子___________。
组成的气体。该气体分子___________。
(3)某些元素的单质或化合物常用于食品加工和保存。下列说法正确的是___________。
(4)土豆中富含淀粉。淀粉___________。
(5)由a、b、d和e四种元素形成的物质可用作糕点膨松剂。下列说法正确的是___________。
| 周期 | ⅠA | 0 | ||||||
| 1 | a | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | b | c | d | |||||
| 3 | e | f | g | h |
(1)仅含a、b、d三种元素的营养物质有___________。
| A.脂肪 | B.葡萄糖 | C.蛋白质 | D.氨基酸 |
 组成的气体。该气体分子___________。
组成的气体。该气体分子___________。A.分子式为 | B.呈四面体结构 |
| C.呈三角锥形结构 | D.所有原子共平面 |
| A.a的单质可与植物油发生加成反应 | B.c的单质充入食品包装袋中可防腐 |
| C.f的单质制作的容器可用于贮存酸菜 | D.e和h形成的化合物可用于腌制食品 |
| A.遇碘溶液变色 | B.可水解得到乙醇 |
| C.由a、b、g三种元素组成 | D.水解的最终产物能发生银镜反应 |
| A.非金属性:b>a>d | B.原子半径:e>b>d |
| C.e的最高价氧化物的水化物是强碱 | D.b、d、e原子具有相同的电子层数 |
您最近一年使用:0次
7 . 某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择酚酞作指示剂。请填写下列空白:
(1)某学生的操作步骤如下:
A.移取20.00mL待测溶液注入洁净的锥形瓶中,并加入2~3滴酚酞试液。
B.用标准溶液润洗滴定管2~3次。
C.调节滴定管旋塞使尖嘴充满溶液,把盛有标准溶液的酸式滴定管固定好。
D.取标准盐酸溶液注入酸式滴定管至零刻度以上2~3cm。
E.调节液面至零刻度(或以下),记下读数V1。
F.用标准溶液滴定至终点,记下滴定管液面的刻度V2。
请写出操作步骤的正确顺序___________ 。
→___________→___________→___________→A→F。
(2)滴定终点的判断方法:___________ 。
(3)滴定结束时,酸式滴定管中的液面如图所示,则读数为___________ mL。
(5)某学生根据三次实验分别记录有关数据如表:
请选用其中合理数据求出该氢氧化钠溶液物质的量浓度:c(NaOH)=___________ mol/L。(计算结果保留4位有效数字)
(6)由于错误操作,使得上述所测氢氧化钠溶液的浓度偏高的是___________(填字母)。
(1)某学生的操作步骤如下:
A.移取20.00mL待测溶液注入洁净的锥形瓶中,并加入2~3滴酚酞试液。
B.用标准溶液润洗滴定管2~3次。
C.调节滴定管旋塞使尖嘴充满溶液,把盛有标准溶液的酸式滴定管固定好。
D.取标准盐酸溶液注入酸式滴定管至零刻度以上2~3cm。
E.调节液面至零刻度(或以下),记下读数V1。
F.用标准溶液滴定至终点,记下滴定管液面的刻度V2。
请写出操作步骤的正确顺序
→___________→___________→___________→A→F。
(2)滴定终点的判断方法:
(3)滴定结束时,酸式滴定管中的液面如图所示,则读数为

A. | B. | C. | D. |
(5)某学生根据三次实验分别记录有关数据如表:
| 滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.1000mol•L-1盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积 | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
(6)由于错误操作,使得上述所测氢氧化钠溶液的浓度偏高的是___________(填字母)。
| A.中和滴定到达终点时俯视滴定管内液面读数 |
| B.碱式滴定管用蒸馏水洗净后立即取用25.00mL待测碱溶液注入锥形瓶进行滴定 |
| C.酸式滴定管用蒸馏水洗净后立即装标准溶液来滴定 |
| D.锥形瓶用待测液润洗 |
您最近一年使用:0次
名校
8 . I、按要求写出下列方程式:
(1)FeCl3水解的离子方程式:___________ 。
(2)NaHCO3水解的离子方程式:___________ 。
(3)NH3•H2O的电离方程式:___________ 。
(4)Mg(OH)2在水中的沉淀溶解平衡用离子方程式表示:___________ 。
Ⅱ、回答下列问题。
(5)25℃时,0.01mol/L的NaOH溶液的pH=___________ ;由水电离出c(H+)=___________ mol/L。
(6)25℃时,将10mLpH=2醋酸溶液稀释到1000mL后溶液的pH___________ 4(填“大于”“小于”或“等于”)。
(7)某温度时,Ksp[AgI]=9.0×10-16,求AgI饱和溶液中c(Ag+)=___________ mol/L
(1)FeCl3水解的离子方程式:
(2)NaHCO3水解的离子方程式:
(3)NH3•H2O的电离方程式:
(4)Mg(OH)2在水中的沉淀溶解平衡用离子方程式表示:
Ⅱ、回答下列问题。
(5)25℃时,0.01mol/L的NaOH溶液的pH=
(6)25℃时,将10mLpH=2醋酸溶液稀释到1000mL后溶液的pH
(7)某温度时,Ksp[AgI]=9.0×10-16,求AgI饱和溶液中c(Ag+)=
您最近一年使用:0次
名校
9 . I:我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成,爆炸时发生的反应为:S+2KNO3+3C=K2S+N2↑+3X↑请回答:
(1)X的化学式是___________ ,按照物质的组成和性质分类,属于___________ (填字母)。
A.单质 B.酸性氧化物 C.化合物 D.盐
(2)在上述反应中,氧化剂是(填化学式)___________ 。
II:如图是一块用FeCl3溶液与Cu反应制作的印刷电路板,其制作原理可用方程式2FeCl3 +Cu = CuCl2 + 2X表示。___________ 。
(4)在上述反应中,氧化剂为___________ ,氧化产物为___________ ,将两者的氧化性相比较,___________ 的氧化性更强。
(5)写出该反应的离子方程式,并用双线桥表示电子转移的方向和数目___________ 。
(1)X的化学式是
A.单质 B.酸性氧化物 C.化合物 D.盐
(2)在上述反应中,氧化剂是(填化学式)
II:如图是一块用FeCl3溶液与Cu反应制作的印刷电路板,其制作原理可用方程式2FeCl3 +Cu = CuCl2 + 2X表示。

(4)在上述反应中,氧化剂为
(5)写出该反应的离子方程式,并用双线桥表示电子转移的方向和数目
您最近一年使用:0次
名校
10 . 阅读下面一段材料并答问题。
高铁酸钾使用说明书
【化学式】 K2FeO4
【性状】暗紫色具有金属光泽的粉末,无臭无味
【产品特点】
①干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气。
②K2FeO4通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。
③K2FeO4与水反应还能产生具有强吸附性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用。
【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理
【用量】消毒净化1L水投放5mg K2FeO4,即可达到卫生标准
(1)K2FeO4中铁元素的化合价为___________ 。
(2)制备K2FeO4需要在___________ (填“酸性”、“碱性”或“中性”)环境中进行。
(3)下列关于K2FeO4的说法中,不正确的是___________ 。
a.是强氧化性的盐
b.固体保存需要防潮
c.其消毒和净化水的原理相同
d.其净水优点有:作用快、安全性好、无异味
(4)高铁酸钠是一种新型的净水剂,可以通过下述反应制取:
2Fe(OH)3 +4NaOH+3NaClO=2Na2FeO4+3NaCl +5H2O
①该反应中的氧化剂是___________ ,___________ 元素被氧化,还原产物为___________ 。
②用单线桥法在化学方程式中标出电子转移的情况___________ 。
高铁酸钾使用说明书
【化学式】 K2FeO4
【性状】暗紫色具有金属光泽的粉末,无臭无味
【产品特点】
①干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气。
②K2FeO4通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。
③K2FeO4与水反应还能产生具有强吸附性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用。
【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理
【用量】消毒净化1L水投放5mg K2FeO4,即可达到卫生标准
(1)K2FeO4中铁元素的化合价为
(2)制备K2FeO4需要在
(3)下列关于K2FeO4的说法中,不正确的是
a.是强氧化性的盐
b.固体保存需要防潮
c.其消毒和净化水的原理相同
d.其净水优点有:作用快、安全性好、无异味
(4)高铁酸钠是一种新型的净水剂,可以通过下述反应制取:
2Fe(OH)3 +4NaOH+3NaClO=2Na2FeO4+3NaCl +5H2O
①该反应中的氧化剂是
②用单线桥法在化学方程式中标出电子转移的情况
您最近一年使用:0次