名校
解题方法
1 . 已知i.2CO(g)+O2(g)=2CO2(g) ΔH1=﹣566.0kJ•mol﹣1;
ⅱ.2H2(g)+O2(g)=2H2O(l) ΔH2=﹣483.6 kJ•mol﹣1;
ⅲ.CO(g)+2H2(g)=CH3OH(g) ΔH3=﹣574.4 kJ•mol﹣1;
写出CH3OH燃烧热的热化学方程式:___________ 。
ⅱ.2H2(g)+O2(g)=2H2O(l) ΔH2=﹣483.6 kJ•mol﹣1;
ⅲ.CO(g)+2H2(g)=CH3OH(g) ΔH3=﹣574.4 kJ•mol﹣1;
写出CH3OH燃烧热的热化学方程式:
您最近一年使用:0次
名校
解题方法
2 . 在恒温下体积为2L的密闭容器中,通入1mol氮气和3mol氢气,2min后达到平衡,测得混合气体中氮气的物质的量为0.8mol,求:
(1)反应开始到达到平衡这段时间内氮气的反应速率___________ 。
(2)平衡时H2的转化率___________ 。
(3)平衡混合气体中NH3的体积分数___________ 。
(1)反应开始到达到平衡这段时间内氮气的反应速率
(2)平衡时H2的转化率
(3)平衡混合气体中NH3的体积分数
您最近一年使用:0次
名校
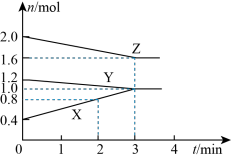
3 . 某温度时,在容积为3L的密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化的曲线如图所示。分析图中数据,回答下列问题:___________ 。
(2)该反应是由___________ (填“正反应”、“逆反应”或“正、逆反应同时”)开始反应的。
(3)下列哪些数据在反应开始至反应达到平衡时。一直保持不变的是___________ (填字母)
a.压强 b.密度 c.相对平均式量 d.反应物的浓度
(2)该反应是由
(3)下列哪些数据在反应开始至反应达到平衡时。一直保持不变的是
a.压强 b.密度 c.相对平均式量 d.反应物的浓度
您最近一年使用:0次
解题方法
4 . “化学﹣我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。请填空:
(1)若金属钠等活泼金属着火时,应该用_______ 来灭火。金属钠应保存在 _______ 中。
(2)在呼吸面具和潜水艇中可用过氧化钠作为供氧剂,请写出其中一个反应的化学方程式____ 。
(3)小苏打的化学式为_______ ,可用于治疗胃酸过多,其反应的离子方程式为_______ 。
(4)氯水和漂白粉都具有漂白作用,也可用于水体的杀菌消毒。漂白粉主要成分的化学式为_____ ,漂白粉能消毒杀菌是因具有_______ 性。
(5)高铁酸钠(Na2FeO4)是水处理过程中的一种新型的绿色多功能净水剂。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便。其净水过程中所发生的化学反应主要为4Na2FeO4+10H2O=4Fe(OH)3(胶体)+3O2↑+8NaOH。高铁酸钠(Na2FeO4)属于_______ (“酸”、 “碱”、 “盐”或“氧化物”),其中铁的化合价为_______ 价;将上述反应的化学方程式改写成离子方程式:_______ 该反应中的O2为_______ (填标号)。
a.氧化产物 b.还原产物 c.既不是氧化产物又不是还原产物
(1)若金属钠等活泼金属着火时,应该用
(2)在呼吸面具和潜水艇中可用过氧化钠作为供氧剂,请写出其中一个反应的化学方程式
(3)小苏打的化学式为
(4)氯水和漂白粉都具有漂白作用,也可用于水体的杀菌消毒。漂白粉主要成分的化学式为
(5)高铁酸钠(Na2FeO4)是水处理过程中的一种新型的绿色多功能净水剂。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便。其净水过程中所发生的化学反应主要为4Na2FeO4+10H2O=4Fe(OH)3(胶体)+3O2↑+8NaOH。高铁酸钠(Na2FeO4)属于
a.氧化产物 b.还原产物 c.既不是氧化产物又不是还原产物
您最近一年使用:0次
解题方法
5 . 有下列物质:①Ba(OH)2固体;②熔融的KHSO4;③HNO3;④稀硫酸;⑤CO2;⑥铜;⑦NaOH溶液;⑧蔗糖晶体;⑨FeCl3固体;⑩CH3COOH。请用序号填空。
(1)上述状态下的物质可导电的是_______ (请用序号填空)。
(2)属于电解质的是_______ ,属于非电解质的是 _______ (请用序号填空)。
(3)写出⑦的溶液和⑩的溶液反应的离子方程式_______ 。
(4)将⑨的饱和溶液滴入沸水中,继续煮沸直至溶液呈_______ 色,即可制得Fe(OH)3胶体,反应方程式为_______ 。
(1)上述状态下的物质可导电的是
(2)属于电解质的是
(3)写出⑦的溶液和⑩的溶液反应的离子方程式
(4)将⑨的饱和溶液滴入沸水中,继续煮沸直至溶液呈
您最近一年使用:0次
名校
6 . 现有下列十种物质:
①铝;②NaCl;③CO2;④H2SO4;⑤Ba(OH)2;⑥氨水;⑦红褐色的氢氧化铁胶体;⑧盐酸;⑨CaCO3;⑩蔗糖
(1)按物质的树状分类法填写表格的空白处:
(2)写出⑤的电离方程式___________ 。
(3)上述十种物质中,有两种物质之间可发生H++OH-=H2O,该离子反应对应的化学方程式为___________ 。
(4)写出制备⑦的化学方程式:___________ 。
①铝;②NaCl;③CO2;④H2SO4;⑤Ba(OH)2;⑥氨水;⑦红褐色的氢氧化铁胶体;⑧盐酸;⑨CaCO3;⑩蔗糖
(1)按物质的树状分类法填写表格的空白处:
| 类别 | 金属单质 | 氧化物 | 电解质 | 非电解质 | |
| 属于该类的物质(填标号) | ① | ⑥⑧ |
(3)上述十种物质中,有两种物质之间可发生H++OH-=H2O,该离子反应对应的化学方程式为
(4)写出制备⑦的化学方程式:
您最近一年使用:0次
7 . Ⅰ.已知表中所示的一组物质:
(1)常温时,0.1mol/L的溶液呈碱性的是___________ 。(填序号)
(2)常温时,向CH3COOH 溶液中加入少量NH4Cl固体,电离平衡常数Ka___________ 。(填“增大”、“减小”或“不变”)
(3)不断加热FeCl3溶液蒸干其水分并灼烧,得到的固体是___________ (填化学式)。
(4)在配制FeCl3溶液时,加入盐酸的目的是______________________ 。(结合离子方程式和必要的文字说明)
Ⅱ.已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
(5)物质的量浓度均为0.1mol/L的四种溶液:pH由小到大排列的顺序是_______ (用编号填写)
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(6)向NaClO溶液中通入少量CO2反应的离子方程式:_____________________ 。
(7)向20mLCH3COOH溶液中加入同浓度的NaOH溶液至中性,所需NaOH溶液体积_______ 20mL(填“>”“<”或“=”)。
(8)常温下,0.1mol/L CH3COOH溶液加水稀释过程中,下列表达式中数据变大的是_______。
| 序号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 物质 | H2SO4 | NaOH | CH3COOH | NH3•H2O | Na2CO3 | NH4Cl | HCl | NaCl |
(2)常温时,向CH3COOH 溶液中加入少量NH4Cl固体,电离平衡常数Ka
(3)不断加热FeCl3溶液蒸干其水分并灼烧,得到的固体是
(4)在配制FeCl3溶液时,加入盐酸的目的是
Ⅱ.已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | Ka=1.8×10﹣5 | Ka1=4.3×10﹣7 Ka2=5.6×10﹣11 | Ka=3.0×10﹣8 |
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(6)向NaClO溶液中通入少量CO2反应的离子方程式:
(7)向20mLCH3COOH溶液中加入同浓度的NaOH溶液至中性,所需NaOH溶液体积
(8)常温下,0.1mol/L CH3COOH溶液加水稀释过程中,下列表达式中数据变大的是_______。
| A.c(H+) | B. | C.c(H+)·c(OH-) | D.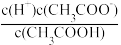 |
您最近一年使用:0次
8 . 下表是元素周期表的一部分,根据所给的10种元素,完成以下各小题。
(1)金属性最强的元素是___________ (填元素符号)。最不活泼元素的原子结构示意图为___________ 。
(2)第3周期元素中,其最高价氧化物对应的水化物具有两性的元素是___________ (填元素名称)。Na、Mg两种元素中,原子半径较大的是___________ 。
(3)第3周期元素中,其元素的一种氧化物是形成酸雨的主要物质,该氧化物的化学式为___________ 。
(4)工业上可以用Cl2和H2来制取盐酸,该反应的化学方程式为___________ 。
(5)由碳与氢元素形成的最简单有机物的化学式为___________ ,该物质中碳元素与氢元素的质量比为___________ ,其分子立体构型为___________ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | H | |||||||
| 2 | C | N | F | Ne | ||||
| 3 | Na | Mg | Al | S | Cl |
(2)第3周期元素中,其最高价氧化物对应的水化物具有两性的元素是
(3)第3周期元素中,其元素的一种氧化物是形成酸雨的主要物质,该氧化物的化学式为
(4)工业上可以用Cl2和H2来制取盐酸,该反应的化学方程式为
(5)由碳与氢元素形成的最简单有机物的化学式为
您最近一年使用:0次
解题方法
9 . 在1~18号的短周期主族元素中,表中的字母代表一种元素,回答下列问题:
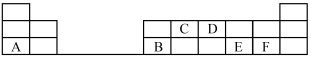
(1)写出D单质的电子式:___________ 。
(2)写出C的最高价氧化物的结构式:___________ 。
(3)E和F分别形成的气态氢化物中较稳定的是___________ (填氢化物的化学式)。
(4)A最高价氧化物的水化物所含化学键为___________ ,其水溶液与F单质反应的离子方程式为___________ 。

(1)写出D单质的电子式:
(2)写出C的最高价氧化物的结构式:
(3)E和F分别形成的气态氢化物中较稳定的是
(4)A最高价氧化物的水化物所含化学键为
您最近一年使用:0次
名校
解题方法
10 . 有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。在101 kPa下,1 g氢气完全燃烧生成液态水放出142.9 kJ的热量。
(1)请写出表示氢气燃烧热的热化学方程式__________________ 。
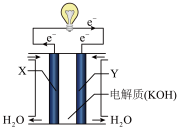
(2)将上述反应设计成下图所示的原电池,其中Y为________ 极(填“正”或“负”),该极电极反应式为___________________ 。

(1)请写出表示氢气燃烧热的热化学方程式
(2)将上述反应设计成下图所示的原电池,其中Y为
您最近一年使用:0次



