1 . 现有A、B、C、D四种烃,其球棍模型或比例模型如图1:
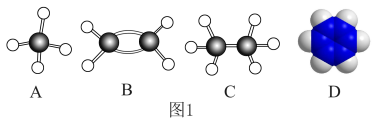
(1)可以用来鉴别A和B的试剂是_________
(2)上述四种物质互为同系物的是___________ (填字母)。
(3)在一定条件下,B能转化为C,写出该反应的方程式___________ 。
(4)上述四种物质中有一种可以在一定条件 下与浓硝酸反应,请写出反应的化学方程式:___________ 。
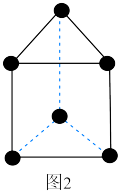
(5)E是一种新合成的烃,其碳架呈三棱柱体(如图2所示),1 mol 该烃与足量氯气光照条件下充分反应,会消耗___________ mol Cl2。

(1)可以用来鉴别A和B的试剂是_________
| A.水 | B.稀硫酸 | C.溴的四氯化碳溶液 | D.酸性高锰酸钾溶液 |
(2)上述四种物质互为同系物的是
(3)在一定条件下,B能转化为C,写出该反应的方程式
(4)上述四种物质中有一种可以在一定条件 下与浓硝酸反应,请写出反应的化学方程式:
(5)E是一种新合成的烃,其碳架呈三棱柱体(如图2所示),1 mol 该烃与足量氯气光照条件下充分反应,会消耗

您最近一年使用:0次
19-20高一·浙江·阶段练习
名校
解题方法
2 . 某同学用如下实验探究Fe2+、Fe3+的性质。请回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol·L-1的溶液,在FeCl3溶液中需加入少量铁屑,发生反应的化学方程式为_______ 。
(2)甲同学取2 mL FeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化,FeCl2溶液与氯水反应的化学方程式为_______ 。
(3)乙同学认为甲同学的实验不够严谨,该同学在2 mL FeCl2溶液中先加入0.5 mL煤油,再于液面下依次加入1滴KSCN溶液和几滴氯水,溶液变红,煤油的作用是_______ 。
(4)丁同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为_______ 。
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol·L-1的溶液,在FeCl3溶液中需加入少量铁屑,发生反应的化学方程式为
(2)甲同学取2 mL FeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化,FeCl2溶液与氯水反应的化学方程式为
(3)乙同学认为甲同学的实验不够严谨,该同学在2 mL FeCl2溶液中先加入0.5 mL煤油,再于液面下依次加入1滴KSCN溶液和几滴氯水,溶液变红,煤油的作用是
(4)丁同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为
您最近一年使用:0次
2023-02-03更新
|
235次组卷
|
5卷引用:黑龙江省鸡西市第一中学2021-2022学年高一上学期期中考试化学试题
黑龙江省鸡西市第一中学2021-2022学年高一上学期期中考试化学试题(已下线)【浙江新东方】双师 (44).新疆巴音郭楞蒙古自治州第一中学等两校2022-2023学年高一上学期期末联考化学试题第2课时 铁盐和亚铁盐(已下线)【定心卷】3.1.2 铁的重要化合物随堂练习-人教版2023-2024学年必修第一册
解题方法
3 . NaNO2易溶于水,外观和食盐相似,有咸味,人误食会中毒。已知NaNO2能发生如下反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。且①HI的溶液中不存在HI分子;②碘单质(I2)遇淀粉溶液显蓝色。请回答下列问题:
(1)上述反应氧化性:NaNO2_______ I2(填“强”或“弱”)。
(2)HI是_______ 电解质(填“强”或“弱”)。
(3)上述反应的离子方程式为_______ 。
(4)上述反应中氧化剂是_______ ;NaI_______ (填序号)。
①是氧化产物;②是还原产物;③既不是氧化产物,又不是还原产物;④既是氧化产物,又是还原产物。
(1)上述反应氧化性:NaNO2
(2)HI是
(3)上述反应的离子方程式为
(4)上述反应中氧化剂是
①是氧化产物;②是还原产物;③既不是氧化产物,又不是还原产物;④既是氧化产物,又是还原产物。
您最近一年使用:0次
解题方法
4 . 完成下列问题
(1)下面是某同学对有关物质进行分类的列表:
每组分类均有错误,其错误的物质分别是_______ 、_______ 、_______ (填化学式)。
(2)写出Na2O2与CO2反应的方程式_______ (并用双线桥法标出电子转移情况)
(3)KHSO4在水溶液中的电离方程式可以表示为_______ ;
(4)向KHSO4溶液中加入碳酸氢钠,可以观察到的现象是_______ ,反应的离子方程式为_______ 。
(5)向KHSO4溶液中加入锌片,反应的离子方程式为_______ 。
(1)下面是某同学对有关物质进行分类的列表:
| 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
| 第一组 | Na2CO3 | H2SO4 | NaHCO3 | CaO | CO2 |
| 第二组 | NaOH | HCl | NaCl | Na2O2 | SO3 |
| 第三组 | KOH | CH3COOH | CaF2 | Al2O3 | SO2 |
(2)写出Na2O2与CO2反应的方程式
(3)KHSO4在水溶液中的电离方程式可以表示为
(4)向KHSO4溶液中加入碳酸氢钠,可以观察到的现象是
(5)向KHSO4溶液中加入锌片,反应的离子方程式为
您最近一年使用:0次
解题方法
5 . 请找出常见物质与其用途的对应关系_______ 。
| (1)氯气 | A、呼吸面具中氧气来源 | |
| (2)碳酸氢钠 | B、漂白粉的有效成分 | |
| (3)氧化铁 | C、用于自来水杀菌消毒 | |
| (4)过氧化钠 | D、制作红色油漆的颜料 | |
| (5)次氯酸钙 | E、发酵粉的成分或治疗胃酸过多 |
您最近一年使用:0次
6 . 实验室制备Cl2的化学方程式为MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O。请完成下列问题:
MnCl2+Cl2↑+2H2O。请完成下列问题:
(1)用双线桥法标出电子转移方向和数目:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O____________ 。
(2)该反应中HCl表现出的作用是_______________ (填“氧化性”、“还原性”或“酸性”)。
(3)该反应中氧化剂是____________ 。
(4)8.7g MnO2参加反应,被还原的HCl的质量为______________ g。
(5)已知“氧化性:氧化剂>氧化产物”,根据该反应可比较氧化性的强弱顺序是______________ 。
 MnCl2+Cl2↑+2H2O。请完成下列问题:
MnCl2+Cl2↑+2H2O。请完成下列问题:(1)用双线桥法标出电子转移方向和数目:MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O(2)该反应中HCl表现出的作用是
(3)该反应中氧化剂是
(4)8.7g MnO2参加反应,被还原的HCl的质量为
(5)已知“氧化性:氧化剂>氧化产物”,根据该反应可比较氧化性的强弱顺序是
您最近一年使用:0次
7 . 非金属氟化物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态F原子核外电子的运动状态有_______ 种。
(2)O、F、Cl电负性由大到小的顺序为_______ ;OF2分子的空间构型为_______ ;OF2的熔、沸点_______ (填“高于”或“低于”)Cl2O。
(3)Xe是第五周期的稀有气体元素,与F形成的XeF2室温下易升华。XeF2中心原子的价层电子对数为_______ ,下列对XeF2中心原子杂化方式推断合理的是_______ (填标号)。
A.sp B.sp2 C.sp3 D.sp3d
(4)XeF2晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有_______ 个XeF2分子。

(1)基态F原子核外电子的运动状态有
(2)O、F、Cl电负性由大到小的顺序为
(3)Xe是第五周期的稀有气体元素,与F形成的XeF2室温下易升华。XeF2中心原子的价层电子对数为
A.sp B.sp2 C.sp3 D.sp3d
(4)XeF2晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有

您最近一年使用:0次
解题方法
8 . 如图是一个电化学过程的示意图,请按要求回答下列问题
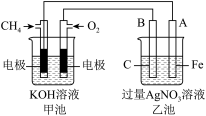
(1)甲池是_______ 装置(填“原电池”或“电解池”)
(2)写出电极反应式:通入CH4的电极_______ 。
(3)反应一段时间后,甲池中消耗1.6g甲烷,则乙池中某电极的质量增_______ g。
(4)反应一段时间后,乙池中溶液成分发生了变化,想要完全恢复到电解前可加入的物质是____
(5)某工厂烟气中主要含SO2,可用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如下图所示(电极材料为石墨)。
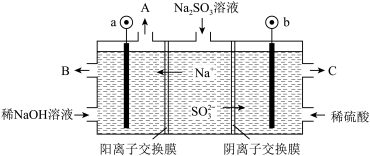
①图中a极要连接电源的_______ (填“正”或“负”)极,C口流出的物质是_______ 。
② 放电的电极反应式为
放电的电极反应式为_______ 。

(1)甲池是
(2)写出电极反应式:通入CH4的电极
(3)反应一段时间后,甲池中消耗1.6g甲烷,则乙池中某电极的质量增
(4)反应一段时间后,乙池中溶液成分发生了变化,想要完全恢复到电解前可加入的物质是
(5)某工厂烟气中主要含SO2,可用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如下图所示(电极材料为石墨)。

①图中a极要连接电源的
②
 放电的电极反应式为
放电的电极反应式为
您最近一年使用:0次
9 . 下表有三组物质,每组均有甲、乙、丙三种物质(酸、碱、盐均为溶液):
(1)第三组中有一种物质能与第_________ 组中的所有物质反应,这种物质是_________ 。
(2)第二组中有一种物质与第一组所有物质都不发生反应,但能与第三组中所有物质发生反应,其化学方程式分别为
①_________ ;
②_________ ;
③_________ 。
| 第一组 | 第二组 | 第三组 | |
| 甲 | BaCl2 | Fe | Cu(NO3)2 |
| 乙 | Fe2O3 | K2SO4 | H2SO4 |
| 丙 | Mg | NaOH | MgCl2 |
(1)第三组中有一种物质能与第
(2)第二组中有一种物质与第一组所有物质都不发生反应,但能与第三组中所有物质发生反应,其化学方程式分别为
①
②
③
您最近一年使用:0次
10 . 凡是养鱼的人都知道一种很不错的消毒剂,这就是被称为当今第四代消毒产品的二氧化氯。其属于A1级别安全高效消毒剂之一,并且可以在极低的浓度下对病菌有杀灭作用,功效显而易见。一起来看看它的使用方法吧。KClO3和浓盐酸在一定温度下反应生成黄绿色的易爆物二氧化氯。完成以下问题:
(1)请完成该化学方程式并配平(未知物化学式和系数填入框内)_________ 。
□KClO3+□HCl(浓)→□KCl+ClO2↑+Cl2+□_________
(2)浓盐酸在反应中显示出来的性质是_________ (填序号)。
①只有还原性②还原性和酸性③只有氧化性④氧化性和酸性
(3)每产生1分子Cl2,转移的电子为_________ 个。
(4)ClO2具有很强的氧化性,因此常被用作消毒剂,其消毒效率(以单位质量得到的电子数表示)是Cl2的_________ 倍(保留小数点后两位)。
(1)请完成该化学方程式并配平(未知物化学式和系数填入框内)
□KClO3+□HCl(浓)→□KCl+ClO2↑+Cl2+□_________
(2)浓盐酸在反应中显示出来的性质是
①只有还原性②还原性和酸性③只有氧化性④氧化性和酸性
(3)每产生1分子Cl2,转移的电子为
(4)ClO2具有很强的氧化性,因此常被用作消毒剂,其消毒效率(以单位质量得到的电子数表示)是Cl2的
您最近一年使用:0次



