名校
1 . 卤族元素的单质和化合物在生产生活中有重要的用途。请回答:
(1)卤素元素位于元素周期表的___________ 区,溴原子的原子核外有___________ 种不同运动状态的电子,其M能层电子排布式为___________ 。
(2) 中心原子的杂化类型为
中心原子的杂化类型为___________ , 的空间构型为
的空间构型为___________ 。
(3)一定条件下 与
与 以物质的量之比为
以物质的量之比为 混舍得到一种固态离子化合物,其结构组成可能为:(a)
混舍得到一种固态离子化合物,其结构组成可能为:(a)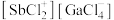 或(b)
或(b)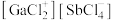 ,该离子化合物最可能的结构组成为
,该离子化合物最可能的结构组成为___________ (填“a”或“b”),理由是___________ 。
(4)在离子晶体中,当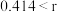 (阳离子)
(阳离子)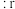 (阴离子)
(阴离子)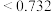 时,
时, 型化合物往往采用和
型化合物往往采用和 晶体相同的晶体结构(如下图1)。已知
晶体相同的晶体结构(如下图1)。已知 ,但在室温下,
,但在室温下, 的晶体结构如下图2所示,称为六方碘化银。
的晶体结构如下图2所示,称为六方碘化银。 的配位数为
的配位数为___________ ,造成 晶体结构不同于
晶体结构不同于 晶体结构的原因不可能是
晶体结构的原因不可能是___________ 。
a.几何因素 b.电荷因素 c.键性因素
若六方碘化银晶胞底边边长为 ,高为
,高为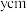 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,碘化银晶体的密度为
,碘化银晶体的密度为___________ 列出计算式。
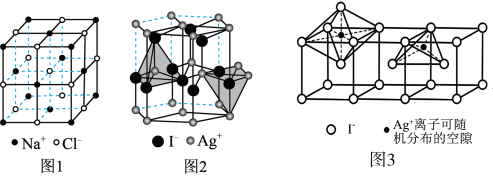
(5)当温度处于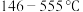 间时,六方碘化银转化为
间时,六方碘化银转化为 (如图3),
(如图3), 可随机地分布在四面体空隙和八面体空隙中,多面体空隙间又彼此共面相连,则在
可随机地分布在四面体空隙和八面体空隙中,多面体空隙间又彼此共面相连,则在 晶体中,
晶体中, (八面体空隙):n(四面体空隙)=
(八面体空隙):n(四面体空隙)=___________ 。
(1)卤素元素位于元素周期表的
(2)
 中心原子的杂化类型为
中心原子的杂化类型为 的空间构型为
的空间构型为(3)一定条件下
 与
与 以物质的量之比为
以物质的量之比为 混舍得到一种固态离子化合物,其结构组成可能为:(a)
混舍得到一种固态离子化合物,其结构组成可能为:(a)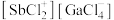 或(b)
或(b)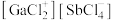 ,该离子化合物最可能的结构组成为
,该离子化合物最可能的结构组成为(4)在离子晶体中,当
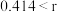 (阳离子)
(阳离子)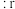 (阴离子)
(阴离子)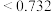 时,
时, 型化合物往往采用和
型化合物往往采用和 晶体相同的晶体结构(如下图1)。已知
晶体相同的晶体结构(如下图1)。已知 ,但在室温下,
,但在室温下, 的晶体结构如下图2所示,称为六方碘化银。
的晶体结构如下图2所示,称为六方碘化银。 的配位数为
的配位数为 晶体结构不同于
晶体结构不同于 晶体结构的原因不可能是
晶体结构的原因不可能是a.几何因素 b.电荷因素 c.键性因素
若六方碘化银晶胞底边边长为
 ,高为
,高为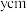 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,碘化银晶体的密度为
,碘化银晶体的密度为
(5)当温度处于
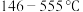 间时,六方碘化银转化为
间时,六方碘化银转化为 (如图3),
(如图3), 可随机地分布在四面体空隙和八面体空隙中,多面体空隙间又彼此共面相连,则在
可随机地分布在四面体空隙和八面体空隙中,多面体空隙间又彼此共面相连,则在 晶体中,
晶体中, (八面体空隙):n(四面体空隙)=
(八面体空隙):n(四面体空隙)=
您最近一年使用:0次
2 .  的固定和利用对降低温室气体排放具有重要作用,
的固定和利用对降低温室气体排放具有重要作用, 加氢合成甲醇不仅可以有效缓解减排压力,而且还是
加氢合成甲醇不仅可以有效缓解减排压力,而且还是 综合利用的一条新途径。
综合利用的一条新途径。 加氢过程,主要发生的两个竞争反应为:
加氢过程,主要发生的两个竞争反应为:
i.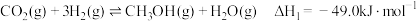
ii.
回答下列问题:
(1)由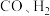 合成甲醇的热化学方程式为
合成甲醇的热化学方程式为___________ 。
(2)在某催化剂作用下, 和
和 除发生反应i外,还发生反应ii.维持压强不变,按固定初始投料比将
除发生反应i外,还发生反应ii.维持压强不变,按固定初始投料比将 和
和 按一定流速通过该催化剂,经过相同时间测得实验数据:
按一定流速通过该催化剂,经过相同时间测得实验数据:
注:甲醇的选择性是指发生反应的 中转化为甲醇的百分比。
中转化为甲醇的百分比。
表中数据说明,升高温度, 的实际转化率提高而甲醇的选择性降低,其原因是
的实际转化率提高而甲醇的选择性降低,其原因是___________ 。
(3)恒温恒压条件下(此时甲醇为气态),发生反应i(此时不考虑反应ii)。在开始为 的密闭容器中充入
的密闭容器中充入 和
和 ,达平衡时
,达平衡时 的转化率为50%,则反应i的
的转化率为50%,则反应i的
___________ 。
(4)反应i可能的反应历程下图所示。
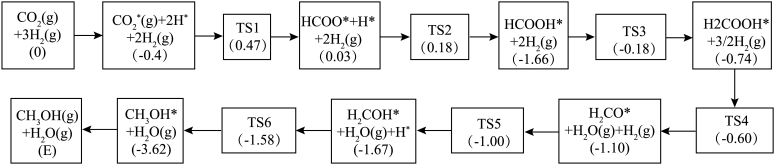
注:方框内包含微粒种类及数目、微粒的相对总能量(括号里的数字或字母,单位: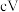 )。其中,
)。其中, 表示过渡态、*表示吸附在催化剂上的微粒。
表示过渡态、*表示吸附在催化剂上的微粒。
①反应历程中,生成甲醇的快速步骤的反应方程式为___________ 。
②相对总能量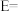
___________  (计算结果保留2位小数)。(已知:
(计算结果保留2位小数)。(已知: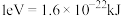 )
)
(5)以纳米二氧化钛膜为工作电极,稀硫酸为电解质溶液,在一定条件下通入 电解,在阴极可制得低密度聚乙烯
电解,在阴极可制得低密度聚乙烯 (简称
(简称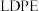 )。
)。
①电解时,阴极的电极反应式是___________ 。
②工业上生产 的
的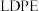 ,理论上需要标准状况下
,理论上需要标准状况下___________ L的 。
。
 的固定和利用对降低温室气体排放具有重要作用,
的固定和利用对降低温室气体排放具有重要作用, 加氢合成甲醇不仅可以有效缓解减排压力,而且还是
加氢合成甲醇不仅可以有效缓解减排压力,而且还是 综合利用的一条新途径。
综合利用的一条新途径。 加氢过程,主要发生的两个竞争反应为:
加氢过程,主要发生的两个竞争反应为:i.
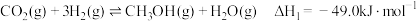
ii.

回答下列问题:
(1)由
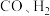 合成甲醇的热化学方程式为
合成甲醇的热化学方程式为(2)在某催化剂作用下,
 和
和 除发生反应i外,还发生反应ii.维持压强不变,按固定初始投料比将
除发生反应i外,还发生反应ii.维持压强不变,按固定初始投料比将 和
和 按一定流速通过该催化剂,经过相同时间测得实验数据:
按一定流速通过该催化剂,经过相同时间测得实验数据: |  实际转化率(%) 实际转化率(%) | 甲醇选择性(%) |
| 673 | 22.3 | 63.2 |
| 773 | 25.7 | 49.1 |
 中转化为甲醇的百分比。
中转化为甲醇的百分比。表中数据说明,升高温度,
 的实际转化率提高而甲醇的选择性降低,其原因是
的实际转化率提高而甲醇的选择性降低,其原因是(3)恒温恒压条件下(此时甲醇为气态),发生反应i(此时不考虑反应ii)。在开始为
 的密闭容器中充入
的密闭容器中充入 和
和 ,达平衡时
,达平衡时 的转化率为50%,则反应i的
的转化率为50%,则反应i的
(4)反应i可能的反应历程下图所示。

注:方框内包含微粒种类及数目、微粒的相对总能量(括号里的数字或字母,单位:
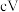 )。其中,
)。其中, 表示过渡态、*表示吸附在催化剂上的微粒。
表示过渡态、*表示吸附在催化剂上的微粒。①反应历程中,生成甲醇的快速步骤的反应方程式为
②相对总能量
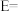
 (计算结果保留2位小数)。(已知:
(计算结果保留2位小数)。(已知: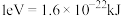 )
)(5)以纳米二氧化钛膜为工作电极,稀硫酸为电解质溶液,在一定条件下通入
 电解,在阴极可制得低密度聚乙烯
电解,在阴极可制得低密度聚乙烯 (简称
(简称 )。
)。①电解时,阴极的电极反应式是
②工业上生产
 的
的 ,理论上需要标准状况下
,理论上需要标准状况下 。
。
您最近一年使用:0次
名校
3 . 草酸 及其化合广泛分布于动植物体中。
及其化合广泛分布于动植物体中。
Ⅰ.某实验小组用灼烧检验法对菠菜中的铁元素(主要以难溶的 形式存在)进行检测。
形式存在)进行检测。
实验如下:
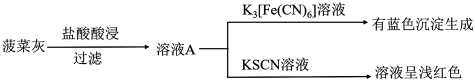
(1)灼烧菠菜时应将其放在___________ (填仪器名称)中加热。
(2)写出菠菜灰加盐酸酸浸时发生的主要离子方程式___________ 。
(3)甲同学取少量溶液A,滴加酸性 溶液,振荡后,溶液紫色消失,因此得出结论,溶液A含有
溶液,振荡后,溶液紫色消失,因此得出结论,溶液A含有 ,乙同学认为甲同学的实验方法不严谨,理由是
,乙同学认为甲同学的实验方法不严谨,理由是___________ 。
Ⅱ.草酸晶体的组成可表示为 。为测定草酸晶体中草酸的质量分数,进行下列实验。
。为测定草酸晶体中草酸的质量分数,进行下列实验。
①称取 草酸晶体,配成
草酸晶体,配成 溶液。
溶液。
②取 所配草酸溶液放入于锥形瓶中,加入适量稀
所配草酸溶液放入于锥形瓶中,加入适量稀 后,用浓度为
后,用浓度为 溶液滴定。请回答下列问题:
溶液滴定。请回答下列问题:
(4)本实验滴定过程中操作滴定管的图示正确的是___________ (填编号)。
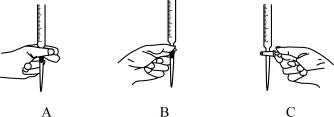
(5)判断达到滴定终点的现象是___________ 。
(6)若滴定时,滴定前后两次读数分别为 和
和 ,由此计算出草酸晶体中草酸的质量分数为
,由此计算出草酸晶体中草酸的质量分数为___________ 。若读取读数a时仰视,读取读数b时俯视,则所测得草酸的质量分数___________ (选填“偏大”、“偏小”或“不变”)。
Ⅲ.
(7)25℃时,用 溶液滴定
溶液滴定 溶液,溶液中
溶液,溶液中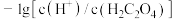 和
和 或
或 和
和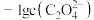 关系如图所示,下列说法正确的是________(填选项)。
关系如图所示,下列说法正确的是________(填选项)。

 及其化合广泛分布于动植物体中。
及其化合广泛分布于动植物体中。Ⅰ.某实验小组用灼烧检验法对菠菜中的铁元素(主要以难溶的
 形式存在)进行检测。
形式存在)进行检测。实验如下:

(1)灼烧菠菜时应将其放在
(2)写出菠菜灰加盐酸酸浸时发生的主要离子方程式
(3)甲同学取少量溶液A,滴加酸性
 溶液,振荡后,溶液紫色消失,因此得出结论,溶液A含有
溶液,振荡后,溶液紫色消失,因此得出结论,溶液A含有 ,乙同学认为甲同学的实验方法不严谨,理由是
,乙同学认为甲同学的实验方法不严谨,理由是Ⅱ.草酸晶体的组成可表示为
 。为测定草酸晶体中草酸的质量分数,进行下列实验。
。为测定草酸晶体中草酸的质量分数,进行下列实验。①称取
 草酸晶体,配成
草酸晶体,配成 溶液。
溶液。②取
 所配草酸溶液放入于锥形瓶中,加入适量稀
所配草酸溶液放入于锥形瓶中,加入适量稀 后,用浓度为
后,用浓度为 溶液滴定。请回答下列问题:
溶液滴定。请回答下列问题:(4)本实验滴定过程中操作滴定管的图示正确的是

(5)判断达到滴定终点的现象是
(6)若滴定时,滴定前后两次读数分别为
 和
和 ,由此计算出草酸晶体中草酸的质量分数为
,由此计算出草酸晶体中草酸的质量分数为Ⅲ.
(7)25℃时,用
 溶液滴定
溶液滴定 溶液,溶液中
溶液,溶液中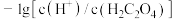 和
和 或
或 和
和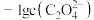 关系如图所示,下列说法正确的是________(填选项)。
关系如图所示,下列说法正确的是________(填选项)。
A.曲线L1表示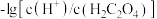 和 和 的关系 的关系 |
B. 的数量级为 的数量级为 |
C. 溶液中 溶液中 |
D.向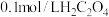 溶液中加入少量水,则 溶液中加入少量水,则 减小 减小 |
您最近一年使用:0次
名校
解题方法
4 . 芳香烃A是合成一种常用的塑料的单体, 芳香烃A最多能与
芳香烃A最多能与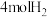 发生加成反应,B分子式为
发生加成反应,B分子式为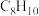 ,G能与
,G能与 溶液反应。某泾类衍生物X的分子式为
溶液反应。某泾类衍生物X的分子式为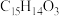 ,能使
,能使 溶液显色。K分子内有两个互为对位的取代基。在一定条件下各物质间有如下的转化关系(部分反应物略去),请回答:
溶液显色。K分子内有两个互为对位的取代基。在一定条件下各物质间有如下的转化关系(部分反应物略去),请回答:
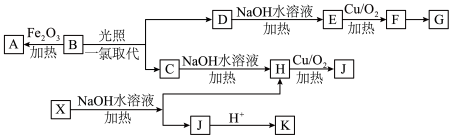
(1)A物质的名称为________ ,以A为单体合成的高分子化合物的结构简式为_________ 。
(2)B生成A的反应类型为___________ ,写出核磁共振谱图中只有2个特征峰的B的同分异构体的结构简式___________ 。
(3)G和H发生反应的类型为___________ ;X的结构简式为___________ ;K中所含的含氧官能团的名称为___________ 。
(4)H到I反应的化学方程式是___________ 。
(5)E的同分异构体有多种,其中含有苯环的有___________ 种,其中一种苯环上有两个取代基,且处于对位,该物质能与甲醛反应制备一种酚醛树脂,写出化学方程式___________ 。
 芳香烃A最多能与
芳香烃A最多能与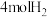 发生加成反应,B分子式为
发生加成反应,B分子式为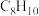 ,G能与
,G能与 溶液反应。某泾类衍生物X的分子式为
溶液反应。某泾类衍生物X的分子式为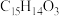 ,能使
,能使 溶液显色。K分子内有两个互为对位的取代基。在一定条件下各物质间有如下的转化关系(部分反应物略去),请回答:
溶液显色。K分子内有两个互为对位的取代基。在一定条件下各物质间有如下的转化关系(部分反应物略去),请回答:
(1)A物质的名称为
(2)B生成A的反应类型为
(3)G和H发生反应的类型为
(4)H到I反应的化学方程式是
(5)E的同分异构体有多种,其中含有苯环的有
您最近一年使用:0次
名校
解题方法
5 . 高纯活性氧化锌可用于光催化、光电极、彩色显影等领域。以工业级氧化锌(含 等)为原料,用硫酸浸出法生产高纯活性氧化锌的工艺流程如下:
等)为原料,用硫酸浸出法生产高纯活性氧化锌的工艺流程如下: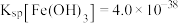 。
。
回答下列问题:
(1)浸出时,为了提高浸出效率可采取的措施有(写两种):___________ 。
(2)氧化时,加入 溶液是为了将浸出液中的
溶液是为了将浸出液中的 和
和 均转化为沉淀而除去,(溶液中
均转化为沉淀而除去,(溶液中 元素全部转化为
元素全部转化为 ),请分别写出
),请分别写出 除去
除去 和
和 的离子方程式
的离子方程式___________ ,___________ 。
(3)加入锌粉的目的是___________ 。
(4)已知 浸出液中,
浸出液中, 、
、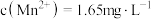 。
。
①若要除尽 上述浸出液中的
上述浸出液中的 和
和 ,需加入
,需加入___________ 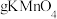 。
。
②加入 溶液反应一段时间后,溶液中
溶液反应一段时间后,溶液中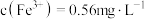 ,若溶液
,若溶液 ,则此时
,则此时
___________ (填“能”或“不能”)生成沉淀。
 等)为原料,用硫酸浸出法生产高纯活性氧化锌的工艺流程如下:
等)为原料,用硫酸浸出法生产高纯活性氧化锌的工艺流程如下: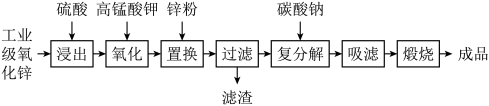
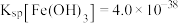 。
。回答下列问题:
(1)浸出时,为了提高浸出效率可采取的措施有(写两种):
(2)氧化时,加入
 溶液是为了将浸出液中的
溶液是为了将浸出液中的 和
和 均转化为沉淀而除去,(溶液中
均转化为沉淀而除去,(溶液中 元素全部转化为
元素全部转化为 ),请分别写出
),请分别写出 除去
除去 和
和 的离子方程式
的离子方程式(3)加入锌粉的目的是
(4)已知
 浸出液中,
浸出液中, 、
、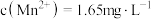 。
。①若要除尽
 上述浸出液中的
上述浸出液中的 和
和 ,需加入
,需加入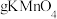 。
。②加入
 溶液反应一段时间后,溶液中
溶液反应一段时间后,溶液中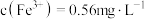 ,若溶液
,若溶液 ,则此时
,则此时
您最近一年使用:0次
2024-02-20更新
|
222次组卷
|
3卷引用:黑龙江省哈尔滨市第三中学校2020-2021学年高三上学期期末考试理科综合试卷-高中化学
黑龙江省哈尔滨市第三中学校2020-2021学年高三上学期期末考试理科综合试卷-高中化学(已下线)专题08 工艺流程综合题-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)江西省南昌十九中2023-2024学年高三下学期第一次模拟考试化学试卷
名校
解题方法
6 . 为了测定某有机物A的结构,某同学做了如下实验:
①将2.3 g该有机物完全燃烧,生成0.1 mol CO2和2.7 g水;
②用质谱仪测定其相对分子质量,得左图所示的质谱图;
③用核磁共振仪处理该化合物,得右图所示图谱,图中三个峰的面积之比是1:2:3。
试回答下列问题:

(1)有机物A的相对分子质量是___________ , 分子式为___________ 。
(2)有机物A与乙酸发生反应的方程式为___________ ,产物用装有___________ 溶液的试管接收。
(3)写出乙二酸和乙二醇发生缩聚反应的化学方程式___________ 。
(4)已知:CH2=CHCH3 CH2=CHCH2Cl,写出以丙烯为原料制备丙三醇的合成路线流程图(无机试剂任用)
CH2=CHCH2Cl,写出以丙烯为原料制备丙三醇的合成路线流程图(无机试剂任用)___________ 。 合成路线流程图示例如下:原料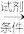 ∙∙∙∙∙∙
∙∙∙∙∙∙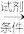 产物。
产物。
①将2.3 g该有机物完全燃烧,生成0.1 mol CO2和2.7 g水;
②用质谱仪测定其相对分子质量,得左图所示的质谱图;
③用核磁共振仪处理该化合物,得右图所示图谱,图中三个峰的面积之比是1:2:3。
试回答下列问题:

(1)有机物A的相对分子质量是
(2)有机物A与乙酸发生反应的方程式为
(3)写出乙二酸和乙二醇发生缩聚反应的化学方程式
(4)已知:CH2=CHCH3
 CH2=CHCH2Cl,写出以丙烯为原料制备丙三醇的合成路线流程图(无机试剂任用)
CH2=CHCH2Cl,写出以丙烯为原料制备丙三醇的合成路线流程图(无机试剂任用) ∙∙∙∙∙∙
∙∙∙∙∙∙ 产物。
产物。
您最近一年使用:0次
名校
解题方法
7 . 用乙烯与甲苯为主要原料,按下列路线合成一种香料W:

(1)已知实现反应①的试剂及条件为氯气、光照,则A是___________ ,C是___________ 。
(2)乙炔到氯乙烯的反应类型为___________ ,氯乙烯到聚氯乙烯的反应化学方程式为___________ 。
(3)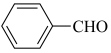 的官能团名称为
的官能团名称为_________ ,写出②的反应方程式_________ 。
(4)已知香料W是一种高分子化合物,下列还属于高分子化合物的有___________ ,能水解的有___________ 。
A.核酸 B.油脂 C.脱氧核糖 D.蛋白质

(1)已知实现反应①的试剂及条件为氯气、光照,则A是
(2)乙炔到氯乙烯的反应类型为
(3)
 的官能团名称为
的官能团名称为(4)已知香料W是一种高分子化合物,下列还属于高分子化合物的有
A.核酸 B.油脂 C.脱氧核糖 D.蛋白质
您最近一年使用:0次
名校
解题方法
8 . 兴趣小组围绕乙醇的性质进行了探究。请完成下列问题:
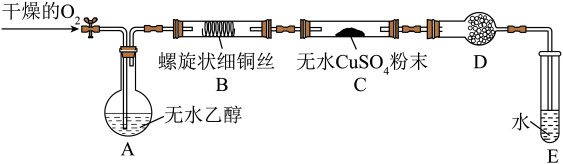
已知:乙醇的沸点为78°C,易溶于水;乙醛的沸点为20.8°C,易溶于水。
(1)乙醇发生催化氧化反应的化学方程式为___________ 。
(2)实验时上述装置需要加热,其中应该首先加热的是装置___________ (填字母),为使装置A中的乙醇形成稳定的蒸气,适宜的加热方法是___________ 。
(3)实验开始后,间歇性地通入氧气,装置B中观察到的现象是___________ 。
(4)装置C的作用是___________ ,若去掉装置D,对该实验是否有影响?__________ (填“是”或“否”),原因是___________ 。

已知:乙醇的沸点为78°C,易溶于水;乙醛的沸点为20.8°C,易溶于水。
(1)乙醇发生催化氧化反应的化学方程式为
(2)实验时上述装置需要加热,其中应该首先加热的是装置
(3)实验开始后,间歇性地通入氧气,装置B中观察到的现象是
(4)装置C的作用是
您最近一年使用:0次
名校
解题方法
9 . 二甲醚(DME)被誉为“21世纪的清洁燃料”,由合成气制备二甲醚的主要原理如下:
①CO(g)+2H2(g) CH3OH(g) ΔH1=-90.7 kJ·mol-1 K1
CH3OH(g) ΔH1=-90.7 kJ·mol-1 K1
②2CH3OH(g) CH3OCH3(g)+H2O(g) ΔH2=-23.5 kJ·mol-1 K2
CH3OCH3(g)+H2O(g) ΔH2=-23.5 kJ·mol-1 K2
③CO(g)+H2O(g) CO2(g)+H2(g) ΔH3=-41.2 kJ·mol-1 K3
CO2(g)+H2(g) ΔH3=-41.2 kJ·mol-1 K3
回答下列问题:
(1)反应3H2(g)+3CO(g) CH3OCH3(g)+CO2(g)的ΔH=
CH3OCH3(g)+CO2(g)的ΔH=___________ kJ·mol-1;该反应的平衡常数K=___________ (用K1、K2、K3表示)。
(2)下列措施中,能提高(1)中CH3OCH3产率的有___________ 。
A.使用过量的CO B.升高温度 C.增大压强
(3)一定温度下,将0.2 mol CO和0.1 mol H2O(g)通入2 L恒容密闭容器中,发生反应③,5 min后达到化学平衡,平衡后测得H2的体积分数为0.1.则0~5 min内v(H2O)=___________ ,CO的转化率α(CO)=___________ 。
(4)将合成气以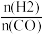 =2通入1 L的反应器中,一定条件下发生反应:4H2(g)+2CO(g)
=2通入1 L的反应器中,一定条件下发生反应:4H2(g)+2CO(g) CH3OCH3(g)+H2O(g) ΔH,其中CO的平衡转化率随温度、压强的变化关系如图1所示,下列说法正确的是
CH3OCH3(g)+H2O(g) ΔH,其中CO的平衡转化率随温度、压强的变化关系如图1所示,下列说法正确的是___________ (填字母)。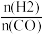 =3,则平衡时,α(CO)小于50%
=3,则平衡时,α(CO)小于50%
(5)采用一种新型的催化剂(主要成分是CuMn的合金),利用CO和H2制备二甲醚(DME)。观察图2,当 约为
约为___________ 时最有利于二甲醚的合成。
①CO(g)+2H2(g)
 CH3OH(g) ΔH1=-90.7 kJ·mol-1 K1
CH3OH(g) ΔH1=-90.7 kJ·mol-1 K1②2CH3OH(g)
 CH3OCH3(g)+H2O(g) ΔH2=-23.5 kJ·mol-1 K2
CH3OCH3(g)+H2O(g) ΔH2=-23.5 kJ·mol-1 K2③CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH3=-41.2 kJ·mol-1 K3
CO2(g)+H2(g) ΔH3=-41.2 kJ·mol-1 K3回答下列问题:
(1)反应3H2(g)+3CO(g)
 CH3OCH3(g)+CO2(g)的ΔH=
CH3OCH3(g)+CO2(g)的ΔH=(2)下列措施中,能提高(1)中CH3OCH3产率的有
A.使用过量的CO B.升高温度 C.增大压强
(3)一定温度下,将0.2 mol CO和0.1 mol H2O(g)通入2 L恒容密闭容器中,发生反应③,5 min后达到化学平衡,平衡后测得H2的体积分数为0.1.则0~5 min内v(H2O)=
(4)将合成气以
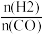 =2通入1 L的反应器中,一定条件下发生反应:4H2(g)+2CO(g)
=2通入1 L的反应器中,一定条件下发生反应:4H2(g)+2CO(g) CH3OCH3(g)+H2O(g) ΔH,其中CO的平衡转化率随温度、压强的变化关系如图1所示,下列说法正确的是
CH3OCH3(g)+H2O(g) ΔH,其中CO的平衡转化率随温度、压强的变化关系如图1所示,下列说法正确的是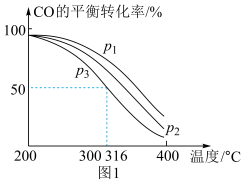
 =3,则平衡时,α(CO)小于50%
=3,则平衡时,α(CO)小于50%(5)采用一种新型的催化剂(主要成分是CuMn的合金),利用CO和H2制备二甲醚(DME)。观察图2,当
 约为
约为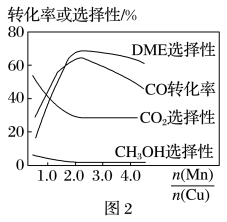
您最近一年使用:0次
2023-09-29更新
|
221次组卷
|
16卷引用:黑龙江省八校2021-2022学年高二上学期期中联合考试化学试题
黑龙江省八校2021-2022学年高二上学期期中联合考试化学试题吉林省长春外国语学校2021-2022学年高二上学期第一次月考化学试题山西省吕梁市柳林县2021-2022学年高二上学期期中考试化学试题黑龙江省佳木斯市第一中学2023-2024学年高二上学期10月月考化学试题山东省师范大学附属中学2019-2020学年高二上学期第五次学分认定考试化学试题山东省实验中学2019-2020学年高二上学期期中考试化学试题辽宁省六校协作体2020-2021学年高二上学期期中联考化学试题辽宁省铁岭市六校协作体2021-2022学年高一下学期期末联考化学试题第二章化学反应速率与化学平衡湖南省衡阳市田家炳实验中学2022-2023学年高二上学期9月月考化学试题重庆市璧山来凤中学2023-2024学年高二上学期9月月考化学试题广东省深圳市南山为明学校2023-2024学年高二上学期期中考试化学试题广东省深圳市罗湖外语学校2023-2024学年高二上学期期中考试化学试题陕西省西安市铁一中学2023-2024学年高二上学期期末考试化学试题湖南省长沙市周南中学2023-2024学年高二下学期第一次月考化学试题云南省下关第一中学2023-2024学年高二下学期5月期中考试化学试题
10 . 在实验室里制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计下列实验图以确认上述混合气体中有C2H4和SO2。回答下列问题:

(1)I、II、III、IV装置可盛放的试剂是:I___________ ;II___________ ;III___________ ;IV___________ (将下列有关试剂的序号填入空格内)。
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液
(2)能说明SO2气体存在的现象是___________ 。
(3)使用装置II的目的是___________ 。
(4)使用装置III的目的是___________ 。
(5)确定含有乙烯的现象是___________ 。

(1)I、II、III、IV装置可盛放的试剂是:I
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液
(2)能说明SO2气体存在的现象是
(3)使用装置II的目的是
(4)使用装置III的目的是
(5)确定含有乙烯的现象是
您最近一年使用:0次
2023-06-29更新
|
69次组卷
|
18卷引用:黑龙江省双鸭山市第一中学2020-2021学年高二下学期4月月考化学试题
黑龙江省双鸭山市第一中学2020-2021学年高二下学期4月月考化学试题黑龙江省大兴安岭地区漠河县第一中学2018-2019学年高二上学期第一次月考化学试题云南省元阳县一中2020-2021学年高一下学期6月份考试化学试题(已下线)2012年人教版高中化学选修5 2.1脂肪烃练习卷(已下线)2014年高一化学人教版必修2 3.2.1乙烯练习卷内蒙古北京八中乌兰察布分校2016-2017学年高一下学期第二次调考化学试题高二人教版选修5 第三章 烃的含氧衍生物 第一节 醇酚云南省绥江县一中2018-2019学年高一下学期期末考试化学试题吉林省公主岭市范家屯镇第一中学2019-2020学年高二上学期第二次月考化学试题课时1 石油的炼制 乙烯——A学习区 夯实基础(鲁科版必修2)课时1 甲烷 石油的炼制与乙烯——A学习区 夯实基础(鲁科版(2019)第二册)山东省德州市齐河县实验中学2019-2020学年高一下学期期中考试化学试题福建省莆田第七中学2020-2021学年高二上学期第一次月考化学试题上海市奉城高级中学2018-2019学年高二上学期期末考试化学试题安徽省安庆桐城市第八中学2020-2021学年高二上学期第一次段考化学试题陕西省西安市蓝田县大学区联考2022-2023学年高二下学期6月期末考试化学试题2.1.1有机化学反应的主要类型(课前)-鲁科版选择性必修3陕西省西安市蓝田县大学区联考2022-2023学年高二下学期4月期中考试化学试题



