1 . 唑草酮是一种广谱除草剂,在农业上应用范围比较广,除草效果比较好。唑草酮的一种合成路线如下图。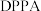 是一种叠氮化试剂。
是一种叠氮化试剂。
回答下列问题:
(1)C中官能团的名称为___________ 。
(2)由A生成C的反应类型为___________ ,该反应的目的是___________ 。
(3) 的化学方程式为
的化学方程式为___________ 。
(4)已知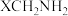 中
中 键的极性越大,则
键的极性越大,则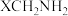 的碱性越弱。下列物质的碱性由强到弱的顺序为
的碱性越弱。下列物质的碱性由强到弱的顺序为___________ (填标号)。___________ 种。
①含有苯环,且苯环上有3个取代基
②能发生银镜反应
③含有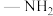
(6)化合物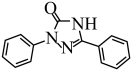 的合成路线如下图(部分反应条件已略去),其中M和N的结构简式分别为
的合成路线如下图(部分反应条件已略去),其中M和N的结构简式分别为___________ 和___________ 。

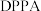 是一种叠氮化试剂。
是一种叠氮化试剂。回答下列问题:
(1)C中官能团的名称为
(2)由A生成C的反应类型为
(3)
 的化学方程式为
的化学方程式为(4)已知
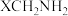 中
中 键的极性越大,则
键的极性越大,则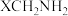 的碱性越弱。下列物质的碱性由强到弱的顺序为
的碱性越弱。下列物质的碱性由强到弱的顺序为a. 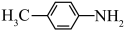 b.
b. 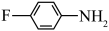 c.
c.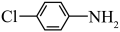
①含有苯环,且苯环上有3个取代基
②能发生银镜反应
③含有
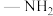
(6)化合物
 的合成路线如下图(部分反应条件已略去),其中M和N的结构简式分别为
的合成路线如下图(部分反应条件已略去),其中M和N的结构简式分别为
您最近一年使用:0次
解题方法
2 . 铁的化合物在工业生产中具有重要的应用。以硅酸铁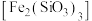 作为载氧体实现甲烷部分氧化,发生的主要反应有:
作为载氧体实现甲烷部分氧化,发生的主要反应有:
i. ;
;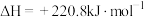
ii. ;
;
iii.
iv.
回答下列问题:
(1)在元素周期表中,Fe元素位于___________ 区(填“s”“p”“d”或“ds”)。
(2)反应i___________ (填“能”或“不能”)在高温条件下自发进行。反应ii的正反应活化能___________ (填“大于”“小于”或“等于”)逆反应活化能。
(3)反应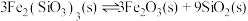 的
的
___________  。
。
(4)在恒温恒容条件下,仅发生反应i,下列说法不能表明反应i已达到化学平衡的是___________(填标号)。
(5)载氧体 为
为 转化为氧化物提供氧原子,
转化为氧化物提供氧原子, 与
与 物质的量之比
物质的量之比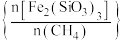 是影响
是影响 转化为合成气
转化为合成气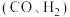 的重要因素。在
的重要因素。在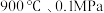 下,向密闭容器投入
下,向密闭容器投入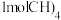 发生上述反应,不同
发生上述反应,不同 对部分物种的平衡量的影响如图所示。
对部分物种的平衡量的影响如图所示。 的选择性(S)公式如下:
的选择性(S)公式如下: ,
, 。
。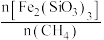 值为
值为___________ (填标号)。
A.1.5 B.0.45 C.0.38 D.0.3
②当 平衡转化率为98%时,测得体系中
平衡转化率为98%时,测得体系中 ,则
,则
___________ %(保留1位小数)。
(6)在恒压密闭容器中,加入甲烷和水蒸气各 ,一定条件下发生反应:
,一定条件下发生反应: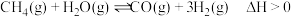 。测得平衡时
。测得平衡时 的体积分数与温度、压强的关系如图所示。
的体积分数与温度、压强的关系如图所示。
___________  (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。
②温度为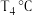 、压强为,
、压强为,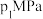 时,N点表示的正、逆反应速率
时,N点表示的正、逆反应速率
___________ 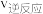 (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。
③ 时该反应的压强平衡常数
时该反应的压强平衡常数
___________  (用含
(用含 的代数式表示)。
的代数式表示)。
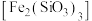 作为载氧体实现甲烷部分氧化,发生的主要反应有:
作为载氧体实现甲烷部分氧化,发生的主要反应有:i.
 ;
;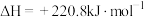
ii.
 ;
;
iii.

iv.

回答下列问题:
(1)在元素周期表中,Fe元素位于
(2)反应i
(3)反应
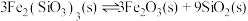 的
的
 。
。(4)在恒温恒容条件下,仅发生反应i,下列说法不能表明反应i已达到化学平衡的是___________(填标号)。
A.相同时间内,气态反应物有 键断裂的同时气态产物有 键断裂的同时气态产物有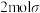 键生成 键生成 |
| B.容器中气体的密度不再变化 |
| C.固体中所含氧元素的质量分数不再变化 |
| D.容器中气体的平均相对分子质量不再变化 |
(5)载氧体
 为
为 转化为氧化物提供氧原子,
转化为氧化物提供氧原子, 与
与 物质的量之比
物质的量之比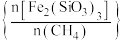 是影响
是影响 转化为合成气
转化为合成气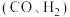 的重要因素。在
的重要因素。在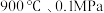 下,向密闭容器投入
下,向密闭容器投入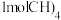 发生上述反应,不同
发生上述反应,不同 对部分物种的平衡量的影响如图所示。
对部分物种的平衡量的影响如图所示。 的选择性(S)公式如下:
的选择性(S)公式如下: ,
, 。
。
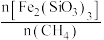 值为
值为A.1.5 B.0.45 C.0.38 D.0.3
②当
 平衡转化率为98%时,测得体系中
平衡转化率为98%时,测得体系中 ,则
,则
(6)在恒压密闭容器中,加入甲烷和水蒸气各
 ,一定条件下发生反应:
,一定条件下发生反应: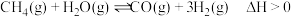 。测得平衡时
。测得平衡时 的体积分数与温度、压强的关系如图所示。
的体积分数与温度、压强的关系如图所示。

 (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。②温度为
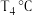 、压强为,
、压强为,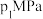 时,N点表示的正、逆反应速率
时,N点表示的正、逆反应速率
 (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。③
 时该反应的压强平衡常数
时该反应的压强平衡常数
 (用含
(用含 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解题方法
3 . 高铁酸盐是一种优良的净水剂。实验室合成高铁酸钾( )的过程如图所示:
)的过程如图所示:
回答下列问题:
(1)Fe位于元素周期表第___________ 周期第___________ 族, 中Fe的化合价为
中Fe的化合价为___________ 。
(2)“反应1”中氧化剂与还原剂的物质的量之比为___________ 。
(3)“洗气”操作可选用的装置为___________ (填字母)。___________ (填化学式)。从饱和KOH溶液中得到白色沉淀b需要使用的玻璃仪器为___________ 。
(5)“反应2”发生主要反应的化学方程式为___________ 。
(6)高铁酸盐还可用电解法制备。利用纯铁作电极插入浓的NaOH溶液电解制得 的工作原理如图所示。
的工作原理如图所示。 的电极反应式为
的电极反应式为___________ 。
②对装置进行改进,在阴、阳电极间设置阳离子交换膜,能有效提高 产率,离子交换膜的作用是
产率,离子交换膜的作用是___________ 。
 )的过程如图所示:
)的过程如图所示: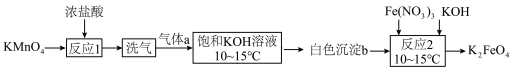
回答下列问题:
(1)Fe位于元素周期表第
 中Fe的化合价为
中Fe的化合价为(2)“反应1”中氧化剂与还原剂的物质的量之比为
(3)“洗气”操作可选用的装置为

(5)“反应2”发生主要反应的化学方程式为
(6)高铁酸盐还可用电解法制备。利用纯铁作电极插入浓的NaOH溶液电解制得
 的工作原理如图所示。
的工作原理如图所示。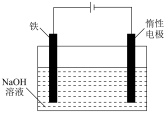
 的电极反应式为
的电极反应式为②对装置进行改进,在阴、阳电极间设置阳离子交换膜,能有效提高
 产率,离子交换膜的作用是
产率,离子交换膜的作用是
您最近一年使用:0次
名校
解题方法
4 . 全球首个批准上市的CDK4/6激酶抑制剂-帕博西尼(N)的合成路线如下,已知Boc-的结构简式为
(1)N中含氧官能团的名称为___________ ,核磁共振氢谱有___________ 组吸收峰。
(2) 的化学方程式为
的化学方程式为___________ 。
(3)物质D为存在顺反异构的羧酸,写出D的结构简式___________ 。 的过程分两步进行且反应类型相同,该过程的反应类型为
的过程分两步进行且反应类型相同,该过程的反应类型为___________ 。
(4) 生成H的两种反应机理如下:
生成H的两种反应机理如下:___________ 。
①能发生银镜反应 ②含有3种不同化学环境的氢原子


(1)N中含氧官能团的名称为
(2)
 的化学方程式为
的化学方程式为(3)物质D为存在顺反异构的羧酸,写出D的结构简式
 的过程分两步进行且反应类型相同,该过程的反应类型为
的过程分两步进行且反应类型相同,该过程的反应类型为(4)
 生成H的两种反应机理如下:
生成H的两种反应机理如下: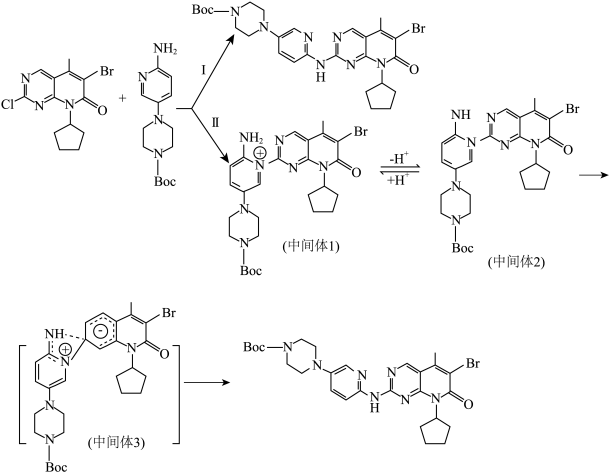
中间体2与H的关系为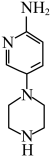 ,结合以上反应机理及最终产物N解释原因
,结合以上反应机理及最终产物N解释原因
①能发生银镜反应 ②含有3种不同化学环境的氢原子
您最近一年使用:0次
5 . 氮氧化物( 、NO等)的处理和资源化利用具有重要意义。
、NO等)的处理和资源化利用具有重要意义。
(1)反应 分为三步基元反应完成。
分为三步基元反应完成。
第一步: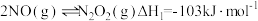 决速步骤)
决速步骤)
第二步: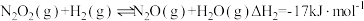
①活化能最高的是第___________ 步。
②为了提高总反应中NO的反应速率和转化率可采用的措施为___________ (写两条)。
(2)已知反应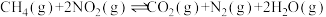 。某温度下向2.0L刚性密闭容器中充入
。某温度下向2.0L刚性密闭容器中充入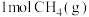 和
和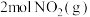 ,发生该反应,测得容器内气体总压强(p)与时间(t)的变化如下表所示:
,发生该反应,测得容器内气体总压强(p)与时间(t)的变化如下表所示:
①用 表示0~4min内平均反应速率为
表示0~4min内平均反应速率为___________ 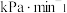 。
。
②该温度下的压强平衡常数
___________ kPa。
(3)NO催化分解ICl制取 和
和 的原理为:
的原理为:
反应I: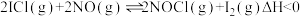 ;
;
反应Ⅱ: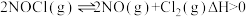 ;
; 。
。
反应的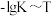 的关系如图所示。
的关系如图所示。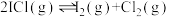 的
的
___________
(4)催化电解NO吸收液可生成多种物质,其中将NO还原为 的催化机理如图甲所示。在相同条件下,恒定通过电解池的电量,电解得到部分还原产物的法拉第效率(FE%,法拉第效率之比等于转移电子的物质的量之比)随电解电压的变化如图乙所示。
的催化机理如图甲所示。在相同条件下,恒定通过电解池的电量,电解得到部分还原产物的法拉第效率(FE%,法拉第效率之比等于转移电子的物质的量之比)随电解电压的变化如图乙所示。 的电极反应式为
的电极反应式为___________ 。
②当电解电压为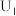 时,电解生成的
时,电解生成的 和
和 的物质的量之比为
的物质的量之比为___________ 。
 、NO等)的处理和资源化利用具有重要意义。
、NO等)的处理和资源化利用具有重要意义。(1)反应
 分为三步基元反应完成。
分为三步基元反应完成。第一步:
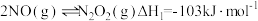 决速步骤)
决速步骤)第二步:
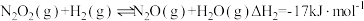
①活化能最高的是第
②为了提高总反应中NO的反应速率和转化率可采用的措施为
(2)已知反应
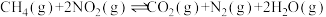 。某温度下向2.0L刚性密闭容器中充入
。某温度下向2.0L刚性密闭容器中充入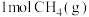 和
和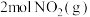 ,发生该反应,测得容器内气体总压强(p)与时间(t)的变化如下表所示:
,发生该反应,测得容器内气体总压强(p)与时间(t)的变化如下表所示:| 反应时间(t)/min | 0 | 2 | 4 | 6 | 8 | 10 |
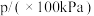 | 4.80 | 5.44 | 5.76 | 5.92 | 6.00 | 6.00 |
 表示0~4min内平均反应速率为
表示0~4min内平均反应速率为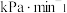 。
。②该温度下的压强平衡常数

(3)NO催化分解ICl制取
 和
和 的原理为:
的原理为:反应I:
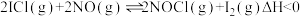 ;
;
反应Ⅱ:
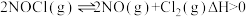 ;
; 。
。反应的
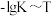 的关系如图所示。
的关系如图所示。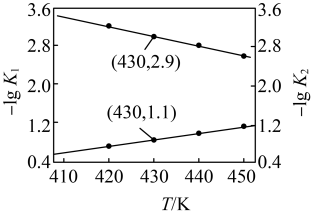
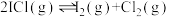 的
的
(4)催化电解NO吸收液可生成多种物质,其中将NO还原为
 的催化机理如图甲所示。在相同条件下,恒定通过电解池的电量,电解得到部分还原产物的法拉第效率(FE%,法拉第效率之比等于转移电子的物质的量之比)随电解电压的变化如图乙所示。
的催化机理如图甲所示。在相同条件下,恒定通过电解池的电量,电解得到部分还原产物的法拉第效率(FE%,法拉第效率之比等于转移电子的物质的量之比)随电解电压的变化如图乙所示。
 的电极反应式为
的电极反应式为②当电解电压为
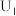 时,电解生成的
时,电解生成的 和
和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
名校
解题方法
6 . 山梨酸是国际上应用最广的防腐剂之一,实验室通过巴豆醛和丙酮缩合法制备山梨酸 反应原理:
反应原理:
③酸化反应
实验步骤:
①向三颈烧瓶中加入 丙酮、少量
丙酮、少量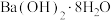 ,加热至丙酮出现回流时,在加热搅拌下缓慢滴入
,加热至丙酮出现回流时,在加热搅拌下缓慢滴入 巴豆醛。控制温度约为70℃、回流2.5h后停止反应,过滤、蒸馏得到巴豆烯叉丙酮。
巴豆醛。控制温度约为70℃、回流2.5h后停止反应,过滤、蒸馏得到巴豆烯叉丙酮。
②在室温下,将 溶液、20%
溶液、20% 溶液依次滴加到巴豆烯叉丙酮中,并不断搅拌直至有机相液体体积不再增大,停止搅拌,将混合液转入分液漏斗中,静置、分离得到山梨酸钠水溶液,再用
溶液依次滴加到巴豆烯叉丙酮中,并不断搅拌直至有机相液体体积不再增大,停止搅拌,将混合液转入分液漏斗中,静置、分离得到山梨酸钠水溶液,再用 处理水溶液中过量的
处理水溶液中过量的 。
。
③将质量分数为30%的稀 缓慢滴入山梨酸钠水溶液中,并不断搅拌至溶液
缓慢滴入山梨酸钠水溶液中,并不断搅拌至溶液 ,过滤、洗涤得山梨酸粗产品。
,过滤、洗涤得山梨酸粗产品。
④将适量蒸馏水加入粗产品中,加热溶解,冷却结晶,减压过滤,干燥后得到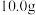 山梨酸。已知:
山梨酸。已知:
①山梨酸微溶于水,易溶于有机溶剂。易被强氧化剂HClO等氧化;
②部分有机物密度为:巴豆醛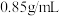 ,氯仿
,氯仿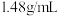 ,丙酮
,丙酮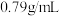 。
。
回答下列问题:
(1)步骤①分离出巴豆烯叉丙酮的装置如图1所示(加热及夹持装置省略),虚线框内连接的仪器为___________ (填名称),尾接管连接抽气泵的目的是___________ ,毛细管连通大气的主要作用是___________ 。___________ (填“a”或“b”)
(3)用 处理过量的
处理过量的 时反应的离子方程式为
时反应的离子方程式为___________ ;不可以在步骤③酸化后再加入 除去过量的
除去过量的 ,原因是
,原因是___________ 。
(4)步骤③中,检测洗涤是否完成的操作是___________ 。
(5)本实验中山梨酸的产率为___________ (保留3位有效数字)。
 反应原理:
反应原理:①缩合反应

③酸化反应

实验步骤:
①向三颈烧瓶中加入
 丙酮、少量
丙酮、少量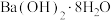 ,加热至丙酮出现回流时,在加热搅拌下缓慢滴入
,加热至丙酮出现回流时,在加热搅拌下缓慢滴入 巴豆醛。控制温度约为70℃、回流2.5h后停止反应,过滤、蒸馏得到巴豆烯叉丙酮。
巴豆醛。控制温度约为70℃、回流2.5h后停止反应,过滤、蒸馏得到巴豆烯叉丙酮。②在室温下,将
 溶液、20%
溶液、20% 溶液依次滴加到巴豆烯叉丙酮中,并不断搅拌直至有机相液体体积不再增大,停止搅拌,将混合液转入分液漏斗中,静置、分离得到山梨酸钠水溶液,再用
溶液依次滴加到巴豆烯叉丙酮中,并不断搅拌直至有机相液体体积不再增大,停止搅拌,将混合液转入分液漏斗中,静置、分离得到山梨酸钠水溶液,再用 处理水溶液中过量的
处理水溶液中过量的 。
。③将质量分数为30%的稀
 缓慢滴入山梨酸钠水溶液中,并不断搅拌至溶液
缓慢滴入山梨酸钠水溶液中,并不断搅拌至溶液 ,过滤、洗涤得山梨酸粗产品。
,过滤、洗涤得山梨酸粗产品。④将适量蒸馏水加入粗产品中,加热溶解,冷却结晶,减压过滤,干燥后得到
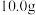 山梨酸。已知:
山梨酸。已知:①山梨酸微溶于水,易溶于有机溶剂。易被强氧化剂HClO等氧化;
②部分有机物密度为:巴豆醛
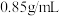 ,氯仿
,氯仿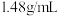 ,丙酮
,丙酮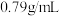 。
。回答下列问题:
(1)步骤①分离出巴豆烯叉丙酮的装置如图1所示(加热及夹持装置省略),虚线框内连接的仪器为

(3)用
 处理过量的
处理过量的 时反应的离子方程式为
时反应的离子方程式为 除去过量的
除去过量的 ,原因是
,原因是(4)步骤③中,检测洗涤是否完成的操作是
(5)本实验中山梨酸的产率为
您最近一年使用:0次
名校
解题方法
7 . CCTV在“新闻30分”中介绍:王者归“铼”,我国发现超级铁矿,飞机上天全靠它。铼(Re)是一种稀散金属,广泛应用于航空航天领域。工业上从高铼废料(含 等)中提取铼的一种工艺流程如图所示:
等)中提取铼的一种工艺流程如图所示: 。
。
回答下列问题:
(1)“焙烧”时,高铼废料粉末与富氧空气逆流混合的目的为___________ 。该工序中,ReS2发生反应的化学方程式为___________ 。
(2)其他条件相同时,“离子交换”过程中料液和D296体积比与铼交换率、铼交换量的变化关系如图1所示;混合溶液的pH与 提取率的变化关系如图2所示。
提取率的变化关系如图2所示。___________ 。
②其他条件相同,混合溶液的pH>1.5时, 的提取率降低的主要原因为
的提取率降低的主要原因为___________ 。
(3)“反萃取”时,选用的试剂X为盐酸的理由为___________ 。
(4)另一种途径从炼铜废液中来提取铼,其简易工艺流程如图,(部分副产物省略,铼在废液中以 形式存在):
形式存在):___________ 方法提纯高铼酸铵晶体。
(5)废料中的Ni元素经一系列操作可得到金属镍,金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图及晶胞参数如图所示。该晶体的化学式为___________ ;晶体密度为___________ g∙cm-3 (列出含a、b、NA的计算表达式,NA表示阿伏加德罗常数的值)。
 等)中提取铼的一种工艺流程如图所示:
等)中提取铼的一种工艺流程如图所示:
 。
。回答下列问题:
(1)“焙烧”时,高铼废料粉末与富氧空气逆流混合的目的为
(2)其他条件相同时,“离子交换”过程中料液和D296体积比与铼交换率、铼交换量的变化关系如图1所示;混合溶液的pH与
 提取率的变化关系如图2所示。
提取率的变化关系如图2所示。
②其他条件相同,混合溶液的pH>1.5时,
 的提取率降低的主要原因为
的提取率降低的主要原因为(3)“反萃取”时,选用的试剂X为盐酸的理由为
(4)另一种途径从炼铜废液中来提取铼,其简易工艺流程如图,(部分副产物省略,铼在废液中以
 形式存在):
形式存在):
(5)废料中的Ni元素经一系列操作可得到金属镍,金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图及晶胞参数如图所示。该晶体的化学式为

您最近一年使用:0次
8 . 无水三氯化铬( )是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧化。实验室利用反应
)是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧化。实验室利用反应 制取
制取 的
的 (俗称光气)有毒,遇水发生水解,实验所需装置如图所示。
(俗称光气)有毒,遇水发生水解,实验所需装置如图所示。
(1)上述装置的正确连接顺序为___________ (填字母,按气流方向从左到右)。
(2)装置A中所盛放的试剂是___________ ,装置A中竖直长玻璃管的作用是___________ 。装置D中n瓶的作用是___________ 。实验过程中为了避免装置A中长玻璃管中液面上升,可以采用的方法为___________ (填序号)。
①对m处导管进行加热 ②将m处导管加粗 ③持续通入氮气
(3)装置E中发生反应的离子方程式为___________ 。无水 的作用是
的作用是___________ 。
(4)已知 分子中各原子均满足最外层8电子稳定结构,则1mol
分子中各原子均满足最外层8电子稳定结构,则1mol 含有
含有 键的个数为
键的个数为___________ ( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(5) 的结构有三种,且铬的配位数均为6,等物质的量的三种物质电离出的氯离子数目之比为3∶2∶1,对应的颜色分别为紫色、浅绿色和蓝绿色。其中浅绿色的结构中配离子的化学式为
的结构有三种,且铬的配位数均为6,等物质的量的三种物质电离出的氯离子数目之比为3∶2∶1,对应的颜色分别为紫色、浅绿色和蓝绿色。其中浅绿色的结构中配离子的化学式为___________ 。哈勃-韦斯(Haber-Weiss)原理表明,某些金属离子可以催化双氧水分解的原因是其次外层未排满的d轨道可以存取电子,降低活化能,使分解反应容易发生。则
___________ (填“能”或“不能”)催化双氧水分解。
 )是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧化。实验室利用反应
)是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧化。实验室利用反应 制取
制取 的
的 (俗称光气)有毒,遇水发生水解,实验所需装置如图所示。
(俗称光气)有毒,遇水发生水解,实验所需装置如图所示。
(1)上述装置的正确连接顺序为
(2)装置A中所盛放的试剂是
①对m处导管进行加热 ②将m处导管加粗 ③持续通入氮气
(3)装置E中发生反应的离子方程式为
 的作用是
的作用是(4)已知
 分子中各原子均满足最外层8电子稳定结构,则1mol
分子中各原子均满足最外层8电子稳定结构,则1mol 含有
含有 键的个数为
键的个数为 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。(5)
 的结构有三种,且铬的配位数均为6,等物质的量的三种物质电离出的氯离子数目之比为3∶2∶1,对应的颜色分别为紫色、浅绿色和蓝绿色。其中浅绿色的结构中配离子的化学式为
的结构有三种,且铬的配位数均为6,等物质的量的三种物质电离出的氯离子数目之比为3∶2∶1,对应的颜色分别为紫色、浅绿色和蓝绿色。其中浅绿色的结构中配离子的化学式为
您最近一年使用:0次
9 . 无水 常用于合成媒染剂。实验室可用熔融的锡与氯气反应制备无水
常用于合成媒染剂。实验室可用熔融的锡与氯气反应制备无水 ,可选用的装置如图所示:
,可选用的装置如图所示:
i.熔融Sn与 反应生成
反应生成 (无色液体)时放出大量的热,
(无色液体)时放出大量的热, 熔点为-33℃,沸点为114℃,在潮湿空气中极易潮解(水解生成
熔点为-33℃,沸点为114℃,在潮湿空气中极易潮解(水解生成 ),且
),且 易溶于
易溶于 。
。
ii.Sn熔点为232℃;无水 熔点为246℃、沸点为652℃,具有强还原性。
熔点为246℃、沸点为652℃,具有强还原性。
回答下列问题:
(1)装置A中发生反应的化学方程式为___________ 。
(2)从平衡移动的角度解释 难溶于饱和食盐水的原因:
难溶于饱和食盐水的原因:___________ 。
(3)为了获得较纯的产品,当装置D处具支试管中___________ 时,再点燃装置D处酒精灯。反应制得的产品中可能会含有杂质 ,为加快反应速率并防止产品中混有
,为加快反应速率并防止产品中混有 ,除了通入过量
,除了通入过量 外,还应控制反应的最佳温度范围为
外,还应控制反应的最佳温度范围为___________ 。装置E的收集器中收集到的液体略显黄色,原因是___________ 。
(4)装置F的作用是___________ ;若缺少装置F,则装置E的收集器中发生反应的化学方程式为___________ 。
(5)碘氧化法滴定分析产品中 的含量。准确称取ag产品于锥形瓶中,用蒸馏水溶解,淀粉溶液作指示剂,用
的含量。准确称取ag产品于锥形瓶中,用蒸馏水溶解,淀粉溶液作指示剂,用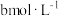 碘标准溶液滴定,发生反应:
碘标准溶液滴定,发生反应: 。滴定终点消耗碘标准溶液
。滴定终点消耗碘标准溶液 ,则产品中
,则产品中 的质量分数为
的质量分数为___________ (用含a、b、V的代数式表示)。
 常用于合成媒染剂。实验室可用熔融的锡与氯气反应制备无水
常用于合成媒染剂。实验室可用熔融的锡与氯气反应制备无水 ,可选用的装置如图所示:
,可选用的装置如图所示: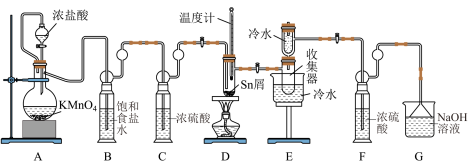
i.熔融Sn与
 反应生成
反应生成 (无色液体)时放出大量的热,
(无色液体)时放出大量的热, 熔点为-33℃,沸点为114℃,在潮湿空气中极易潮解(水解生成
熔点为-33℃,沸点为114℃,在潮湿空气中极易潮解(水解生成 ),且
),且 易溶于
易溶于 。
。ii.Sn熔点为232℃;无水
 熔点为246℃、沸点为652℃,具有强还原性。
熔点为246℃、沸点为652℃,具有强还原性。回答下列问题:
(1)装置A中发生反应的化学方程式为
(2)从平衡移动的角度解释
 难溶于饱和食盐水的原因:
难溶于饱和食盐水的原因:(3)为了获得较纯的产品,当装置D处具支试管中
 ,为加快反应速率并防止产品中混有
,为加快反应速率并防止产品中混有 ,除了通入过量
,除了通入过量 外,还应控制反应的最佳温度范围为
外,还应控制反应的最佳温度范围为(4)装置F的作用是
(5)碘氧化法滴定分析产品中
 的含量。准确称取ag产品于锥形瓶中,用蒸馏水溶解,淀粉溶液作指示剂,用
的含量。准确称取ag产品于锥形瓶中,用蒸馏水溶解,淀粉溶液作指示剂,用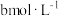 碘标准溶液滴定,发生反应:
碘标准溶液滴定,发生反应: 。滴定终点消耗碘标准溶液
。滴定终点消耗碘标准溶液 ,则产品中
,则产品中 的质量分数为
的质量分数为
您最近一年使用:0次
名校
解题方法
10 . 有机物M作为一种高性能发光材料,广泛用于有机电致发光器件(OLED)。M的一种合成路线如下所示,部分试剂及反应条件省略 的反应类型为
的反应类型为___________ ,G中所含官能团名称为___________ 。
(2)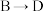 的化学反应方程式为
的化学反应方程式为___________ 。
(3)E的结构简式为___________ 。
(4)F与I反应除生成M外,另一种产物为___________ (填化学式)。
(5)G的同分异构体中,含有两个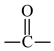 的化合物有
的化合物有___________ 种(不含G且不考虑立体异构),其中核磁共振氢谱有两组峰,且峰面积比为 的化合物为L,L与足量新制的
的化合物为L,L与足量新制的 反应的化学方程式为
反应的化学方程式为___________ 。
(6)以甲醇、苯胺和有机物Ⅰ为原料,利用上述合成路线中的相关试剂,合成另一种发光材料Q( )。制备Q的合成路线为
)。制备Q的合成路线为___________ 。
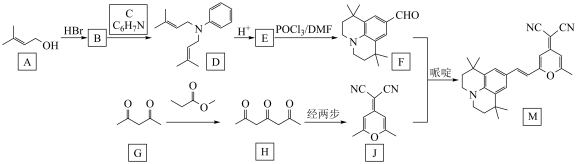
已知: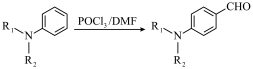 (R1和R2为烃基)。
(R1和R2为烃基)。
 的反应类型为
的反应类型为(2)
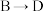 的化学反应方程式为
的化学反应方程式为(3)E的结构简式为
(4)F与I反应除生成M外,另一种产物为
(5)G的同分异构体中,含有两个
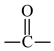 的化合物有
的化合物有 的化合物为L,L与足量新制的
的化合物为L,L与足量新制的 反应的化学方程式为
反应的化学方程式为(6)以甲醇、苯胺和有机物Ⅰ为原料,利用上述合成路线中的相关试剂,合成另一种发光材料Q(
 )。制备Q的合成路线为
)。制备Q的合成路线为
您最近一年使用:0次



