解题方法
1 . 回答下列问题:
(1)用活性炭可以还原处理氮氧化物,有关反应为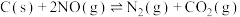 。在恒容条件下,能判断该反应一定达到化学平衡状态的依据是________(填标号)。
。在恒容条件下,能判断该反应一定达到化学平衡状态的依据是________(填标号)。
(2)有科学家经过研究发现,用 和
和 在210∼290℃,催化剂条件下可转化生成甲醇
在210∼290℃,催化剂条件下可转化生成甲醇 蒸气和水蒸气。一定条件下,往
蒸气和水蒸气。一定条件下,往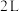 恒容密闭容器中充入
恒容密闭容器中充入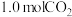 和
和 ,在不同催化剂作用下,反应相同时间内
,在不同催化剂作用下,反应相同时间内 的转化率随温度变化如图所示。催化剂效果最佳的是催化剂
的转化率随温度变化如图所示。催化剂效果最佳的是催化剂________ (填“Ⅰ”“Ⅰ”或“Ⅲ”)。 点
点 (正)
(正)________ (填“>”“<”或“=”) (逆)。此反应在
(逆)。此反应在 点时已达平衡状态,
点时已达平衡状态, 点的转化率比
点的转化率比 点高的原因是
点高的原因是________ 。 ,则图中
,则图中 点对应温度下反应的平衡常数
点对应温度下反应的平衡常数
________ ( 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。
(4)一定条件下, 和
和 也可以发生反应
也可以发生反应
 ,一定温度下,在
,一定温度下,在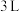 容积可变的密闭容器中,已知
容积可变的密闭容器中,已知 与反应时间
与反应时间 变化曲线如图所示,若在
变化曲线如图所示,若在 时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ或曲线Ⅲ。当曲线Ⅰ变为曲线Ⅱ时,改变的条件是
时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ或曲线Ⅲ。当曲线Ⅰ变为曲线Ⅱ时,改变的条件是________ 。当曲线Ⅰ变为曲线Ⅲ时,改变的条件是________ 。
(1)用活性炭可以还原处理氮氧化物,有关反应为
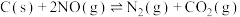 。在恒容条件下,能判断该反应一定达到化学平衡状态的依据是________(填标号)。
。在恒容条件下,能判断该反应一定达到化学平衡状态的依据是________(填标号)。A.单位时间内生成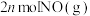 的同时消耗 的同时消耗 |
| B.混合气体的密度不再发生改变 |
| C.反应体系的压强不再发生改变 |
| D.混合气体的平均相对分子质量不再改变 |
(2)有科学家经过研究发现,用
 和
和 在210∼290℃,催化剂条件下可转化生成甲醇
在210∼290℃,催化剂条件下可转化生成甲醇 蒸气和水蒸气。一定条件下,往
蒸气和水蒸气。一定条件下,往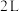 恒容密闭容器中充入
恒容密闭容器中充入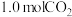 和
和 ,在不同催化剂作用下,反应相同时间内
,在不同催化剂作用下,反应相同时间内 的转化率随温度变化如图所示。催化剂效果最佳的是催化剂
的转化率随温度变化如图所示。催化剂效果最佳的是催化剂 点
点 (正)
(正) (逆)。此反应在
(逆)。此反应在 点时已达平衡状态,
点时已达平衡状态, 点的转化率比
点的转化率比 点高的原因是
点高的原因是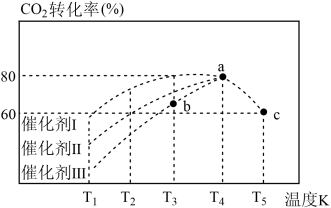
 ,则图中
,则图中 点对应温度下反应的平衡常数
点对应温度下反应的平衡常数
 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。(4)一定条件下,
 和
和 也可以发生反应
也可以发生反应
 ,一定温度下,在
,一定温度下,在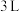 容积可变的密闭容器中,已知
容积可变的密闭容器中,已知 与反应时间
与反应时间 变化曲线如图所示,若在
变化曲线如图所示,若在 时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ或曲线Ⅲ。当曲线Ⅰ变为曲线Ⅱ时,改变的条件是
时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ或曲线Ⅲ。当曲线Ⅰ变为曲线Ⅱ时,改变的条件是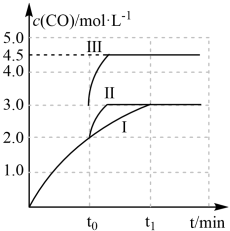
您最近一年使用:0次
解题方法
2 . 回答下列问题:
(1)肼 是一种良好的火箭推进剂,其与适当的氧化剂(如过氧化氢、氧气等)配合,可组成液体推进剂。
是一种良好的火箭推进剂,其与适当的氧化剂(如过氧化氢、氧气等)配合,可组成液体推进剂。
①液态肼和液态过氧化氢混合反应时,即产生大量氮气和水蒸气,并放出大量热。若每生成 ,放出
,放出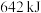 的热量,则该反应的热化学方程式为
的热量,则该反应的热化学方程式为________ ,消耗 液态肼放出的热量为
液态肼放出的热量为________ 。
②已知:
 ,键能数据如下表:
,键能数据如下表:
则氮氮三键的键能为________  。
。
(2)已知 的反应热
的反应热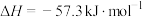 ,用
,用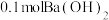 稀溶液与足量稀硝酸反应,回答下列有关中和反应的问题:
稀溶液与足量稀硝酸反应,回答下列有关中和反应的问题: 的名称是
的名称是________ ,作用是________ 。
②通过实验测定的中和反应反应热的数值常常小于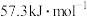 ,其原因可能是
,其原因可能是________ 。
③用相同浓度和体积的氨水代替 溶液进行上述实验,测得的反应热的数值
溶液进行上述实验,测得的反应热的数值________ (填“偏大”“偏小”或“无影响”,下同)。用足量稀硫酸代替稀硝酸溶液进行上述实验,测得的中和反应反应热的数值________ 。
(1)肼
 是一种良好的火箭推进剂,其与适当的氧化剂(如过氧化氢、氧气等)配合,可组成液体推进剂。
是一种良好的火箭推进剂,其与适当的氧化剂(如过氧化氢、氧气等)配合,可组成液体推进剂。①液态肼和液态过氧化氢混合反应时,即产生大量氮气和水蒸气,并放出大量热。若每生成
 ,放出
,放出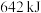 的热量,则该反应的热化学方程式为
的热量,则该反应的热化学方程式为 液态肼放出的热量为
液态肼放出的热量为②已知:

 ,键能数据如下表:
,键能数据如下表:化学键 |
|
|
|
|
键能/( | 193 | 391 | 497 | 463 |
 。
。(2)已知
 的反应热
的反应热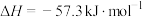 ,用
,用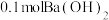 稀溶液与足量稀硝酸反应,回答下列有关中和反应的问题:
稀溶液与足量稀硝酸反应,回答下列有关中和反应的问题: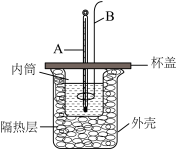
 的名称是
的名称是②通过实验测定的中和反应反应热的数值常常小于
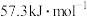 ,其原因可能是
,其原因可能是③用相同浓度和体积的氨水代替
 溶液进行上述实验,测得的反应热的数值
溶液进行上述实验,测得的反应热的数值
您最近一年使用:0次
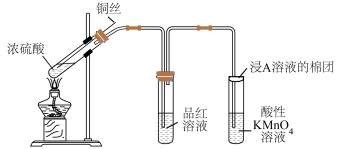
3 . 铜与浓硫酸在加热条件下可发生化学反应,为检验部分产物的性质,某研究小组设计了如图所示的实验。据此回答下列问题。________ 。
(2)反应过程中观察到品红溶液________ ,说明产物二氧化硫具有________ 性。
(3)反应过程中观察到酸性 溶液褪色,说明产物二氧化硫具有
溶液褪色,说明产物二氧化硫具有________ 性。
(4)浸 溶液的棉团的作用是吸收多余的尾气,防止污染空气,
溶液的棉团的作用是吸收多余的尾气,防止污染空气, 是
是________ 。
(5)工业生产中二氧化硫的大量排放使雨水的
________ (填“>”或“<”)5.6,会形成________ ,使土壤、湖泊酸化,还能加速建筑物的腐蚀。
(6)实验室中 的检验方法:向溶液中加入稀盐酸,然后加入
的检验方法:向溶液中加入稀盐酸,然后加入________ ,观察是否有白色沉淀生成。
(2)反应过程中观察到品红溶液
(3)反应过程中观察到酸性
 溶液褪色,说明产物二氧化硫具有
溶液褪色,说明产物二氧化硫具有(4)浸
 溶液的棉团的作用是吸收多余的尾气,防止污染空气,
溶液的棉团的作用是吸收多余的尾气,防止污染空气, 是
是(5)工业生产中二氧化硫的大量排放使雨水的

(6)实验室中
 的检验方法:向溶液中加入稀盐酸,然后加入
的检验方法:向溶液中加入稀盐酸,然后加入
您最近一年使用:0次
解题方法
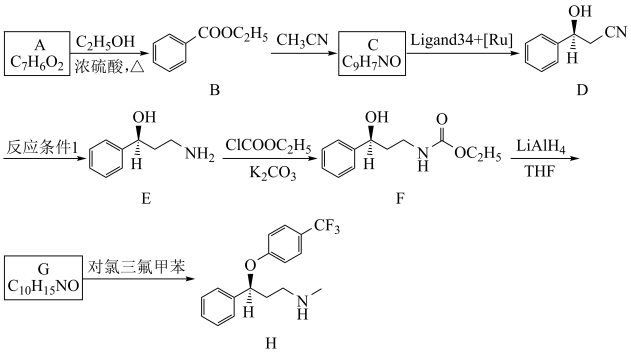
4 . “百优解”被誉为传奇抗抑郁药,其化学名称为盐酸氟西汀。一种利用聚合物支持的手性磺酰胺催化剂(Ligand34+[Ru])实现不对称合成氟西汀(化合物H)的路线如图所示:回答下列问题:___________ ,F中有___________ 个手性碳原子。
(2)已知B→C的反应中有乙醇生成,则B→C的化学方程式为___________ ,D生成E的反应条件1可以选择___________ (填标号)。
a.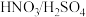 b.
b.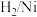 c.
c.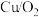 d.新制
d.新制
(3)化合物E中官能团的名称为___________ ,合成路线中E→F的反应类型为___________ 。
(4)化合物D中碳原子的杂化轨道类型有 和
和___________ ,G的结构简式为___________ 。
(5)参照上述路线,利用化合物B合成 (
(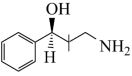 )的路线如下。其中X、K的结构简式分别为
)的路线如下。其中X、K的结构简式分别为___________ 、___________ 。
(2)已知B→C的反应中有乙醇生成,则B→C的化学方程式为
a.
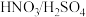 b.
b.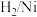 c.
c. d.新制
d.新制
(3)化合物E中官能团的名称为
(4)化合物D中碳原子的杂化轨道类型有
 和
和(5)参照上述路线,利用化合物B合成
 (
( )的路线如下。其中X、K的结构简式分别为
)的路线如下。其中X、K的结构简式分别为B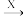 J
J K
K

您最近一年使用:0次
5 . 利用铝灰(主要成分为Al、 、AlN、FeO等)制备铝鞣剂[主要成分为
、AlN、FeO等)制备铝鞣剂[主要成分为 ]的一种工艺如下:
]的一种工艺如下:
(1)气体A能使湿润的红色石蕊试纸变蓝,A为___________ (填化学式)。铝灰在90℃时水解生成A的化学方程式为___________ ,“水解”采用90℃而不在室温下进行的原因是___________ 。
(2)“酸溶”时, ,发生反应的离子方程式为
,发生反应的离子方程式为___________ 。
(3)“氧化”时,发生反应的离子方程式为___________ 。
(4)“废渣”的成分为___________ (填化学式)。
(5)采用喷雾干燥而不用蒸发的原因是___________ 。
 、AlN、FeO等)制备铝鞣剂[主要成分为
、AlN、FeO等)制备铝鞣剂[主要成分为 ]的一种工艺如下:
]的一种工艺如下: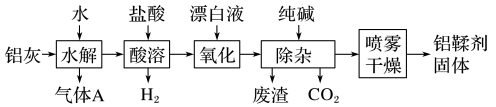
(1)气体A能使湿润的红色石蕊试纸变蓝,A为
(2)“酸溶”时,
 ,发生反应的离子方程式为
,发生反应的离子方程式为(3)“氧化”时,发生反应的离子方程式为
(4)“废渣”的成分为
(5)采用喷雾干燥而不用蒸发的原因是
您最近一年使用:0次
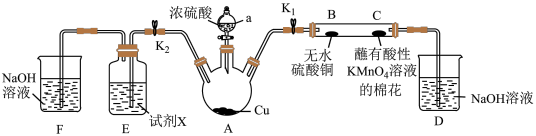
6 . 二氧化硫是一把“双刃剑”,既是重要的化工原料,又是大气污染物。某化学小组用如图装置制备SO2,并验证SO2的部分性质(夹持及加热仪器已省略)。
I检查气密性后,加入药品,开始实验,关闭K2,打开K1和仪器a活塞,至B处固体变蓝;
II.关闭K1,打开K2。
回答下列问题:
(1)仪器a的名称为_______ ,装置D的作用是_______ 。
(2)实验过程中观察到C处蘸有酸性KMnO4溶液的棉花褪色,写出C处发生反应的离子方程式:_______ (已知 转化为Mn2+)。
转化为Mn2+)。
(3)装置A_____ (填“需要”或“不需要”)加热,装置A中发生的化学反应方程式为______ 。
(4)若试剂X是Na2S溶液,反应一段时间,可观察到现象为_______ ,该反应中SO2表现_______ 性。
(5)若试剂X是1mol⋅L-1的 溶液,装置E中得到了大量白色沉淀;而用1mol⋅L-1的BaCl2溶液,装置E中无白色沉淀生成。
溶液,装置E中得到了大量白色沉淀;而用1mol⋅L-1的BaCl2溶液,装置E中无白色沉淀生成。
①前者生成的白色沉淀为BaSO4,生成该沉淀的原因是_______ (由语言描述)。
②后者无白色沉淀生成,可说明酸性:H2SO3_______ (填“>”或“<”)HCl。
I检查气密性后,加入药品,开始实验,关闭K2,打开K1和仪器a活塞,至B处固体变蓝;
II.关闭K1,打开K2。
回答下列问题:
(1)仪器a的名称为
(2)实验过程中观察到C处蘸有酸性KMnO4溶液的棉花褪色,写出C处发生反应的离子方程式:
 转化为Mn2+)。
转化为Mn2+)。(3)装置A
(4)若试剂X是Na2S溶液,反应一段时间,可观察到现象为
(5)若试剂X是1mol⋅L-1的
 溶液,装置E中得到了大量白色沉淀;而用1mol⋅L-1的BaCl2溶液,装置E中无白色沉淀生成。
溶液,装置E中得到了大量白色沉淀;而用1mol⋅L-1的BaCl2溶液,装置E中无白色沉淀生成。①前者生成的白色沉淀为BaSO4,生成该沉淀的原因是
②后者无白色沉淀生成,可说明酸性:H2SO3
您最近一年使用:0次
解题方法
7 . SO2和NO2都是大气污染物。回答下列有关问题:
(1)NO2为_______ 色的气体,空气中的NO2与水反应可形成硝酸型酸雨,该反应中氧化产物和还原产物的物质的量之比为_______ 。
(2)利用氨水可以将SO2和NO2吸收,原理如图所示:_______ 。
②NH4HSO3不稳定,常温下易分解。NH4HSO3溶液可以使得品红溶液褪色的原因是_______ 。
③检验铵盐溶液中阴离子的操作为_______ 。
(3)工、农业废水以及生活污水中浓度较高的 会造成氮污染。工业上处理水体中
会造成氮污染。工业上处理水体中 的一种方法是零价铁化学还原法。某小组用废铁屑和硝酸盐溶液模拟此过程,实验如下。
的一种方法是零价铁化学还原法。某小组用废铁屑和硝酸盐溶液模拟此过程,实验如下。
①将KNO3溶液的pH调至2.5,从氧化还原的角度分析调浓度低溶液pH的原因是_______ 。已知:pH越小表示溶液中 越大。
越大。
②将上述处理过的足量铁屑投入①调节pH后的溶液中。如图表示该反应过程中,体系内相关离子浓度、pH随时间变化的关系。 时刻前主要发生反应的离子方程式是
时刻前主要发生反应的离子方程式是_______ 。
(1)NO2为
(2)利用氨水可以将SO2和NO2吸收,原理如图所示:
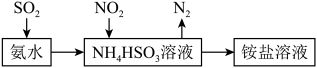
②NH4HSO3不稳定,常温下易分解。NH4HSO3溶液可以使得品红溶液褪色的原因是
③检验铵盐溶液中阴离子的操作为
(3)工、农业废水以及生活污水中浓度较高的
 会造成氮污染。工业上处理水体中
会造成氮污染。工业上处理水体中 的一种方法是零价铁化学还原法。某小组用废铁屑和硝酸盐溶液模拟此过程,实验如下。
的一种方法是零价铁化学还原法。某小组用废铁屑和硝酸盐溶液模拟此过程,实验如下。①将KNO3溶液的pH调至2.5,从氧化还原的角度分析调浓度低溶液pH的原因是
 越大。
越大。②将上述处理过的足量铁屑投入①调节pH后的溶液中。如图表示该反应过程中,体系内相关离子浓度、pH随时间变化的关系。
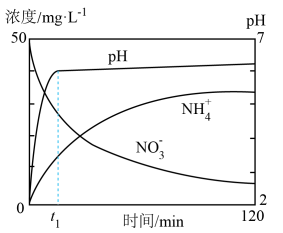
 时刻前主要发生反应的离子方程式是
时刻前主要发生反应的离子方程式是
您最近一年使用:0次
解题方法
8 . 铜是重要的过渡金属元素,被广泛应用于电子工业和航天领域中。回答下列问题:
(1)与Cu元素同周期,且基态原子有2个未成对电子的金属元素有___________ 种。
(2)向CuSO4溶液中滴加氨水可以得到1∶1型离子化合物,其阳离子结构如图所示。___________ 。
②在硫酸铜溶液中逐滴滴加氨水至过量,先出现蓝色沉淀,最后溶解形成深蓝色溶液。写出此蓝色沉淀溶解的离子方程式;___________ 。
(3)我国科学家制取了一种铜的配合物如下图所示,该配合物中sp2杂化的碳原子与sp3杂化的碳原子个数比为___________ 。___________ (填晶体类型),其中 的空间结构为
的空间结构为___________ 。
②胆矾晶体中含有的化学键类型为___________ (填字母)。
a.离子键 b.氢键 c 配位键 d 共价键
(1)与Cu元素同周期,且基态原子有2个未成对电子的金属元素有
(2)向CuSO4溶液中滴加氨水可以得到1∶1型离子化合物,其阳离子结构如图所示。
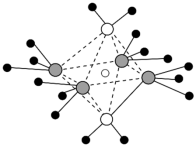
②在硫酸铜溶液中逐滴滴加氨水至过量,先出现蓝色沉淀,最后溶解形成深蓝色溶液。写出此蓝色沉淀溶解的离子方程式;
(3)我国科学家制取了一种铜的配合物如下图所示,该配合物中sp2杂化的碳原子与sp3杂化的碳原子个数比为
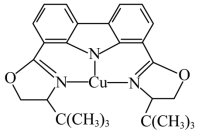

 的空间结构为
的空间结构为②胆矾晶体中含有的化学键类型为
a.离子键 b.氢键 c 配位键 d 共价键
您最近一年使用:0次
名校
解题方法
9 . 治疗抑郁症的药物帕罗西汀(N)的合成路线如图所示。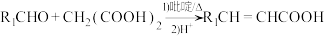 ;
;
ii.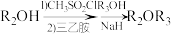 ;
;
iii. 为反式结构。
为反式结构。
回答下列问题:
(1)第一电离能:
____ (填“>”或“<”) 。
。
(2) 的结构简式为
的结构简式为______ 。
(3) 的反应类型为
的反应类型为______ 。
(4)下列有关 的说法正确的是
的说法正确的是_______ (填标号)。
a. 的焰色试验呈黄色
的焰色试验呈黄色
b. 中碳原子的杂化方式为
中碳原子的杂化方式为 和
和
c.基态氯原子核外电子的空间运动状态有17种
d.常温下,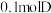 与足量的
与足量的 溶液反应,理论上可得到
溶液反应,理论上可得到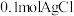
(5)I中含氧官能团的名称为_____ 。
(6)J的同分异构体中,既能发生银镜反应又能发生水解反应,且能与 溶液发生显色反应的结构有
溶液发生显色反应的结构有____ 种。其中核磁共振氢谐显示有4组峰,且峰面积之比为 的结构简式为
的结构简式为____ 。
(7)结合所学知识并参考上述合成路线,设计以乙醛和 为碳源合成
为碳源合成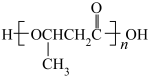 的路线
的路线______ 。
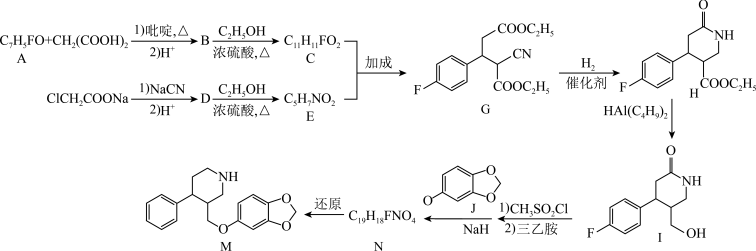
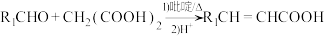 ;
;ii.
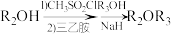 ;
;iii.
 为反式结构。
为反式结构。回答下列问题:
(1)第一电离能:

 。
。(2)
 的结构简式为
的结构简式为(3)
 的反应类型为
的反应类型为(4)下列有关
 的说法正确的是
的说法正确的是a.
 的焰色试验呈黄色
的焰色试验呈黄色b.
 中碳原子的杂化方式为
中碳原子的杂化方式为 和
和
c.基态氯原子核外电子的空间运动状态有17种
d.常温下,
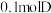 与足量的
与足量的 溶液反应,理论上可得到
溶液反应,理论上可得到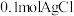
(5)I中含氧官能团的名称为
(6)J的同分异构体中,既能发生银镜反应又能发生水解反应,且能与
 溶液发生显色反应的结构有
溶液发生显色反应的结构有 的结构简式为
的结构简式为(7)结合所学知识并参考上述合成路线,设计以乙醛和
 为碳源合成
为碳源合成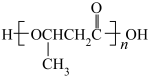 的路线
的路线
您最近一年使用:0次
名校
10 . 半导体芯片的发明促进了人类信息技术的发展,单晶硅、砷化镓(GaAs),碳化硅等是制作半导体芯片的关键材料,也是我国优先发展的新材料。回答下列问题:
(1)基态硅原子的价层电子排布式为______ 。
(2)和碳位于同一周期,且未成对电子数与碳相同的元素有____ 种。
(3)基态 原子中占据最高能级的电子的电子云轮廓图为
原子中占据最高能级的电子的电子云轮廓图为_____ 形。
(4)β-SiC的晶胞结构如图所示。
已知:i.晶体密度为 ;
;
ii.设 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。
① 属于
属于_____ (填“离子晶体”“分子晶体”或“共价晶体”)。
② 、
、 两原子的核间距为
两原子的核间距为____  (用含
(用含 的代数式表示)
的代数式表示)
③沸点:
_____ (填“>”或“<”) ,判断的理由为
,判断的理由为______ 。 的晶胞结构如图甲。将
的晶胞结构如图甲。将 掺杂到
掺杂到 的晶体中得到稀磁性半导体材料(图乙)。
的晶体中得到稀磁性半导体材料(图乙)。 晶胞中距离
晶胞中距离 原子最近的
原子最近的 原子的个数为
原子的个数为_____ 。
②掺杂 之后,晶体中
之后,晶体中 、
、 、
、 的原子个数比为
的原子个数比为____ (化为最简整数比)
(1)基态硅原子的价层电子排布式为
(2)和碳位于同一周期,且未成对电子数与碳相同的元素有
(3)基态
 原子中占据最高能级的电子的电子云轮廓图为
原子中占据最高能级的电子的电子云轮廓图为(4)β-SiC的晶胞结构如图所示。
已知:i.晶体密度为
 ;
;ii.设
 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。①
 属于
属于②
 、
、 两原子的核间距为
两原子的核间距为 (用含
(用含 的代数式表示)
的代数式表示)③沸点:

 ,判断的理由为
,判断的理由为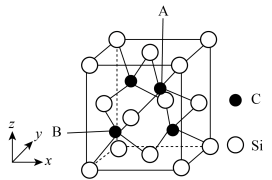
 的晶胞结构如图甲。将
的晶胞结构如图甲。将 掺杂到
掺杂到 的晶体中得到稀磁性半导体材料(图乙)。
的晶体中得到稀磁性半导体材料(图乙)。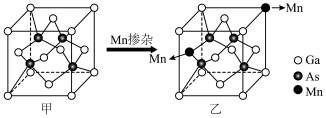
 晶胞中距离
晶胞中距离 原子最近的
原子最近的 原子的个数为
原子的个数为②掺杂
 之后,晶体中
之后,晶体中 、
、 、
、 的原子个数比为
的原子个数比为
您最近一年使用:0次





 )
)

