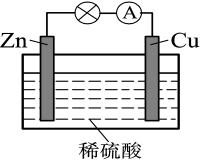有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。在101 kPa下,1 g氢气完全燃烧生成液态水放出142.9 kJ的热量。
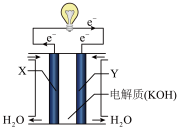
(1)请写出表示氢气燃烧热的热化学方程式__________________ 。
(2)将上述反应设计成下图所示的原电池,其中Y为________ 极(填“正”或“负”),该极电极反应式为___________________ 。

(1)请写出表示氢气燃烧热的热化学方程式
(2)将上述反应设计成下图所示的原电池,其中Y为
更新时间:2024-03-27 23:00:10
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】解决能源短缺问题,工业生产中应合理利用化学能。
(1)25 ℃、1.01×105 Pa时,实验测得,4 g氢气在O2中完全燃烧生成液态水,放出572 kJ的热量,则表示H2的燃烧热的热化学方程式为______________________ 。
(2)从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。
已知:N2(g)+3H2(g)===2NH3(g) ΔH=-93 kJ·mol-1。试根据表中所列键能数据计算a的数值____________ 。
(3)已知:C(s,石墨)+O2(g)===CO2(g)ΔH1=-393.5 kJ·mol-1 ①
2H2(g)+O2(g)===2H2O(l)ΔH2=-571.6 kJ·mol-1 ②
2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l)ΔH3=-2599 kJ·mol-1 ③
根据盖斯定律,计算反应2C(s,石墨)+H2(g)===C2H2(g) ΔH=________ 。
(1)25 ℃、1.01×105 Pa时,实验测得,4 g氢气在O2中完全燃烧生成液态水,放出572 kJ的热量,则表示H2的燃烧热的热化学方程式为
(2)从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。
| 化学键 | H—H | N—H | N≡N |
| 键能/kJ·mol-1 | 436 | a | 945 |
(3)已知:C(s,石墨)+O2(g)===CO2(g)ΔH1=-393.5 kJ·mol-1 ①
2H2(g)+O2(g)===2H2O(l)ΔH2=-571.6 kJ·mol-1 ②
2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l)ΔH3=-2599 kJ·mol-1 ③
根据盖斯定律,计算反应2C(s,石墨)+H2(g)===C2H2(g) ΔH=
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】依据叙述,写出下列反应的热化学方程式。
(1)在25℃、101kPa下,1g甲醇(液态)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为______________ 。
(2)用NA表示阿伏加 德罗常数,在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,放出650kJ的热量。其热化学方程式为______________ 。
(1)在25℃、101kPa下,1g甲醇(液态)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为
(2)用NA表示阿伏加 德罗常数,在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,放出650kJ的热量。其热化学方程式为
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:

(1)电极X的材料是_______ ;电解质溶液Y是_______ ;
(2)银电极为电池的_______ 极,发生的电极反应式为_______ ;X电极上发生的电极反应为_______ 反应;(填“氧化”或“还原”)
(3)外电路中的电子_______ (填“流出”或“流向”)Ag电极。

(1)电极X的材料是
(2)银电极为电池的
(3)外电路中的电子
您最近半年使用:0次
填空题
|
较易
(0.85)
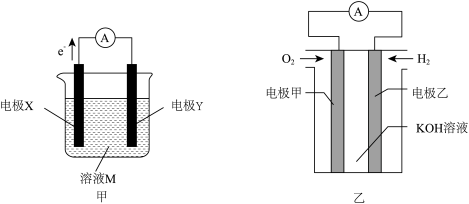
【推荐2】原电池是利用氧化还原反应设计的装置,该装置的特点是使氧化反应和还原反应在两个电极进行,“迫使”电子沿着特定的路线移动,从而产生电能。甲、乙两个原电池装置如图所示:
回答下列问题:
(1)若装置甲的溶液M为稀硫酸,两个电极采用镁棒和铝棒。
①电极X为_______ (填“正极”或“负极”),该电极反应式为_______ 。
②该电池的正极是_______ (填“镁棒”或“铝棒”),该电极产物W是_______ (填化学式)。
③该原电池总反应的化学方程式是_______ 。
(2)若装置甲中两电极质量变化与时间的关系如图所示,其中一个电极为Ag电极,则该电池的电解质溶液为_______ (填化学式)溶液,电极X为_______ (填字母)
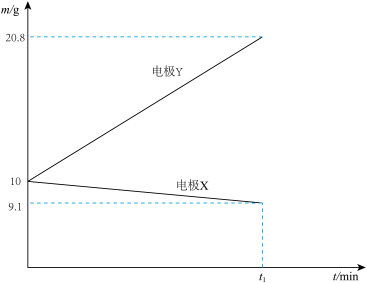
a.Fe电极 b.Mg电极 c.Cu电极 d.Al电极
(3)将(1)中原电池生成的气体产物W通入装置乙中可制备燃料电池。
①正极为_______ (填“电极甲”或“电极乙”),该电极发生_______ (填“氧化反应”或“还原反应”)。
②该电池工作时,外电路中电子由_______ (填“电极甲”或“电极乙”,下同)流出;电解质溶液中的 移向
移向_______ 。

回答下列问题:
(1)若装置甲的溶液M为稀硫酸,两个电极采用镁棒和铝棒。
①电极X为
②该电池的正极是
③该原电池总反应的化学方程式是
(2)若装置甲中两电极质量变化与时间的关系如图所示,其中一个电极为Ag电极,则该电池的电解质溶液为

a.Fe电极 b.Mg电极 c.Cu电极 d.Al电极
(3)将(1)中原电池生成的气体产物W通入装置乙中可制备燃料电池。
①正极为
②该电池工作时,外电路中电子由
 移向
移向
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】镍镉可充电电池在现代生活中有着广泛的应用,装置如图所示,它的充、放电反应为Cd+2NiOOH+2H2O Cd(OH)2+2Ni(OH)2。
Cd(OH)2+2Ni(OH)2。

请回答下列问题:
(1)放电时,还原反应在____ (填“a”或“b”)极进行,负极的电极反应式为____________ ,在放电过程中,正极附近的电解质溶液碱性会____ (填“增强”或“减弱”)。
(2)镍镉废旧电池必须进行回收并集中处理,最主要的原因是________________ 。
 Cd(OH)2+2Ni(OH)2。
Cd(OH)2+2Ni(OH)2。
请回答下列问题:
(1)放电时,还原反应在
(2)镍镉废旧电池必须进行回收并集中处理,最主要的原因是
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】某化学小组探究不同条件下化学能转变为电能的装置如下图。回答问题:
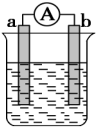
(1)若电极a为 、电极b为
、电极b为 、电解质溶液为稀硫酸时,正极的电极反应式为:
、电解质溶液为稀硫酸时,正极的电极反应式为:_______ 。
(2)若电极a为 、电极b为
、电极b为 、电解质溶液为浓硝酸时,该装置
、电解质溶液为浓硝酸时,该装置_______ (填“能”或“不能”)形成原电池。
(3)燃料电池的工作原理是将燃料和氧化剂(如 )反应所放出的化学能直接转化为电能.现设计一燃料电池,以电极a为正极,电极b为负极,
)反应所放出的化学能直接转化为电能.现设计一燃料电池,以电极a为正极,电极b为负极, 为燃料,采用酸性溶液为电解液;则
为燃料,采用酸性溶液为电解液;则 应通入
应通入_______ 极(填a或b,下同),电子从_______ 极流出。电池的负极反应式为:_______ 。

(1)若电极a为
 、电极b为
、电极b为 、电解质溶液为稀硫酸时,正极的电极反应式为:
、电解质溶液为稀硫酸时,正极的电极反应式为:(2)若电极a为
 、电极b为
、电极b为 、电解质溶液为浓硝酸时,该装置
、电解质溶液为浓硝酸时,该装置(3)燃料电池的工作原理是将燃料和氧化剂(如
 )反应所放出的化学能直接转化为电能.现设计一燃料电池,以电极a为正极,电极b为负极,
)反应所放出的化学能直接转化为电能.现设计一燃料电池,以电极a为正极,电极b为负极, 为燃料,采用酸性溶液为电解液;则
为燃料,采用酸性溶液为电解液;则 应通入
应通入
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】完成下列小题
(1)铅蓄电池(原电池),其电极分别是PbO2和Pb,电解质溶液为稀H2SO4溶液,工作时原电池的总反应是:PbO2 + Pb + 2H2SO4 = 2PbSO4 +2H2O,根据上述变化判断:原电池的负极是___________ (填电极材料);工作时蓄电池正极反应为___________ ; 工作时蓄电池里电解质溶液pH___________ (填增大、不变或减小)。
(2)用锌片、铜片连接后浸入稀硫酸溶液中,构成了原电池。工作一段时间,锌片的质量减少了3.25 g,铜表面析出氢气___________ L(标准状况下);导线中通过___________ 个电子。
(1)铅蓄电池(原电池),其电极分别是PbO2和Pb,电解质溶液为稀H2SO4溶液,工作时原电池的总反应是:PbO2 + Pb + 2H2SO4 = 2PbSO4 +2H2O,根据上述变化判断:原电池的负极是
(2)用锌片、铜片连接后浸入稀硫酸溶液中,构成了原电池。工作一段时间,锌片的质量减少了3.25 g,铜表面析出氢气
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐1】氢氧燃料电池
| 电解质 | H2SO4溶液 | KOH溶液 | 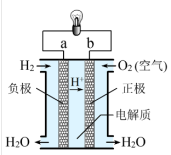 |
| 总反应 | 2H2+O2=2H2O | ||
| 负极反应式 | |||
| 正极反应式 | |||
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】生活中,电池无处不在。形式多样化的电池,满足不同的市场需求。下列是几种不同类型的原电池装置。
(1)某实验小组设计了如图甲所示装置:a为铝棒,b为镁棒。
①若容器中盛有 溶液,a极为
溶液,a极为_______ (填“正极”或“负极”);b极附近观察到的现象是_______ 。
②若容器中盛有浓硫酸,b极的电极反应式是_______ ,导线中电子的流动方向是_______ (填“a→b”或“b→a”)。
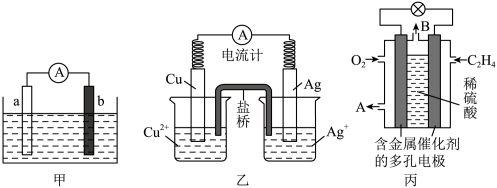
(2)铜—银原电池装置如图乙所示,下列有关叙述正确的是_______ (填标号)。
A.银电极上发生还原反应
B.电池工作一段时间后,铜极的质量增加
C.取出盐桥后,电流计依旧发生偏转
D.电池工作时,每转移0.1mol电子,两电极的质量差会增加14g
(3)乙烯是水果的催熟剂,又可用作燃料,由 和
和 组成的燃料电池的结构如图丙所示。
组成的燃料电池的结构如图丙所示。
①乙烯燃料电池的正极反应式是_______ 。
②物质B的化学名称为_______ 。
③当消耗2.8g乙烯时,生成物质B的体积为_______ L(标准状况下)。
(1)某实验小组设计了如图甲所示装置:a为铝棒,b为镁棒。
①若容器中盛有
 溶液,a极为
溶液,a极为②若容器中盛有浓硫酸,b极的电极反应式是

(2)铜—银原电池装置如图乙所示,下列有关叙述正确的是
A.银电极上发生还原反应
B.电池工作一段时间后,铜极的质量增加
C.取出盐桥后,电流计依旧发生偏转
D.电池工作时,每转移0.1mol电子,两电极的质量差会增加14g
(3)乙烯是水果的催熟剂,又可用作燃料,由
 和
和 组成的燃料电池的结构如图丙所示。
组成的燃料电池的结构如图丙所示。①乙烯燃料电池的正极反应式是
②物质B的化学名称为
③当消耗2.8g乙烯时,生成物质B的体积为
您最近半年使用:0次

 在氧气中燃烧完全转化为S单质放出
在氧气中燃烧完全转化为S单质放出 热量,完全转化为
热量,完全转化为 放出
放出 热量,写出表示
热量,写出表示 燃烧热的热化学方程式
燃烧热的热化学方程式 ]可以作净水剂的原因是
]可以作净水剂的原因是 是一种一元酸,写出它的正盐水解的离子方程式
是一种一元酸,写出它的正盐水解的离子方程式 溶液可通过调节
溶液可通过调节 改变颜色,原因是
改变颜色,原因是 固体放入水中,写出该反应的化学方程式
固体放入水中,写出该反应的化学方程式