在1~18号的短周期主族元素中,表中的字母代表一种元素,回答下列问题:
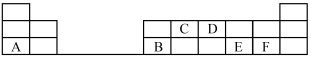
(1)写出D单质的电子式:___________ 。
(2)写出C的最高价氧化物的结构式:___________ 。
(3)E和F分别形成的气态氢化物中较稳定的是___________ (填氢化物的化学式)。
(4)A最高价氧化物的水化物所含化学键为___________ ,其水溶液与F单质反应的离子方程式为___________ 。

(1)写出D单质的电子式:
(2)写出C的最高价氧化物的结构式:
(3)E和F分别形成的气态氢化物中较稳定的是
(4)A最高价氧化物的水化物所含化学键为
更新时间:2024-04-03 16:41:24
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】根据要求填写下列空白。
(1)甲基的电子式为__ 。
(2)乙二酸二乙酯的结构简式为__ 。
(3)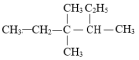 的系统命名为
的系统命名为__ 。
(4)已知:①2NO(g) N2(g)+O2(g)△H1=-180.5kJ·mol-1
N2(g)+O2(g)△H1=-180.5kJ·mol-1
②CO(g)+ O2(g)
O2(g) CO2(g)△H2=-283kJ·mol-1
CO2(g)△H2=-283kJ·mol-1
则NO与CO反应生成两种无毒气体的热化学方程式为__ 。
(5)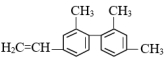 分子中处于同一直线上的碳原子最多有
分子中处于同一直线上的碳原子最多有__ 个,分子中最多有__ 个碳原子处于同一平面上。
(1)甲基的电子式为
(2)乙二酸二乙酯的结构简式为
(3)
 的系统命名为
的系统命名为(4)已知:①2NO(g)
 N2(g)+O2(g)△H1=-180.5kJ·mol-1
N2(g)+O2(g)△H1=-180.5kJ·mol-1②CO(g)+
 O2(g)
O2(g) CO2(g)△H2=-283kJ·mol-1
CO2(g)△H2=-283kJ·mol-1则NO与CO反应生成两种无毒气体的热化学方程式为
(5)
 分子中处于同一直线上的碳原子最多有
分子中处于同一直线上的碳原子最多有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】短周期元素在周期表中的位置如图所示。请按要求回答下列问题。
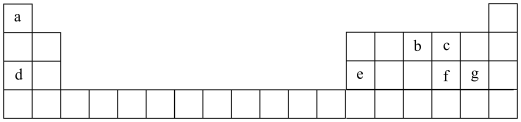
(1)由a、c、d形成的化合物的电子式为___________ ,该物质属于___________ 化合物(填“离子”或“共价”)。可能含有的化学键类型有___________ 。
(2)a与b形成的二元化合物中,所含电子数为10的分子的电子式为___________ ,a与c形成的二元化合物中,所含电子数为18的物质的结构式为___________ 。
(3)在全国抗击“新冠肺炎”的“战疫”中用了大量的“84”来消毒杀菌,84消毒液和洁厕灵混合使用时产生了一种有毒气体,写出两者混合时的化学反应方程式:___________ 。
(4)写出d与e两种元素的最高价氧化物对应的水化物相互反应的离子方程式:___________ 。

(1)由a、c、d形成的化合物的电子式为
(2)a与b形成的二元化合物中,所含电子数为10的分子的电子式为
(3)在全国抗击“新冠肺炎”的“战疫”中用了大量的“84”来消毒杀菌,84消毒液和洁厕灵混合使用时产生了一种有毒气体,写出两者混合时的化学反应方程式:
(4)写出d与e两种元素的最高价氧化物对应的水化物相互反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】硅、硫、氮是重要的非金属元素。回答下列问题:
(1)SiO2属于_______ (填“酸性”“碱性”或“两性”)氧化物。盛装NaOH等碱性溶液的试剂瓶不能用玻璃塞,其原因为_______ (用化学方程式表示)。
(2)工业上用石英砂和焦炭混合高温制取粗硅,其反应的化学方程式为_______ ;硅的用途有_______ (任写1个)。
(3)由SO3制备H2SO₄的过程中,一般用98.3%的浓硫酸吸收SO3,而不是直接用蒸馏水吸收的原因是_______ 。
(4)实验室利用含Fe3+的溶液吸收SO2,从而实现SO2的回收利用。写出Fe3+与SO2在水溶液中发生反应的离子方程式:_______ ;SO2_______ (填“被氧化”或“被还原”);每消耗32gSO2,转移电子的物质的量为_______ mol。
(5)氨气遇氯化氢时会产生白烟,写出白烟化学成分的电子式:_______ 。
(1)SiO2属于
(2)工业上用石英砂和焦炭混合高温制取粗硅,其反应的化学方程式为
(3)由SO3制备H2SO₄的过程中,一般用98.3%的浓硫酸吸收SO3,而不是直接用蒸馏水吸收的原因是
(4)实验室利用含Fe3+的溶液吸收SO2,从而实现SO2的回收利用。写出Fe3+与SO2在水溶液中发生反应的离子方程式:
(5)氨气遇氯化氢时会产生白烟,写出白烟化学成分的电子式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分,回答下列有关问题:

(1)画出原子的结构示意图:④______________
(2)在①~⑫元素中,非金属性最强的元素是____ ,最不活泼的元素是_____ 。(均填元素符号)
(3)元素⑦与元素⑧相比,非金属性较强的是______ (用元素符号表示),下列表述中能证明这一事实的是________ 。
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(4)元素⑤的最高价氧化物的水化物分别与元素③⑧的最高价氧化物的水化物反应的离子方程式_________ ,
(5)第三周期中原子半径最大的元素跟它同周期原子半径最小的元素它们可以形成化合物,用电子式表示其形成过程:_____ 。
(6)已知某元素原子最外层电子数是其次外层电子数的2倍,该元素可以与⑧形成一种AB4型的化合物,请用电子式表示其形成过程:______

(1)画出原子的结构示意图:④
(2)在①~⑫元素中,非金属性最强的元素是
(3)元素⑦与元素⑧相比,非金属性较强的是
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(4)元素⑤的最高价氧化物的水化物分别与元素③⑧的最高价氧化物的水化物反应的离子方程式
(5)第三周期中原子半径最大的元素跟它同周期原子半径最小的元素它们可以形成化合物,用电子式表示其形成过程:
(6)已知某元素原子最外层电子数是其次外层电子数的2倍,该元素可以与⑧形成一种AB4型的化合物,请用电子式表示其形成过程:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】短周期主族元素 、
、 、
、 、
、 的原子序数依次增大,
的原子序数依次增大, 的简单氢化物可用作制冷剂,
的简单氢化物可用作制冷剂, 的原子半径是所有短周期主族元素中最大的。由
的原子半径是所有短周期主族元素中最大的。由 、
、 和
和 三种元素形成的一种盐溶于水后,加入稀盐酸,有黄色沉淀析出,同时有刺激性气体产生。则
三种元素形成的一种盐溶于水后,加入稀盐酸,有黄色沉淀析出,同时有刺激性气体产生。则 、
、 、
、 、
、 分别为
分别为_______ 。
 、
、 、
、 、
、 的原子序数依次增大,
的原子序数依次增大, 的简单氢化物可用作制冷剂,
的简单氢化物可用作制冷剂, 的原子半径是所有短周期主族元素中最大的。由
的原子半径是所有短周期主族元素中最大的。由 、
、 和
和 三种元素形成的一种盐溶于水后,加入稀盐酸,有黄色沉淀析出,同时有刺激性气体产生。则
三种元素形成的一种盐溶于水后,加入稀盐酸,有黄色沉淀析出,同时有刺激性气体产生。则 、
、 、
、 、
、 分别为
分别为
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
【推荐3】金刚石、SiC具有优良的耐磨、耐腐蚀特性,应用广泛.
(1)碳与短周期元素Q的单质化合仅能生成两种常见气态化合物,其中一种化合物R为非极性分子.碳元素在周期表中的位置是_____________ ,Q是_____________ ,R的电子式为_____________ .
(2)一定条件下,Na还原CCl4可制备金刚石,反应结束冷却至室温后,回收其中的CCl4的实验操作名称为_____________ ,除去粗产品中少量钠的试剂为_____________ .
(3)碳还原SiO2制SiC,其粗产品中杂质为Si和SiO2.现将20.0g SiC粗产品加入到过量的NaOH溶液中充分反应,收集到0.1mol氢气,过滤得SiC固体11.4g,滤液稀释到1L.生成氢气的离子方程式为_____________ ,硅酸盐的物质的量浓度为_____________ .
(4)下列叙述正确的有_____________ (填序号).
①Na还原CCl4的反应、Cl2与H2O的反应均是置换反应
②水晶、干冰熔化时克服粒子间作用力的类型相同
③Na2SiO3溶液与SO3的反应可用于推断Si与S的非金属性强弱
④钠、锂分别在空气中燃烧,生成的氧化物中阴阳离子数目比均为1:2.
(1)碳与短周期元素Q的单质化合仅能生成两种常见气态化合物,其中一种化合物R为非极性分子.碳元素在周期表中的位置是
(2)一定条件下,Na还原CCl4可制备金刚石,反应结束冷却至室温后,回收其中的CCl4的实验操作名称为
(3)碳还原SiO2制SiC,其粗产品中杂质为Si和SiO2.现将20.0g SiC粗产品加入到过量的NaOH溶液中充分反应,收集到0.1mol氢气,过滤得SiC固体11.4g,滤液稀释到1L.生成氢气的离子方程式为
(4)下列叙述正确的有
①Na还原CCl4的反应、Cl2与H2O的反应均是置换反应
②水晶、干冰熔化时克服粒子间作用力的类型相同
③Na2SiO3溶液与SO3的反应可用于推断Si与S的非金属性强弱
④钠、锂分别在空气中燃烧,生成的氧化物中阴阳离子数目比均为1:2.
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表是元素周期表的一部分,回答下列问题
(1)写出①、⑥两种元素的名称:__________ 、____________ 。
(2)这些元素的最高价氧化物对应水化物中,酸性最强的是__________ (填化学式,下同);碱性最强的是________ ;能形成两性氢氧化物的元素是__________ (填元素符号)。
(3)比较⑤和⑥的化学性质,________ (填元素符号)更活泼,试用实验证明 (简述操作、现象和结论)____
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
(1)写出①、⑥两种元素的名称:
(2)这些元素的最高价氧化物对应水化物中,酸性最强的是
(3)比较⑤和⑥的化学性质,
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】用化学用语回答下列问题
(1)写出二氧化碳分子的电子式___________ ;写出氮气分子的结构式___________ 。
(2)A+、B-、C、D四种粒子(分子或离子),它们都分别含10个电子,已知它们有如下转化关系:A++B- C+D,则A的电子式
C+D,则A的电子式___________ 。比较C和D的稳定性的强弱∶___________ (用化学式表示)。
(3)用电子式表示MgCl2的形成过程___________
(4)①CaBr2;②H2O;③NH4Cl;④H2O2;⑤Na2O2;⑥Ca(OH)2;⑦HClO;⑧I2;⑨He;只含有离子键的是(用序号回答)___________ ,含有共价键的离子化合物是(用序号回答)___________ ,含有非极性共价键的共价化合物是(用序号回答)___________ ,常温时为固体,当其熔化时,不破坏化学键的是(用序号回答)___________ 。
(1)写出二氧化碳分子的电子式
(2)A+、B-、C、D四种粒子(分子或离子),它们都分别含10个电子,已知它们有如下转化关系:A++B-
 C+D,则A的电子式
C+D,则A的电子式(3)用电子式表示MgCl2的形成过程
(4)①CaBr2;②H2O;③NH4Cl;④H2O2;⑤Na2O2;⑥Ca(OH)2;⑦HClO;⑧I2;⑨He;只含有离子键的是(用序号回答)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氮、磷、砷(As)、锑(Sb)、铋(Bi)、镆(Mo)为元素周期表中原子序数依次增大的同族元素。回答下列问题:
(1)砷在元素周期表中的位置
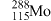 的中子数为
的中子数为已知:
P(s,白磷)=P(s,黑磷) 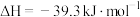 ;
;
P(s,白磷)=P(s,红磷) 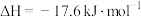 ;
;
由此推知,其中最稳定的磷单质是
(2)氮和磷氢化物性质的比较:
热稳定性:

沸点:
 。
。
(3)
 和
和 与卤化氢的反应相似,产物的结构和性质也相似。下列对
与卤化氢的反应相似,产物的结构和性质也相似。下列对 与HI反应产物的推断正确的是
与HI反应产物的推断正确的是a.不能与NaOH反应 b.含离子键、共价键 c.其溶液显碱性
(4)
 能发生较强烈的水解,生成难溶的SbOCl,因此,配制
能发生较强烈的水解,生成难溶的SbOCl,因此,配制 溶液应注意
溶液应注意(5)解释碳酸钠溶液显碱性的原因
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表是元素周期表的一部分,回答相关问题。
(1)元素①和⑦形成的化合物的化学式为___________ 。
(2)元素⑥的过氧化物的电子式___________ ,其最高价氧化物对应的水化物中含有的化学键类型为___________ 。
(3)元素⑥、⑦、⑧、⑨的简单离子半径由大到小的顺序为___________ (用离子符号表示);元素④、⑤、⑧、⑨的最简单氢化物中稳定性最强的是___________ (填化学式)。
(4)最近,德国科学家实现了铷原子气体超流体态与绝缘体态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。关于铷的下列说法不正确的是___________ (填序号)。
a.与水反应比钠反应更剧烈
b.单质具有很强的氧化性
c.Rb2O在空气中不会吸收水和二氧化碳
d.Rb2O2能与水剧烈反应并释放氧气
e.RbOH的碱性比同浓度的NaOH溶液弱
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | ⑤ | ||||
| 三 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
(2)元素⑥的过氧化物的电子式
(3)元素⑥、⑦、⑧、⑨的简单离子半径由大到小的顺序为
(4)最近,德国科学家实现了铷原子气体超流体态与绝缘体态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。关于铷的下列说法不正确的是
a.与水反应比钠反应更剧烈
b.单质具有很强的氧化性
c.Rb2O在空气中不会吸收水和二氧化碳
d.Rb2O2能与水剧烈反应并释放氧气
e.RbOH的碱性比同浓度的NaOH溶液弱
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按下列要求作答:
(1)有下列几种物质:A. ;B.冰;C.氯化铵;D.
;B.冰;C.氯化铵;D. ;E.烧碱。分子中只含共价键的化合物是
;E.烧碱。分子中只含共价键的化合物是_______ (填字母,下同),属于离子化合物的是_______ 。
(2)以 为催化剂的光热化学循环分解
为催化剂的光热化学循环分解 反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。

①上述过程中,能量的变化形式是由_______ 转化为_______ 。
②该反应的化学方程式为_______ (不写反应条件)。
③根据图中数据计算,分解1mol 需
需_______ (填“吸收”或“放出”)_______ kJ的能量。
(1)有下列几种物质:A.
 ;B.冰;C.氯化铵;D.
;B.冰;C.氯化铵;D. ;E.烧碱。分子中只含共价键的化合物是
;E.烧碱。分子中只含共价键的化合物是(2)以
 为催化剂的光热化学循环分解
为催化剂的光热化学循环分解 反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
①上述过程中,能量的变化形式是由
②该反应的化学方程式为
③根据图中数据计算,分解1mol
 需
需
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】I.请根据有关知识,填写下列空白:
(1)下列反应中,属于吸热反应的是______ (填数字序号,下同),属于放热反应的是______ 。
①煅烧石灰石制生石灰;②氢氧化钠固体溶于水;③碳与水蒸气的反应;④酸碱中和反应;⑤生石灰与水作用制熟石灰;⑥食物因氧化而腐败
(2)已知H2和O2反应放热,且断开1 mol H−H、1 mol O=O、1 mol O−H键需要吸收的能量分别为Q1kJ、Q2kJ、Q3kJ,由此可以推知下列关系正确的是______ (填字母编号)。
A.Q1+ Q2> Q3 B.2Q1+ Q2<4Q3 C.Q1+Q2>2Q3 D.2Q1+Q2<2Q3
II.下列物质:①CaBr2 ②H2O ③NH4Cl ④H2O2 ⑤Na2O2 ⑥Ca(OH)2 ⑦HClO ⑧ I2
(3)只存在非极性键的是_____ (用序号填空,下同)。
(4)既含有共价键又含有离子键的是______________ 。
(5)当其熔化时,不破坏化学键的是______________ 。
(1)下列反应中,属于吸热反应的是
①煅烧石灰石制生石灰;②氢氧化钠固体溶于水;③碳与水蒸气的反应;④酸碱中和反应;⑤生石灰与水作用制熟石灰;⑥食物因氧化而腐败
(2)已知H2和O2反应放热,且断开1 mol H−H、1 mol O=O、1 mol O−H键需要吸收的能量分别为Q1kJ、Q2kJ、Q3kJ,由此可以推知下列关系正确的是
A.Q1+ Q2> Q3 B.2Q1+ Q2<4Q3 C.Q1+Q2>2Q3 D.2Q1+Q2<2Q3
II.下列物质:①CaBr2 ②H2O ③NH4Cl ④H2O2 ⑤Na2O2 ⑥Ca(OH)2 ⑦HClO ⑧ I2
(3)只存在非极性键的是
(4)既含有共价键又含有离子键的是
(5)当其熔化时,不破坏化学键的是
您最近一年使用:0次



