下表是元素周期表的一部分,根据所给的10种元素,完成以下各小题。
(1)金属性最强的元素是___________ (填元素符号)。最不活泼元素的原子结构示意图为___________ 。
(2)第3周期元素中,其最高价氧化物对应的水化物具有两性的元素是___________ (填元素名称)。Na、Mg两种元素中,原子半径较大的是___________ 。
(3)第3周期元素中,其元素的一种氧化物是形成酸雨的主要物质,该氧化物的化学式为___________ 。
(4)工业上可以用Cl2和H2来制取盐酸,该反应的化学方程式为___________ 。
(5)由碳与氢元素形成的最简单有机物的化学式为___________ ,该物质中碳元素与氢元素的质量比为___________ ,其分子立体构型为___________ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | H | |||||||
| 2 | C | N | F | Ne | ||||
| 3 | Na | Mg | Al | S | Cl |
(2)第3周期元素中,其最高价氧化物对应的水化物具有两性的元素是
(3)第3周期元素中,其元素的一种氧化物是形成酸雨的主要物质,该氧化物的化学式为
(4)工业上可以用Cl2和H2来制取盐酸,该反应的化学方程式为
(5)由碳与氢元素形成的最简单有机物的化学式为
更新时间:2024-04-24 11:18:23
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】下表是某城市某日空气质量报告:
该市某校研究性学习小组对表中首要污染物 导致酸雨的成因进行探究。
导致酸雨的成因进行探究。
(1)以下氧化物引起的环境问题对应不正确的是___________。
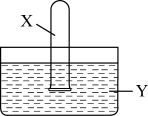
(2)将装满气体X的试管倒置于装有液体Y的水槽中,下列说法合理的是___________。
| 污染指数 | 首要污染物 | 空气质量级别 | 空气质量状况 |
| 55 |  | Ⅱ | 良 |
 导致酸雨的成因进行探究。
导致酸雨的成因进行探究。(1)以下氧化物引起的环境问题对应不正确的是___________。
| 选项 | A | B | C | D |
| 氧化物 |  |  | CO |  |
| 环境问题 | 温室效应 | 酸雨 | 破坏臭氧层 | 光化学烟雾 |
| A.A | B.B | C.C | D.D |
(2)将装满气体X的试管倒置于装有液体Y的水槽中,下列说法合理的是___________。

| 气体X | 液体Y | 试管内现象 | |
| A |  | 滴有品红的水溶液 | 无明显现象 |
| B |  | 水 | 充满无色溶液 |
| C |  | 滴有酚酞的水溶液 | 充满红色溶液 |
| D |  | NaOH溶液 | 无明显现象 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】“环境是民生,青山是美丽,蓝天也是幸福”。对生态环境污染问题,我们必须正视问题、着力解决问题。
Ⅰ.随着我国汽车年销量的大幅增加,空气环境受到了很大的污染。汽车尾气净化装置“催化转化器”是防止尾气(含一氧化碳、氮氧化物等气体)污染的有效方法,能使尾气中的一氧化碳和氮氧化物发生反应生成可参与大气生态循环的无毒气体。
(1)汽车尾气中易造成光化学烟雾的物质是______ 。
a.氮氧化物 b.二氧化碳 c.一氧化碳
(2)汽车尾气装置里,气体在催化剂表面吸附与解吸作用的过程如图所示:______ 。
(3)可利用CH4等气体除去烟气中的氮氧化物,生成物为可参与大气循环的气体,请写出CH4与NO反应的化学方程式______ 。
(4)采用NaOH溶液可以吸收废气中的氮氧化物,反应的化学方程式如下: 。若反应时消耗了10L
。若反应时消耗了10L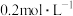 的NaOH溶液,则反应中转移电子的物质的量
的NaOH溶液,则反应中转移电子的物质的量______ mol。
Ⅱ.硫有多种化合物,如H2S、SO2等,它们对环境均有一定的影响,含硫化合物的综合利用既可以消除污染,又可以带来一定的经济效益。
(5)煤液化过程中产生的H2S可生产硫酸,部分过程如图所示:______ 。
(6)有学者提出利用Fe3+、Fe2+等离子的作用,在常温下将SO2氧化成 而实现SO2的回收利用,写出Fe3+将SO2氧化成
而实现SO2的回收利用,写出Fe3+将SO2氧化成 反应的离子方程式
反应的离子方程式______ 。
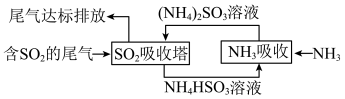
(7)某企业利用下列流程综合处理工厂排放的含;SO2的烟气,以减少其对环境造成的污染。“SO2吸收塔”中发生反应的化学方程式为______ ,该流程中可循环利用的物质为______ (填化学式)。
Ⅰ.随着我国汽车年销量的大幅增加,空气环境受到了很大的污染。汽车尾气净化装置“催化转化器”是防止尾气(含一氧化碳、氮氧化物等气体)污染的有效方法,能使尾气中的一氧化碳和氮氧化物发生反应生成可参与大气生态循环的无毒气体。
(1)汽车尾气中易造成光化学烟雾的物质是
a.氮氧化物 b.二氧化碳 c.一氧化碳
(2)汽车尾气装置里,气体在催化剂表面吸附与解吸作用的过程如图所示:
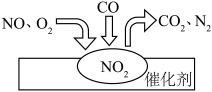
(3)可利用CH4等气体除去烟气中的氮氧化物,生成物为可参与大气循环的气体,请写出CH4与NO反应的化学方程式
(4)采用NaOH溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
 。若反应时消耗了10L
。若反应时消耗了10L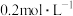 的NaOH溶液,则反应中转移电子的物质的量
的NaOH溶液,则反应中转移电子的物质的量Ⅱ.硫有多种化合物,如H2S、SO2等,它们对环境均有一定的影响,含硫化合物的综合利用既可以消除污染,又可以带来一定的经济效益。
(5)煤液化过程中产生的H2S可生产硫酸,部分过程如图所示:

(6)有学者提出利用Fe3+、Fe2+等离子的作用,在常温下将SO2氧化成
 而实现SO2的回收利用,写出Fe3+将SO2氧化成
而实现SO2的回收利用,写出Fe3+将SO2氧化成 反应的离子方程式
反应的离子方程式(7)某企业利用下列流程综合处理工厂排放的含;SO2的烟气,以减少其对环境造成的污染。“SO2吸收塔”中发生反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】硫酸型酸雨的形成原理可简化表示如下:
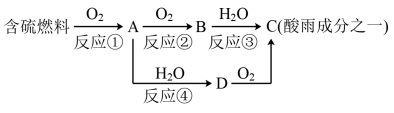
回答下列问题:
(1)A物质的化学式_________ ,B物质的化学式_________ 。
(2)根据SO2的性质,可让工厂的烟道气通过________ 除去SO2,达到减少污染的目的。
(3)现有雨水样品1份,每隔一段时间测定该雨水样品的pH,所得数据如下:
注 溶液的pH越大,H+的物质的量浓度就越小。
①雨水样品的pH变化的原因是____________ (用化学方程式表示)。
②如果将刚取样的上述雨水和用氯气消毒的自来水相混合,pH将_________ (填“增大”“减小”或“不变”),原因是(用化学方程式表示):_____________ 。
(4)你认为减少酸雨产生可采用的措施是_________ (填序号)。
①少用煤做燃料;②把工厂烟囱造高;③燃料脱硫;④在已酸化的土壤中加石灰;⑤开发新能源

回答下列问题:
(1)A物质的化学式
(2)根据SO2的性质,可让工厂的烟道气通过
(3)现有雨水样品1份,每隔一段时间测定该雨水样品的pH,所得数据如下:
| 测试时间/h | 0 | 1 | 2 | 3 | 4 |
| 雨水的pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
注 溶液的pH越大,H+的物质的量浓度就越小。
①雨水样品的pH变化的原因是
②如果将刚取样的上述雨水和用氯气消毒的自来水相混合,pH将
(4)你认为减少酸雨产生可采用的措施是
①少用煤做燃料;②把工厂烟囱造高;③燃料脱硫;④在已酸化的土壤中加石灰;⑤开发新能源
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表为元素周期表的一部分,请参照元素①-⑩在表中的位置,用化学用语回答下列问题:
(1)非金属性最强的是___ (填元素名称),化学性质最不活泼的是____ (填元素符号)。
(2)元素①-⑩中半径最大的元素是____ (填元素符号)
(3)②、③、⑨的最高价含氧酸的酸性由强到弱的顺序是________ 。(填化学式)
(4)表中能形成两性氢氧化物的元素是______ (填元素符号)
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
1 | ① | |||||||
2 | ② | ③ | ④ | ⑤ | ||||
3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)元素①-⑩中半径最大的元素是
(3)②、③、⑨的最高价含氧酸的酸性由强到弱的顺序是
(4)表中能形成两性氢氧化物的元素是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】元素周期表反映了元素之间的内在联系,是研究物质性质的重要工具。下图是元素周期表的一部分,请结合推断回答下列问题:________ (填元素符号);简单离子半径最小的元素是:________ (填离子符号)。
(2)由这些元素中原子半径最大与最小的两种元素形成的化合物X的电子式为________ ;画出X中阴离子的离子结构示意图:________ 。
(3)⑦⑧两种元素的最高价氧化物的水化物酸性较强的是________ (填化学式)。
(4)⑥的单质与强碱反应的离子方程式为________ 。
(5)根据周期表的结构特点,推断在第四周期中与⑤和⑥同族的元素原子序数相差________ 。
(6)查阅资料可知:⑤的单质可以在①的最高价氧化物中燃烧,瓶壁上出现大量白色和黑色的颗粒,试写出发生反应的化学方程式:________ 。
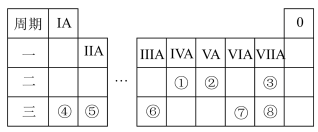
(2)由这些元素中原子半径最大与最小的两种元素形成的化合物X的电子式为
(3)⑦⑧两种元素的最高价氧化物的水化物酸性较强的是
(4)⑥的单质与强碱反应的离子方程式为
(5)根据周期表的结构特点,推断在第四周期中与⑤和⑥同族的元素原子序数相差
(6)查阅资料可知:⑤的单质可以在①的最高价氧化物中燃烧,瓶壁上出现大量白色和黑色的颗粒,试写出发生反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】元素周期表的一部分如图所示。回答下列问题:
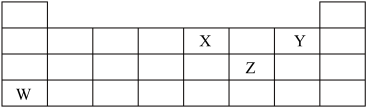
(1)X的原子结构示意图为____ ,其最简单氢化物的电子式为_____ 。
(2)Y 元素位于元素周期表中第_____ 周期_______ 族。
(3)Z、Y 最简单氢化物热稳定性由强到弱的顺序为________ (填化学式)。
(4)W 的最高价氧化物对应水化物的化学式为_____ ,该水化物中含有______ (填“共价键”、“离子键”)。
(5)用电子式表示 WY 的形成过程:__________ 。

(1)X的原子结构示意图为
(2)Y 元素位于元素周期表中第
(3)Z、Y 最简单氢化物热稳定性由强到弱的顺序为
(4)W 的最高价氧化物对应水化物的化学式为
(5)用电子式表示 WY 的形成过程:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分,其中每个数字序号代表一种短周期元素。
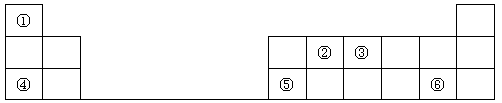
请按要求回答下列问题:
(1) 写出②的元素名称__________ ;
(2) 将④、⑤和⑥三种元素相比较,金属性最强的是__________ (填元素符号);
(3) 元素③的最高价氧化物对应的水化物的化学式为____________________ ;
(4) 元素③和元素⑥的氢化物均极易溶于水,用两根玻璃棒分别蘸取它们的浓溶液,相互接近时,可看到大量的白烟,写出产生该现象的化学方程式___________________ 。

请按要求回答下列问题:
(1) 写出②的元素名称
(2) 将④、⑤和⑥三种元素相比较,金属性最强的是
(3) 元素③的最高价氧化物对应的水化物的化学式为
(4) 元素③和元素⑥的氢化物均极易溶于水,用两根玻璃棒分别蘸取它们的浓溶液,相互接近时,可看到大量的白烟,写出产生该现象的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下表列出了 九种元素在周期表中的位置:
九种元素在周期表中的位置:
请回答下列问题:
(1)i元素与h元素形成化合物的电子式是_____ ,高温灼烧该化合物时,火焰呈_____ 色。
(2)b、c、g三种元素的简单离子半径由大到小的顺序是_____ (填离子符号);b、f、g三种元素对应简单氢化物的热稳定性由强到弱的顺序是_____ (填化学式)。
(3)元素 的单质与氢氧化钠溶液反应的离子方程式为
的单质与氢氧化钠溶液反应的离子方程式为_____ 。
(4)c元素氢化物与 发生反应的化学方程式为
发生反应的化学方程式为_____ ,所得溶液的
_____ 7.
(5)由a、h组成的一种化合物,分子中a、h原子最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,该化合物的结构式为_____ 。
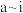 九种元素在周期表中的位置:
九种元素在周期表中的位置:| 周期 | 族 | |||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | a | b | ||||||
| 3 | c | d | e | f | g | h | ||
| 4 | i | |||||||
(1)i元素与h元素形成化合物的电子式是
(2)b、c、g三种元素的简单离子半径由大到小的顺序是
(3)元素
 的单质与氢氧化钠溶液反应的离子方程式为
的单质与氢氧化钠溶液反应的离子方程式为(4)c元素氢化物与
 发生反应的化学方程式为
发生反应的化学方程式为
(5)由a、h组成的一种化合物,分子中a、h原子最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,该化合物的结构式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下列曲线表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的性质);

把与下面的元素有关性质相符的曲线的标号填入相应括号中:
(1)ⅡA族元素的价电子数( )
(2)ⅦA族元素氢化物的沸点( )
(3)第三周期元素单质的熔点( )
(4)第三周期元素的最高正化合价( )
(5)IA族元素单质熔点( )
(6)F-、 Na+、Mg2+、 Al3+四种离子的离子半径( )
(7)某短周期元素的原子半径( )
(8)某短周期元素的第一电离能( )
(9)电离能是指由蒸气状态的孤立原子失去电子形成阳离子需要的能量。从中性原子中移去第一个电子所需要的能量为第一电离能(I1),移去第二个电子所需要的能量为第二电离能(I2),依次类推,现有5种元素,A、B、 C、 D、 E,其I1~I3分别如下表,根据表中数据判断其中最有可能是稀有气体元素的是____ ,最活泼的金属元素是_____ 。

把与下面的元素有关性质相符的曲线的标号填入相应括号中:
(1)ⅡA族元素的价电子数
(2)ⅦA族元素氢化物的沸点
(3)第三周期元素单质的熔点
(4)第三周期元素的最高正化合价
(5)IA族元素单质熔点
(6)F-、 Na+、Mg2+、 Al3+四种离子的离子半径
(7)某短周期元素的原子半径
(8)某短周期元素的第一电离能
(9)电离能是指由蒸气状态的孤立原子失去电子形成阳离子需要的能量。从中性原子中移去第一个电子所需要的能量为第一电离能(I1),移去第二个电子所需要的能量为第二电离能(I2),依次类推,现有5种元素,A、B、 C、 D、 E,其I1~I3分别如下表,根据表中数据判断其中最有可能是稀有气体元素的是
| 元 素 | I1/eV | I2/eV | I3/eV |
| A | 13.0 | 23.9 | 40.0 |
| B | 4.3 | 31.9 | 47.8 |
| C | 5.7 | 47.4 | 71.8 |
| D | 7.7 | 15.1 | 80.3 |
| E | 21.6 | 41.1 | 65.2 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】元素周期表可以用于探寻各种元素间的内在联系。
(1)下列关于元素周期表的说法错误的是______ 。
a.门捷列夫按照原子的核电荷数由小到大排列制出了第一张元素周期表
b.元素周期表由三个短周期,四个长周期构成
c.在金属和非金属的分界线处寻找半导体材料
d.元素周期表中含有主族、副族、第VⅢ族、0族等十八个族
(2)利用元素在周期表中的位置、结构、性质的关系,得出的结论正确的是______ 。
a.原子半径:Li>Na>K b.酸性:H3PO4>H2SO4>HClO4
c.稳定性:H2Se>H2S>H2O d.碱性:NaOH>Mg(OH)2>Al(OH)3
(3)碳族元素包括:C、Si、Ge、Sn、Pb、Fl(放射性元素)
①请完成CO2和KOH溶液恰好反应生成正盐的离子方程式_______ 。
②写出Si在元素周期表中的位置_______ 。由碳族元素结构特点,可推测Pb3O4中Pb的化合价为_____ 。
(4)卤族元素包括:F、Cl、Br、I、At(放射性元素)
①Br与F的原子序数的差值为______ 。
②已知某溶液中只含有Fe2+、Cl﹣、Br﹣、I﹣,且c(Cl﹣):c(Br﹣):c(I﹣)=1:1:2,则c(Fe2+):c(Br﹣)=____ 。向其中通入一定量的氯气发生反应,当c(Fe2+):c(Cl﹣)=1:4时,离子方程式为_____ 。
(1)下列关于元素周期表的说法错误的是
a.门捷列夫按照原子的核电荷数由小到大排列制出了第一张元素周期表
b.元素周期表由三个短周期,四个长周期构成
c.在金属和非金属的分界线处寻找半导体材料
d.元素周期表中含有主族、副族、第VⅢ族、0族等十八个族
(2)利用元素在周期表中的位置、结构、性质的关系,得出的结论正确的是
a.原子半径:Li>Na>K b.酸性:H3PO4>H2SO4>HClO4
c.稳定性:H2Se>H2S>H2O d.碱性:NaOH>Mg(OH)2>Al(OH)3
(3)碳族元素包括:C、Si、Ge、Sn、Pb、Fl(放射性元素)
①请完成CO2和KOH溶液恰好反应生成正盐的离子方程式
②写出Si在元素周期表中的位置
(4)卤族元素包括:F、Cl、Br、I、At(放射性元素)
①Br与F的原子序数的差值为
②已知某溶液中只含有Fe2+、Cl﹣、Br﹣、I﹣,且c(Cl﹣):c(Br﹣):c(I﹣)=1:1:2,则c(Fe2+):c(Br﹣)=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下表是元素周期表的一部分,请回答有关问题:
(1)①的元素符号为 _________ ;
(2)第3周期主族元素中,原子半径最小的是_________ (用元素符号表示)。
(3)表中元素的气态氢化物中最稳定的是______________ (用化学式表示)。
(4)①、②、⑦、⑧四种元素的最高价氧化物的水化物中酸性最强的是______ (用化学式表示)。
(5)①和⑧形成化合物的电子式为_________________
(6)④和⑥两种元素的最高价氧化物的水化物在水溶液中反应的离子方程式为__________ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)第3周期主族元素中,原子半径最小的是
(3)表中元素的气态氢化物中最稳定的是
(4)①、②、⑦、⑧四种元素的最高价氧化物的水化物中酸性最强的是
(5)①和⑧形成化合物的电子式为
(6)④和⑥两种元素的最高价氧化物的水化物在水溶液中反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】门捷列夫认为氮、碳、氧、氢是“四大天王”元素,它们与宇宙和生命的形成都有密切联系,可以相互结合成很多化合物。
(1)四种元素中,核外未成对电子数目相同的元素有___________ (填写元素符号,下同);四种元素的原子半径由大到小的顺序为___________ 。
(2)HCN是生命演化过程中的基础物质之一。已知HCN中C、N都满足8电子稳定结构,则HCN的电子式为___________ ;其中C、N之间的共用电子对偏向的元素是___________ ,从原子结构角度解释其原因___________ 。
(3)N2O是医学上的一-种麻醉剂,可以通过反应NH3+O2→N2O+H2O制得,配平该反应的化学方程式___________ ,若生成1.8g水,转移的电子数目为___________ 个(结构保留两位有效数字)。
(1)四种元素中,核外未成对电子数目相同的元素有
(2)HCN是生命演化过程中的基础物质之一。已知HCN中C、N都满足8电子稳定结构,则HCN的电子式为
(3)N2O是医学上的一-种麻醉剂,可以通过反应NH3+O2→N2O+H2O制得,配平该反应的化学方程式
您最近一年使用:0次



