解题方法
1 . 下列装置或试剂合理且能达到实验目的的是
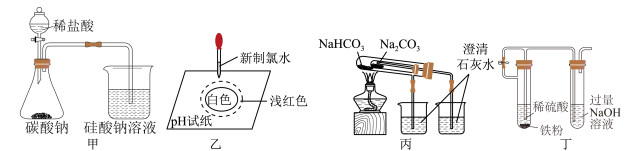
A.用装置甲可以证明非金属性强弱: |
B.乙实验说明新制氯水中含有 和 和 |
C.装置丙可以用于比较 和 和 的热稳定性 的热稳定性 |
| D.装置丁能较长时间观察到有白色沉淀生成 |
您最近半年使用:0次
名校
2 . 下表列出①~⑦七种元素在周期表中的位置。
请按要求回答:
(1)七种元素中,原子半径最大的是(填元素符号)____________ 。
(2)③与⑦的气态氢化物中,稳定性较强的是(填化学式)___________ 。
(3)元素⑥的最高价氧化物对应的水化物是(填化学式)__________ 。含有元素⑥的物质中用于制芯片和太阳能电池的是__________ (填物质名称),用于生产光导纤维的是___________ (填物质名称)。
(4)由①、②、③三种元素组成的离子化合物是_____________ 。
(5)含有上述元素的物质间存在以下转化。__________ 。X生成⑤的单质的化学方程式是____________ 。
族 周期 | ⅠA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ||||||
3 | ④ | ⑤ | ⑥ | ⑦ | ||||
(1)七种元素中,原子半径最大的是(填元素符号)
(2)③与⑦的气态氢化物中,稳定性较强的是(填化学式)
(3)元素⑥的最高价氧化物对应的水化物是(填化学式)
(4)由①、②、③三种元素组成的离子化合物是
(5)含有上述元素的物质间存在以下转化。
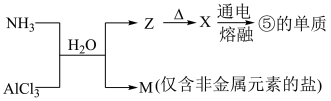
您最近半年使用:0次
3 . 已知短周期元素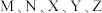 分布在三个周期,
分布在三个周期, 最外层电子数相同,
最外层电子数相同, 原子序数大于
原子序数大于 ,其中
,其中 的简单离子半径在同周期中最小,
的简单离子半径在同周期中最小, 单质极易与常见无色无味液态物质发生置换反应且作氧化剂,在短周期中
单质极易与常见无色无味液态物质发生置换反应且作氧化剂,在短周期中 的最高价氧化物对应水化物的碱性最强。回答下列问题:
的最高价氧化物对应水化物的碱性最强。回答下列问题:
(1) 在元素周期表中的位置是
在元素周期表中的位置是___________ , 元素的离子结构示意图:
元素的离子结构示意图:___________ ,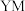 的电子式:
的电子式:___________ 。
(2) 的简单氢化物熔、沸点更高的是
的简单氢化物熔、沸点更高的是___________ (填化学式),原因是___________ 。
(3)在 与
与 的混合液中,通入足量
的混合液中,通入足量 ,是工业制取
,是工业制取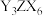 的一种方法,写出该反应的化学方程式:
的一种方法,写出该反应的化学方程式:___________ 。
(4)镓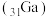 的化合物氮化镓(
的化合物氮化镓(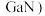 和砷化镓(
和砷化镓( )作为第三代半导体材料,具有耐高温、耐高电压等特性,随着
)作为第三代半导体材料,具有耐高温、耐高电压等特性,随着 技术的发展,它们的商用价值进入“快车道”。
技术的发展,它们的商用价值进入“快车道”。
①下列有关说法正确的是___________ 。(填字母)
a. 位于元素周期表第四周期第ⅣA族
位于元素周期表第四周期第ⅣA族
b. 为门捷列夫预言的“类铝”
为门捷列夫预言的“类铝”
c. 的最高价氧化物对应水化物的碱性比
的最高价氧化物对应水化物的碱性比 元素最高价氧化物对应水化物的碱性强
元素最高价氧化物对应水化物的碱性强
d.酸性:
②废弃的含 的半导体材料可以用浓硝酸溶解,放出
的半导体材料可以用浓硝酸溶解,放出 气体,同时生成
气体,同时生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
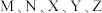 分布在三个周期,
分布在三个周期, 最外层电子数相同,
最外层电子数相同, 原子序数大于
原子序数大于 ,其中
,其中 的简单离子半径在同周期中最小,
的简单离子半径在同周期中最小, 单质极易与常见无色无味液态物质发生置换反应且作氧化剂,在短周期中
单质极易与常见无色无味液态物质发生置换反应且作氧化剂,在短周期中 的最高价氧化物对应水化物的碱性最强。回答下列问题:
的最高价氧化物对应水化物的碱性最强。回答下列问题:(1)
 在元素周期表中的位置是
在元素周期表中的位置是 元素的离子结构示意图:
元素的离子结构示意图: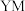 的电子式:
的电子式:(2)
 的简单氢化物熔、沸点更高的是
的简单氢化物熔、沸点更高的是(3)在
 与
与 的混合液中,通入足量
的混合液中,通入足量 ,是工业制取
,是工业制取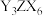 的一种方法,写出该反应的化学方程式:
的一种方法,写出该反应的化学方程式:(4)镓
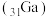 的化合物氮化镓(
的化合物氮化镓(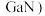 和砷化镓(
和砷化镓( )作为第三代半导体材料,具有耐高温、耐高电压等特性,随着
)作为第三代半导体材料,具有耐高温、耐高电压等特性,随着 技术的发展,它们的商用价值进入“快车道”。
技术的发展,它们的商用价值进入“快车道”。①下列有关说法正确的是
a.
 位于元素周期表第四周期第ⅣA族
位于元素周期表第四周期第ⅣA族b.
 为门捷列夫预言的“类铝”
为门捷列夫预言的“类铝”c.
 的最高价氧化物对应水化物的碱性比
的最高价氧化物对应水化物的碱性比 元素最高价氧化物对应水化物的碱性强
元素最高价氧化物对应水化物的碱性强d.酸性:

②废弃的含
 的半导体材料可以用浓硝酸溶解,放出
的半导体材料可以用浓硝酸溶解,放出 气体,同时生成
气体,同时生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为
您最近半年使用:0次
解题方法
4 . 下图是部分短周期元素原子半径与原子序数的关系图。下列说法正确的是
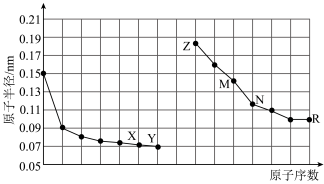
A. 两种元素只形成一种化合物 两种元素只形成一种化合物 |
B. 与 与 形成的化合物是共价化合物 形成的化合物是共价化合物 |
C.最高价氧化物对应的水化物的碱性: |
D. 元素气态氢化物的稳定性: 元素气态氢化物的稳定性: |
您最近半年使用:0次
解题方法
5 . 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验:
(1)将大小相同的钠、镁、铝(除去氧化膜)分别投入到冷水中,反应最剧烈的是___________ ;分别向新制取的 沉淀中滴加稀盐酸和氢氧化钠溶液,结果沉淀都溶解,说明
沉淀中滴加稀盐酸和氢氧化钠溶液,结果沉淀都溶解,说明 是
是___________ 氢氧化物,其中 与氢氧化钠溶液反应的离子方程式为
与氢氧化钠溶液反应的离子方程式为___________ 。
(2)利用如图装置验证碳、硅、硫三种元素的非金属性强弱。
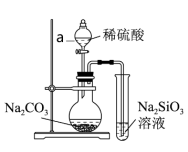
①图中仪器a的名称是___________ ,圆底烧瓶中发生反应的离子方程式为___________ 。
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是___________ ,该实验能证明非金属性强弱,依据的原理是___________ 。
(1)将大小相同的钠、镁、铝(除去氧化膜)分别投入到冷水中,反应最剧烈的是
 沉淀中滴加稀盐酸和氢氧化钠溶液,结果沉淀都溶解,说明
沉淀中滴加稀盐酸和氢氧化钠溶液,结果沉淀都溶解,说明 是
是 与氢氧化钠溶液反应的离子方程式为
与氢氧化钠溶液反应的离子方程式为(2)利用如图装置验证碳、硅、硫三种元素的非金属性强弱。

①图中仪器a的名称是
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是
您最近半年使用:0次
6 . 下图是短周期元素 在元素周期表中的位置。
在元素周期表中的位置。 在周期表中的位置是第
在周期表中的位置是第___________ 周期第___________ 族。
(2)b、c、e三种元素原子半径由大到小的顺序是___________ (填元素符号)。
(3)非金属性:e___________ f(填“ ”或“
”或“ ”),从原子结构角度解释其原因是
”),从原子结构角度解释其原因是___________ 。
(4)b、f两种元素形成的化合物有重要的用途,高温灼烧该化合物时,火焰呈___________ 色;用电子式表示a、f形成化合物的过程___________ 。
 在元素周期表中的位置。
在元素周期表中的位置。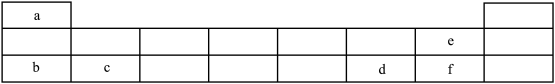
 在周期表中的位置是第
在周期表中的位置是第(2)b、c、e三种元素原子半径由大到小的顺序是
(3)非金属性:e
 ”或“
”或“ ”),从原子结构角度解释其原因是
”),从原子结构角度解释其原因是(4)b、f两种元素形成的化合物有重要的用途,高温灼烧该化合物时,火焰呈
您最近半年使用:0次
名校
解题方法
7 . X、Y、Z、M、Q、R皆为前20号元素,其原子半径与化合价的关系如图所示。下列说法错误的是
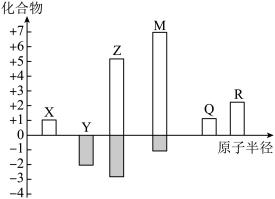
| A.Q位于第三周期第ⅠA族 |
| B.X、Y、Z三种元素组成的化合物可能是盐或碱 |
| C.Y、Z最简单氢化物稳定性:Z>Y |
| D.Z与M的最高价氧化物对应的水化物均为强酸 |
您最近半年使用:0次
名校
解题方法
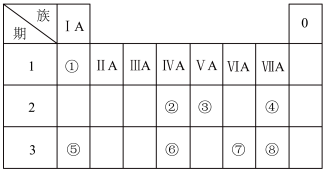
8 . 下表是元素周期表的一部分,表中所列的数字分别代表某一种元素。针对表中①~⑧号元素回答下列问题。________ ,它的沸点比PH3高,原因是________________ ;
(2)测定文物年代需要利用元素②的一种中子数为8的核素,该核素符号可表示为________ ;
(3)元素①和氧元素形成的18电子化合物的名称是:________ ,该化合物中含有的化学键有________ (填“离子键、极性键、非极性键”);
(4)元素④、⑤、⑧中,原子半径最大的是________ (填元素符号),离子半径最大的是________ (填化学式)。
(5)可以证明元素⑧比元素⑦非金属性强的一个化学反应方程式是:________ 。
(2)测定文物年代需要利用元素②的一种中子数为8的核素,该核素符号可表示为
(3)元素①和氧元素形成的18电子化合物的名称是:
(4)元素④、⑤、⑧中,原子半径最大的是
(5)可以证明元素⑧比元素⑦非金属性强的一个化学反应方程式是:
您最近半年使用:0次
名校
9 . 13Al、15P、16S、17Cl是周期表中的短周期主族元素。下列有关说法正确的是
| A.元素Al在周期表中位于第三周期IIA族 |
| B.元素P的简单气态氢化物的化学式为PH4 |
| C.原子半径:r(Al)<r(P)<r(S)<r(Cl) |
| D.最高价氧化物的水化物的酸性:H3PO4<H2SO4<HClO4 |
您最近半年使用:0次
名校
10 . 反应Na2HPO4+NH3·H2O+MgCl2=NH4MgPO4↓+2NaCl+H2O可用于处理含磷废水,下列说法正确的是
| A.半径大小:r(Na+)>r(Mg2+) | B.酸性强弱:H3PO4>HClO4 |
| C.碱性强弱:Mg(OH)2>NaOH | D.非金属性强弱:N>O |
您最近半年使用:0次



