I、按要求写出下列方程式:
(1)FeCl3水解的离子方程式:___________ 。
(2)NaHCO3水解的离子方程式:___________ 。
(3)NH3•H2O的电离方程式:___________ 。
(4)Mg(OH)2在水中的沉淀溶解平衡用离子方程式表示:___________ 。
Ⅱ、回答下列问题。
(5)25℃时,0.01mol/L的NaOH溶液的pH=___________ ;由水电离出c(H+)=___________ mol/L。
(6)25℃时,将10mLpH=2醋酸溶液稀释到1000mL后溶液的pH___________ 4(填“大于”“小于”或“等于”)。
(7)某温度时,Ksp[AgI]=9.0×10-16,求AgI饱和溶液中c(Ag+)=___________ mol/L
(1)FeCl3水解的离子方程式:
(2)NaHCO3水解的离子方程式:
(3)NH3•H2O的电离方程式:
(4)Mg(OH)2在水中的沉淀溶解平衡用离子方程式表示:
Ⅱ、回答下列问题。
(5)25℃时,0.01mol/L的NaOH溶液的pH=
(6)25℃时,将10mLpH=2醋酸溶液稀释到1000mL后溶液的pH
(7)某温度时,Ksp[AgI]=9.0×10-16,求AgI饱和溶液中c(Ag+)=
更新时间:2024-05-20 20:08:01
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】(1)书写氢氧化铝的电离方程式:___ 。
(2)书写明矾净水的离子方程式:___ 。
(3)铝与氢氧化钠溶液反应的化学反应方程式:___ 。
(4)用一个化学反应方程式来证明氯元素的非金属性比硫元素强:___ 。
(5)书写铁和水反应的化学方程式:___ 。
(2)书写明矾净水的离子方程式:
(3)铝与氢氧化钠溶液反应的化学反应方程式:
(4)用一个化学反应方程式来证明氯元素的非金属性比硫元素强:
(5)书写铁和水反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】下列物质中①CO2 ②NaClO溶液 ③NaHCO3固体 ④C12H22O11(蔗糖) ⑤H2SO4溶液 ⑥铁
(1)能导电的是______ ;属于非电解质的是______ ;(以上填写物质编号);
(2)属于电解质的写出在水溶液中的电离方程式_____________________ 。
(3)配平化学方程式:NaClO+NaI═NaIO3+NaCl__________ 。
(1)能导电的是
(2)属于电解质的写出在水溶液中的电离方程式
(3)配平化学方程式:NaClO+NaI═NaIO3+NaCl
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】I.根据物质的组成、结构、性质等进行分类,可预测物质的性质及变化:
现有下列九种物质:①HCl气体②固体Cu③乙醇④CO2⑤熔融NaCl⑥Al2O3固体⑦硫酸溶液⑧NaHCO3固体⑨BaSO4固体。按照不同的依据对其进行分类:
(1)所给状态能导电的是________ ,属于电解质的是_______ ;(均填序号)。
(2)属于酸式盐的物质为___________ (填序号),其电离方程式为___________ 。
Ⅱ.物质的量是联系宏观和微观的桥梁:
(3)40.5g某金属氧化物MCl2中含0.6molCl-,则该氯化物的摩尔质量为___________ 。
(4)标准状况下,与34g的H2S气体含相同H原子数的CH4的体积为___________ 。
(5)在同温同压下,等质量的CO和CO2.其体积之比为___________ ,密度之比为___________ 。
现有下列九种物质:①HCl气体②固体Cu③乙醇④CO2⑤熔融NaCl⑥Al2O3固体⑦硫酸溶液⑧NaHCO3固体⑨BaSO4固体。按照不同的依据对其进行分类:
(1)所给状态能导电的是
(2)属于酸式盐的物质为
Ⅱ.物质的量是联系宏观和微观的桥梁:
(3)40.5g某金属氧化物MCl2中含0.6molCl-,则该氯化物的摩尔质量为
(4)标准状况下,与34g的H2S气体含相同H原子数的CH4的体积为
(5)在同温同压下,等质量的CO和CO2.其体积之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】类别万千的酸碱溶液共同构筑了化学世界的丰富多彩。
(1)现有常温下pH=2的盐酸(甲)、pH=2的醋酸溶液(乙)和0.1mol/LNH3∙H2O(丙),请根据下列操作回答:
①常温下,将丙溶液加水稀释,下列数值一定变小的是_____ (填字母)。
A. B.
B. C.
C. D.
D.
②常温下,取甲、乙各1mL分别稀释至100mL,稀释后,水的电离程度:乙_____ 甲(填“>”“<”或“=”)。
(2)①某温度时,测得0.01mol/LNaOH溶液pH为11,则该温度_____ 25℃。(填“>”“<”或“=”)
②相同条件下,取等体积、等pH的Ba(OH)2、NaOH和NH3∙H2O三种碱溶液,分别滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为 、
、 、
、 ,则三者的大小关系为
,则三者的大小关系为_____ 。
(3)已知:在25℃,有关弱电解质的电离平衡常数如下表有下表:
①将SO2通入氨水中,当c(OH-)降至1.0×10-7mol∙L-1时,溶液中的 =
=_____ 。
②下列微粒在溶液中不能大量共存的是_____ 。
A. 、
、 B.
B. 、
、 C.
C. 、
、 D.
D. 、
、
(1)现有常温下pH=2的盐酸(甲)、pH=2的醋酸溶液(乙)和0.1mol/LNH3∙H2O(丙),请根据下列操作回答:
①常温下,将丙溶液加水稀释,下列数值一定变小的是
A.
 B.
B. C.
C. D.
D.
②常温下,取甲、乙各1mL分别稀释至100mL,稀释后,水的电离程度:乙
(2)①某温度时,测得0.01mol/LNaOH溶液pH为11,则该温度
②相同条件下,取等体积、等pH的Ba(OH)2、NaOH和NH3∙H2O三种碱溶液,分别滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为
 、
、 、
、 ,则三者的大小关系为
,则三者的大小关系为(3)已知:在25℃,有关弱电解质的电离平衡常数如下表有下表:
| 弱电解质 | H2SO3 | H2CO3 | HClO | NH3∙H2O |
| 电离平衡常数 |   |   |  |  |
 =
=②下列微粒在溶液中不能大量共存的是
A.
 、
、 B.
B. 、
、 C.
C. 、
、 D.
D. 、
、
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1)联氨(又称肼,N2H4,无色液体)为二元弱碱,在水中的电离方式与氨相似。写出在水中联氨第一步电离反应的方程式_______________ 。氯化镁溶液在某条件下可生Mg(OH)Cl沉淀,请写出相关离子方程式_________
(2)实验室可通过向盛装有碱石灰的锥形瓶中滴加浓氨水来制取氨气,请利用相关化学反应原理来解释______________________________
(3)室温下向10mL0.1 mol/L NaOH溶液中加入0.1mol/L的一元酸HA,溶液pH的变化曲线如图所示

则HA为_______ 电解质(填“强”或“弱”),a点所示溶液c(Na)_____ c(A)(填“>”、“<”或“”=),a、b两点所示溶液中水的电离程度a_______ b(填“>”、“<”或“"=)。
(4)25℃时0.05mol/L的醋酸溶液,pH=______ 该溶液中水电离出的c(H+)=____ (已知室温下醋酸电离平衡常数为2.0×10-5)
(5)常温下,0.01mol/L的HCN溶液加水稀释1000倍的过程中,下列选项增大的是_____
A.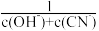 B.Kac(HCN) C.
B.Kac(HCN) C. D.
D.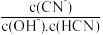
(2)实验室可通过向盛装有碱石灰的锥形瓶中滴加浓氨水来制取氨气,请利用相关化学反应原理来解释
(3)室温下向10mL0.1 mol/L NaOH溶液中加入0.1mol/L的一元酸HA,溶液pH的变化曲线如图所示

则HA为
(4)25℃时0.05mol/L的醋酸溶液,pH=
(5)常温下,0.01mol/L的HCN溶液加水稀释1000倍的过程中,下列选项增大的是
A.
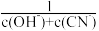 B.Kac(HCN) C.
B.Kac(HCN) C. D.
D.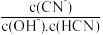
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】写出下列离子方程式:
(1)Na3PO4水解的离子方程式_____________________________________
(2)H2SO3的电离方程式__________________________________________
(3)CuCl2水解的离子方程式______________________________________
(4)碳酸钡的电离方程式_______________________________
(5)醋酸铵的电离方程式_______________________________
(6)Al2(SO4)3溶液和NaHCO3溶液混合的离子方程式_________________________________
(1)Na3PO4水解的离子方程式
(2)H2SO3的电离方程式
(3)CuCl2水解的离子方程式
(4)碳酸钡的电离方程式
(5)醋酸铵的电离方程式
(6)Al2(SO4)3溶液和NaHCO3溶液混合的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】请按照下列要求回答问题:
(1)电解氯化钠溶液的化学方程式:__________________________________ 。
(2)硫化钠水解的离子方程式:________________________________ 。
(3)0.1 mol/L 的碳酸钠溶液中离子浓度由大到小顺序为:__________________________ 。
(4)浓的 Al2(SO4)3 溶液和浓的小苏打(NaHCO3)溶液混合可用于灭火,请用离子反应方程式表示灭火的原理__________________________ 。
(5)将25℃下 pH=12 的 Ba(OH)2 溶液aL与 pH=1的HCl溶液bL 混合,若所得混合液为中性,则 a:b=__________________________ 。(溶液体积变化忽略不计)。
(6)pH=3 的 NH4Cl 溶液,由水电离出的 c(H+)=__________________________ 。
(7)常温时,Fe(OH)3 的溶度积常数 Ksp=1×10-38,要使溶液中的 Fe3+沉淀完全(残留的 c(Fe3+)<10-5 mol·L-1),则 溶液的 pH 应大于____________________________ 。
(1)电解氯化钠溶液的化学方程式:
(2)硫化钠水解的离子方程式:
(3)0.1 mol/L 的碳酸钠溶液中离子浓度由大到小顺序为:
(4)浓的 Al2(SO4)3 溶液和浓的小苏打(NaHCO3)溶液混合可用于灭火,请用离子反应方程式表示灭火的原理
(5)将25℃下 pH=12 的 Ba(OH)2 溶液aL与 pH=1的HCl溶液bL 混合,若所得混合液为中性,则 a:b=
(6)pH=3 的 NH4Cl 溶液,由水电离出的 c(H+)=
(7)常温时,Fe(OH)3 的溶度积常数 Ksp=1×10-38,要使溶液中的 Fe3+沉淀完全(残留的 c(Fe3+)<10-5 mol·L-1),则 溶液的 pH 应大于
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】二氧化硫直接排放会危害环境。利用工业废碱渣(主要成分Na2CO3)可吸收烟气中的SO2并制备无水Na2SO3,其流程如图1。

已知:H2SO3、HSO3−、SO32−在水溶液中的物质的量分数随pH的分布如图2,Na2SO3·7H2O和Na2SO3的溶解度曲线如图3。


(1)Na2CO3溶液显碱性,用离子方程式解释其原因:_____________________ 。
(2)吸收烟气
①为提高NaHSO3的产率,应控制吸收塔中的pH为________ 。
②已知下列反应:
SO2(g)+2OH−(aq)==SO32−(aq)+H2O(l)ΔH1=−164.3kJ·mol−1
CO2(g)+2OH−(aq)==CO32−(aq)+H2O(l)ΔH2=−109.4kJ·mol−1
2HSO3−(aq)==SO32−(aq)+SO2(g)+H2O(l)ΔH3=+34.0kJ·mol−1
吸收塔中Na2CO3溶液吸收SO2生成HSO3−的热化学方程式是________ 。
③吸收塔中的温度不宜过高,可能的原因是________ (写出1种即可)。
(3)制备无水Na2SO3
①中和塔中反应的离子方程式为_________________________________ 。
②从中和塔得到的Na2SO3溶液中要获得无水Na2SO3固体,需控制温度____________ ,同时还要_______________ ,以防止Na2SO3氧化。

已知:H2SO3、HSO3−、SO32−在水溶液中的物质的量分数随pH的分布如图2,Na2SO3·7H2O和Na2SO3的溶解度曲线如图3。


(1)Na2CO3溶液显碱性,用离子方程式解释其原因:
(2)吸收烟气
①为提高NaHSO3的产率,应控制吸收塔中的pH为
②已知下列反应:
SO2(g)+2OH−(aq)==SO32−(aq)+H2O(l)ΔH1=−164.3kJ·mol−1
CO2(g)+2OH−(aq)==CO32−(aq)+H2O(l)ΔH2=−109.4kJ·mol−1
2HSO3−(aq)==SO32−(aq)+SO2(g)+H2O(l)ΔH3=+34.0kJ·mol−1
吸收塔中Na2CO3溶液吸收SO2生成HSO3−的热化学方程式是
③吸收塔中的温度不宜过高,可能的原因是
(3)制备无水Na2SO3
①中和塔中反应的离子方程式为
②从中和塔得到的Na2SO3溶液中要获得无水Na2SO3固体,需控制温度
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】(1)如图1表示用相同浓度的NaOH溶液分别滴定浓度相同的3种一元酸,由图可确定酸性最强的是____ (填“①”、“②“或“③”)。如图2表示用相同浓度的硝酸银标准溶液分别滴定浓度相同的含Cl-、Br-及I-的混合溶液,由图可确定首先沉淀的离子是 _____ 。

(2)25℃时,Ksp(AgCl)=1.8×10-10,若向1L 0.1 mol·L-1的NaCl溶液中加入1L 0.2mol·L-1的硝酸银溶液,充分反应后溶液中c(Cl-)=________ (不考虑混合后溶液体积的变化)。

(2)25℃时,Ksp(AgCl)=1.8×10-10,若向1L 0.1 mol·L-1的NaCl溶液中加入1L 0.2mol·L-1的硝酸银溶液,充分反应后溶液中c(Cl-)=
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】通过计算比较铬酸银和氯化银溶解度的大小_______ ,已知Ksp(Ag2CrO4) = 1.12×10-12,而Ksp(AgCl) = 1.77×10-10。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】已知:部分难溶化合物的相关数据如下表所示:
用废电池的锌皮制备ZnSO4·7H2O的过程中,需除去锌皮中的少量杂质铁,其方法是加稀H2SO4和H2O2溶解,铁变为Fe3+,常温下加碱调节至pH为___________ 时,铁刚好沉淀完全(离子浓度小于1×10-5 mol·L-1时,即可认为该离子沉淀完全);继续加碱至pH为___________ 时,锌开始沉淀(假定Zn2+浓度为0.1 mol·L-1)。若上述过程不加H2O2,后果是___________ ,原因是___________ 。
| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-17 | 10-17 | 10-38 |
您最近一年使用:0次



