名校
解题方法
1 . Ⅰ.能源是人类物质文明发展的基石,太阳能是一种清洁、绿色的能量,基于太阳能广泛应用的太阳能电池主要类型有硅太阳能电池、薄膜太阳能电池、钙钛矿太阳能电池。
(1)下列关于太阳能电池的说法正确的是_______(填选项字母,下同)。
(2)硅是构成硅太阳能电池的主要材料,下列关于硅的说法错误的是_______。
(3)晶体硅的晶胞结构如图所示:_______ 个硅原子,晶胞中最近的两个硅原子的距离为_______  ,晶体硅的密度是
,晶体硅的密度是_______  。
。
Ⅱ.工业上高纯晶体硅的制备流程如下: 中元素的电负性由大到小的顺序是
中元素的电负性由大到小的顺序是_______ (填元素符号), 分子属于
分子属于_______ 分子(填“极性”或“非极性”)。
(1)下列关于太阳能电池的说法正确的是_______(填选项字母,下同)。
| A.太阳能电池能将太阳能百分之百地转化为电能 |
| B.太阳能电池与锂电池一样可以反复充电 |
| C.漆黑的夜晚太阳能电池也能实现太阳能向电能的转化 |
| D.戈壁、沙漠等日照充足、干旱少雨的地区适合大规模安装太阳能电池 |
(2)硅是构成硅太阳能电池的主要材料,下列关于硅的说法错误的是_______。
A.硅原子的价层电子排布式为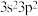 | B.硅原子核外有5种不同的空间运动状态 |
| C.硅原子核外有14种不同的电子运动状态 | D.硅元素属于s区元素 |
(3)晶体硅的晶胞结构如图所示:

 ,晶体硅的密度是
,晶体硅的密度是 。
。Ⅱ.工业上高纯晶体硅的制备流程如下:

 中元素的电负性由大到小的顺序是
中元素的电负性由大到小的顺序是 分子属于
分子属于
您最近一年使用:0次
名校
2 . 某温度时,在一个容积为2L的密闭容器中,X、Y、Z(Z为气体)三种物质的物质的量随时间的变化曲线如图所示:_______ 。
(2)反应开始至2min时,气体Z的平均反应速率为_______ 。
(3)若X、Y均为气体。
①反应达到平衡时压强是开始时的_______ 倍。
②反应达到平衡后,若将容器的体积缩小为原来的 ,重新达到平衡时,容器内温度升高(容器不与外界进行热交换),则该反应的正反应为
,重新达到平衡时,容器内温度升高(容器不与外界进行热交换),则该反应的正反应为_______ (填“放热”或“吸热”)反应。
(4)25℃时,取 的盐酸和醋酸各1mL,分别加水稀释,测得pH随溶液体积变化的曲线如图所示:
的盐酸和醋酸各1mL,分别加水稀释,测得pH随溶液体积变化的曲线如图所示:_______ 曲线(填“Ⅰ”或“Ⅱ”)代表盐酸的稀释过程。
②a点的导电性比c点的导电性_______ (填“强”或“弱”)。
③若将a、b两点的溶液加热至30℃,则 的值将
的值将_______ (填“变大”、“变小”或“不变”)。

(2)反应开始至2min时,气体Z的平均反应速率为
(3)若X、Y均为气体。
①反应达到平衡时压强是开始时的
②反应达到平衡后,若将容器的体积缩小为原来的
 ,重新达到平衡时,容器内温度升高(容器不与外界进行热交换),则该反应的正反应为
,重新达到平衡时,容器内温度升高(容器不与外界进行热交换),则该反应的正反应为(4)25℃时,取
 的盐酸和醋酸各1mL,分别加水稀释,测得pH随溶液体积变化的曲线如图所示:
的盐酸和醋酸各1mL,分别加水稀释,测得pH随溶液体积变化的曲线如图所示: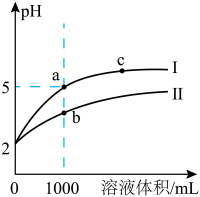
②a点的导电性比c点的导电性
③若将a、b两点的溶液加热至30℃,则
 的值将
的值将
您最近一年使用:0次
3 . N、S元素化合物知识在高中化学体系中占有重要地位,请根据题意回答下列问题。
(1)工业制硝酸中NH3的催化氧化化学方程式_______ 。
(2)检验溶液中含有NH4+的离子方程式_______ ,实验室一般使用_______ 检验该反应有氨气生成。
(3)向蔗糖中滴加浓硫酸,蔗糖变黑并膨胀,散发刺激性气味,说明浓硫酸具有_______ 和_______ 。(填浓硫酸的性质)
(4)铜与浓硫酸的化学反应方程式为_______ 。
(5)请用方程式解释实验室盛放碱液的试剂瓶不用玻璃塞的原因_______ 。
(1)工业制硝酸中NH3的催化氧化化学方程式
(2)检验溶液中含有NH4+的离子方程式
(3)向蔗糖中滴加浓硫酸,蔗糖变黑并膨胀,散发刺激性气味,说明浓硫酸具有
(4)铜与浓硫酸的化学反应方程式为
(5)请用方程式解释实验室盛放碱液的试剂瓶不用玻璃塞的原因
您最近一年使用:0次
名校
4 . 根据已学知识,请回答下列问题
(1)物质A的结构简式为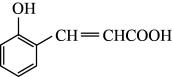 ,写出A中的含氧官能团名称
,写出A中的含氧官能团名称_____________________________ 。
(2)有机化合物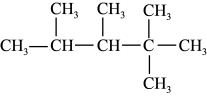 的名称是
的名称是_________________ ,其在核磁共振氢谱上有_________ 组峰。
(3)键线式 表示的有机物的分子式为
表示的有机物的分子式为 _________ ,其中等效氢个数比为_________________ 。
(4)写出1,3一丁二烯与 发生1,4-加成的反应方程式:
发生1,4-加成的反应方程式:_________________________________________________ 。
(5)与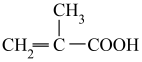 具有相同官能团的一种同分异构体的结构简式为
具有相同官能团的一种同分异构体的结构简式为_____________________ 。
(1)物质A的结构简式为
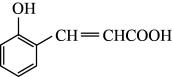 ,写出A中的含氧官能团名称
,写出A中的含氧官能团名称(2)有机化合物
 的名称是
的名称是(3)键线式
 表示的有机物的分子式为
表示的有机物的分子式为 (4)写出1,3一丁二烯与
 发生1,4-加成的反应方程式:
发生1,4-加成的反应方程式:(5)与
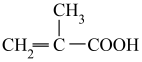 具有相同官能团的一种同分异构体的结构简式为
具有相同官能团的一种同分异构体的结构简式为
您最近一年使用:0次
名校
5 . 图所示为利用分类法对一组物质进行的分类。回答下列问题  属于
属于___________  填“酸性”或“碱性”
填“酸性”或“碱性” 氧化物,书写
氧化物,书写 与
与 反应的化学方程式
反应的化学方程式___________ ,依据该反应,可以说明
___________  填“属于”或“不属于”
填“属于”或“不属于” 碱性氧化物。
碱性氧化物。
(2)上述物质中属于电解质的是___________ 。
(3)某学生完成钠与水反应的实验,实验过程如图 、
、 、
、 所示,下列有关实验现象及结论的叙述
所示,下列有关实验现象及结论的叙述不正确 的是___________。 填序号
填序号
(4)工业上常用 与
与 溶液反应制取消毒液,该反应的化学方程式为
溶液反应制取消毒液,该反应的化学方程式为___________ 。
(5)向 溶液中加入NaOH溶液,对应的离子方程式为
溶液中加入NaOH溶液,对应的离子方程式为___________ 。
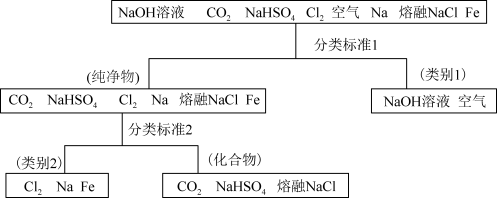
 属于
属于 填“酸性”或“碱性”
填“酸性”或“碱性” 氧化物,书写
氧化物,书写 与
与 反应的化学方程式
反应的化学方程式
 填“属于”或“不属于”
填“属于”或“不属于” 碱性氧化物。
碱性氧化物。(2)上述物质中属于电解质的是
(3)某学生完成钠与水反应的实验,实验过程如图
 、
、 、
、 所示,下列有关实验现象及结论的叙述
所示,下列有关实验现象及结论的叙述 填序号
填序号
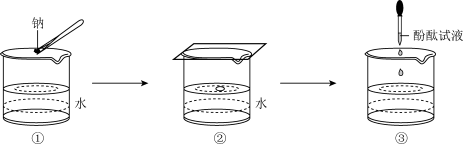
A.图 中钠熔成小球,说明钠与水反应放热且钠的熔点低 中钠熔成小球,说明钠与水反应放热且钠的熔点低 |
B.图 中钠四处游动并嘶嘶作响,说明反应产生了气体 中钠四处游动并嘶嘶作响,说明反应产生了气体 |
C.图 中滴加酚酞试液后溶液变红,说明有碱性物质生成 中滴加酚酞试液后溶液变红,说明有碱性物质生成 |
D.钠与水反应的离子方程式是: 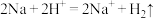 |
(4)工业上常用
 与
与 溶液反应制取消毒液,该反应的化学方程式为
溶液反应制取消毒液,该反应的化学方程式为(5)向
 溶液中加入NaOH溶液,对应的离子方程式为
溶液中加入NaOH溶液,对应的离子方程式为
您最近一年使用:0次
名校
6 . 氯气是现代工业和生活中常用的杀菌消毒剂。回答下列问题:
(1)实验室常用 固体和浓盐酸在加热条件下制取
固体和浓盐酸在加热条件下制取 ,反应的离子方程式为
,反应的离子方程式为___________ 。实验室还可用 固体和浓盐酸在室温条件下制取少量氯气(同时生成
固体和浓盐酸在室温条件下制取少量氯气(同时生成 和
和 ),可选用图中的
),可选用图中的___________ (选填“A”或“B”)作为发生装置,反应的离子方程式为___________ 。
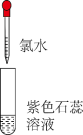
(说明:试管中溶液均为 ,均滴入氯水5滴;淀粉遇
,均滴入氯水5滴;淀粉遇 变蓝)
变蓝)
①实验I中反应方程式为___________ ,由此推断氧化性:
___________  (填“
(填“ ”或“
”或“ ”)。
”)。
②实验Ⅱ中溶液变红是由于溶液中含有___________ (填微粒符号,下同);使溶液褪色的微粒是___________ 。
(1)实验室常用
 固体和浓盐酸在加热条件下制取
固体和浓盐酸在加热条件下制取 ,反应的离子方程式为
,反应的离子方程式为 固体和浓盐酸在室温条件下制取少量氯气(同时生成
固体和浓盐酸在室温条件下制取少量氯气(同时生成 和
和 ),可选用图中的
),可选用图中的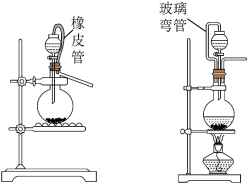
| 实验Ⅰ | 实验Ⅱ | |
| 实验操作 |
|
|
| 实验现象 | 溶液变蓝 | 石蕊溶液先变红,后褪色 |
 ,均滴入氯水5滴;淀粉遇
,均滴入氯水5滴;淀粉遇 变蓝)
变蓝)①实验I中反应方程式为

 (填“
(填“ ”或“
”或“ ”)。
”)。②实验Ⅱ中溶液变红是由于溶液中含有
您最近一年使用:0次
7 . 硫的氧化物、氮的氧化物、硅的氧化物都是重要的化工原料。将其合理利用,既能减少污染,又能充分利用资源,创造价值。
(1)耐辐照石英玻璃是航天器姿态控制系统的核心元件。石英的成分是_______ (填化学式),该物质的类别属于_______ 氧化物(填“碱性”、 “酸性”或“两性”),实验室中不能用带玻璃塞的试剂瓶盛放NaOH溶液,原因是_______________ (用离子方程式表示)。
(2)玻璃是常用的硅酸盐材料,生产普通玻璃的主要材料有________ 、_______ 、_______ ,工艺师常用_________ (填物质名称)来雕刻玻璃,其作用过程产生________ 气体。
(3)石英坩埚可以用来灼烧下面哪种物质_______。(填字母)
(4)SiO2在自然界中广泛存在,它是制备现代通讯材料_________ (写该材料名称)的主要原料
(5)在一定量的浓硫酸中加入过量铜片,加热使之反应,反应结束后。若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为_________________ 。
(6)硝酸是一种重要的工业原料。在实验室中通常保存在棕色试剂瓶中,则原因是_______________ (用化学方程式表示)。硝酸是一种易挥发性的酸,用蘸浓硝酸和蘸浓氨水的玻璃棒靠近会产生大量白烟,白烟的成分是__________ 。
(1)耐辐照石英玻璃是航天器姿态控制系统的核心元件。石英的成分是
(2)玻璃是常用的硅酸盐材料,生产普通玻璃的主要材料有
(3)石英坩埚可以用来灼烧下面哪种物质_______。(填字母)
| A.碳酸钠 | B.氢氧化钠 | C.氢氧化钾 | D.氯化钠 |
(5)在一定量的浓硫酸中加入过量铜片,加热使之反应,反应结束后。若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为
(6)硝酸是一种重要的工业原料。在实验室中通常保存在棕色试剂瓶中,则原因是
您最近一年使用:0次
8 . 下表是元素周期表的一部分,根据所给的10种元素,完成以下各小题。
(1)金属性最强的元素是___________ (填元素符号)。最不活泼元素的原子结构示意图为___________ 。
(2)第3周期元素中,其最高价氧化物对应的水化物具有两性的元素是___________ (填元素名称)。Na、Mg两种元素中,原子半径较大的是___________ 。
(3)第3周期元素中,其元素的一种氧化物是形成酸雨的主要物质,该氧化物的化学式为___________ 。
(4)工业上可以用Cl2和H2来制取盐酸,该反应的化学方程式为___________ 。
(5)由碳与氢元素形成的最简单有机物的化学式为___________ ,该物质中碳元素与氢元素的质量比为___________ ,其分子立体构型为___________ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | H | |||||||
| 2 | C | N | F | Ne | ||||
| 3 | Na | Mg | Al | S | Cl |
(2)第3周期元素中,其最高价氧化物对应的水化物具有两性的元素是
(3)第3周期元素中,其元素的一种氧化物是形成酸雨的主要物质,该氧化物的化学式为
(4)工业上可以用Cl2和H2来制取盐酸,该反应的化学方程式为
(5)由碳与氢元素形成的最简单有机物的化学式为
您最近一年使用:0次
名校
9 . 请回答下列问题:
(1)由磷原子核形成的三种微粒:① 、②
、② 、③
、③ ,半径由大到小的顺序为
,半径由大到小的顺序为_______ (填标号,下同);再失去一个电子所需最低能量由大到小的顺序为_______ 。
(2)比较H-O-H键角大小;H3O+_______ H2O(填“>”、“<”或“=”)。
(3)胍(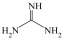 )分子中所有原子共平面,胍中N杂化方式为
)分子中所有原子共平面,胍中N杂化方式为_______ 。
(4)干冰晶体中,每个CO2周围等距离且紧邻的CO2有_______ 个;在冰晶体结构中,每个水分子最多与相邻的_______ 个水分子相连接。同为分子晶体,但干冰中CO2的配位数大于冰中水分子的配位数,其原因是_______ 。
(1)由磷原子核形成的三种微粒:①
 、②
、② 、③
、③ ,半径由大到小的顺序为
,半径由大到小的顺序为(2)比较H-O-H键角大小;H3O+
(3)胍(
 )分子中所有原子共平面,胍中N杂化方式为
)分子中所有原子共平面,胍中N杂化方式为(4)干冰晶体中,每个CO2周围等距离且紧邻的CO2有
您最近一年使用:0次
解题方法
10 . 研究物质性质具有重要的价值,根据所学知识回答下列问题:
(1)FeCl3是黑棕色晶体,主要用于金属蚀刻,污水处理。按照物质的分类方法,FeCl3应属于___________ (填序号)。
①酸;②氯化物;③混合物;④盐;⑤化合物;⑥电解质;⑦易溶于水物质
(2)将饱和FeCl3溶液逐滴加入沸水中,继续煮沸可制取氢氧化铁胶体,氢氧化铁胶体可处理污水,该反应的化学方程式为___________ ;判断胶体制备是否成功可利用胶体的___________ ;
(3)铁元素是组成人体必不可少的元素之一,以下几种常见的铁元素粒子,既有氧化性又有还原性的是___________ 。
A.Fe B.Fe2+ C.Fe3+
(4)火药是中国的四大发明之一,永远值得华夏儿女骄傲。黑火药在发生爆炸时,发生反应:2KNO3+3C+S=K2S+N2↑+3CO2↑。上述反应中氧化剂:___________ ;氧化产物:___________ 。
(1)FeCl3是黑棕色晶体,主要用于金属蚀刻,污水处理。按照物质的分类方法,FeCl3应属于
①酸;②氯化物;③混合物;④盐;⑤化合物;⑥电解质;⑦易溶于水物质
(2)将饱和FeCl3溶液逐滴加入沸水中,继续煮沸可制取氢氧化铁胶体,氢氧化铁胶体可处理污水,该反应的化学方程式为
(3)铁元素是组成人体必不可少的元素之一,以下几种常见的铁元素粒子,既有氧化性又有还原性的是
A.Fe B.Fe2+ C.Fe3+
(4)火药是中国的四大发明之一,永远值得华夏儿女骄傲。黑火药在发生爆炸时,发生反应:2KNO3+3C+S=K2S+N2↑+3CO2↑。上述反应中氧化剂:
您最近一年使用:0次