名校
解题方法
1 . 氢气在社会发展中有着重要的作用,如新能源的开发,氢能源的储存一直是科学界在研究的方向。利用氨热分解法制氢气是可行方法之一,一定条件下,利用催化剂将氨气分解为氮气和氢气。
(1)已知氨分解的反应的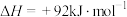 ,
,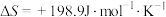 ,在下列哪个温度下反应能自发进行?_____(填标号)
,在下列哪个温度下反应能自发进行?_____(填标号)
(2)已知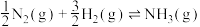 ,
, 该反应化学平衡常数K与温度T的关系如表所示:
该反应化学平衡常数K与温度T的关系如表所示:
请完成下列问题:
①试比较 、
、 的大小,
的大小,
_____  (填“>”、“<”或“=”);
(填“>”、“<”或“=”);
②400℃时,在 容器中反应
容器中反应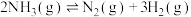 的化学平衡常数为
的化学平衡常数为_____ 。某时刻测得 、
、 和
和 物质的量分别为
物质的量分别为 、
、 和
和 时,则该反应的
时,则该反应的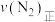
_____  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(3)如图是合成氨反应平衡混合气中 的体积分数随温度或压强变化的曲线,图中L(
的体积分数随温度或压强变化的曲线,图中L( 、
、 )、X分别代表温度或压强,其中X代表的是
)、X分别代表温度或压强,其中X代表的是_____ (填“温度”或“压强”)。判断 、
、 的大小关系:
的大小关系:
_____  (填“>”、“<或“=”),请说明理由
(填“>”、“<或“=”),请说明理由_____ 。
(1)已知氨分解的反应的
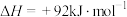 ,
,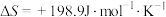 ,在下列哪个温度下反应能自发进行?_____(填标号)
,在下列哪个温度下反应能自发进行?_____(填标号)| A.50℃ | B.100℃ | C.150℃ | D.200℃ |
(2)已知
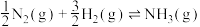 ,
, 该反应化学平衡常数K与温度T的关系如表所示:
该反应化学平衡常数K与温度T的关系如表所示:| T/℃ | 200 | 300 | 400 |
| K |  |  | 0.5 |
①试比较
 、
、 的大小,
的大小,
 (填“>”、“<”或“=”);
(填“>”、“<”或“=”);②400℃时,在
 容器中反应
容器中反应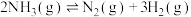 的化学平衡常数为
的化学平衡常数为 、
、 和
和 物质的量分别为
物质的量分别为 、
、 和
和 时,则该反应的
时,则该反应的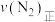
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(3)如图是合成氨反应平衡混合气中
 的体积分数随温度或压强变化的曲线,图中L(
的体积分数随温度或压强变化的曲线,图中L( 、
、 )、X分别代表温度或压强,其中X代表的是
)、X分别代表温度或压强,其中X代表的是 、
、 的大小关系:
的大小关系:
 (填“>”、“<或“=”),请说明理由
(填“>”、“<或“=”),请说明理由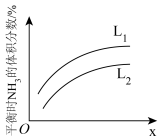
您最近一年使用:0次
名校
2 . Ⅰ.以下实验中分别利用了硫酸的哪些性质?请将正确答案的序号分别填在横线上。
①脱水性②强氧化性③吸水性④强酸性
(1)浓硫酸干燥氯气:_____ ;
(2)适量浓硫酸与蔗糖混合后,体积膨胀颜色变黑:_____ ;
(3)把浓硫酸滴加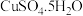 晶体中:
晶体中:_____ 。
Ⅱ.已知:浓硝酸和铜在常温下反应的化学方程式为: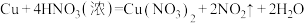 。回答下列问题:
。回答下列问题:
(4)在这个反应中,浓硝酸表现的化学性质是酸性和_____ 性(填“氧化”或“还原”)。
(5) 的电离方程式为
的电离方程式为_____ 。
(6)在离子方程式中,只有强酸、强碱和可溶性盐拆写成离子形式,该反应的离子方程式为_____ 。
(7)随着反应的进行,硝酸的浓度减小,发生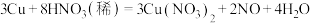 反应。在该反应中,有3molCu反应,有
反应。在该反应中,有3molCu反应,有_____ 个 转化为NO气体。
转化为NO气体。
(8)氮的氧化物有毒。用NaOH溶液吸收的方程式为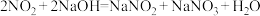 ,该反应消耗2mol
,该反应消耗2mol 转移的电子的物质的量是
转移的电子的物质的量是_____ 。
①脱水性②强氧化性③吸水性④强酸性
(1)浓硫酸干燥氯气:
(2)适量浓硫酸与蔗糖混合后,体积膨胀颜色变黑:
(3)把浓硫酸滴加
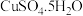 晶体中:
晶体中:Ⅱ.已知:浓硝酸和铜在常温下反应的化学方程式为:
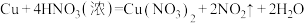 。回答下列问题:
。回答下列问题:(4)在这个反应中,浓硝酸表现的化学性质是酸性和
(5)
 的电离方程式为
的电离方程式为(6)在离子方程式中,只有强酸、强碱和可溶性盐拆写成离子形式,该反应的离子方程式为
(7)随着反应的进行,硝酸的浓度减小,发生
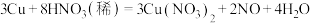 反应。在该反应中,有3molCu反应,有
反应。在该反应中,有3molCu反应,有 转化为NO气体。
转化为NO气体。(8)氮的氧化物有毒。用NaOH溶液吸收的方程式为
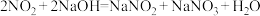 ,该反应消耗2mol
,该反应消耗2mol 转移的电子的物质的量是
转移的电子的物质的量是
您最近一年使用:0次
解题方法
3 . 现有下列几种有机物或微粒:
(1)上述物质中属于芳香烃的是________ (填编号,下同),互为同分异构体的是_________ 。
(2)④与等物质的量的HBr发生加成反应的产物可能为___________ (填结构简式)。
(3)⑧中只含碳、氢、氧三种元素,其分子结构模型中小球表示原子,球与球之间的短线代表单键或双键。⑧中所含官能团的名称为___________ 。
(4)⑤的一种同分异构体B为芳香族化合物,其核磁共振氢谱图如图所示:___________ ,下列关于B的说法正确的是___________ (填字母)。
A.该物质可与氢气反应,1mol该物质最多消耗氢气的物质的量为4mol
B.在光照条件下,该物质可以和氯水发生取代反应
C.该物质可以使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色,均发生氧化反应
(5)⑦是最简单的碳正离子,它的中心原子的杂化方式为___________ ; 并不稳定,原因是
并不稳定,原因是___________ 。
①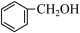 ②
②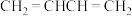 ③
③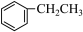 ④
④ ⑤
⑤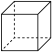 ⑥
⑥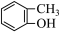 ⑦
⑦ ⑧
⑧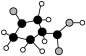
(1)上述物质中属于芳香烃的是
(2)④与等物质的量的HBr发生加成反应的产物可能为
(3)⑧中只含碳、氢、氧三种元素,其分子结构模型中小球表示原子,球与球之间的短线代表单键或双键。⑧中所含官能团的名称为
(4)⑤的一种同分异构体B为芳香族化合物,其核磁共振氢谱图如图所示:

A.该物质可与氢气反应,1mol该物质最多消耗氢气的物质的量为4mol
B.在光照条件下,该物质可以和氯水发生取代反应
C.该物质可以使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色,均发生氧化反应
(5)⑦是最简单的碳正离子,它的中心原子的杂化方式为
 并不稳定,原因是
并不稳定,原因是
您最近一年使用:0次
名校
4 . I.回答下列问题:
(1)请用以下物质的序号填空:
①NaCl② ③NaOH④
③NaOH④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨He⑩
⑨He⑩
其中只含有共价键的化合物有___________ ,含有非极性共价键的离子化合物有___________ ,含有极性共价键的离子化合物有___________ ,不含共价键的化合物有___________ 。
(2)X、Y两种主族元素能形成 型化合物,已知
型化合物,已知 中共有38个电子,若
中共有38个电子,若 为常见元素形成的离子化合物,其电子式为
为常见元素形成的离子化合物,其电子式为___________ ;若 为共价化合物,其结构式为
为共价化合物,其结构式为___________ 。
II.已知:在常温常压下,断开1molAB(g)分子中的化学键使其分别生成气态原子A(g)和B(g)所吸收的能量叫做键能。几种共价键的键能如下表所示:
(3)2molHBr(g)和 反应生成2molHF(g)和
反应生成2molHF(g)和
___________ (填“吸收”或“放出”)___________ KJ能量。
(1)请用以下物质的序号填空:
①NaCl②
 ③NaOH④
③NaOH④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨He⑩
⑨He⑩
其中只含有共价键的化合物有
(2)X、Y两种主族元素能形成
 型化合物,已知
型化合物,已知 中共有38个电子,若
中共有38个电子,若 为常见元素形成的离子化合物,其电子式为
为常见元素形成的离子化合物,其电子式为 为共价化合物,其结构式为
为共价化合物,其结构式为II.已知:在常温常压下,断开1molAB(g)分子中的化学键使其分别生成气态原子A(g)和B(g)所吸收的能量叫做键能。几种共价键的键能如下表所示:
| 共价键 |  |  |  |  |  |  |  |
键能 | 266 | 159 | 327 | 565 | 363 | 193 | 347 |
 反应生成2molHF(g)和
反应生成2molHF(g)和
您最近一年使用:0次
名校
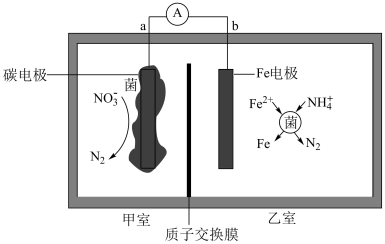
5 . I.铁碳微电池法在弱酸性条件下处理含氮废水技术的研究获得突破性进展,其工作原理如图所示。___________
(2)工作时 透过质子交换膜的移动方向由
透过质子交换膜的移动方向由___________ (填“乙→甲”或“甲→乙”)
(3)碳电极上的电极反应式为___________
(4)处理含 的废水,若处理
的废水,若处理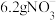 ,则有
,则有___________ 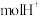 透过质子交换膜。
透过质子交换膜。
II.一种新型微生物电池可将有机废水中的 转化为
转化为 ,其工作原理如图所示(a、b极均为惰性电极)。
,其工作原理如图所示(a、b极均为惰性电极)。___________ (填“a到b”或“b到a”);a极反应式为___________
(6)已知该装置能实现海水的淡化,图中NaCl溶液就是在模拟海水。阴离子交换膜只允许阴离子通过,阳离子交换膜只允许阳离子通过,隔膜1和隔膜2一个是阴离子交换膜,一个为阳离子交换膜,则隔膜___________ 是阳离子交换膜(填“1”或“2”)。
(2)工作时
 透过质子交换膜的移动方向由
透过质子交换膜的移动方向由(3)碳电极上的电极反应式为
(4)处理含
 的废水,若处理
的废水,若处理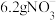 ,则有
,则有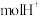 透过质子交换膜。
透过质子交换膜。II.一种新型微生物电池可将有机废水中的
 转化为
转化为 ,其工作原理如图所示(a、b极均为惰性电极)。
,其工作原理如图所示(a、b极均为惰性电极)。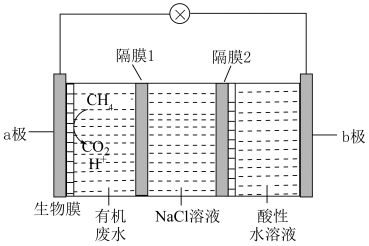
(6)已知该装置能实现海水的淡化,图中NaCl溶液就是在模拟海水。阴离子交换膜只允许阴离子通过,阳离子交换膜只允许阳离子通过,隔膜1和隔膜2一个是阴离子交换膜,一个为阳离子交换膜,则隔膜
您最近一年使用:0次
名校
解题方法
6 . ①金刚石②氧化钙③干冰④石墨⑤碘⑥金刚砂⑦氯化铯⑧银⑨冰⑩二氧化硅
(1)以上晶体中属于离子晶体的是_______ (填序号,下同);金属晶体的是_______ ;共价晶体的是_______ ;分子晶体的是_______ 。
(2)从结构的角度解释金刚石的熔点比金刚砂的熔点高的原因_______ 。
(3)干冰晶体中每个 周围等距离且紧邻的
周围等距离且紧邻的 有
有_______ 个;冰结构中,每个水分子最多与相邻的_______ 个水分子相连接。同为同类型晶体,但干冰中 的配位数大于冰中水分子的配位数,其原因
的配位数大于冰中水分子的配位数,其原因_______ 。
(1)以上晶体中属于离子晶体的是
(2)从结构的角度解释金刚石的熔点比金刚砂的熔点高的原因
(3)干冰晶体中每个
 周围等距离且紧邻的
周围等距离且紧邻的 有
有 的配位数大于冰中水分子的配位数,其原因
的配位数大于冰中水分子的配位数,其原因
您最近一年使用:0次
7 . 现有a~f共6种有机物,结构简式如下:
a.CH2=CHCH2CH3 b.CH≡C-CH3,c.CH3CH2CH2Cl
(1)按官能团分类:属于卤代烃的是_______ (填标号,下同),属于醇的是_______ 。
(2)_______ (填标号)属于芳香烃,其含有_______ 种官能团。
(3)a与HCl发生加成反应,含有手性碳原子的产物的结构简式为_______ (与四个不同的原子或原子团相连的碳原子)。
(4)b中最多有_______ 个原子在同一条直线上,一定条件下其发生加聚反应的化学方程式为_______ 。
(5)e的名称为_______ ,其与浓溴水发生反应的化学方程式为_______ 。
a.CH2=CHCH2CH3 b.CH≡C-CH3,c.CH3CH2CH2Cl
d.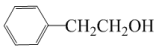 e.
e. 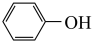 f.
f. 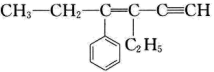
(1)按官能团分类:属于卤代烃的是
(2)
(3)a与HCl发生加成反应,含有手性碳原子的产物的结构简式为
(4)b中最多有
(5)e的名称为
您最近一年使用:0次
名校
8 . I.现有下列10种物质:。①铜②熔融 ③
③ ④
④ ⑤
⑤ 晶体⑥胆矾⑦碳酸钙⑧
晶体⑥胆矾⑦碳酸钙⑧ ⑨盐酸⑩酒精
⑨盐酸⑩酒精
(1)上述物质中属于电解质的有___________ 。
(2)属于非电解质的有___________ ,能导电的有___________ 。(填序号)
(3)⑧在熔化状态下电离方程式为:___________ 。
(4)少量④通入③的溶液中,反应的离子方程式为:___________ 。
(5)写出⑤在水溶液中的电离方程式:___________ 。
(6)向 溶液逐滴加入
溶液逐滴加入 溶液至
溶液至 恰好完全沉淀,发生反应的离子方程式为
恰好完全沉淀,发生反应的离子方程式为___________ ,然后继续滴加 溶液时,此步发生反应的离子方程式为
溶液时,此步发生反应的离子方程式为___________ 。
II.现有课外活动小组进行胶体的制备并检验其性质,甲同学在小烧杯中加入 蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和
蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和 溶液,继续煮沸溶液呈红褐色,停止加热,即制得胶体。
溶液,继续煮沸溶液呈红褐色,停止加热,即制得胶体。
(7)① 胶粒带
胶粒带___________ 电荷(填“正”或“负”),写出制备 胶体的离子反应方程式
胶体的离子反应方程式___________ 。
②乙同学将用氯化铁溶液制得的氢氧化铁胶体放入半透膜制成的袋内,如图所示:
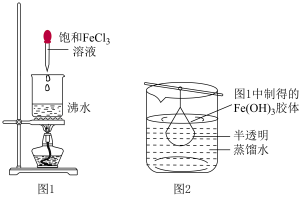
取图2中半透膜内的液体少许于试管中,向其中逐滴滴加稀硫酸,可观察到现象为___________ ,请写出此过程中发生反应的离子方程式___________ 。
 ③
③ ④
④ ⑤
⑤ 晶体⑥胆矾⑦碳酸钙⑧
晶体⑥胆矾⑦碳酸钙⑧ ⑨盐酸⑩酒精
⑨盐酸⑩酒精(1)上述物质中属于电解质的有
(2)属于非电解质的有
(3)⑧在熔化状态下电离方程式为:
(4)少量④通入③的溶液中,反应的离子方程式为:
(5)写出⑤在水溶液中的电离方程式:
(6)向
 溶液逐滴加入
溶液逐滴加入 溶液至
溶液至 恰好完全沉淀,发生反应的离子方程式为
恰好完全沉淀,发生反应的离子方程式为 溶液时,此步发生反应的离子方程式为
溶液时,此步发生反应的离子方程式为II.现有课外活动小组进行胶体的制备并检验其性质,甲同学在小烧杯中加入
 蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和
蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和 溶液,继续煮沸溶液呈红褐色,停止加热,即制得胶体。
溶液,继续煮沸溶液呈红褐色,停止加热,即制得胶体。(7)①
 胶粒带
胶粒带 胶体的离子反应方程式
胶体的离子反应方程式②乙同学将用氯化铁溶液制得的氢氧化铁胶体放入半透膜制成的袋内,如图所示:

取图2中半透膜内的液体少许于试管中,向其中逐滴滴加稀硫酸,可观察到现象为
您最近一年使用:0次
名校
9 . 针对表中10种元素及由这些元素形成的单质和化合物,完成以下问题。
(1)最活泼的金属元素是___________ (填元素符号),酸性最强的最高价氧化物对应水化物是___________ (填化学式)。
(2)写出⑤和⑨两种元素组成的化合物的电子式________ ,该化合物中含有________ (填“离子键”“共价键”)
(3)③④⑤⑧的简单离子半径由大到小的顺序为___________ (填离子符号)。
(4)写出元素⑥的单质与元素④最高价氧化物对应水化物反应的化学方程式___________ 。
(5)能够比较元素⑧与⑨的非金属性强弱的依据是___________ (填序号)。
a.氢化物酸性:⑧弱于⑨ b.⑨单质能与⑧氢化物成应得到⑧单质
c.单质与 反应:⑨比⑧容易 d.含氧酸的酸性;⑨强于⑧
反应:⑨比⑧容易 d.含氧酸的酸性;⑨强于⑧
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 2 | ① | ② | ③ | ||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ |
(2)写出⑤和⑨两种元素组成的化合物的电子式
(3)③④⑤⑧的简单离子半径由大到小的顺序为
(4)写出元素⑥的单质与元素④最高价氧化物对应水化物反应的化学方程式
(5)能够比较元素⑧与⑨的非金属性强弱的依据是
a.氢化物酸性:⑧弱于⑨ b.⑨单质能与⑧氢化物成应得到⑧单质
c.单质与
 反应:⑨比⑧容易 d.含氧酸的酸性;⑨强于⑧
反应:⑨比⑧容易 d.含氧酸的酸性;⑨强于⑧
您最近一年使用:0次
2024-02-23更新
|
186次组卷
|
2卷引用:安徽省合肥市六校联盟2023-2024学年高一上学期1月期末化学试题
名校
解题方法
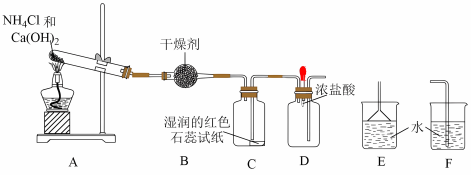
10 . 某实验小组利用以下装置制取氨气并探究氨气的性质:_____ 。
(2)装置B中的干燥剂是_____ (填名称)。
(3)装置C中的现象是_____ 。
(4)实验进行一段时间后,挤压装置D中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是_____ ,发生反应的化学方程式为_____ 。
(5)为防止过量氨气外逸,需在上述装置末端增加尾气吸收装置,应选用的装置是_____ (填“E”或“F”)。
(2)装置B中的干燥剂是
(3)装置C中的现象是
(4)实验进行一段时间后,挤压装置D中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是
(5)为防止过量氨气外逸,需在上述装置末端增加尾气吸收装置,应选用的装置是
您最近一年使用:0次
2024-02-03更新
|
939次组卷
|
5卷引用:安徽省蚌埠市2023-2024学年高一上学期期末考试化学试题



