1 . 按要求写出下列方程式
(1)碳酸钠与足量盐酸反应的离子方程式:___________ ;
(2)氯气的实验室制法的离子方程式:___________ ;
(3)用氨水吸收过量的SO2的离子方程式:___________ ;
(4)过量Fe与稀HNO3反应的离子方程式:___________ ;
(5)二氧化硫通入氯化铁溶液中的离子方程式:___________ ;
(6)铜和浓硫酸反应的化学方程式:___________ ;
(7)氨气的实验室制备的化学方程式:___________ ;
(8)氨的催化氧化的化学方程式:___________ ;
(9)Ca(OH)2与少量NaHCO3溶液反应化学方程式:___________ ;
(10)硝酸见光分解的化学方程式:___________ 。
(1)碳酸钠与足量盐酸反应的离子方程式:
(2)氯气的实验室制法的离子方程式:
(3)用氨水吸收过量的SO2的离子方程式:
(4)过量Fe与稀HNO3反应的离子方程式:
(5)二氧化硫通入氯化铁溶液中的离子方程式:
(6)铜和浓硫酸反应的化学方程式:
(7)氨气的实验室制备的化学方程式:
(8)氨的催化氧化的化学方程式:
(9)Ca(OH)2与少量NaHCO3溶液反应化学方程式:
(10)硝酸见光分解的化学方程式:
您最近一年使用:0次
2 . (Ⅰ)氢氧燃料电池以 溶液作电解质溶液时,
溶液作电解质溶液时,
(1)负极反应式为_______ 。
(2)正极反应式为_______ 。
(Ⅱ)按要求回完成以下化学反应:
(3)氯乙烯发生加聚反应的化学方程式_______ 。
(4)乙烯通入溴水的化学方程式为_______ 。
(5)乙酸和乙醇的酯化反应的化学方程式_______ 。
(Ⅲ)t℃时,将 气体A和1mol气体B充入容积为
气体A和1mol气体B充入容积为 的恒容密闭容器中,发生如下反应:
的恒容密闭容器中,发生如下反应: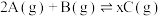 ,2min时化学反应达到限度(温度仍为t℃),此时B还有
,2min时化学反应达到限度(温度仍为t℃),此时B还有 ,并测得C的浓度为
,并测得C的浓度为 ,请回答下列问题:
,请回答下列问题:
(6)判断该反应达到限度的标志是_______ 。
a.容器中的压强保持不变
b.A的生成速率与B的消耗速率之比为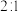
c.容器内混合气体的密度保持不变
d.A的百分含量保持不变
e.B和C的物质的量浓度之比为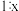
(7)保持温度不变增大容器体积,则正反应速率_______ (填“增大”、“减小”或“不变”)。
(8)化学反应达到限度时,A的转化率为_______ 。
 溶液作电解质溶液时,
溶液作电解质溶液时,(1)负极反应式为
(2)正极反应式为
(Ⅱ)按要求回完成以下化学反应:
(3)氯乙烯发生加聚反应的化学方程式
(4)乙烯通入溴水的化学方程式为
(5)乙酸和乙醇的酯化反应的化学方程式
(Ⅲ)t℃时,将
 气体A和1mol气体B充入容积为
气体A和1mol气体B充入容积为 的恒容密闭容器中,发生如下反应:
的恒容密闭容器中,发生如下反应: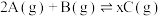 ,2min时化学反应达到限度(温度仍为t℃),此时B还有
,2min时化学反应达到限度(温度仍为t℃),此时B还有 ,并测得C的浓度为
,并测得C的浓度为 ,请回答下列问题:
,请回答下列问题:(6)判断该反应达到限度的标志是
a.容器中的压强保持不变
b.A的生成速率与B的消耗速率之比为
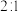
c.容器内混合气体的密度保持不变
d.A的百分含量保持不变
e.B和C的物质的量浓度之比为
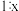
(7)保持温度不变增大容器体积,则正反应速率
(8)化学反应达到限度时,A的转化率为
您最近一年使用:0次
3 . 完成下列填空。
(1)某学习小组依据氧化还原反应原理: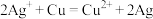 设计成的原电池如图所示。
设计成的原电池如图所示。___________ ;
②负极的电极材料为___________ ;(填化学式)
③正极发生的电极反应___________ ;
④若银电极增重5.4g,外电路转移电子的物质的量___________ mol。
(2)温度一定,在一个2L的恒容密闭容器中,A、B、C三种气体物质的浓度随时间的变化曲线如图所示。根据图中数据,试填写下列空白:___________ 。从开始到平衡时C的反应速率为___________ ,A的转化率为___________ 。
②下列叙述能说明该反应已达到化学平衡状态的是___________ (填序号)。
A.A与C的浓度相等
B.相同时间内消耗3nmolA,同时生成3nmolA
C.相同时间内消耗3nmolA,同时消耗nmolB
D.混合气体的总质量不随时间的变化而变化
E.B的体积分数不再发生变化
F.混合气体的密度不再发生变化
G.混合气体的压强不再发生变化
(1)某学习小组依据氧化还原反应原理:
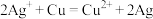 设计成的原电池如图所示。
设计成的原电池如图所示。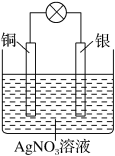
②负极的电极材料为
③正极发生的电极反应
④若银电极增重5.4g,外电路转移电子的物质的量
(2)温度一定,在一个2L的恒容密闭容器中,A、B、C三种气体物质的浓度随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
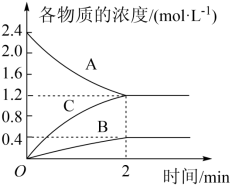
②下列叙述能说明该反应已达到化学平衡状态的是
A.A与C的浓度相等
B.相同时间内消耗3nmolA,同时生成3nmolA
C.相同时间内消耗3nmolA,同时消耗nmolB
D.混合气体的总质量不随时间的变化而变化
E.B的体积分数不再发生变化
F.混合气体的密度不再发生变化
G.混合气体的压强不再发生变化
您最近一年使用:0次
4 . 烃类物质是整个有机化学的基础,烃及其衍生物共同构成了庞大的有机物世界。
(1)实验室中用如图所示的装置进行甲烷与氯气在光照下反应的实验。___________ 。___________ (填化学式)。
③甲烷与氯气反应生成的产物最多的是___________ (填化学式)。
④若将1molCH4与一定量的 反应,得到等物质的量的4种有机产物,则消耗
反应,得到等物质的量的4种有机产物,则消耗 的物质的量为
的物质的量为___________ mol。
(2)我国已对酒驾实行了“醉驾入刑”,酒的主要成分是乙醇。乙醇的官能团名称是___________ 。使用酸性 溶液可以检测酒驾,利用了乙醇的
溶液可以检测酒驾,利用了乙醇的___________ (填“氧化性”或“还原性”),其原理是:司机口中呼出的乙醇可以使检测仪中的橙色重铬酸钾(K2Cr2O)转变为绿色的硫酸铬[Cr2(SO4)3],上述反应涉及的乙醇性质有___________ 。
A.无色液体 B.密度比水的小 C.易挥发 D.具有还原性
(1)实验室中用如图所示的装置进行甲烷与氯气在光照下反应的实验。

A.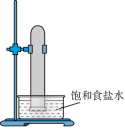 B.
B. C.
C.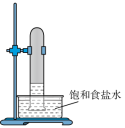 D.
D.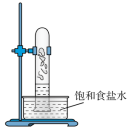
③甲烷与氯气反应生成的产物最多的是
④若将1molCH4与一定量的
 反应,得到等物质的量的4种有机产物,则消耗
反应,得到等物质的量的4种有机产物,则消耗 的物质的量为
的物质的量为(2)我国已对酒驾实行了“醉驾入刑”,酒的主要成分是乙醇。乙醇的官能团名称是
 溶液可以检测酒驾,利用了乙醇的
溶液可以检测酒驾,利用了乙醇的A.无色液体 B.密度比水的小 C.易挥发 D.具有还原性
您最近一年使用:0次
名校
5 . 请回答下列关于有机物的问题:
(1)下列有机物属于芳香烃的是______(填正确答案编号,下同)。
(2)下列有机物只有四种同分异构体(不考虑立体异构)的是______ 。
A.甲苯的一溴取代物 B.分子式为 的二氯取代物
的二氯取代物
C.对二甲苯的二氯取代物 D.分子式为 的有机物
的有机物
写出分子式为 的所有链状同分异构体(不考虑立体异构)
的所有链状同分异构体(不考虑立体异构)______ 。
(3) 核磁共振谱是指有机物分子中的氢原子核所处的化学环境(即其附近的基团)不同,表现出的核磁性就不同,代表核磁性特征的峰在核磁共振图中坐标的位置(化学位移,符号为
核磁共振谱是指有机物分子中的氢原子核所处的化学环境(即其附近的基团)不同,表现出的核磁性就不同,代表核磁性特征的峰在核磁共振图中坐标的位置(化学位移,符号为 )也就不同。现有一物质的
)也就不同。现有一物质的 核磁共振谱如图所示:
核磁共振谱如图所示:
(4)有机物C常用于食品行业。已知9.0gC在足量 中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,经检验剩余气体为
中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,经检验剩余气体为 。
。
①C分子的质谱图如图所示,从图中可知其相对分子质量是______ ,则C的分子式是______ 。 溶液发生反应,C一定含有的官能团是
溶液发生反应,C一定含有的官能团是______ 。
③C分子的核磁共振氢谱有4个峰,峰面积之比是1:1:1:3;则C的结构简式是______ 。
(1)下列有机物属于芳香烃的是______(填正确答案编号,下同)。
A. | B.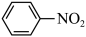 | C. | D. |
(2)下列有机物只有四种同分异构体(不考虑立体异构)的是
A.甲苯的一溴取代物 B.分子式为
 的二氯取代物
的二氯取代物C.对二甲苯的二氯取代物 D.分子式为
 的有机物
的有机物写出分子式为
 的所有链状同分异构体(不考虑立体异构)
的所有链状同分异构体(不考虑立体异构)(3)
 核磁共振谱是指有机物分子中的氢原子核所处的化学环境(即其附近的基团)不同,表现出的核磁性就不同,代表核磁性特征的峰在核磁共振图中坐标的位置(化学位移,符号为
核磁共振谱是指有机物分子中的氢原子核所处的化学环境(即其附近的基团)不同,表现出的核磁性就不同,代表核磁性特征的峰在核磁共振图中坐标的位置(化学位移,符号为 )也就不同。现有一物质的
)也就不同。现有一物质的 核磁共振谱如图所示:
核磁共振谱如图所示:
A.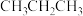 | B. | C.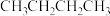 | D.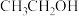 |
(4)有机物C常用于食品行业。已知9.0gC在足量
 中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,经检验剩余气体为
中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,经检验剩余气体为 。
。①C分子的质谱图如图所示,从图中可知其相对分子质量是

 溶液发生反应,C一定含有的官能团是
溶液发生反应,C一定含有的官能团是③C分子的核磁共振氢谱有4个峰,峰面积之比是1:1:1:3;则C的结构简式是
您最近一年使用:0次
名校
6 . 氮是地球上极为丰富的元素。回答下列问题:
(1)氮化锂( )晶体中氮以
)晶体中氮以 存在,基态
存在,基态 核外电子排布式为
核外电子排布式为______ ,基态 核外电子占据的最高能级电子的电子云轮廓图形状为
核外电子占据的最高能级电子的电子云轮廓图形状为______ 。
(2)胸腺嘧啶是构成DNA的一种含氮碱基,结构简式如图所示。______ 。
②其分子中σ键和π键的数目之比为______ 。
③该胸腺嘧啶中含有官能团的名称______ 。
(3)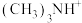 和
和 可形成离子液体,熔点低于100℃其挥发性一般比有机溶剂
可形成离子液体,熔点低于100℃其挥发性一般比有机溶剂______ (填“大”或“小”), 的空间结构为
的空间结构为______ 。
(4) 与
与 形成化合物的晶胞如图所示,与同一个
形成化合物的晶胞如图所示,与同一个 最近且等距的
最近且等距的 有
有______ 个。
(1)氮化锂(
 )晶体中氮以
)晶体中氮以 存在,基态
存在,基态 核外电子排布式为
核外电子排布式为 核外电子占据的最高能级电子的电子云轮廓图形状为
核外电子占据的最高能级电子的电子云轮廓图形状为(2)胸腺嘧啶是构成DNA的一种含氮碱基,结构简式如图所示。
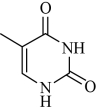
②其分子中σ键和π键的数目之比为
③该胸腺嘧啶中含有官能团的名称
(3)
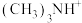 和
和 可形成离子液体,熔点低于100℃其挥发性一般比有机溶剂
可形成离子液体,熔点低于100℃其挥发性一般比有机溶剂 的空间结构为
的空间结构为(4)
 与
与 形成化合物的晶胞如图所示,与同一个
形成化合物的晶胞如图所示,与同一个 最近且等距的
最近且等距的 有
有
您最近一年使用:0次
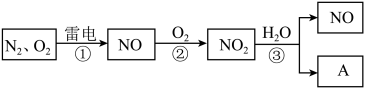
7 . 以下是氮循环的一部分:_____ ;
(2)反应 的化学方程式是
的化学方程式是_____ ;
(3) 易溶于水,并和水发生化学反应。该反应中,氧化剂是
易溶于水,并和水发生化学反应。该反应中,氧化剂是_____ ;
(4)化合物 的化学式是
的化学式是_____ ;
(5)治理汽车尾气的一种方法是用催化剂使 与
与 发生反应:
发生反应: 。当生成
。当生成 时,被还原的
时,被还原的 为
为_____  。
。
(2)反应
 的化学方程式是
的化学方程式是(3)
 易溶于水,并和水发生化学反应。该反应中,氧化剂是
易溶于水,并和水发生化学反应。该反应中,氧化剂是(4)化合物
 的化学式是
的化学式是(5)治理汽车尾气的一种方法是用催化剂使
 与
与 发生反应:
发生反应: 。当生成
。当生成 时,被还原的
时,被还原的 为
为 。
。
您最近一年使用:0次
8 . 按要求回答下列问题。
(1)铁盐可用作净水剂,用离子方程式表示其原理:___________ 。配制 溶液时,需将
溶液时,需将 晶体溶解到较浓的
晶体溶解到较浓的___________ 中,然后再加水稀释到所需的浓度。将 溶液蒸干并灼烧,得到的产物是
溶液蒸干并灼烧,得到的产物是___________ (填化学式)。
(2)某 溶液中含有
溶液中含有 杂质,可向溶液中加入足量的
杂质,可向溶液中加入足量的___________ ,充分反应后过滤,即可除去 。
。
(3)在 的
的 溶液中,含有杂质
溶液中,含有杂质 。若通过直接调节
。若通过直接调节 的方法使
的方法使 沉淀完全,是否同时会有
沉淀完全,是否同时会有 沉淀生成?
沉淀生成?___________ (填“是”或“否”)。向溶液中加入 将
将 氧化为
氧化为 ,调节
,调节 使
使 恰好沉淀完全(浓度等于
恰好沉淀完全(浓度等于 ),此时溶液的
),此时溶液的 约为
约为___________ 。(已知 时
时 、
、 、
、 的
的 分别为
分别为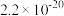 、
、 、
、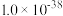 )
)
(1)铁盐可用作净水剂,用离子方程式表示其原理:
 溶液时,需将
溶液时,需将 晶体溶解到较浓的
晶体溶解到较浓的 溶液蒸干并灼烧,得到的产物是
溶液蒸干并灼烧,得到的产物是(2)某
 溶液中含有
溶液中含有 杂质,可向溶液中加入足量的
杂质,可向溶液中加入足量的 。
。(3)在
 的
的 溶液中,含有杂质
溶液中,含有杂质 。若通过直接调节
。若通过直接调节 的方法使
的方法使 沉淀完全,是否同时会有
沉淀完全,是否同时会有 沉淀生成?
沉淀生成? 将
将 氧化为
氧化为 ,调节
,调节 使
使 恰好沉淀完全(浓度等于
恰好沉淀完全(浓度等于 ),此时溶液的
),此时溶液的 约为
约为 时
时 、
、 、
、 的
的 分别为
分别为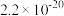 、
、 、
、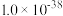 )
)
您最近一年使用:0次
9 . 现有等体积、等浓度的① 、②
、② 、③
、③ 三种溶液,回答下列问题。
三种溶液,回答下列问题。
(1)三种溶液中铵根离子浓度由大到小的顺序为___________ (用序号表示,用>连接)。
(2)写出溶液①显酸性的原因___________ (用离子方程式表示)。
(3)写出溶液①的电荷守恒___________ (用离子浓度表示);该溶液中离子浓度由大到小的顺序为___________ (用离子浓度表示,用>连接)
(4)写出溶液③的物料守恒___________ (用离子浓度表示)。
 、②
、② 、③
、③ 三种溶液,回答下列问题。
三种溶液,回答下列问题。(1)三种溶液中铵根离子浓度由大到小的顺序为
(2)写出溶液①显酸性的原因
(3)写出溶液①的电荷守恒
(4)写出溶液③的物料守恒
您最近一年使用:0次
解题方法
10 . 现有常温下浓度均为1mol•L-1的下列四种溶液:①H2SO4溶液②NaHCO3溶液③NH4Cl溶液④NaOH溶液⑤(NH4)2SO4溶液。
(1)这5种溶液pH由大到小的顺序是______ 。(填序号)
(2)②中各离子浓度由大到小的顺序是_______ ,NaHCO3的水解平衡常数Kh=______ 。(已知碳酸的电离常数K1=4×10-7,K2=5.6×10-11)
(3)向③中通入少量氨气,此时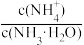 的值
的值______ (填“增大”、“减小”或“不变”)。
(4)若将③和④混合后溶液恰好呈中性,则混合前③的体积______ ④的体积(填“大于”、“小于”或“等于”)。
(5)一定量的稀H2SO4溶液与足量的Zn反应,为减缓产生的H2速率但又不影响H2的总量,可采取的措施是______ (填字母)。
A.加CH3COONa固体 B.加NH4Cl固体 C.加Ba(NO3)2溶液 D.加氨水 E.加Na2SO4溶液
(6)常温下,向FeCl3溶液中加入NaHCO3溶液发生反应的离子方程式为______ ,若将所得悬浊液的pH值调整为4,则溶液中Fe3+的溶液为_____ mol/L(已知常温下Ksp[Fe(OH)3]=4.0×10-38)。
(1)这5种溶液pH由大到小的顺序是
(2)②中各离子浓度由大到小的顺序是
(3)向③中通入少量氨气,此时
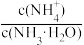 的值
的值(4)若将③和④混合后溶液恰好呈中性,则混合前③的体积
(5)一定量的稀H2SO4溶液与足量的Zn反应,为减缓产生的H2速率但又不影响H2的总量,可采取的措施是
A.加CH3COONa固体 B.加NH4Cl固体 C.加Ba(NO3)2溶液 D.加氨水 E.加Na2SO4溶液
(6)常温下,向FeCl3溶液中加入NaHCO3溶液发生反应的离子方程式为
您最近一年使用:0次



