1 . (Ⅰ)某温度时,在一个 的密闭容器中,
的密闭容器中, 三种物质的物质的量随时间的变化曲线如图所示。试根据图中数据,填写下列空白:
三种物质的物质的量随时间的变化曲线如图所示。试根据图中数据,填写下列空白:_______  时,到达反应最大限度;
时,到达反应最大限度;
(2)从开始到反应最大限度时间内, 的平均反应速率为
的平均反应速率为_______ ;
(3)该反应的化学方程式为_______ ;
(4)该反应达到平衡时, 的转化率为
的转化率为_______ ;
(5)该反应达到平衡时, 的体积分数为
的体积分数为_______ ;
(Ⅱ)在一固定容积的密闭容器中,进行反应:
(6)若容器容积为 ,反应
,反应 氢气质量增加
氢气质量增加 ,则该时间内一氧化碳的反应速率为
,则该时间内一氧化碳的反应速率为_______ 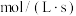 ;
;
(7)若增加碳的量,则正反应速率_______ ;(选填“增大”、“减小”、“不变”)
(8)该反应达到平衡状态的标志是_______ 。
a.混合气体的总压强不再变化
b.
c.混合气体的密度不再变化
d.
 的密闭容器中,
的密闭容器中, 三种物质的物质的量随时间的变化曲线如图所示。试根据图中数据,填写下列空白:
三种物质的物质的量随时间的变化曲线如图所示。试根据图中数据,填写下列空白: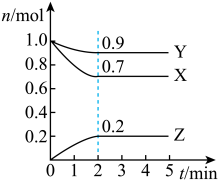
 时,到达反应最大限度;
时,到达反应最大限度;(2)从开始到反应最大限度时间内,
 的平均反应速率为
的平均反应速率为(3)该反应的化学方程式为
(4)该反应达到平衡时,
 的转化率为
的转化率为(5)该反应达到平衡时,
 的体积分数为
的体积分数为(Ⅱ)在一固定容积的密闭容器中,进行反应:

(6)若容器容积为
 ,反应
,反应 氢气质量增加
氢气质量增加 ,则该时间内一氧化碳的反应速率为
,则该时间内一氧化碳的反应速率为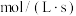 ;
;(7)若增加碳的量,则正反应速率
(8)该反应达到平衡状态的标志是
a.混合气体的总压强不再变化
b.

c.混合气体的密度不再变化
d.

您最近一年使用:0次
2 . 乙烯(CH2=CH2)是非常重要的化工基础原料,由乙烯可以制备很多有机物。
在恒温1L的刚性密闭容器中,加入1mol乙烯和1mol氢气,发生CH2=CH2(g)+H2(g)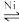 C2H6(g),容器内气体的压强与反应时间的关系如下图:
C2H6(g),容器内气体的压强与反应时间的关系如下图:
(1)有机物C2H6的名称是___________ 。该有机物属于___________ (填序号)。
A.烯烃 B.芳香烃 C.环状饱和烃 D.链状饱和烃(烷烃)
(2)该反应的类型属于___________(填序号)。
(3)达到化学平衡状态时,下列数值与开始时相同的是___________(填序号)
(4)反应进行到10min时,乙烯(CH2=CH2)的转化率a%=___________ 。
在恒温1L的刚性密闭容器中,加入1mol乙烯和1mol氢气,发生CH2=CH2(g)+H2(g)
 C2H6(g),容器内气体的压强与反应时间的关系如下图:
C2H6(g),容器内气体的压强与反应时间的关系如下图:| 时间(min) | 0 | 2 | 4 | 6 | 8 | 10 |
| 乙烯的物质的量(mol) | 1.00 | 0.80 | 0.70 | 0.64 | 0.60 | 0.60 |
A.烯烃 B.芳香烃 C.环状饱和烃 D.链状饱和烃(烷烃)
(2)该反应的类型属于___________(填序号)。
| A.取代反应 | B.加成反应 | C.加成聚合反应 | D.聚合反应 |
| A.容器内气体的压强 | B.容器内n(H2) | C.容器内c(CH2=CH2) | D.容器内气体的总质量 |
您最近一年使用:0次
名校
3 . 按要求书写方程式:
(1)工业合成氨每转移7.2mol电子放热112.8kJ,其热化学方程式为______ 。
(2)11.2g铁与2.7g水蒸气反应吸收30kJ热量,其热化学方程式为______ 。
(3)燃烧1.3g乙炔( )气体时。放出热量65kJ,表示乙炔燃烧热的热化学反应方程式为
)气体时。放出热量65kJ,表示乙炔燃烧热的热化学反应方程式为______ 。已知: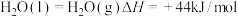 ,则11.2L(标准状况)乙炔完全燃烧生成气态水时放出的热量是
,则11.2L(标准状况)乙炔完全燃烧生成气态水时放出的热量是______ kJ。
(4)2.3g的 气体溶于水,放出akJ热量,其热化学方程式为
气体溶于水,放出akJ热量,其热化学方程式为______ 。
(5) 溶液中滴加硫酸,其离子方程式为
溶液中滴加硫酸,其离子方程式为______ 。
(6)工业上由黄铁矿制硫酸的第二步反应,其化学方程式为______ 。
(7)请用化学方程式解释,在无氧环境中才能观察到氢氧化亚铁沉淀颜色______ 。
(8)检验 的方法,其离子方程式为
的方法,其离子方程式为______ 。
(9)工业制漂白粉,其化学方程式为______ 。
(10)氨水与稀硫酸反应生成1mol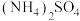 放热24.2kJ;已知
放热24.2kJ;已知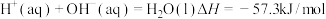 ,
, 电离的热化学方程式为
电离的热化学方程式为______ 。
(1)工业合成氨每转移7.2mol电子放热112.8kJ,其热化学方程式为
(2)11.2g铁与2.7g水蒸气反应吸收30kJ热量,其热化学方程式为
(3)燃烧1.3g乙炔(
 )气体时。放出热量65kJ,表示乙炔燃烧热的热化学反应方程式为
)气体时。放出热量65kJ,表示乙炔燃烧热的热化学反应方程式为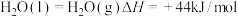 ,则11.2L(标准状况)乙炔完全燃烧生成气态水时放出的热量是
,则11.2L(标准状况)乙炔完全燃烧生成气态水时放出的热量是(4)2.3g的
 气体溶于水,放出akJ热量,其热化学方程式为
气体溶于水,放出akJ热量,其热化学方程式为(5)
 溶液中滴加硫酸,其离子方程式为
溶液中滴加硫酸,其离子方程式为(6)工业上由黄铁矿制硫酸的第二步反应,其化学方程式为
(7)请用化学方程式解释,在无氧环境中才能观察到氢氧化亚铁沉淀颜色
(8)检验
 的方法,其离子方程式为
的方法,其离子方程式为(9)工业制漂白粉,其化学方程式为
(10)氨水与稀硫酸反应生成1mol
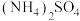 放热24.2kJ;已知
放热24.2kJ;已知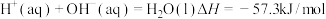 ,
, 电离的热化学方程式为
电离的热化学方程式为
您最近一年使用:0次
名校
解题方法
4 . I.有下列物质:___________ 。
(2)属于苯的同系物的是___________ 。
(3)⑤和⑥的一氯代物分别有___________ 、___________ 种。
Ⅱ.写出下列反应的化学方程式:
(4)丙烯变聚丙烯___________ 。
(5)用甲苯制TNT的反应___________ 。
(6)l,2-二氯乙烷与NaOH溶液共热___________ 。
①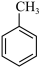 ②
②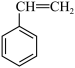 ③
③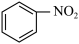 ④
④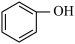
⑤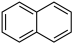 ⑥
⑥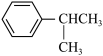 ⑦
⑦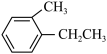
(2)属于苯的同系物的是
(3)⑤和⑥的一氯代物分别有
Ⅱ.写出下列反应的化学方程式:
(4)丙烯变聚丙烯
(5)用甲苯制TNT的反应
(6)l,2-二氯乙烷与NaOH溶液共热
您最近一年使用:0次
2024-04-28更新
|
406次组卷
|
2卷引用:天津市耀华中学2023-2024学年高二下学期期中考试化学试卷
名校
解题方法
5 . I.化学反应在发生物质变化的同时伴随着能量变化,请回答下列问题:
(1)汽车发动机工作时会引发 和
和 反应,生成
反应,生成 等污染大气,其中生成
等污染大气,其中生成 的能量变化如图所示,则图中三种分子最稳定的是
的能量变化如图所示,则图中三种分子最稳定的是___________ ,图中对应反应的热化学方程式为___________ 。 可转化为
可转化为 ,
, 在空气中加热反应可制得铁系氧化物材料。
在空气中加热反应可制得铁系氧化物材料。
已知25℃,101 时:
时:
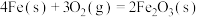
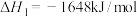


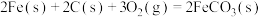
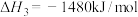
则

___________ 。
Ⅱ.某实验小组设计用0.55 的
的 溶液100
溶液100 与0.50
与0.50 的盐酸100
的盐酸100 置于如图所示的装置中进行测定中和反应反应热的实验。
置于如图所示的装置中进行测定中和反应反应热的实验。___________ ,装置中还存在的错误有___________ ;大烧杯杯口若不盖泡沫塑料板,测得中和反应的反应热 将
将___________ (填“偏大”、“偏小”或“无影响”)。
(4)实验中,所用 稍过量的原因是
稍过量的原因是___________ 。
(5)该实验小组做了三次实验,每次取盐酸和 溶液各100
溶液各100 ,并记录原始数据:
,并记录原始数据:
已知盐酸、 溶液密度均近似为1.00
溶液密度均近似为1.00 ,中和后混合液
,中和后混合液 ,则该中和反应的反应热
,则该中和反应的反应热
___________ 。(保留到小数点后1位)
(1)汽车发动机工作时会引发
 和
和 反应,生成
反应,生成 等污染大气,其中生成
等污染大气,其中生成 的能量变化如图所示,则图中三种分子最稳定的是
的能量变化如图所示,则图中三种分子最稳定的是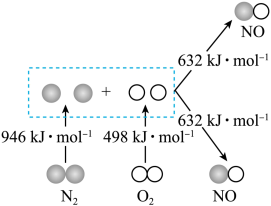
 可转化为
可转化为 ,
, 在空气中加热反应可制得铁系氧化物材料。
在空气中加热反应可制得铁系氧化物材料。已知25℃,101
 时:
时: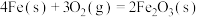
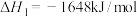


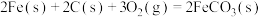
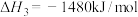
则


Ⅱ.某实验小组设计用0.55
 的
的 溶液100
溶液100 与0.50
与0.50 的盐酸100
的盐酸100 置于如图所示的装置中进行测定中和反应反应热的实验。
置于如图所示的装置中进行测定中和反应反应热的实验。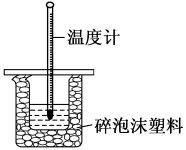
 将
将(4)实验中,所用
 稍过量的原因是
稍过量的原因是(5)该实验小组做了三次实验,每次取盐酸和
 溶液各100
溶液各100 ,并记录原始数据:
,并记录原始数据:| 实验序号 | 起始温度 /℃ /℃ | 终止温度 /℃ /℃ | 温差 /℃ /℃ | ||
| 盐酸 |  溶液 溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 28.0 | 3.0 |
| 2 | 25.1 | 25.1 | 25.1 | 28.2 | 3.1 |
| 3 | 25.1 | 25.1 | 25.1 | 28.0 | 2.9 |
 溶液密度均近似为1.00
溶液密度均近似为1.00 ,中和后混合液
,中和后混合液 ,则该中和反应的反应热
,则该中和反应的反应热
您最近一年使用:0次
2024-04-02更新
|
228次组卷
|
2卷引用:天津市第二十中学2023-2024学年高一下学期学情调研(二)(期中)化学试卷
6 . 按要求填空:
(1)在 、
、 、
、 、
、 、S、
、S、 、
、 中,只有氧化性的是
中,只有氧化性的是___________ ,只有还原性的是___________ ,既有氧化性又有还原性的是___________ 。
(2)某同学写出以下三个化学方程式(未配平):
① ;②
;②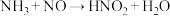 ;③
;③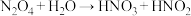
其中你认为一定不可能实现的是___________ 。
(3)下列三个氧化还原反应中,氧化性最强的物质是___________ 。
①
②
③
若溶质中 与
与 共存,为了氧化
共存,为了氧化 而
而 不被氧化,除单质外,还可用上述反应中的
不被氧化,除单质外,还可用上述反应中的_______ 作氧化剂。
(1)在
 、
、 、
、 、
、 、S、
、S、 、
、 中,只有氧化性的是
中,只有氧化性的是(2)某同学写出以下三个化学方程式(未配平):
①
 ;②
;②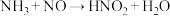 ;③
;③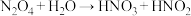
其中你认为一定不可能实现的是
(3)下列三个氧化还原反应中,氧化性最强的物质是
①

②

③

若溶质中
 与
与 共存,为了氧化
共存,为了氧化 而
而 不被氧化,除单质外,还可用上述反应中的
不被氧化,除单质外,还可用上述反应中的
您最近一年使用:0次
解题方法
7 . 根据所学电化学知识填空。
(1)如图为锌铜原电池的装置示意图,其中盐桥内装有含饱和KCl溶液的琼胶。请回答下列问题:
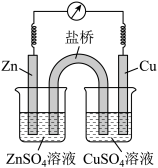
①Zn电极为电池的______ (填“正极”或“负极”)。
②写出电极反应式:Zn电极______ ,Cu电极______ 。
③盐桥中向CuSO4溶液中迁移的离子是______ (填离子符号)。
(2)金属腐蚀现象在生产生活中普遍存在,依据下列两种腐蚀现象回答下列问题:
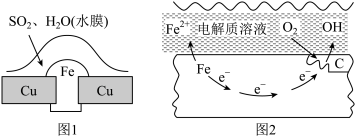
①图1中被腐蚀的金属为______ (填化学式);图2中金属腐蚀类型属于______ (填字母)。
A.化学腐蚀 B.析氢腐蚀 C.吸氧腐蚀
②图1中Cu的作用是______ (填“负极”或“正极”)。
③图2中铁的生锈过程中正极反应式为______ 。
(1)如图为锌铜原电池的装置示意图,其中盐桥内装有含饱和KCl溶液的琼胶。请回答下列问题:

①Zn电极为电池的
②写出电极反应式:Zn电极
③盐桥中向CuSO4溶液中迁移的离子是
(2)金属腐蚀现象在生产生活中普遍存在,依据下列两种腐蚀现象回答下列问题:

①图1中被腐蚀的金属为
A.化学腐蚀 B.析氢腐蚀 C.吸氧腐蚀
②图1中Cu的作用是
③图2中铁的生锈过程中正极反应式为
您最近一年使用:0次
解题方法
8 . 下表列出了①~⑥六种元素在周期表中的位置。
回答下列问题:(用化学用语填空)
(1)元素①的一种核素中,含有1个质子和1个中子,表示该核素组成的符号是_______ 。
(2)元素⑤的原子结构示意图是_______ 。
(3)上述元素中,原子半径最大的是_______ (填元素符号)。
(4)由元素①、⑥组成的化合物的电子式为_______ ,该化合物分子中含有_______ (填“极性”或“非极性”)共价键。
(5)元素⑤和⑥最高价氧化物对应的水化物酸性强的是_______ (填化学式)。
(6)金属性:③_______ ④(填“>”或“<”),它们的最高价氧化物对应的水化物反应的离子方程式为_______ 。
(7)下列说法正确的是_______ (填序号)。
a.元素②、③组成的化合物只有一种
b.元素②的气态氢化物稳定性高于元素⑤的气态氢化物
c.元素⑥在化合物中呈现的最高化合价为+7价
族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ |
(1)元素①的一种核素中,含有1个质子和1个中子,表示该核素组成的符号是
(2)元素⑤的原子结构示意图是
(3)上述元素中,原子半径最大的是
(4)由元素①、⑥组成的化合物的电子式为
(5)元素⑤和⑥最高价氧化物对应的水化物酸性强的是
(6)金属性:③
(7)下列说法正确的是
a.元素②、③组成的化合物只有一种
b.元素②的气态氢化物稳定性高于元素⑤的气态氢化物
c.元素⑥在化合物中呈现的最高化合价为+7价
您最近一年使用:0次
9 . 结合下表回答下列问题(均为常温下的数据):
请回答下列问题:
(1)下列四种离子结合同浓度的 、
、 、
、 、
、 中结合
中结合 的能力最强的是
的能力最强的是_______ 。
(2)向 醋酸中加入蒸馏水,将其稀释到
醋酸中加入蒸馏水,将其稀释到 后,下列说法正确的是_______。
后,下列说法正确的是_______。
(3)请写出 溶液中通入少量二氧化碳的离子方程式
溶液中通入少量二氧化碳的离子方程式_______ 。
(4)向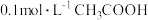 溶液中滴加
溶液中滴加 溶液至
溶液至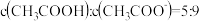 ,此时溶液
,此时溶液
_______ 。
(5)盐碱地(含有较多的 、
、 )不利于农作物生长,通过施加适量的石膏可以降低土壤的碱性。试用离子方程式表示盐碱地呈碱性的原因
)不利于农作物生长,通过施加适量的石膏可以降低土壤的碱性。试用离子方程式表示盐碱地呈碱性的原因_______ ,用石膏降低其碱性的反应原理_______ (用离子方程式及必要的文字说明)。
(6)盐酸肼 是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与
是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与 类似。
类似。
①写出盐酸肼第一步水解反应的离子方程式_______ 。
②盐酸肼水溶液中离子浓度的排列顺序正确的是_______ (填序号)。
A.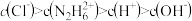
B.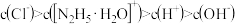
C.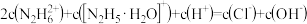
D.
| 化学式 |  |  |  |
电离常数( ) ) |  |  | 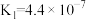 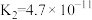 |
(1)下列四种离子结合同浓度的
 、
、 、
、 、
、 中结合
中结合 的能力最强的是
的能力最强的是(2)向
 醋酸中加入蒸馏水,将其稀释到
醋酸中加入蒸馏水,将其稀释到 后,下列说法正确的是_______。
后,下列说法正确的是_______。A. 的电离程度增大 的电离程度增大 | B.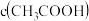 增大 增大 |
C. 的数目增多 的数目增多 | D.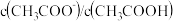 增大 增大 |
 溶液中通入少量二氧化碳的离子方程式
溶液中通入少量二氧化碳的离子方程式(4)向
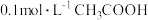 溶液中滴加
溶液中滴加 溶液至
溶液至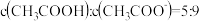 ,此时溶液
,此时溶液
(5)盐碱地(含有较多的
 、
、 )不利于农作物生长,通过施加适量的石膏可以降低土壤的碱性。试用离子方程式表示盐碱地呈碱性的原因
)不利于农作物生长,通过施加适量的石膏可以降低土壤的碱性。试用离子方程式表示盐碱地呈碱性的原因(6)盐酸肼
 是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与
是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与 类似。
类似。①写出盐酸肼第一步水解反应的离子方程式
②盐酸肼水溶液中离子浓度的排列顺序正确的是
A.
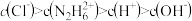
B.
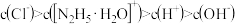
C.
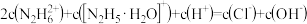
D.

您最近一年使用:0次
10 . 钠是一种非常活泼、具有广泛应用的金属。
(1)钠的原子结构示意图为 ,钠在反应中容易
,钠在反应中容易___________ 电子(填“得到”或“失去”)。
(2)金属钠非常活泼,通常保存在___________ 里,以隔绝空气。
(3)汽车安全气囊的气体发生剂 可由金属钠生产。某汽车安全气囊内含
可由金属钠生产。某汽车安全气囊内含 、
、 和
和 等物质。
等物质。
①当汽车发生较严重的碰撞时,引发 分解
分解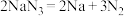 ,从而为气囊充气。
,从而为气囊充气。 的电子式为
的电子式为___________ 。
②产生的 立即与
立即与 发生置换反应生成
发生置换反应生成 ,化学方程式是
,化学方程式是___________ 。
③ 是冷却剂,吸收产气过程释放的热量。
是冷却剂,吸收产气过程释放的热量。 起冷却作用时发生反应的化学方程式为
起冷却作用时发生反应的化学方程式为___________ 。
④一个安全气囊通常装有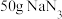 ,其完全分解所释放的
,其完全分解所释放的 为
为___________  。
。
(4)工业通过电解 生产金属钠:
生产金属钠: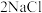 (熔融)
(熔融)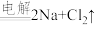 ,过程如下:
,过程如下:

已知:电解时需要将 加热至熔融状态。
加热至熔融状态。 的熔点为801℃,为降低能耗,通常加入
的熔点为801℃,为降低能耗,通常加入 从而把熔点降至约580℃。
从而把熔点降至约580℃。
①把 固体加热至熔融状态,目的是
固体加热至熔融状态,目的是___________ 。
②粗钠中含有少量杂质 ,过程Ⅱ除去
,过程Ⅱ除去 的化学方程式是
的化学方程式是___________ 。
③过程Ⅰ中, 能发生像
能发生像 那样的电解反应而被消耗。但在过程Ⅰ中
那样的电解反应而被消耗。但在过程Ⅰ中 却不断地被重新生成,原因是
却不断地被重新生成,原因是___________ 。
(1)钠的原子结构示意图为
 ,钠在反应中容易
,钠在反应中容易(2)金属钠非常活泼,通常保存在
(3)汽车安全气囊的气体发生剂
 可由金属钠生产。某汽车安全气囊内含
可由金属钠生产。某汽车安全气囊内含 、
、 和
和 等物质。
等物质。①当汽车发生较严重的碰撞时,引发
 分解
分解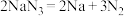 ,从而为气囊充气。
,从而为气囊充气。 的电子式为
的电子式为②产生的
 立即与
立即与 发生置换反应生成
发生置换反应生成 ,化学方程式是
,化学方程式是③
 是冷却剂,吸收产气过程释放的热量。
是冷却剂,吸收产气过程释放的热量。 起冷却作用时发生反应的化学方程式为
起冷却作用时发生反应的化学方程式为④一个安全气囊通常装有
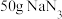 ,其完全分解所释放的
,其完全分解所释放的 为
为 。
。(4)工业通过电解
 生产金属钠:
生产金属钠: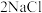 (熔融)
(熔融)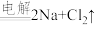 ,过程如下:
,过程如下:
已知:电解时需要将
 加热至熔融状态。
加热至熔融状态。 的熔点为801℃,为降低能耗,通常加入
的熔点为801℃,为降低能耗,通常加入 从而把熔点降至约580℃。
从而把熔点降至约580℃。①把
 固体加热至熔融状态,目的是
固体加热至熔融状态,目的是②粗钠中含有少量杂质
 ,过程Ⅱ除去
,过程Ⅱ除去 的化学方程式是
的化学方程式是③过程Ⅰ中,
 能发生像
能发生像 那样的电解反应而被消耗。但在过程Ⅰ中
那样的电解反应而被消耗。但在过程Ⅰ中 却不断地被重新生成,原因是
却不断地被重新生成,原因是
您最近一年使用:0次



