2025高三·全国·专题练习
解题方法
1 . 根据信息书写方程式或描述反应过程。
(1)BMO(Bi2MoO6)是一种高效光催化剂,可用于光催化降解苯酚,弱酸性条件下降解苯酚的反应原理如下图所示。___________ 。
②写出 与苯酚反应的离子方程式:
与苯酚反应的离子方程式:___________ 。
(2)氯化银可以溶于氨水中,写出该反应的离子方程式:___________ 。
(1)BMO(Bi2MoO6)是一种高效光催化剂,可用于光催化降解苯酚,弱酸性条件下降解苯酚的反应原理如下图所示。
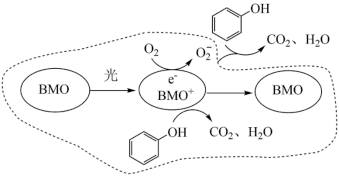
②写出
 与苯酚反应的离子方程式:
与苯酚反应的离子方程式:(2)氯化银可以溶于氨水中,写出该反应的离子方程式:
您最近一年使用:0次
2025高三·全国·专题练习
解题方法
2 .  有较强的配位能力,许多金属离子都可以与
有较强的配位能力,许多金属离子都可以与 形成稳定的配合。反应
形成稳定的配合。反应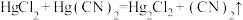 用于制备
用于制备 。
。
(1)上述反应的氧化剂是___________ 。
(2)写出 的结构简式
的结构简式___________ , 的空间构型是
的空间构型是___________ ;1mol 分子中
分子中 键为
键为___________ mol。
(3) 被称为拟卤素,性质与卤素相似,写出
被称为拟卤素,性质与卤素相似,写出 与氢氧化钠溶液反应的离子方程式
与氢氧化钠溶液反应的离子方程式___________ 。
(4)基态N价层电子排布式为___________ 。
 有较强的配位能力,许多金属离子都可以与
有较强的配位能力,许多金属离子都可以与 形成稳定的配合。反应
形成稳定的配合。反应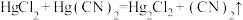 用于制备
用于制备 。
。(1)上述反应的氧化剂是
(2)写出
 的结构简式
的结构简式 的空间构型是
的空间构型是 分子中
分子中 键为
键为(3)
 被称为拟卤素,性质与卤素相似,写出
被称为拟卤素,性质与卤素相似,写出 与氢氧化钠溶液反应的离子方程式
与氢氧化钠溶液反应的离子方程式(4)基态N价层电子排布式为
您最近一年使用:0次
2025高三上·全国·专题练习
3 . 一块表面已被氧化为氧化钠的钠块17.0 g,投入50 g水中,最多能产生0.2 g气体,则:
(1)涉及的化学方程式为_______ ,_______ 。
(2)钠块中钠的质量是_______ g。
(3)钠块中氧化钠的质量是_______ g。
(4)原来钠块中被氧化的钠的质量是_______ g。
(5)设所得溶液的体积为50 mL,求所得溶液溶质物质的量浓度是_______ 。
(1)涉及的化学方程式为
(2)钠块中钠的质量是
(3)钠块中氧化钠的质量是
(4)原来钠块中被氧化的钠的质量是
(5)设所得溶液的体积为50 mL,求所得溶液溶质物质的量浓度是
您最近一年使用:0次
23-24高一下·全国·期末
4 . 回答下列问题:
(1)用20% H2SO4浸取软锰矿(主要成分为MnO2、SiO2等)制备高纯MnO2,酸浸时,通常加入FeSO4作催化剂加快反应速率。为提高酸浸速率,还可以采取的措施有______________ (写一种)。
(2)工业上用稀硫酸浸取碳酸锰矿(主要成分为MnCO3,另含FeO、Fe2O3、CaO等杂质)生产锰酸锂(LiMn2O4),为了提高碳酸锰矿浸出的速率,在“酸浸”时可采取的措施有:①适当升高温度;②搅拌;③_______________ 等。
(3)用NaOH熔盐高钛渣(主要成分为Ti3O5,含少量SiO2、FeO、Fe2O3)制备白色颜料TiO2,为加快反应速率,在维持反应物颗粒大小、反应温度一定的条件下,可采取的措施是________________ 。
(1)用20% H2SO4浸取软锰矿(主要成分为MnO2、SiO2等)制备高纯MnO2,酸浸时,通常加入FeSO4作催化剂加快反应速率。为提高酸浸速率,还可以采取的措施有
(2)工业上用稀硫酸浸取碳酸锰矿(主要成分为MnCO3,另含FeO、Fe2O3、CaO等杂质)生产锰酸锂(LiMn2O4),为了提高碳酸锰矿浸出的速率,在“酸浸”时可采取的措施有:①适当升高温度;②搅拌;③
(3)用NaOH熔盐高钛渣(主要成分为Ti3O5,含少量SiO2、FeO、Fe2O3)制备白色颜料TiO2,为加快反应速率,在维持反应物颗粒大小、反应温度一定的条件下,可采取的措施是
您最近一年使用:0次
5 . 某试样含有 、
、 及㤢性物质。称取试样
及㤢性物质。称取试样 ,溶解后配制到
,溶解后配制到 容量瓶中。吸取
容量瓶中。吸取 ,在
,在 介质中用
介质中用 将
将 还原为
还原为 ,除去过量的
,除去过量的 后调至中性测定
后调至中性测定 ,消耗
,消耗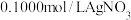 溶液
溶液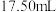 。另吸取
。另吸取 试液用
试液用 酸化后加热除去
酸化后加热除去 ,再调至中性,滴定过剩
,再调至中性,滴定过剩 时消耗了上述
时消耗了上述 溶液
溶液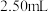 。计算试样中
。计算试样中 、
、 的质量分数
的质量分数_______ 、_______ 。
 、
、 及㤢性物质。称取试样
及㤢性物质。称取试样 ,溶解后配制到
,溶解后配制到 容量瓶中。吸取
容量瓶中。吸取 ,在
,在 介质中用
介质中用 将
将 还原为
还原为 ,除去过量的
,除去过量的 后调至中性测定
后调至中性测定 ,消耗
,消耗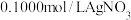 溶液
溶液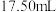 。另吸取
。另吸取 试液用
试液用 酸化后加热除去
酸化后加热除去 ,再调至中性,滴定过剩
,再调至中性,滴定过剩 时消耗了上述
时消耗了上述 溶液
溶液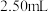 。计算试样中
。计算试样中 、
、 的质量分数
的质量分数
您最近一年使用:0次
名校
解题方法
6 . I.有下列物质:___________ 。
(2)属于苯的同系物的是___________ 。
(3)⑤和⑥的一氯代物分别有___________ 、___________ 种。
Ⅱ.写出下列反应的化学方程式:
(4)丙烯变聚丙烯___________ 。
(5)用甲苯制TNT的反应___________ 。
(6)l,2-二氯乙烷与NaOH溶液共热___________ 。
①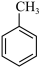 ②
②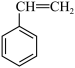 ③
③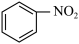 ④
④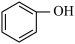
⑤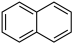 ⑥
⑥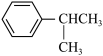 ⑦
⑦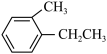
(2)属于苯的同系物的是
(3)⑤和⑥的一氯代物分别有
Ⅱ.写出下列反应的化学方程式:
(4)丙烯变聚丙烯
(5)用甲苯制TNT的反应
(6)l,2-二氯乙烷与NaOH溶液共热
您最近一年使用:0次
2024-04-28更新
|
406次组卷
|
2卷引用:天津市耀华中学2023-2024学年高二下学期期中考试化学试卷
名校
解题方法
7 . 实验探究是化学研究的重要手段。
Ⅰ.工业上利用反应:N2(g)+3H2(g) 2NH3(g) 合成氨气。在1×105Pa和25℃时,反应的ΔH=-92.4kJ·mol-1,回答下列问题:
2NH3(g) 合成氨气。在1×105Pa和25℃时,反应的ΔH=-92.4kJ·mol-1,回答下列问题:
(1)在1×105Pa和25℃时,将1mol N2和足量H2充分反应后,____ (填“吸收”或“放出”)的热量为Q,则Q____ 92.4 kJ(填“>”、“<”或“=”)
(2)合成氨反应在恒容密闭容器中进行,下列叙述能说明反应已达化学平衡状态的是_____ (填序号)。
a.2 v正(N2)=v逆(NH3) b.n(N2):n(H2):n(NH3)=1:3:2
c.容器中气体的密度不随时间而变化 d.容器中压强不变
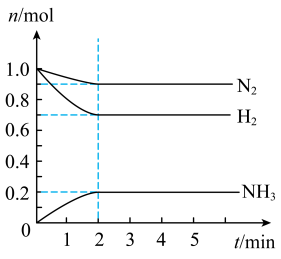
(3)某小组在实验室在2L密闭容器中进行合成氨反应,测出反应中各物质的物质的量变化如图,则反应进行到2min时用NH3表示的平均反应速率为_____ ,H2的转化率为______ 。_____ ,t2到t3反应速率降低的主要原因是 ______ 。
(5)乙图中,a为锌粒与足量稀硫酸反应产生氢气的体积随时间变化情况,其它条件不变,添加适量的下列试剂_____ (填序号),能使a变为b,其原理是_____ 。
A.CuSO4 B.HNO3 C.Na2SO4溶液 D.浓H2SO4
Ⅰ.工业上利用反应:N2(g)+3H2(g)
 2NH3(g) 合成氨气。在1×105Pa和25℃时,反应的ΔH=-92.4kJ·mol-1,回答下列问题:
2NH3(g) 合成氨气。在1×105Pa和25℃时,反应的ΔH=-92.4kJ·mol-1,回答下列问题:(1)在1×105Pa和25℃时,将1mol N2和足量H2充分反应后,
(2)合成氨反应在恒容密闭容器中进行,下列叙述能说明反应已达化学平衡状态的是
a.2 v正(N2)=v逆(NH3) b.n(N2):n(H2):n(NH3)=1:3:2
c.容器中气体的密度不随时间而变化 d.容器中压强不变
(3)某小组在实验室在2L密闭容器中进行合成氨反应,测出反应中各物质的物质的量变化如图,则反应进行到2min时用NH3表示的平均反应速率为
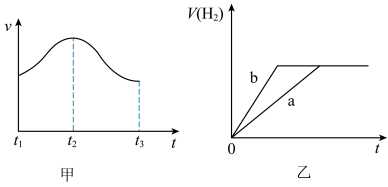
(5)乙图中,a为锌粒与足量稀硫酸反应产生氢气的体积随时间变化情况,其它条件不变,添加适量的下列试剂
A.CuSO4 B.HNO3 C.Na2SO4溶液 D.浓H2SO4
您最近一年使用:0次
解题方法
8 . 完成下列问题。
(1)共轭二烯烃(含有两个碳碳双键,且两个双键被一个单键隔开的烯烃)可以与含碳碳双键的化合物在一定条件下发生第尔斯-阿尔德(Diels-Alder)反应,得到环状产物。_______ (填反应类型)。
②下列不能与乙烯发生Diels-Alder反应的有机物是_______ (填字母)
①A的结构简式为_______ ,A_______ (填“是”或“否”)存在顺反异构。
②写出A与环戊烯发生Diels-Alder反应的化学方程式:_______ 。
(3)已知烯烃与酸性 溶液反应时,不同的结构可以得到不同的氧化产物。如:
溶液反应时,不同的结构可以得到不同的氧化产物。如:
(1)共轭二烯烃(含有两个碳碳双键,且两个双键被一个单键隔开的烯烃)可以与含碳碳双键的化合物在一定条件下发生第尔斯-阿尔德(Diels-Alder)反应,得到环状产物。
例如: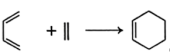
②下列不能与乙烯发生Diels-Alder反应的有机物是
a.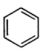 b.
b.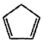 c.
c.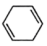 d.
d.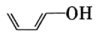
①A的结构简式为
②写出A与环戊烯发生Diels-Alder反应的化学方程式:
(3)已知烯烃与酸性
 溶液反应时,不同的结构可以得到不同的氧化产物。如:
溶液反应时,不同的结构可以得到不同的氧化产物。如: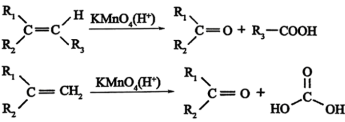
①观察上述氧化过程可知,烃分子中每有一个碳碳双键,则产物中会有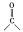 ,产物中元素种类和原子个数与有机反应物相比,未发生变化的元素是
,产物中元素种类和原子个数与有机反应物相比,未发生变化的元素是
②A的一种同系物 用酸性
用酸性 溶液氧化,得到乙酸(
溶液氧化,得到乙酸(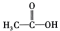 )琥珀酸(
)琥珀酸(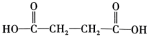 )丙酮
)丙酮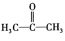 三者的混合物,则B的结构简式为
三者的混合物,则B的结构简式为
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
9 . 硫酸亚铁在工农业生产中有许多用途,如可用作农药防治小麦黑穗病,制造磁性氧化铁、铁催化剂等。回答下列问题:
(1)将 置入抽空的刚性容器中,升高温度发生分解反应:
置入抽空的刚性容器中,升高温度发生分解反应: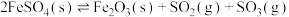 (I)。平衡时
(I)。平衡时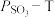 的关系如下图所示。
的关系如下图所示。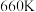 时,该反应的平衡总压
时,该反应的平衡总压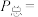
___________  、平衡常数
、平衡常数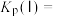
___________  。
。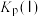 随反应温度升高而
随反应温度升高而___________ (填“增大”“减小”或“不变”)。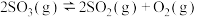 (II),平衡时
(II),平衡时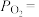
___________ (用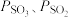 表示)。在
表示)。在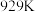 时,
时, ,则
,则
___________  ,
,
___________  (列出计算式)。
(列出计算式)。
(1)将
 置入抽空的刚性容器中,升高温度发生分解反应:
置入抽空的刚性容器中,升高温度发生分解反应: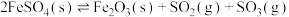 (I)。平衡时
(I)。平衡时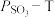 的关系如下图所示。
的关系如下图所示。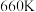 时,该反应的平衡总压
时,该反应的平衡总压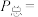
 、平衡常数
、平衡常数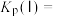
 。
。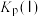 随反应温度升高而
随反应温度升高而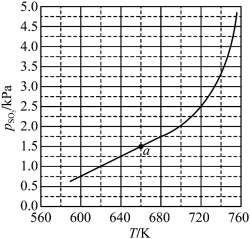
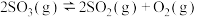 (II),平衡时
(II),平衡时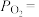
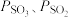 表示)。在
表示)。在 时,
时, ,则
,则
 ,
,
 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
10 . 探究pH对 溶液的配制和保存的影响。
溶液的配制和保存的影响。
I. 溶液的配制
溶液的配制
将 分别溶于10mL蒸馏水或10mL稀硫酸,现象如下:
分别溶于10mL蒸馏水或10mL稀硫酸,现象如下:
II. 溶液的保存
溶液的保存
将实验I中配制的三份溶液分别在空气中放置24小时后,记录如下。
(1)①中的浑浊主要是FeOOH,用离子方程式表示其生成过程_______ 。
(2)该实验的初步结论:保存 溶液的最佳pH是
溶液的最佳pH是_______ 。
(3)进一步探究pH对 变质影响的原因。用下图所示装置完成实验(滴加试剂时溶液体积和导电性变化可忽略)。向右池持续稳定通入氧气,待电流计示数稳定后:
变质影响的原因。用下图所示装置完成实验(滴加试剂时溶液体积和导电性变化可忽略)。向右池持续稳定通入氧气,待电流计示数稳定后: 接近2mol/L,电流没有明显变化;
接近2mol/L,电流没有明显变化;
ii.向右池滴加等量浓硫酸,电流明显增大。
已知:电流增大表明化学反应速率加快,在该实验条件下与物质的氧化性(还原性)增强有关。
a.结合电极反应式分析ii中电流增大的原因_______ 。
b.依据实验i和ii推断:③比②中 更易变质的原因是
更易变质的原因是_______ 。
c.按上述原理进行实验,证实①中 更易变质的主要原因是
更易变质的主要原因是 的还原性增强,氧化速率加快,而与氧气性质变化关系不大。实验方案及预期现象是:向右池持续稳定通入氧气,待电流计示数稳定后,
的还原性增强,氧化速率加快,而与氧气性质变化关系不大。实验方案及预期现象是:向右池持续稳定通入氧气,待电流计示数稳定后,_______ 。
 溶液的配制和保存的影响。
溶液的配制和保存的影响。I.
 溶液的配制
溶液的配制将
 分别溶于10mL蒸馏水或10mL稀硫酸,现象如下:
分别溶于10mL蒸馏水或10mL稀硫酸,现象如下:| 编号 | 溶剂 | 溶液性状 | |
| ① | 蒸馏水 | 浅黄色澄清溶液 |  ;滴加1mol/LKSCN溶液无明显变化 ;滴加1mol/LKSCN溶液无明显变化 |
| ② |  | 无色澄清溶液 |  ;滴加1mol/LKSCN溶液微微变红 ;滴加1mol/LKSCN溶液微微变红 |
| ③ |  | 无色澄清溶液 | 滴加1mol/LKSCN溶液微微变红 |
 溶液的保存
溶液的保存将实验I中配制的三份溶液分别在空气中放置24小时后,记录如下。
| 编号 | 溶液性状 | |
| ① | 橙色浑浊 | 用 酸化后,浊液变澄清,再滴加1mol/LKSCN溶液后变深红 酸化后,浊液变澄清,再滴加1mol/LKSCN溶液后变深红 |
| ② | 无色溶液 | 滴加1mol/L的KSCN溶液后显浅红色 |
| ③ | 无色溶液 | 滴加1mol/L的KSCN溶液后显红色,颜色比②略深 |
(2)该实验的初步结论:保存
 溶液的最佳pH是
溶液的最佳pH是(3)进一步探究pH对
 变质影响的原因。用下图所示装置完成实验(滴加试剂时溶液体积和导电性变化可忽略)。向右池持续稳定通入氧气,待电流计示数稳定后:
变质影响的原因。用下图所示装置完成实验(滴加试剂时溶液体积和导电性变化可忽略)。向右池持续稳定通入氧气,待电流计示数稳定后: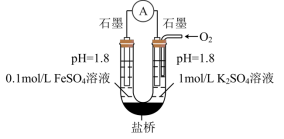
 接近2mol/L,电流没有明显变化;
接近2mol/L,电流没有明显变化;ii.向右池滴加等量浓硫酸,电流明显增大。
已知:电流增大表明化学反应速率加快,在该实验条件下与物质的氧化性(还原性)增强有关。
a.结合电极反应式分析ii中电流增大的原因
b.依据实验i和ii推断:③比②中
 更易变质的原因是
更易变质的原因是c.按上述原理进行实验,证实①中
 更易变质的主要原因是
更易变质的主要原因是 的还原性增强,氧化速率加快,而与氧气性质变化关系不大。实验方案及预期现象是:向右池持续稳定通入氧气,待电流计示数稳定后,
的还原性增强,氧化速率加快,而与氧气性质变化关系不大。实验方案及预期现象是:向右池持续稳定通入氧气,待电流计示数稳定后,
您最近一年使用:0次



