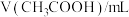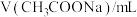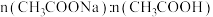名校
解题方法
1 . 回答下列问题。
(1)已知 具有氧化性,与氨气加热反应的产物中含有两种单质。写出在加热条件下
具有氧化性,与氨气加热反应的产物中含有两种单质。写出在加热条件下 和
和 反应的化学方程式:
反应的化学方程式:_______ 。
(2)在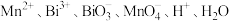 组成的一个氧化还原反应体系中,发生
组成的一个氧化还原反应体系中,发生 的反应过程。将以上物质组成一个正确的离子方程式,并用单线桥标出其电子转移的方向和数目:
的反应过程。将以上物质组成一个正确的离子方程式,并用单线桥标出其电子转移的方向和数目:_______ 。
(3) 与
与 和
和 的混合溶液作用,是一种制备理想的绿色水处理剂
的混合溶液作用,是一种制备理想的绿色水处理剂 的方法,写出该反应的化学方程式:
的方法,写出该反应的化学方程式:_______ 。
(4) 可用于实验室制
可用于实验室制 ,若不加催化剂,
,若不加催化剂, 时
时 分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为
分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为 ,写出该反应的化学方程式:
,写出该反应的化学方程式:_______ 。
(5)某地污水中有机污染物的主要成分是三氯乙烯 ,向该污水中加入
,向该污水中加入 (还原产物为
(还原产物为 )溶液可将其中的三氯乙烯除去,氧化产物只有
)溶液可将其中的三氯乙烯除去,氧化产物只有 ,写出该反应的化学方程式:
,写出该反应的化学方程式:_______ 。
(6)我国稀土资源丰富,氟化镨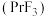 常用于电弧碳棒添加剂。工业上采用方镨矿(主要成分
常用于电弧碳棒添加剂。工业上采用方镨矿(主要成分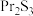 ,难溶于水)制备氟化镨的工艺流程如图所示:
,难溶于水)制备氟化镨的工艺流程如图所示: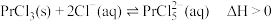 。
。
①步骤I为“溶浸除硫”,反应后镨元素以 形式存在,则反应的离子方程式为
形式存在,则反应的离子方程式为_______ 。
②写出步骤Ⅲ“转化”过程的化学方程式:_______ 。
(1)已知
 具有氧化性,与氨气加热反应的产物中含有两种单质。写出在加热条件下
具有氧化性,与氨气加热反应的产物中含有两种单质。写出在加热条件下 和
和 反应的化学方程式:
反应的化学方程式:(2)在
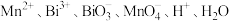 组成的一个氧化还原反应体系中,发生
组成的一个氧化还原反应体系中,发生 的反应过程。将以上物质组成一个正确的离子方程式,并用单线桥标出其电子转移的方向和数目:
的反应过程。将以上物质组成一个正确的离子方程式,并用单线桥标出其电子转移的方向和数目:(3)
 与
与 和
和 的混合溶液作用,是一种制备理想的绿色水处理剂
的混合溶液作用,是一种制备理想的绿色水处理剂 的方法,写出该反应的化学方程式:
的方法,写出该反应的化学方程式:(4)
 可用于实验室制
可用于实验室制 ,若不加催化剂,
,若不加催化剂, 时
时 分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为
分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为 ,写出该反应的化学方程式:
,写出该反应的化学方程式:(5)某地污水中有机污染物的主要成分是三氯乙烯
 ,向该污水中加入
,向该污水中加入 (还原产物为
(还原产物为 )溶液可将其中的三氯乙烯除去,氧化产物只有
)溶液可将其中的三氯乙烯除去,氧化产物只有 ,写出该反应的化学方程式:
,写出该反应的化学方程式:(6)我国稀土资源丰富,氟化镨
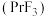 常用于电弧碳棒添加剂。工业上采用方镨矿(主要成分
常用于电弧碳棒添加剂。工业上采用方镨矿(主要成分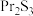 ,难溶于水)制备氟化镨的工艺流程如图所示:
,难溶于水)制备氟化镨的工艺流程如图所示: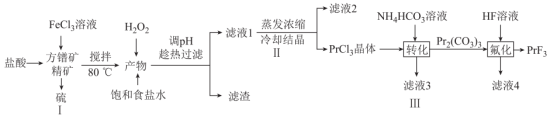
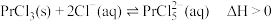 。
。①步骤I为“溶浸除硫”,反应后镨元素以
 形式存在,则反应的离子方程式为
形式存在,则反应的离子方程式为②写出步骤Ⅲ“转化”过程的化学方程式:
您最近一年使用:0次
2024-08-31更新
|
131次组卷
|
2卷引用:2025届广东省部分学校高三上学期一调考试化学试题
名校
2 . 铁是人类生活中很常见的元素。回答下列问题:
I.铁是人体含量最多的微量元素,这些铁在人体中不是以金属单质的形式存在,而是以 和
和 的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁盐,如硫酸亚铁。
的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁盐,如硫酸亚铁。
(1)以下为常见的含铁元素的几种微粒,其中既有氧化性又有还原性的是_______ (填选项字母)。
A. B.
B. C.
C.
(2)工业盐的主要成分是 ,以前有许多起因误食
,以前有许多起因误食 而中毒的事件,其原因是
而中毒的事件,其原因是 会把人体内的
会把人体内的 转化为
转化为 而使其失去与
而使其失去与 结合的能力,这说明
结合的能力,这说明 具有
具有_______ 性;下列不能使 发生这种转化的物质是
发生这种转化的物质是_______ (填选项字母)。
A. B.
B. C.
C. D.浓硫酸
D.浓硫酸
(3)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有_______ 性。
Ⅱ.实验小组发现新配制的 溶液在放置一段时间后,由浅绿色溶液变为黄色浊液a,故进行如下探究。
溶液在放置一段时间后,由浅绿色溶液变为黄色浊液a,故进行如下探究。
(4)判断其中是否存在 的方法与现象为
的方法与现象为_______ ;检验其中的 时可选择的试剂为
时可选择的试剂为_______ 。
(5)取 浊液a,加入足量稀硫酸,再加
浊液a,加入足量稀硫酸,再加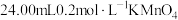 溶液恰好可以完全反应,则浊液a中
溶液恰好可以完全反应,则浊液a中 的浓度为
的浓度为_______  ,氧化率为
,氧化率为_______ (氧化率=被氧化的物质的量占总的物质的量的百分数)。
(6)设 为阿伏加德罗常数的值。在反应
为阿伏加德罗常数的值。在反应 中,每有
中,每有 参加反应,理论上转移电子的数目为
参加反应,理论上转移电子的数目为_______ 个(用 表示)。
表示)。
I.铁是人体含量最多的微量元素,这些铁在人体中不是以金属单质的形式存在,而是以
 和
和 的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁盐,如硫酸亚铁。
的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁盐,如硫酸亚铁。(1)以下为常见的含铁元素的几种微粒,其中既有氧化性又有还原性的是
A.
 B.
B. C.
C.
(2)工业盐的主要成分是
 ,以前有许多起因误食
,以前有许多起因误食 而中毒的事件,其原因是
而中毒的事件,其原因是 会把人体内的
会把人体内的 转化为
转化为 而使其失去与
而使其失去与 结合的能力,这说明
结合的能力,这说明 具有
具有 发生这种转化的物质是
发生这种转化的物质是A.
 B.
B. C.
C. D.浓硫酸
D.浓硫酸(3)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有
Ⅱ.实验小组发现新配制的
 溶液在放置一段时间后,由浅绿色溶液变为黄色浊液a,故进行如下探究。
溶液在放置一段时间后,由浅绿色溶液变为黄色浊液a,故进行如下探究。(4)判断其中是否存在
 的方法与现象为
的方法与现象为 时可选择的试剂为
时可选择的试剂为(5)取
 浊液a,加入足量稀硫酸,再加
浊液a,加入足量稀硫酸,再加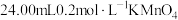 溶液恰好可以完全反应,则浊液a中
溶液恰好可以完全反应,则浊液a中 的浓度为
的浓度为 ,氧化率为
,氧化率为(6)设
 为阿伏加德罗常数的值。在反应
为阿伏加德罗常数的值。在反应 中,每有
中,每有 参加反应,理论上转移电子的数目为
参加反应,理论上转移电子的数目为 表示)。
表示)。
您最近一年使用:0次
2024-08-31更新
|
100次组卷
|
2卷引用:2025届广东省部分学校高三上学期一调考试化学试题
解题方法
3 . 生活离不开化学。家庭厨卫中有许多中学化学常见的物质,括号内为厨卫商品的主要成分。
①食盐(NaCl) ②料酒(乙醇) ③食醋(乙酸) ④碱面(Na2CO3) ⑤发酵粉(NaHCO3和明矾) ⑥84消毒液(NaClO) ⑦洁厕灵(HCl)
回答下列问题:
(1)NaCl的摩尔质量为______ ,当食盐不慎洒落在天然气的火焰上,观察到的现象是______ 。
(2)②③的主要成分可以归为一类物质,其分类的依据是______(填正确答案标号)。
(3)除去Na2CO3固体中混有的少量NaHCO3杂质,应采取的最佳方法是______ ,除杂过程中发生反应的化学方程式为______ 。
(4)①84消毒液和洁厕灵不能混合使用,用离子方程式表示其理由:______ 。
②某同学用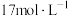 的浓硫酸配制480mL
的浓硫酸配制480mL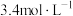 的稀硫酸用于增强84消毒液的消毒能力,需取用浓硫酸的体积为
的稀硫酸用于增强84消毒液的消毒能力,需取用浓硫酸的体积为______ mL。
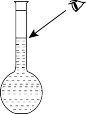
③该同学观察液面时如图所示,对所配溶液的浓度将______ (填“偏高”、“偏低”或“无影响”)。
①食盐(NaCl) ②料酒(乙醇) ③食醋(乙酸) ④碱面(Na2CO3) ⑤发酵粉(NaHCO3和明矾) ⑥84消毒液(NaClO) ⑦洁厕灵(HCl)
回答下列问题:
(1)NaCl的摩尔质量为
(2)②③的主要成分可以归为一类物质,其分类的依据是______(填正确答案标号)。
| A.两种物质都是非电解质 | B.两种物质都是电解质 |
| C.两种物质都是含碳化合物 | D.两种物质都是氧化物 |
(3)除去Na2CO3固体中混有的少量NaHCO3杂质,应采取的最佳方法是
(4)①84消毒液和洁厕灵不能混合使用,用离子方程式表示其理由:
②某同学用
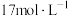 的浓硫酸配制480mL
的浓硫酸配制480mL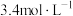 的稀硫酸用于增强84消毒液的消毒能力,需取用浓硫酸的体积为
的稀硫酸用于增强84消毒液的消毒能力,需取用浓硫酸的体积为③该同学观察液面时如图所示,对所配溶液的浓度将
您最近一年使用:0次
4 . Ⅰ.书写以下化学用语:
(1)CO2电子式:______ 。
(2)NaHSO4溶于水的电离方程式:______ 。
(3)铁与氯气在加热条件下的化学方程式:______ 。
(4)Fe3O4溶于稀硫酸的离子方程式:______ 。
Ⅱ.将24.4gNaOH固体溶于水配成100mL溶液:
(5)该溶液中OH﹣的浓度为______ 。
(6)从该溶液中取出10mL,含NaOH的质量为______ ,含NaOH的物质的量为______ 。
(1)CO2电子式:
(2)NaHSO4溶于水的电离方程式:
(3)铁与氯气在加热条件下的化学方程式:
(4)Fe3O4溶于稀硫酸的离子方程式:
Ⅱ.将24.4gNaOH固体溶于水配成100mL溶液:
(5)该溶液中OH﹣的浓度为
(6)从该溶液中取出10mL,含NaOH的质量为
您最近一年使用:0次
名校
解题方法
5 . 已知i.2CO(g)+O2(g)=2CO2(g) ΔH1=﹣566.0kJ•mol﹣1;
ⅱ.2H2(g)+O2(g)=2H2O(l) ΔH2=﹣483.6 kJ•mol﹣1;
ⅲ.CO(g)+2H2(g)=CH3OH(g) ΔH3=﹣574.4 kJ•mol﹣1;
写出CH3OH燃烧热的热化学方程式:___________ 。
ⅱ.2H2(g)+O2(g)=2H2O(l) ΔH2=﹣483.6 kJ•mol﹣1;
ⅲ.CO(g)+2H2(g)=CH3OH(g) ΔH3=﹣574.4 kJ•mol﹣1;
写出CH3OH燃烧热的热化学方程式:
您最近一年使用:0次
名校
解题方法
6 . 在恒温下体积为2L的密闭容器中,通入1mol氮气和3mol氢气,2min后达到平衡,测得混合气体中氮气的物质的量为0.8mol,求:
(1)反应开始到达到平衡这段时间内氮气的反应速率___________ 。
(2)平衡时H2的转化率___________ 。
(3)平衡混合气体中NH3的体积分数___________ 。
(1)反应开始到达到平衡这段时间内氮气的反应速率
(2)平衡时H2的转化率
(3)平衡混合气体中NH3的体积分数
您最近一年使用:0次
7 . 食醋是烹饪美食的调味品,有效成分主要为醋酸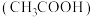 。
。 的应用与其电离平衡密切相关。
的应用与其电离平衡密切相关。
(1)下列事实可证明醋酸具有酸性的是_______。
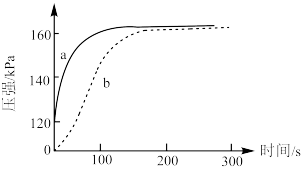
(2)为了探究醋酸的电离程度,先向两个锥形瓶中分别加入形状相同、长度相等的镁条(过量),再分别加入等体积、等浓度的盐酸和醋酸溶液,测得锥形瓶内的气压随时间的变化如图所示。醋酸溶液对应的曲线是_______ (填“a”或“b”),原因是_______ 。 电离平衡的影响因素。
电离平衡的影响因素。
甲同学设计实验方案如下(表中 和
和 溶液浓度均为
溶液浓度均为 );
);
①由实验Ⅰ和Ⅱ可知,稀释 溶液,电离平衡
溶液,电离平衡_______ (填“正”或“逆”)向移动;结合表中数据,给出判断理由:_______ 。
②实验Ⅱ和Ⅲ探究_______ 对 电离平衡的影响,补充数据:
电离平衡的影响,补充数据:
_______ ,
_______ 。
③根据表中数据,计算25℃时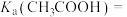
_______ 。
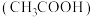 。
。 的应用与其电离平衡密切相关。
的应用与其电离平衡密切相关。(1)下列事实可证明醋酸具有酸性的是_______。
| A.食醋具有杀菌消毒作用 |
| B.食醋可除去水壶中的水垢 |
| C.用醋酸溶液做导电性实验,灯泡很暗 |
D. 醋酸溶液可以使紫色石蕊试液变红 醋酸溶液可以使紫色石蕊试液变红 |
(2)为了探究醋酸的电离程度,先向两个锥形瓶中分别加入形状相同、长度相等的镁条(过量),再分别加入等体积、等浓度的盐酸和醋酸溶液,测得锥形瓶内的气压随时间的变化如图所示。醋酸溶液对应的曲线是
 电离平衡的影响因素。
电离平衡的影响因素。甲同学设计实验方案如下(表中
 和
和 溶液浓度均为
溶液浓度均为 );
);序号 |
|
|
|
| pH |
Ⅰ | 20.00 | / | / | 0 | 2.86 |
Ⅱ | 2.00 | / | 18.00 | 0 | 3.36 |
Ⅲ | 2.00 |
|
|
| 4.72 |
 溶液,电离平衡
溶液,电离平衡②实验Ⅱ和Ⅲ探究
 电离平衡的影响,补充数据:
电离平衡的影响,补充数据:

③根据表中数据,计算25℃时
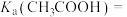
您最近一年使用:0次
名校
解题方法
8 . 用电弧法合成碳纳米管,常伴有大量杂质——碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,其反应的化学方程式为: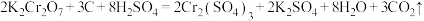
(1)用双线桥法表示出上述反应的电子转移方向和数目_______ 。
(2)此反应的氧化产物和还原产物的物质的量之比为_______ 。
(3)要使10mL 1.0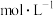
 溶液被还原至少要加入
溶液被还原至少要加入_______ mL2.0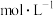 的
的 溶液,消耗C的质量为
溶液,消耗C的质量为_______ g。
(4)若产生6.72L (标准状况下)气体,该反应转移电子的物质的量为
(标准状况下)气体,该反应转移电子的物质的量为_______ mol。
(5)若改用FeSO4还原K2Cr2O7,则还原1mol K2Cr2O7需要_______ mol FeSO4。
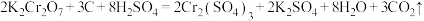
(1)用双线桥法表示出上述反应的电子转移方向和数目
(2)此反应的氧化产物和还原产物的物质的量之比为
(3)要使10mL 1.0
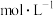
 溶液被还原至少要加入
溶液被还原至少要加入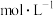 的
的 溶液,消耗C的质量为
溶液,消耗C的质量为(4)若产生6.72L
 (标准状况下)气体,该反应转移电子的物质的量为
(标准状况下)气体,该反应转移电子的物质的量为(5)若改用FeSO4还原K2Cr2O7,则还原1mol K2Cr2O7需要
您最近一年使用:0次
名校
9 . 现有下列8种物质:①液氨;②铜;③熔融NaHSO4;④CaO;⑤盐酸;⑥蔗糖;⑦ HNO3;⑧CuSO4·5H2O,请按下列分类标准回答问题(填写物质编号)。
(1)能导电的是_______ 。
(2)属于电解质是_______ 。
(3)属于非电解质的是_______ 。
(4)写出NaHSO4溶液与Ba(OH)2溶液反应至溶液呈中性时的离子方程式_______ 。
(5)某气态氧化物化学式为RO2,在标准状况下,1.28 g该氧化物的体积是448 mL,则氧化物的摩尔质量为_______ ,R的相对原子质量为_______ 。
(6)在标准状况下①3.36L NH3;②1.204×1023个CH4;③18gH2O;④0.4 mol HCl,氢原子个数由小到大的顺序_______ (用序号回答)。
(1)能导电的是
(2)属于电解质是
(3)属于非电解质的是
(4)写出NaHSO4溶液与Ba(OH)2溶液反应至溶液呈中性时的离子方程式
(5)某气态氧化物化学式为RO2,在标准状况下,1.28 g该氧化物的体积是448 mL,则氧化物的摩尔质量为
(6)在标准状况下①3.36L NH3;②1.204×1023个CH4;③18gH2O;④0.4 mol HCl,氢原子个数由小到大的顺序
您最近一年使用:0次
名校
10 . 某温度时,在容积为3L的密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化的曲线如图所示。分析图中数据,回答下列问题:___________ 。
(2)该反应是由___________ (填“正反应”、“逆反应”或“正、逆反应同时”)开始反应的。
(3)下列哪些数据在反应开始至反应达到平衡时。一直保持不变的是___________ (填字母)
a.压强 b.密度 c.相对平均式量 d.反应物的浓度
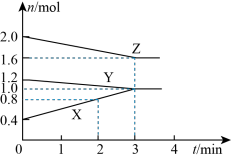
(2)该反应是由
(3)下列哪些数据在反应开始至反应达到平衡时。一直保持不变的是
a.压强 b.密度 c.相对平均式量 d.反应物的浓度
您最近一年使用:0次