回答下列问题。
(1)理论上不能设计为原电池的化学反应是___________ 。
a.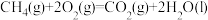
b.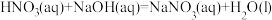
c.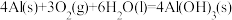
d.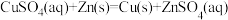
(2)某小组为探究 与
与 能否发生氧化还原反应,设计如下图所示双液原电池(盐桥中为饱和
能否发生氧化还原反应,设计如下图所示双液原电池(盐桥中为饱和 溶液的琼脂)。该装置石墨棒上发生的电极反应式为
溶液的琼脂)。该装置石墨棒上发生的电极反应式为___________ ,盐桥中 向
向___________ 烧杯移动(填“甲”或“乙”)。___________ ,B电极的电极反应方程式为___________ 。 为电解质。工作时负极的电极反应式
为电解质。工作时负极的电极反应式___________ 。
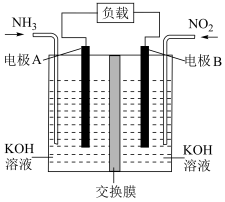
(5)汽车尾气中含有的 是造成城市空气污染的主要因素之一,通过
是造成城市空气污染的主要因素之一,通过 传感器可监测汽车尾气史
传感器可监测汽车尾气史 含量,其工作原理如图所示:
含量,其工作原理如图所示: 电极为
电极为___________ (填“正极”或“负极), 电极上发生的电极反应式为
电极上发生的电极反应式为___________ 。
(1)理论上不能设计为原电池的化学反应是
a.
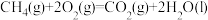
b.
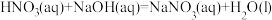
c.
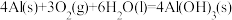
d.
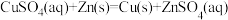
(2)某小组为探究
 与
与 能否发生氧化还原反应,设计如下图所示双液原电池(盐桥中为饱和
能否发生氧化还原反应,设计如下图所示双液原电池(盐桥中为饱和 溶液的琼脂)。该装置石墨棒上发生的电极反应式为
溶液的琼脂)。该装置石墨棒上发生的电极反应式为 向
向
 为电解质。工作时负极的电极反应式
为电解质。工作时负极的电极反应式(5)汽车尾气中含有的
 是造成城市空气污染的主要因素之一,通过
是造成城市空气污染的主要因素之一,通过 传感器可监测汽车尾气史
传感器可监测汽车尾气史 含量,其工作原理如图所示:
含量,其工作原理如图所示:
 电极为
电极为 电极上发生的电极反应式为
电极上发生的电极反应式为
更新时间:2024-05-13 11:34:48
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】某实验小组同学对电化学原理进行了一系列探究活动
(1)如图为该实验小组设计的原电池装置,Fe电极的电势______ (填“高于”或“低于”)石墨的。反应前,两电极质量相等,一端时间后,两电极质量相差24g,则导线中通过_______ mol电子。
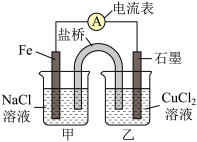
(2)其他条件不变,若将CuCl2溶液换为NH4Cl溶液,则石墨电极的电极反应式为_________ ,该电池电流由_______ (填“铁”或“石墨”下同)电极经外电路流向_____ 电极;
(3)用吸管吸出少许铁片附近的溶液置于试管中,向其中滴加少量新制饱和氯水,然后滴加几滴硫氰化钾溶液,溶液变红,写出该过程中发生的氧化还原反应的离子方程式:_____ 。
(1)如图为该实验小组设计的原电池装置,Fe电极的电势

(2)其他条件不变,若将CuCl2溶液换为NH4Cl溶液,则石墨电极的电极反应式为
(3)用吸管吸出少许铁片附近的溶液置于试管中,向其中滴加少量新制饱和氯水,然后滴加几滴硫氰化钾溶液,溶液变红,写出该过程中发生的氧化还原反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.碳中和作为一种新型环保形式可推动全社会绿色发展。我国争取2060年前实现碳中和,科学家正在研究建立如下图所示的二氧化碳新循环体系。
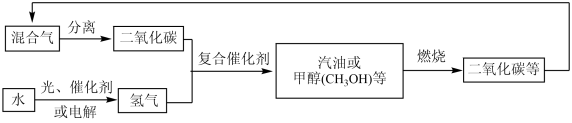
回答下面问题:
(1)结合图示,下列说法正确的是_______ (填序号)。
①燃烧时化学能可以转化为热能
②光能(或电能)可以转化为化学能
③减少碳排放有利于缓解全球变暖
④风电、光伏发电等新能源的开发和使用可减少碳排放
Ⅱ.复合催化是工业合成甲醇 的重要反应,在2L密闭容器中,充入
的重要反应,在2L密闭容器中,充入 和
和 ,在催化剂、200℃的条件下发生反应。部分反应物和产物随时间变化如右图所示:
,在催化剂、200℃的条件下发生反应。部分反应物和产物随时间变化如右图所示:
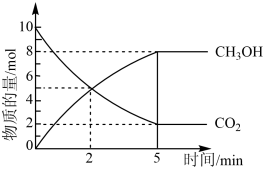
(2)该反应的化学方程式为_______ 。
(3)反应开始至2min末,以 的浓度变化表示该反应的平均速率是
的浓度变化表示该反应的平均速率是_______  。
。
(4)下列情况不能说明该反应一定达到化学平衡状态的是_______ (填字母)。
a.单位时间内消耗1mol ,同时生成1mol
,同时生成1mol
b. 的物质的量保持不变
的物质的量保持不变
c.密闭容器内气体压强不发生变化时
d.密闭容器中 不发生变化时
不发生变化时
(5)在不改变上述反应条件(催化剂、温度、容积和 的物质的量)前提下,要增大反应速率,还可以采取的措施是
的物质的量)前提下,要增大反应速率,还可以采取的措施是_______ 。
(6)写出甲醇 充分燃烧的化学方程式
充分燃烧的化学方程式_______ 。该反应在特殊装置中可以实现原电池反应,分析原因是_______ 。惰性负极上应当通入的物质是_______ (填化学式)。

回答下面问题:
(1)结合图示,下列说法正确的是
①燃烧时化学能可以转化为热能
②光能(或电能)可以转化为化学能
③减少碳排放有利于缓解全球变暖
④风电、光伏发电等新能源的开发和使用可减少碳排放
Ⅱ.复合催化是工业合成甲醇
 的重要反应,在2L密闭容器中,充入
的重要反应,在2L密闭容器中,充入 和
和 ,在催化剂、200℃的条件下发生反应。部分反应物和产物随时间变化如右图所示:
,在催化剂、200℃的条件下发生反应。部分反应物和产物随时间变化如右图所示:
(2)该反应的化学方程式为
(3)反应开始至2min末,以
 的浓度变化表示该反应的平均速率是
的浓度变化表示该反应的平均速率是 。
。(4)下列情况不能说明该反应一定达到化学平衡状态的是
a.单位时间内消耗1mol
 ,同时生成1mol
,同时生成1mol
b.
 的物质的量保持不变
的物质的量保持不变c.密闭容器内气体压强不发生变化时
d.密闭容器中
 不发生变化时
不发生变化时(5)在不改变上述反应条件(催化剂、温度、容积和
 的物质的量)前提下,要增大反应速率,还可以采取的措施是
的物质的量)前提下,要增大反应速率,还可以采取的措施是(6)写出甲醇
 充分燃烧的化学方程式
充分燃烧的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】2020年第七十五届联合国大会上,中国向世界郑重承诺在2030年前实现碳达峰,在2060年前实现碳中和。大力发展绿色能源、清洁能源是实现碳中和的最有效方法。
(1)原电池反应能够提供电能而不产生CO2气体,下图是某原电池装置图。
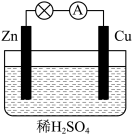
①Zn棒是原电池的___________ 极,发生___________ (填“氧化”或“还原”)反应。
②Cu棒上发生的电极反应是___________ 。
③溶液中H+向___________ (填“Zn”或“Cu”)电极定向移动。
(2)将上述装置中电解质稀H2SO4换为足量AgNO3溶液,灯泡也变亮,电流表指针偏转,无色溶液颜色没有变化。
①原电池的负极是___________ (填“Zn”或“Cu”),正极的电极反应是___________ 。
②若更换电解质时称量两个电极,质量恰好相等,放电一段时间后再称量两个电极,发现质量相差2.81g,则导线上通过的n(e-)=___________ mol。
(3)碱性锌锰电池是日常生活中常用电池,原电池反应是:Zn(①)+ 2MnO2 (②) +2H2O =Zn(OH)2(③)+2MnOOH(④)。该原电池的正极材料是___________ (填序号,下同),负极材料是___________ 。
(1)原电池反应能够提供电能而不产生CO2气体,下图是某原电池装置图。

①Zn棒是原电池的
②Cu棒上发生的电极反应是
③溶液中H+向
(2)将上述装置中电解质稀H2SO4换为足量AgNO3溶液,灯泡也变亮,电流表指针偏转,无色溶液颜色没有变化。
①原电池的负极是
②若更换电解质时称量两个电极,质量恰好相等,放电一段时间后再称量两个电极,发现质量相差2.81g,则导线上通过的n(e-)=
(3)碱性锌锰电池是日常生活中常用电池,原电池反应是:Zn(①)+ 2MnO2 (②) +2H2O =Zn(OH)2(③)+2MnOOH(④)。该原电池的正极材料是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】微型纽扣电池在现代生活中应用广泛。有一种银锌电池,其电极分别是 和Zn,电解质溶液为KOH溶液,总反应式为
和Zn,电解质溶液为KOH溶液,总反应式为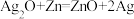 。回答下列问题:
。回答下列问题:
(1)Zn是_________ 极,发生_________ 反应,该电池的正极反应式为___________________________ 。
(2)电池内部电流方向是从_________ (填“ ”或“Zn”,下同)极流向
”或“Zn”,下同)极流向_________ 极,当外电路中有1mol  通过时,负极消耗的物质的质量是
通过时,负极消耗的物质的质量是_________ g。
(3)在使用过程中,电解质溶液中KOH的物质的量_________ (填“增大”“减小”或“不变”)。
 和Zn,电解质溶液为KOH溶液,总反应式为
和Zn,电解质溶液为KOH溶液,总反应式为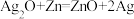 。回答下列问题:
。回答下列问题:(1)Zn是
(2)电池内部电流方向是从
 ”或“Zn”,下同)极流向
”或“Zn”,下同)极流向 通过时,负极消耗的物质的质量是
通过时,负极消耗的物质的质量是(3)在使用过程中,电解质溶液中KOH的物质的量
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】能源是现代社会发展的支柱之一。请回答下列问题:
(1)化学反应中的能量变化,通常主要表现为热量的变化。
①下列反应中,属于放热反应的是___________ (填字母)。
a.Ba(OH)2·8H2O与NH4Cl混合搅拌
b.高温煅烧石灰石
c.铝与盐酸反应
②某同学进行如图所示实验,测量稀盐酸与烧碱溶液中和反应的能量变化。实验表明:反应温度升高,由此判断该反应是__________ (填“吸热”或“放热”)反应,其离子方程式是____________ 。
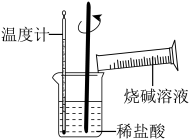
(2)电能是现代社会应用最广泛的能源之一。如图所示的原电池装置中,其负极是___________ ,正极上 能够观察到的现象是____________________ ,正极的电极反应式是___________________ 。原电池工作一段时间后,若消耗锌6.5 g,则放出标准状况下气体__________ L。
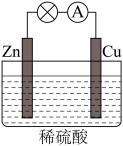
(1)化学反应中的能量变化,通常主要表现为热量的变化。
①下列反应中,属于放热反应的是
a.Ba(OH)2·8H2O与NH4Cl混合搅拌
b.高温煅烧石灰石
c.铝与盐酸反应
②某同学进行如图所示实验,测量稀盐酸与烧碱溶液中和反应的能量变化。实验表明:反应温度升高,由此判断该反应是

(2)电能是现代社会应用最广泛的能源之一。如图所示的原电池装置中,其负极是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】利用反应6NO2+8NH3=7N2+12H2O构成电池的方法,既能实现有效除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示,回答问题:


(1)电流从____ (选填“左”或“右”,下同)侧电极经过负载后流向______ 侧电极。
(2)为使电池持续放电,离子交换膜需选用______ 离子交换膜(选填“阴”或“阳”)。
(3)A电极上的电极反应式为___________________________ 。
(4)当有4.48 L NO2(标准状况)被处理时,转移电子为________ 摩尔。
(5)负载可以测定电流大小,从而确定气体含量,酒驾测定工作原理与其相似。仔细阅读图:写出阴极反应式:____________________________ 。


(1)电流从
(2)为使电池持续放电,离子交换膜需选用
(3)A电极上的电极反应式为
(4)当有4.48 L NO2(标准状况)被处理时,转移电子为
(5)负载可以测定电流大小,从而确定气体含量,酒驾测定工作原理与其相似。仔细阅读图:写出阴极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】依据氧化还原反应:2Ag+(aq)+Cu(s)===Cu2+(aq)+2Ag(s)设计的原电池如图所示。

请回答下列问题:
(1)电极X的材料是_____________ ;电解质溶液Y是_______________ 。
(2)银电极为电池的______ 极,发生的电极反应式为_______________________ ;X电极上发生的电极反应为_______________________________________ 。
(3)盐桥中______ (选填“阳离子”或“阴离子”)向硫酸铜溶液方向移动。

请回答下列问题:
(1)电极X的材料是
(2)银电极为电池的
(3)盐桥中
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】根据所学知识,回答下列问题:
(1)下列变化中,属于吸热反应的是_______ 。(填标号)
①氧化钙与水反应;②石灰石在高温下的分解反应;③酸碱中和反应;④二氧化碳通过炽热的炭发生的反应;⑤食物因氧化而腐败发生的反应;⑥ 与
与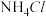 的反应;⑦干冰汽化。
的反应;⑦干冰汽化。
(2)为探究固体M溶于水的热效应,选择如图所示装置进行实验(反应在甲中进行)。观察到烧杯里产生气泡,则M溶于水_______ (填“一定”或“可能”)是放热反应。

(3)铅蓄电池是常用的化学电源,其电极材料分别是Pb和 ,电解液为硫酸。
,电解液为硫酸。
①铅蓄电池属于_______ (填“一次”或“二次”)电池,该蓄电池放电时,电解质溶液中阴离子移向_______ (填“正”或“负”)极。正极反应方程式为_______
②充电时,以氢氧燃料电池(30%KOH溶液为电解质溶液)为电源,则该氢氧燃料电池负极上的电极反应式为_______ 。
③乙醇(C2H5OH)燃料电池(Pt为电极),以KOH为电解质溶液,写出负极电极反应式_______ ,当转移电子1.2mol时,消耗氧气标况下体积为_______ 。
(1)下列变化中,属于吸热反应的是
①氧化钙与水反应;②石灰石在高温下的分解反应;③酸碱中和反应;④二氧化碳通过炽热的炭发生的反应;⑤食物因氧化而腐败发生的反应;⑥
 与
与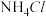 的反应;⑦干冰汽化。
的反应;⑦干冰汽化。(2)为探究固体M溶于水的热效应,选择如图所示装置进行实验(反应在甲中进行)。观察到烧杯里产生气泡,则M溶于水

(3)铅蓄电池是常用的化学电源,其电极材料分别是Pb和
 ,电解液为硫酸。
,电解液为硫酸。①铅蓄电池属于
②充电时,以氢氧燃料电池(30%KOH溶液为电解质溶液)为电源,则该氢氧燃料电池负极上的电极反应式为
③乙醇(C2H5OH)燃料电池(Pt为电极),以KOH为电解质溶液,写出负极电极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】观察图A、B,回答下列问题:
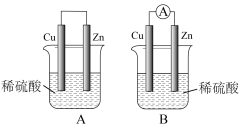
(1)把一块纯净的锌片插入装有稀硫酸的烧杯里,可观察到锌片上有气泡产生,再平行插入一块铜片,可观察到铜片_______ (填“有”或“没有”)气泡产生。再用导线把锌片和铜片连接起来(见图A),组成一个原电池,正极的电极反应式为______ 。
(2)如果烧杯中最初装入的是2mol·L-1500mL的稀硫酸,构成铜锌原电池(见图B,假设产生的气体没有损失,锌失去的电子完全沿导线流入铜电极),当在标准状况下收集到11.2L的氢气时,烧杯内溶液中溶质的物质的量浓度分别为(请指明溶质,溶液体积变化忽略不计)______ 、________ 。
(3)CH3OH燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。其中负极反应式为CH3OH+8OH--6e-=== +6H2O。则下列说法正确的是
+6H2O。则下列说法正确的是______ (填序号)。
①电池放电时通入空气的电极为负极
②电池放电时,电解质溶液的碱性逐渐减弱
③电池放电时每消耗6.4gCH3OH转移1.2mol电子

(1)把一块纯净的锌片插入装有稀硫酸的烧杯里,可观察到锌片上有气泡产生,再平行插入一块铜片,可观察到铜片
(2)如果烧杯中最初装入的是2mol·L-1500mL的稀硫酸,构成铜锌原电池(见图B,假设产生的气体没有损失,锌失去的电子完全沿导线流入铜电极),当在标准状况下收集到11.2L的氢气时,烧杯内溶液中溶质的物质的量浓度分别为(请指明溶质,溶液体积变化忽略不计)
(3)CH3OH燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。其中负极反应式为CH3OH+8OH--6e-===
 +6H2O。则下列说法正确的是
+6H2O。则下列说法正确的是①电池放电时通入空气的电极为负极
②电池放电时,电解质溶液的碱性逐渐减弱
③电池放电时每消耗6.4gCH3OH转移1.2mol电子
您最近一年使用:0次



