微型纽扣电池在现代生活中应用广泛。有一种银锌电池,其电极分别是 和Zn,电解质溶液为KOH溶液,总反应式为
和Zn,电解质溶液为KOH溶液,总反应式为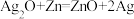 。回答下列问题:
。回答下列问题:
(1)Zn是_________ 极,发生_________ 反应,该电池的正极反应式为___________________________ 。
(2)电池内部电流方向是从_________ (填“ ”或“Zn”,下同)极流向
”或“Zn”,下同)极流向_________ 极,当外电路中有1mol  通过时,负极消耗的物质的质量是
通过时,负极消耗的物质的质量是_________ g。
(3)在使用过程中,电解质溶液中KOH的物质的量_________ (填“增大”“减小”或“不变”)。
 和Zn,电解质溶液为KOH溶液,总反应式为
和Zn,电解质溶液为KOH溶液,总反应式为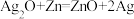 。回答下列问题:
。回答下列问题:(1)Zn是
(2)电池内部电流方向是从
 ”或“Zn”,下同)极流向
”或“Zn”,下同)极流向 通过时,负极消耗的物质的质量是
通过时,负极消耗的物质的质量是(3)在使用过程中,电解质溶液中KOH的物质的量
更新时间:2020-12-30 15:55:32
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
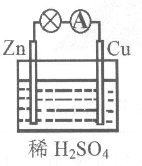
【推荐1】某原电池装置如图所示。
(1)负极的电极反应式是________ ,该反应属于_______ (填“氧化”或“还原”)反应。
(2)电子由________ (填“锌片”或“铜片”)沿导线流出。
(3)当铜表面析出0.224 L氢气(标准状况)时,导线中通过了________ mol电子。
(1)负极的电极反应式是
(2)电子由
(3)当铜表面析出0.224 L氢气(标准状况)时,导线中通过了
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】如图所示,某同学设计了一个燃料电池并探究氯碱工业原理的相关问题,其中乙装置中X为阳离子交换膜。请按要求回答相关问题:
(1)石墨电极(C)作_______ 极,甲中甲烷燃料电池的负极反应式为_______ 。
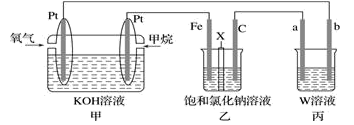
(2)若消耗 (标况)氧气,则乙装置中铁电极上生成的气体体积(标况)为
(标况)氧气,则乙装置中铁电极上生成的气体体积(标况)为_______ L。乙池中总反应的离子方程式_______ 。
(3)若丙中以稀 为电解质溶液,电极材料b为铝,则能使铝表面生成一层致密的氧化膜,该电极反应式为
为电解质溶液,电极材料b为铝,则能使铝表面生成一层致密的氧化膜,该电极反应式为_______ 。
(1)石墨电极(C)作

(2)若消耗
 (标况)氧气,则乙装置中铁电极上生成的气体体积(标况)为
(标况)氧气,则乙装置中铁电极上生成的气体体积(标况)为(3)若丙中以稀
 为电解质溶液,电极材料b为铝,则能使铝表面生成一层致密的氧化膜,该电极反应式为
为电解质溶液,电极材料b为铝,则能使铝表面生成一层致密的氧化膜,该电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】原电池电源在生活、生产中的应用非常广泛,根据题意回答下列问题。
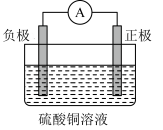
(1)某兴趣小组设计如图装置用锌、铜作电极材料,硫酸铜溶液为电解质溶液的进行原电池实验。负极材料是_______ (填“锌”或“铜”);溶液中硫酸根向_______ (填“正极”或“负极”),当正极质量增加12.8g时,转移了_______ mol电子。
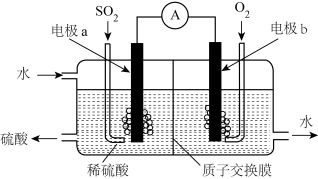
(2)如图所示,运用原电池原理可将SO2转化成硫酸。其中质子交换膜将该原电池分隔成氧化反应室和还原反应室,能阻止气体通过而允许H+通过。则电极a是该原电池的_______ 极(填“正”或“负”),b电极反应式为_______ ,生产过程中H+向_______ (填“a”或“b”)电极区域运动。
(3)铅酸蓄电池是一种典型的可充电电池,其放电时的电池总反应为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。放电时_______ (化学式)被还原,负极的电极反应式为_______ ,正极质量_______ (填“增重”或“减轻”“不变”)。
(4)燃料电池应用前景更加广泛,常见的是燃料主要有氢气、可燃有机物等,则燃料在电池_______ (填“正极”或“负极”)通入。在碱性溶液燃料电池中氧气参与反应的电极反应式为_______ ;若用C2H6为燃料时酸性电解质中负极反应式为_______ 。
(1)某兴趣小组设计如图装置用锌、铜作电极材料,硫酸铜溶液为电解质溶液的进行原电池实验。负极材料是

(2)如图所示,运用原电池原理可将SO2转化成硫酸。其中质子交换膜将该原电池分隔成氧化反应室和还原反应室,能阻止气体通过而允许H+通过。则电极a是该原电池的

(3)铅酸蓄电池是一种典型的可充电电池,其放电时的电池总反应为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。放电时
(4)燃料电池应用前景更加广泛,常见的是燃料主要有氢气、可燃有机物等,则燃料在电池
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)燃料电池是一种高效、环境友好的发电装置。氢氧燃料电池已用于航天飞机。以氢氧化钾溶液为电解质溶液的这种电池的负极反应式为________ ,这种电池在放电使用一段时间后,电解质溶液中的c(OH-)将____ (填“增大”“减小”或“不变”)。
(2)如图是银锌原电池装置的示意图,以硫酸铜为电解质溶液。回答下列问题:
锌为____ 极,该电极上发生_______ 反应(“氧化”或“还原”),电极反应式为___________ ,该原电池的总反应离子方程式为_______ 。
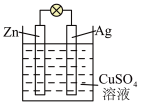
(2)如图是银锌原电池装置的示意图,以硫酸铜为电解质溶液。回答下列问题:
锌为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】完成下列问题
(1)绿色电源“直接二甲醚( )燃料电池”的工作原理如图所示:
)燃料电池”的工作原理如图所示:
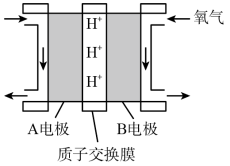
 的移动方向为由
的移动方向为由___________ (填“A”或“B”,下同)电极到___________ 电极。写出A电极的电极反应式: ___________ 。
(2) 和
和 是主要大气污染物,利用下图装置可同时吸收
是主要大气污染物,利用下图装置可同时吸收 和NO。
和NO。
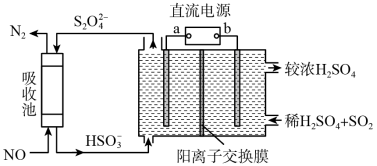
①a是直流电源的___________ 极。
②已知电解池的阴极室中溶液的pH在4~7之间,阴极的电极反应为___________ 。
③用离子方程式表示吸收NO的原理___________ 。
(1)绿色电源“直接二甲醚(
 )燃料电池”的工作原理如图所示:
)燃料电池”的工作原理如图所示:
 的移动方向为由
的移动方向为由(2)
 和
和 是主要大气污染物,利用下图装置可同时吸收
是主要大气污染物,利用下图装置可同时吸收 和NO。
和NO。
①a是直流电源的
②已知电解池的阴极室中溶液的pH在4~7之间,阴极的电极反应为
③用离子方程式表示吸收NO的原理
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】分别按下图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中A为电流表。请回答下列问题:
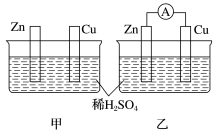
(1)以下叙述中,正确的是_______ (填字母)。
A.甲中锌片是负极,乙中铜片是正极
B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液氢离子浓度均减小
D.产生气泡的速度甲中比乙中慢
E.乙的外电路中电流方向
F.乙溶液中 向铜片方向移动
向铜片方向移动
(2)变化过程中能量转化的主要形式:甲为_______ ;乙为_______ 。
(3)在乙实验中,某同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是_______ 。
(4)在乙实验中,如果把硫酸换成硫酸铜溶液,请写出铜电极的电极反应方程式及总反应离子方程式:铜电极:_______ ,总反应:_______ 。当电路中转移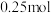 电子时,消耗负极材料的质量为
电子时,消耗负极材料的质量为_______ g。

(1)以下叙述中,正确的是
A.甲中锌片是负极,乙中铜片是正极
B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液氢离子浓度均减小
D.产生气泡的速度甲中比乙中慢
E.乙的外电路中电流方向

F.乙溶液中
 向铜片方向移动
向铜片方向移动(2)变化过程中能量转化的主要形式:甲为
(3)在乙实验中,某同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是
(4)在乙实验中,如果把硫酸换成硫酸铜溶液,请写出铜电极的电极反应方程式及总反应离子方程式:铜电极:
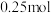 电子时,消耗负极材料的质量为
电子时,消耗负极材料的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】某原电池如图所示,电池总反应为2Ag+Cl2=2AgCl。
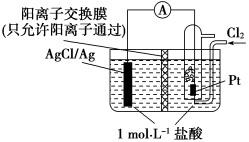
(1)放电时,交换膜____ (“左侧”或“右侧”)溶液中有大量白色沉淀生成;若用氯化钠溶液代替盐酸,则电池总反应____ (“会”或“不会”)随之改变。
(2)当电路中转移0.01mole-时,交换膜左侧溶液中约减少____ mol离子。

(1)放电时,交换膜
(2)当电路中转移0.01mole-时,交换膜左侧溶液中约减少
您最近一年使用:0次
【推荐2】回答下列问题:
(1)高铁电池是一种能量密度大的新型二次电源,被广泛应用于电动公交车。我国在高铁电池研究方面居于世界领先水平。如图是某高铁电池与某常用的高能碱性电池的放电曲线对比示意图。请回答:
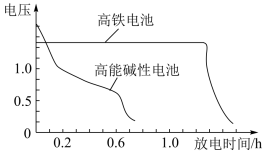
①高铁电池的优点是:_____ 。
②某高铁电池可发生如下反应:2K2FeO4+3Zn+8H2O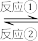 3Zn(OH)2+2Fe(OH)3+4KOH,则放电时的正极反应式:
3Zn(OH)2+2Fe(OH)3+4KOH,则放电时的正极反应式:_____ 。
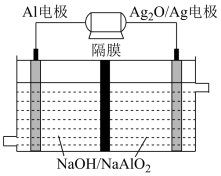
(2)我国自行设计并使用的蛟龙号载人深海潜水器使用了性能优越的Al-Ag2O电池。其原理如图所示。该电池反应的化学方程式为:_____ 。
(3)铅蓄电池是常用的化学电源,电极材料分别是Pb和PbO2,电解液为硫酸。根据上述情况判断:
①该蓄电池充电时,Pb极应连接电源的_____ (填“正极”或“负极”),正极附近溶液的pH_____ (填“增大”、“减小”或“不变”)。
②实验室用铅蓄电池作电源电解饱和食盐水制取氯气,今若制得0.050molCl2,这时电池内消耗的H2SO4的物质的量至少是_____ 。
(1)高铁电池是一种能量密度大的新型二次电源,被广泛应用于电动公交车。我国在高铁电池研究方面居于世界领先水平。如图是某高铁电池与某常用的高能碱性电池的放电曲线对比示意图。请回答:

①高铁电池的优点是:
②某高铁电池可发生如下反应:2K2FeO4+3Zn+8H2O
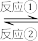 3Zn(OH)2+2Fe(OH)3+4KOH,则放电时的正极反应式:
3Zn(OH)2+2Fe(OH)3+4KOH,则放电时的正极反应式:(2)我国自行设计并使用的蛟龙号载人深海潜水器使用了性能优越的Al-Ag2O电池。其原理如图所示。该电池反应的化学方程式为:

(3)铅蓄电池是常用的化学电源,电极材料分别是Pb和PbO2,电解液为硫酸。根据上述情况判断:
①该蓄电池充电时,Pb极应连接电源的
②实验室用铅蓄电池作电源电解饱和食盐水制取氯气,今若制得0.050molCl2,这时电池内消耗的H2SO4的物质的量至少是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】化学电源在日常生活中有着广泛的应用。
(1)一种以石墨为电极、稀硫酸为电解质溶液处理废气SO2的电池,工作原理如下图所示。___________ 流向电极___________ 。
②理论上每消耗1 molO2,可产生H2SO4质量为___________ g。
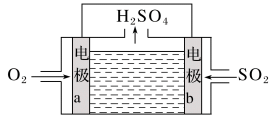
(2)如图所示是甲烷燃料电池的原理示意图:___________ (填“a”或“b”)电极,该电极的反应式为___________ 。
②电池工作一段时间后,电解质溶液的pH___________ (填“增大”、“减小”或“不变”)。
(3)研究人员发明了一种“水”电池,这种电池能利用淡水与海水之间含盐量的差别进行发电,电池的总反应方程式为5MnO2+2Ag+2NaCl=Na2Mn5O10 +2AgCl。
①该电池负极的电极反应式为___________ 。
②电池中,Na+不断移动到“水”电池的___________ 极(填“正”或“负”)。
③外电路每通过4mol电子时,生成Na2Mn5O10的物质的量是___________ mol。
(1)一种以石墨为电极、稀硫酸为电解质溶液处理废气SO2的电池,工作原理如下图所示。
②理论上每消耗1 molO2,可产生H2SO4质量为
(2)如图所示是甲烷燃料电池的原理示意图:
②电池工作一段时间后,电解质溶液的pH
(3)研究人员发明了一种“水”电池,这种电池能利用淡水与海水之间含盐量的差别进行发电,电池的总反应方程式为5MnO2+2Ag+2NaCl=Na2Mn5O10 +2AgCl。
①该电池负极的电极反应式为
②电池中,Na+不断移动到“水”电池的
③外电路每通过4mol电子时,生成Na2Mn5O10的物质的量是
您最近一年使用:0次



