根据所学知识,回答下列问题:
(1)下列变化中,属于吸热反应的是_______ 。(填标号)
①氧化钙与水反应;②石灰石在高温下的分解反应;③酸碱中和反应;④二氧化碳通过炽热的炭发生的反应;⑤食物因氧化而腐败发生的反应;⑥ 与
与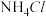 的反应;⑦干冰汽化。
的反应;⑦干冰汽化。
(2)为探究固体M溶于水的热效应,选择如图所示装置进行实验(反应在甲中进行)。观察到烧杯里产生气泡,则M溶于水_______ (填“一定”或“可能”)是放热反应。

(3)铅蓄电池是常用的化学电源,其电极材料分别是Pb和 ,电解液为硫酸。
,电解液为硫酸。
①铅蓄电池属于_______ (填“一次”或“二次”)电池,该蓄电池放电时,电解质溶液中阴离子移向_______ (填“正”或“负”)极。正极反应方程式为_______
②充电时,以氢氧燃料电池(30%KOH溶液为电解质溶液)为电源,则该氢氧燃料电池负极上的电极反应式为_______ 。
③乙醇(C2H5OH)燃料电池(Pt为电极),以KOH为电解质溶液,写出负极电极反应式_______ ,当转移电子1.2mol时,消耗氧气标况下体积为_______ 。
(1)下列变化中,属于吸热反应的是
①氧化钙与水反应;②石灰石在高温下的分解反应;③酸碱中和反应;④二氧化碳通过炽热的炭发生的反应;⑤食物因氧化而腐败发生的反应;⑥
 与
与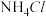 的反应;⑦干冰汽化。
的反应;⑦干冰汽化。(2)为探究固体M溶于水的热效应,选择如图所示装置进行实验(反应在甲中进行)。观察到烧杯里产生气泡,则M溶于水

(3)铅蓄电池是常用的化学电源,其电极材料分别是Pb和
 ,电解液为硫酸。
,电解液为硫酸。①铅蓄电池属于
②充电时,以氢氧燃料电池(30%KOH溶液为电解质溶液)为电源,则该氢氧燃料电池负极上的电极反应式为
③乙醇(C2H5OH)燃料电池(Pt为电极),以KOH为电解质溶液,写出负极电极反应式
更新时间:2023-07-30 09:18:08
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率,请回答下列问题。

(1)某实验小组同学进行如下实验,以检验化学反应中的能量变化,实验中发现,反应后①中的温度升高;②中的温度降低。由此判断铝条与盐酸的反应是_______ 热反应,Ba(OH)2·8H2O与NH4Cl的反应是_______ 热反应。反应过程_______ (填“①”或“②”)的能量变化可用图2表示。
(2)氢气在O2中燃烧为放热反应,从化学反应的本质角度来看,氢气的燃烧是由于断裂反应物中的化学键吸收的总能量_______ (填“大于”、“小于”或“等于”)形成产物的化学键放出的总能量。已知破坏1mol H—H键、1mol O=O键、1mol H—O键时分别需要吸收a kJ、b kJ、c kJ的能量。则2mol H2(g)和1mol O2(g)转化为2mol H2O(g)时放出的热量为_______ 。
(3)用CH4和O2组合形成的质子交换膜燃料电池的结构示意图如下:
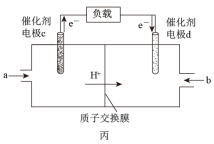
①则d电极是_______ (填“正极”或“负极”),c电极的反应方程式为_______ 。
②若线路中转移2mol电子,则上述燃料电池,消耗的O2在标准状况下的体积为_______ L。

(1)某实验小组同学进行如下实验,以检验化学反应中的能量变化,实验中发现,反应后①中的温度升高;②中的温度降低。由此判断铝条与盐酸的反应是
(2)氢气在O2中燃烧为放热反应,从化学反应的本质角度来看,氢气的燃烧是由于断裂反应物中的化学键吸收的总能量
(3)用CH4和O2组合形成的质子交换膜燃料电池的结构示意图如下:

①则d电极是
②若线路中转移2mol电子,则上述燃料电池,消耗的O2在标准状况下的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知下列热化学方程式:
①H2(g)+1/2O2(g)===H2O(l) ΔH=-285.8 kJ·mol-1
②H2(g)+1/2O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1
③C(s)+1/2O2(g)===CO(g) ΔH=-110.5 kJ·mol-1
④C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
回答下列各问题:
(1)上述反应中属于放热反应的是_____ 。
(2)燃烧10 g H2生成液态水,放出的热量为__ 。
(3)CO的燃烧热为________________ ;其热化学方程式为______________ 。
①H2(g)+1/2O2(g)===H2O(l) ΔH=-285.8 kJ·mol-1
②H2(g)+1/2O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1
③C(s)+1/2O2(g)===CO(g) ΔH=-110.5 kJ·mol-1
④C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
回答下列各问题:
(1)上述反应中属于放热反应的是
(2)燃烧10 g H2生成液态水,放出的热量为
(3)CO的燃烧热为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】乙醇(C2H5OH)是重要的工业原料,它的应用和制备方法是科研人员研究的热点,其在生产生活上用途很多。回答下列问题:
(1)乙醇汽油代替铅基汽油解决了铅基汽油燃烧对环境的污染。
①C2H5OH燃烧时将____ 能转化为____ 能。
②C2H5OH完全燃烧的化学方程式为____ ,该反应过程中能量变化的图象符合____ (填“图a”或“图b”)。
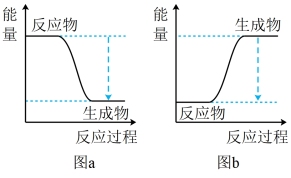
(2)某碱性C2H5OH燃料电池工作原理如图c,总化学方程式C2H5OH+3O2+4KOH=2K2CO3+5H2O。
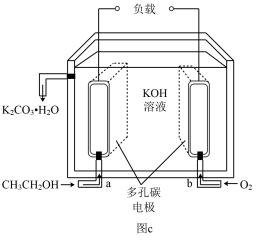
①该电池工作时,电子____ (填“由a极经外电路流向b极”或“由b极经外电路流向a极”)。
②负极电极反应式为____ 。
(3)工业上通过CO与H2反应制取C2H5OH(2CO+4H2 C2H5OH+H2O),温度为T时CO与C2H5OH的物质的量的浓度与时间的关系如图d(生成物、反应物均为气体)。
C2H5OH+H2O),温度为T时CO与C2H5OH的物质的量的浓度与时间的关系如图d(生成物、反应物均为气体)。
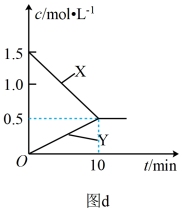
①X为____ (填化学式)。
②反应前10min,CO的转化率=_____ %(精确到小数点后一位)。
(1)乙醇汽油代替铅基汽油解决了铅基汽油燃烧对环境的污染。
①C2H5OH燃烧时将
②C2H5OH完全燃烧的化学方程式为

(2)某碱性C2H5OH燃料电池工作原理如图c,总化学方程式C2H5OH+3O2+4KOH=2K2CO3+5H2O。

①该电池工作时,电子
②负极电极反应式为
(3)工业上通过CO与H2反应制取C2H5OH(2CO+4H2
 C2H5OH+H2O),温度为T时CO与C2H5OH的物质的量的浓度与时间的关系如图d(生成物、反应物均为气体)。
C2H5OH+H2O),温度为T时CO与C2H5OH的物质的量的浓度与时间的关系如图d(生成物、反应物均为气体)。
①X为
②反应前10min,CO的转化率=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】KMnO4是实验室中常用的一种试剂。回答下列问题:
(1)K+的结构示意图为___ 。
(2)在酸性高锰酸钾溶液中滴加过量的草酸(H2C2O4,弱酸)溶液,振荡,溶液紫色变无色。发生的化学反应为2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O,若将该反应设计成原电池,则负极反应式为___ 。
(3)在10mL0.1mol·L-1KMnO4溶液(含稀硫酸)中加入15mL0.5mol.L-1草酸溶液,收集到的CO2的量与时间的关系如图所示。
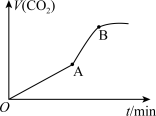
AB段反应速率增大的原因可能是___ (填字母)。
a.该反应是放热反应
b.反应物浓度增大
c.K2SO4起催化作用
d.MnSO4起催化作用
(4)为了探究外界条件对化学反应速率的影响,设计如下方案:
①V=___ 。
②该实验方案不能探究对反应速率有影响的因素是___ 。
A.浓度 B.酸度 C.温度 D.催化剂
③若测得结果:t4<t1,则实验结论是___ 。
(1)K+的结构示意图为
(2)在酸性高锰酸钾溶液中滴加过量的草酸(H2C2O4,弱酸)溶液,振荡,溶液紫色变无色。发生的化学反应为2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O,若将该反应设计成原电池,则负极反应式为
(3)在10mL0.1mol·L-1KMnO4溶液(含稀硫酸)中加入15mL0.5mol.L-1草酸溶液,收集到的CO2的量与时间的关系如图所示。

AB段反应速率增大的原因可能是
a.该反应是放热反应
b.反应物浓度增大
c.K2SO4起催化作用
d.MnSO4起催化作用
(4)为了探究外界条件对化学反应速率的影响,设计如下方案:
实验 | 0.1mol·L-1KMnO4/mL | 0.5mol·L-1H2C2O4/mL | 0.1mol·L-1H2SO4/mL | 水浴 温度/℃ | 蒸馏水 /mL | 褪色时间 /min |
| I | 5.0 | 15.0 | 5.0 | 35 | 0 | t1 |
| II | 5.0 | 10.0 | 5.0 | 35 | V | t2 |
| III | 5.0 | 15.0 | 3.0 | 35 | 2.0 | t3 |
| IV | 5.0 | 15.0 | 5.0 | 45 | 0 | t4 |
②该实验方案不能探究对反应速率有影响的因素是
A.浓度 B.酸度 C.温度 D.催化剂
③若测得结果:t4<t1,则实验结论是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】一定温度下,在体积为0.5L的恒容密闭容器中, 和
和 之间发生反应:
之间发生反应: (无色),反应过程中各物质的物质的量与时间的关系如图所示。回答下列问题:
(无色),反应过程中各物质的物质的量与时间的关系如图所示。回答下列问题:
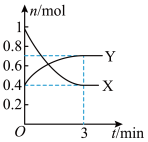
(1)曲线___________ (填“X”或“Y”)表示 的物质的量随时间的变化曲线。
的物质的量随时间的变化曲线。
(2)在 内,用
内,用 表示的反应速率为
表示的反应速率为___________ 。
(3)该反应达到平衡状态的标志是___________ (填字母)。
A.Y的体积分数在混合气体中保持不变
B.X、Y的反应速率比为
C.容器内气体压强保持不变
D.容器内气体的总质量保持不变
E.生成 的同时消耗
的同时消耗
F.容器内气体的颜色保持不变
G.容器内气体的密度保持不变
(4)汽车排放的尾气中含有的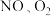 是大气污染的主要来源,通过
是大气污染的主要来源,通过 传感器可监测汽车尾气中
传感器可监测汽车尾气中 的含量,其工作原理如图所示。
的含量,其工作原理如图所示。
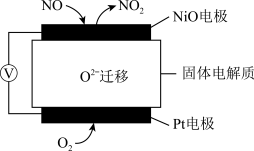
①NiO电极上发生的是___________ (填“氧化”或“还原”)反应。
②外电路中,电子流动方向是从___________ 电极流向___________ 电极。(填“NiO”或“Pt”)
③Pt电极上的电极反应式为___________ 。
 和
和 之间发生反应:
之间发生反应: (无色),反应过程中各物质的物质的量与时间的关系如图所示。回答下列问题:
(无色),反应过程中各物质的物质的量与时间的关系如图所示。回答下列问题:
(1)曲线
 的物质的量随时间的变化曲线。
的物质的量随时间的变化曲线。(2)在
 内,用
内,用 表示的反应速率为
表示的反应速率为(3)该反应达到平衡状态的标志是
A.Y的体积分数在混合气体中保持不变
B.X、Y的反应速率比为

C.容器内气体压强保持不变
D.容器内气体的总质量保持不变
E.生成
 的同时消耗
的同时消耗
F.容器内气体的颜色保持不变
G.容器内气体的密度保持不变
(4)汽车排放的尾气中含有的
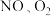 是大气污染的主要来源,通过
是大气污染的主要来源,通过 传感器可监测汽车尾气中
传感器可监测汽车尾气中 的含量,其工作原理如图所示。
的含量,其工作原理如图所示。
①NiO电极上发生的是
②外电路中,电子流动方向是从
③Pt电极上的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】对下图中两极加以必要的连接并填空:
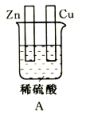
(1)在图A中,使铜片上产生氢气。
①若加以导线连接,则锌片发生____________ (填“氧化”或“还原”);铜片上的电极反应式:____________________________ 。
②若外加电源,则铜片作为该装置的______ 极,连接电源的_______ 极;锌片上发生的电极反应式为________________________ 。
(2)在图B中,使a极析出铜。
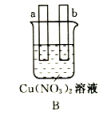
①若a、b电极均为石墨电极并加以必要的连接,则连接后的装置应为____________ (填“原电池”或“电解池”);该装置工作时,溶液中阴离子向________ 极作定向移动(填“a”或“b”); 经过一段时间后,停止反应并搅匀溶液,溶液的酸性__________ (填“增强”、“降低”或“不变”)。
②若a、b电极加以导线连接,且a极为铜电极,则b极可以为________ 电极(填序号)。
A.铂 B.铁 C.石墨 D.银 E.锌
该装置工作时,溶液中阴离子向________ 极作定向移动(填“a”或“b”)。

(1)在图A中,使铜片上产生氢气。
①若加以导线连接,则锌片发生
②若外加电源,则铜片作为该装置的
(2)在图B中,使a极析出铜。

①若a、b电极均为石墨电极并加以必要的连接,则连接后的装置应为
②若a、b电极加以导线连接,且a极为铜电极,则b极可以为
A.铂 B.铁 C.石墨 D.银 E.锌
该装置工作时,溶液中阴离子向
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】根据题中提供的信息,请回答下列问题:
(1)学习原电池原理后,小江同学根据反应 设计了一个原电池并得到老师的肯定,则小江同学选用的负极材料是
设计了一个原电池并得到老师的肯定,则小江同学选用的负极材料是______ ,正极材料可能是______ (填一种)。
(2)小河同学设计了如图所示的原电池,利用不同的电解质溶液进行实验。______ 。
②当以NaOH溶液作为电解质溶液时,电流表指针也发生了偏转,若负极失去1mol电子,理论上负极的质量变化为______ g。
(3)燃料电池是一种高效化学电池,以稀硫酸为电解质溶液的氢氧燃料电池的工作原理如图所示,a和b都是Pt电极(惰性电极)。______ 。
②该电池工作时,电解质溶液中 的移动方向是
的移动方向是______ 。(填“a向b”或“b向a”,下同),外电路中电子的流动方向是______ 。
③若将a极通入的气体换为 ,同时将电解质溶液换为NaOH溶液,则a极的电极反应式为
,同时将电解质溶液换为NaOH溶液,则a极的电极反应式为______ 。当a极有1mol 发生反应时,理论上b极参加反应的氧气在标准状况下的体积为
发生反应时,理论上b极参加反应的氧气在标准状况下的体积为______ L。
(4)小海同学在做氢气的制备实验时,用锌粒和稀硫酸为原料,结果发现反应速率较慢。其他同学给出以下建议,其中能加快制备 的反应速率的有______(填字母)。
的反应速率的有______(填字母)。
(1)学习原电池原理后,小江同学根据反应
 设计了一个原电池并得到老师的肯定,则小江同学选用的负极材料是
设计了一个原电池并得到老师的肯定,则小江同学选用的负极材料是(2)小河同学设计了如图所示的原电池,利用不同的电解质溶液进行实验。

②当以NaOH溶液作为电解质溶液时,电流表指针也发生了偏转,若负极失去1mol电子,理论上负极的质量变化为
(3)燃料电池是一种高效化学电池,以稀硫酸为电解质溶液的氢氧燃料电池的工作原理如图所示,a和b都是Pt电极(惰性电极)。

②该电池工作时,电解质溶液中
 的移动方向是
的移动方向是③若将a极通入的气体换为
 ,同时将电解质溶液换为NaOH溶液,则a极的电极反应式为
,同时将电解质溶液换为NaOH溶液,则a极的电极反应式为 发生反应时,理论上b极参加反应的氧气在标准状况下的体积为
发生反应时,理论上b极参加反应的氧气在标准状况下的体积为(4)小海同学在做氢气的制备实验时,用锌粒和稀硫酸为原料,结果发现反应速率较慢。其他同学给出以下建议,其中能加快制备
 的反应速率的有______(填字母)。
的反应速率的有______(填字母)。| A.将稀硫酸换成质量分数为98%的浓硫酸 | B.向反应液中滴入几滴硫酸铜溶液 |
| C.改换合适的装置并适当加热 | D.将锌粒换成质量相等的锌粉 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图所示,A为新型高效的甲烷燃料电池,采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液。B为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,C、D为电解槽,其电极材料、电解质溶液见图。
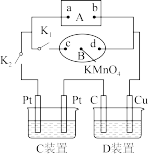
(1)甲烷燃料电池正极、负极的电极反应式分别为____ ;____ 。
(2)关闭K1,打开K2,通电后,B的KMnO4紫红色液滴向d端移动,则电源a端为___ 极,通电一段时间后,观察到滤纸c端出现的现象是_____ 。
(3)已知C装置中溶液为AgNO3溶液,D装置的溶液为Cu(NO3)2溶液,打开K1,关闭K2,通电一段时间后,D装置中Cu极的电极反应式为____ ,C装置中总反应的离子方程式为___ 。
(4)若C装置中AgNO3溶液足量,且溶液体积为1L,电解一段时间后,C装置中产生O2的体积为0.56 L(标准状况下),则电路通过的电子的物质的量为___ ,溶液的pH为___ (忽略溶液体积变化)。

(1)甲烷燃料电池正极、负极的电极反应式分别为
(2)关闭K1,打开K2,通电后,B的KMnO4紫红色液滴向d端移动,则电源a端为
(3)已知C装置中溶液为AgNO3溶液,D装置的溶液为Cu(NO3)2溶液,打开K1,关闭K2,通电一段时间后,D装置中Cu极的电极反应式为
(4)若C装置中AgNO3溶液足量,且溶液体积为1L,电解一段时间后,C装置中产生O2的体积为0.56 L(标准状况下),则电路通过的电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】二氧化硫—空气质子交换膜燃料电池将化学能转变成电能的同时,实现了制硫酸、发电、环保三位一体的结合,降低了成本提高了效益,其原理如图所示。请回答下列问题:
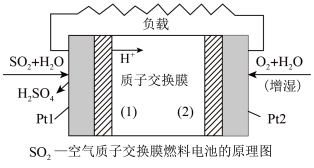
(1)Pt1电极附近发生的反应为______________________________
(2)Pt2电极附近发生的反应为______________________________
(3)该电池放电时电子从______ 电极经过外电路流到_____ 电极(填“Ptl”、“Pt2”)。
(4)相同条件下,放电过程中消耗的 和
和 的体积比为
的体积比为_____________ 。

(1)Pt1电极附近发生的反应为
(2)Pt2电极附近发生的反应为
(3)该电池放电时电子从
(4)相同条件下,放电过程中消耗的
 和
和 的体积比为
的体积比为
您最近一年使用:0次



