“神舟十五号”载人飞船成功发射,创下了我国在超低温天气成功发射载人飞船的新纪录。肼(N2H4)是火箭常用高能燃料,可与O2发生反应:
N2H4(g)+O2(g)=N2(g)+2H2O(g)。
(1)已知上述反应的能量变化如图所示:___________ (填“吸收”或“放出”)能量。
②N2H4(g)完全燃烧生成1molH2O(g)的反应中放出___________ 能量。
(2)反应N2H4(g)+O2(g)=N2(g)+2H2O(l)可设计为燃料电池,电池中用惰性电极铂(Pt),装置如图所示:___________ (填化学式),该装置工作时, 移向电极
移向电极 ___________ (填“Pt1”或“Pt2”)。
②电极Pt1为___________ (填“负极”或“正极”),发生的电极反应为 ___________ 。
N2H4(g)+O2(g)=N2(g)+2H2O(g)。
(1)已知上述反应的能量变化如图所示:
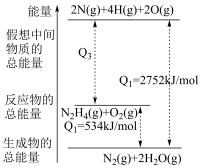
②N2H4(g)完全燃烧生成1molH2O(g)的反应中放出
(2)反应N2H4(g)+O2(g)=N2(g)+2H2O(l)可设计为燃料电池,电池中用惰性电极铂(Pt),装置如图所示:
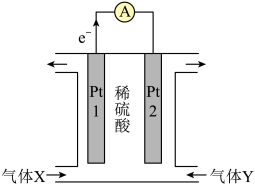
 移向电极
移向电极 ②电极Pt1为
更新时间:2024-05-22 16:21:32
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】发射卫星可用肼(N2H4)为燃料。
(1)已知将16g气态肼在O2中燃烧,生成氮气和水蒸气,放出250kJ热量,则该反应的热化学方程式为___________ ,请在下图甲中画出气态肼与氧气反应的“反应过程—能量”示意图,在图中标注出该反应的活化能B和反应热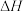 。
。___________

(2)已知氮气与氧气反应过程的能量变化如图乙所示,则该反应的热化学方程式为___________ 。

(3)由上述两个反应可推出:气态肼和二氧化氮气体反应生成氮气和水蒸气的热化学方程式为___________ 。
(4)从化学键的断裂和形成角度分析(2)中的反应表现为吸热反应的原因:___________ 。
(1)已知将16g气态肼在O2中燃烧,生成氮气和水蒸气,放出250kJ热量,则该反应的热化学方程式为
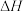 。
。
(2)已知氮气与氧气反应过程的能量变化如图乙所示,则该反应的热化学方程式为

(3)由上述两个反应可推出:气态肼和二氧化氮气体反应生成氮气和水蒸气的热化学方程式为
(4)从化学键的断裂和形成角度分析(2)中的反应表现为吸热反应的原因:
您最近一年使用:0次
【推荐2】在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示。请认真观察图象,然后回答问题:
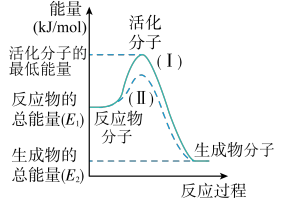
(1)图中所示反应是______ (填“吸热”或“放热”)反应,该反应______ (填“需要”或“不需要”)加热,该反应的ΔH=______ (用含E1、E2的代数式表示 );
);
(2)对于同一反应,图中虚线(Ⅱ)与实线(Ⅰ)相比,活化能大大降低,活化分子的百分数增多,反应速率加快,你认为最可能的原因是___________ 。
(3)已知红磷比白磷稳定,则反应:
P4(白磷,s)+5O2(g) = 2P2O5(s) ΔH1;
4P(红磷,s)+5O2(g) = 2P2O5(s) ΔH2;
ΔH1和ΔH2的关系是ΔH1________ ΔH2(填“>”“<”或“=”)。
(4)在298 K、101 kPa时,已知:
2H2O(g)= O2(g)+2H2(g) ΔH1
Cl2(g)+H2(g)=2HCl(g) ΔH2
2Cl2(g)+2H2O(g) = 4HCl(g)+O2(g) ΔH3
则ΔH3与ΔH1和ΔH2之间的关系正确的是________ 。
A.ΔH3=ΔH1+2ΔH2B.ΔH3=ΔH1+ΔH2
C.ΔH3=ΔH1-2ΔH2D.ΔH3=ΔH1-ΔH2
(5)已知H2(g)+Br2(l) = 2HBr(g) ΔH=-72 kJ·mol-1,蒸发1 mol Br2(l)需要吸收的能量为30 kJ,其他相关数据如下表:
则表中a=________ 。

(1)图中所示反应是
 );
);(2)对于同一反应,图中虚线(Ⅱ)与实线(Ⅰ)相比,活化能大大降低,活化分子的百分数增多,反应速率加快,你认为最可能的原因是
(3)已知红磷比白磷稳定,则反应:
P4(白磷,s)+5O2(g) = 2P2O5(s) ΔH1;
4P(红磷,s)+5O2(g) = 2P2O5(s) ΔH2;
ΔH1和ΔH2的关系是ΔH1
(4)在298 K、101 kPa时,已知:
2H2O(g)= O2(g)+2H2(g) ΔH1
Cl2(g)+H2(g)=2HCl(g) ΔH2
2Cl2(g)+2H2O(g) = 4HCl(g)+O2(g) ΔH3
则ΔH3与ΔH1和ΔH2之间的关系正确的是
A.ΔH3=ΔH1+2ΔH2B.ΔH3=ΔH1+ΔH2
C.ΔH3=ΔH1-2ΔH2D.ΔH3=ΔH1-ΔH2
(5)已知H2(g)+Br2(l) = 2HBr(g) ΔH=-72 kJ·mol-1,蒸发1 mol Br2(l)需要吸收的能量为30 kJ,其他相关数据如下表:
| 物质 | H2(g) | Br2(g) | HBr(g) |
| 1 mol分子中的化学键断 裂时需要吸收的能量(kJ) | 436 | 200 | a |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某些共价键的键能数据如下表(单位:kJ·mol-1):
(1)把1 mol Cl2分解为气态原子时,需要_______ (填 “吸收”或“放出”)_______ kJ能量。
(2)由表中所列化学键形成的单质分子中,最稳定的是_______ ,最不稳定的是_______ ;形成的化合物分子中最稳定的是_______ 。
(3)试通过键能数据估算下列反应的反应热:H2(g)+Cl2(g)=2HCl(g) ΔH=_______ 。
| 共价键 | H—H | Cl—Cl | Br—Br | H—Cl | H—I |
| 键能 | 436 | 243 | 193 | 432 | 298 |
| 共价键 | I—I | N≡N | H—O | H—N | |
| 键能 | 151 | 946 | 463 | 393 |
(2)由表中所列化学键形成的单质分子中,最稳定的是
(3)试通过键能数据估算下列反应的反应热:H2(g)+Cl2(g)=2HCl(g) ΔH=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】请仔细观察下列几种装置的构造示意图,完成下列问题:

(1)碱性锌锰电池比普通锌锰电池(干电池)性能好,放电电流大。结合图1图2,从影响反应速率的因素分析其原因是___________ 。
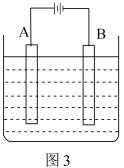
(2)①已知粗锌中含有的杂质有铝、铁和铜,图3若为电解精炼锌,则A极应接____ (填“粗锌”或“纯锌”),电解一段时间后,电解质溶液中含有的金属阳离子有________ ;
②图3若为铜上镀银装置,已知电镀前A、B电极质量相等,电镀完成后两电极质量差为6.48g时,则电路中通过的电子数为___________ 。
③若图3使用的电源为一种高效耐用的新型可充电电池,其放电反应为:3Zn + 2K2FeO4 + 8H2O = 3Zn(OH)2 +2Fe(OH)3 +4KOH写出该电池放电时正极电极方程式_________ ;
(3)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示(电极材料为石墨)。图中a极接电源的___________ (填“正”或“负”)极,SO 放电的电极反应式为
放电的电极反应式为___________ 。




(1)碱性锌锰电池比普通锌锰电池(干电池)性能好,放电电流大。结合图1图2,从影响反应速率的因素分析其原因是
(2)①已知粗锌中含有的杂质有铝、铁和铜,图3若为电解精炼锌,则A极应接
②图3若为铜上镀银装置,已知电镀前A、B电极质量相等,电镀完成后两电极质量差为6.48g时,则电路中通过的电子数为
③若图3使用的电源为一种高效耐用的新型可充电电池,其放电反应为:3Zn + 2K2FeO4 + 8H2O = 3Zn(OH)2 +2Fe(OH)3 +4KOH写出该电池放电时正极电极方程式
(3)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示(电极材料为石墨)。图中a极接电源的
 放电的电极反应式为
放电的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】探究原电池原理并应用原电池原理制作多种电池,对现实生活具有重要的意义。
(1)某化学兴趣小组为了探究铝电极在原电池中的作用时,设计了如下实验:
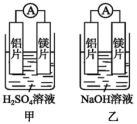
①甲、乙两装置工作时,电流计指针的偏转方向是否相同?_______ 。乙装置中负极的电极反应式是_______ 。
②根据上述实验结果分析,下列说法正确的是__________
a.构成原电池负极的金属总是比正极活泼
b.镁的金属活泼性不一定比铝的强
c.金属在原电池中作正极还是负极,既与金属活泼性有关,还与电解质溶液的成分有关
(2)铅酸蓄电池是常见的二次电池,放电时发生反应为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。该电池的负极材料为_______ ;该电池充电时,其能量转化形式为_______ 。
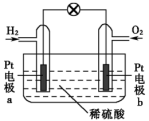
(3)氢氧燃料电池具有清洁、安全、高效的特点,其简易装置如图所示:铂电极b上的电极反应式为_______ ,室温下,若该电池消耗1molH2时可提供电能257.4kJ的能量,则该燃料电池的能量转化率为_______ 。(已知:室温下,1molH2完全燃烧生成液态水时,释放286.0kJ的能量。)
(1)某化学兴趣小组为了探究铝电极在原电池中的作用时,设计了如下实验:

①甲、乙两装置工作时,电流计指针的偏转方向是否相同?
②根据上述实验结果分析,下列说法正确的是
a.构成原电池负极的金属总是比正极活泼
b.镁的金属活泼性不一定比铝的强
c.金属在原电池中作正极还是负极,既与金属活泼性有关,还与电解质溶液的成分有关
(2)铅酸蓄电池是常见的二次电池,放电时发生反应为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。该电池的负极材料为
(3)氢氧燃料电池具有清洁、安全、高效的特点,其简易装置如图所示:铂电极b上的电极反应式为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】I.高铁酸盐在能源、环保等方面有着广泛的用途。高铁酸钾(K2FeO4)不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。下图是高铁电池的模拟实验装置:
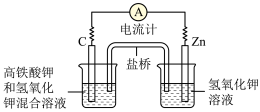
(1)该电池放电时正极的电极反应式为____ 。
(2)盐桥中盛有饱和KCl溶液,此盐桥中氯离子向_____ (填“左”或“右”)移动;若用阳离子交换膜代替盐桥,则钾离子向_____ (填“左”或“右”)移动。
(3)下图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有____ 。

II.电解制取KIO3
电解前,先将一定量的精制碘溶于过量氢氧化钾溶液,溶解时发生反应3I2+6KOH= 5KI+KIO3+3H2O,将该溶液加入阳极区,另将氢氧化钾溶液加入阴极区,电解槽用水冷却。电解时,阳极上发生反应的电极反应式为____ ;电解过程中阴极附近溶液pH____ (填“变大”“变小”或“不变”)。

(1)该电池放电时正极的电极反应式为
(2)盐桥中盛有饱和KCl溶液,此盐桥中氯离子向
(3)下图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有

II.电解制取KIO3
电解前,先将一定量的精制碘溶于过量氢氧化钾溶液,溶解时发生反应3I2+6KOH= 5KI+KIO3+3H2O,将该溶液加入阳极区,另将氢氧化钾溶液加入阴极区,电解槽用水冷却。电解时,阳极上发生反应的电极反应式为
您最近一年使用:0次



