研究有机物的结构和性质对生产生活意义深远。
 .已知A-F六种有机化合物,根据要求回答问题。
.已知A-F六种有机化合物,根据要求回答问题。___________ ,B物质的分子式为:___________ 。
(2)按官能团分类,D所属的类别是___________ 。
(3)1molE与足量的金属钠反应产生___________ L氢气(标况下)。
(4)实验室制取C的化学方程式___________ 。
 .蔬菜和水果中富含维生素C,维生素C具有还原性,其又被称为抗坏血酸,在酸性溶液中可以被
.蔬菜和水果中富含维生素C,维生素C具有还原性,其又被称为抗坏血酸,在酸性溶液中可以被 等氧化剂氧化为脱氢维生素C.根据要求回答问题。
等氧化剂氧化为脱氢维生素C.根据要求回答问题。___________ (填名称)。
(6)脱氢维生素C中,键角①___________ 键角②(填“>”、“=”或“<”)。
(7)向碘和淀粉溶液中加入维生素C,可能观察到的现象是___________ 。
(8)标出维生素C中所有的手性碳原子(用*标注)___________ 。
 .已知A-F六种有机化合物,根据要求回答问题。
.已知A-F六种有机化合物,根据要求回答问题。A. 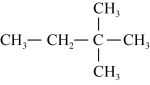 B.
B. 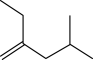 C.
C. D.
D. 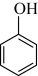 E.
E.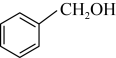
(2)按官能团分类,D所属的类别是
(3)1molE与足量的金属钠反应产生
(4)实验室制取C的化学方程式
 .蔬菜和水果中富含维生素C,维生素C具有还原性,其又被称为抗坏血酸,在酸性溶液中可以被
.蔬菜和水果中富含维生素C,维生素C具有还原性,其又被称为抗坏血酸,在酸性溶液中可以被 等氧化剂氧化为脱氢维生素C.根据要求回答问题。
等氧化剂氧化为脱氢维生素C.根据要求回答问题。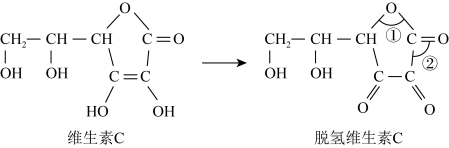
(6)脱氢维生素C中,键角①
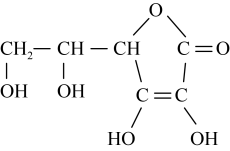
(7)向碘和淀粉溶液中加入维生素C,可能观察到的现象是
(8)标出维生素C中所有的手性碳原子(用*标注)
更新时间:2024-05-25 11:14:49
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】 和
和 在水处理过程中分别被还原为
在水处理过程中分别被还原为 和
和 。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么
。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么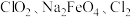 三种消毒杀菌剂的消毒效率由大到小的顺序是_______>_______>_______(填化学式)。
三种消毒杀菌剂的消毒效率由大到小的顺序是_______>_______>_______(填化学式)。_______
 和
和 在水处理过程中分别被还原为
在水处理过程中分别被还原为 和
和 。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么
。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么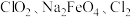 三种消毒杀菌剂的消毒效率由大到小的顺序是_______>_______>_______(填化学式)。
三种消毒杀菌剂的消毒效率由大到小的顺序是_______>_______>_______(填化学式)。
您最近一年使用:0次
【推荐2】ClO2是一种新型消毒剂,以下反应均能制得ClO2。
Ⅰ.2NaCl+6H2O 2ClO2↑+5H2↑+2NaOH
2ClO2↑+5H2↑+2NaOH
Ⅱ.5NaClO3+6HCl=6ClO2↑+3H2O+5NaCl
Ⅲ.Cl2+2NaClO2=2ClO2↑+2NaCl
(1)请表示反应Ⅰ中电子转移的方向和数目___________ 。
(2)由反应②可知,氧化性NaClO3____ ClO2;
(3)通过反应Ⅱ和Ⅲ分别制备标准状况下2.24LClO2,转移电子物质的量之比为___________ 。
(4)从氯元素利用率的角度分析,以上三种方法中,制备ClO2的最佳方法是___________ 。(填序号)
Ⅰ.2NaCl+6H2O
 2ClO2↑+5H2↑+2NaOH
2ClO2↑+5H2↑+2NaOHⅡ.5NaClO3+6HCl=6ClO2↑+3H2O+5NaCl
Ⅲ.Cl2+2NaClO2=2ClO2↑+2NaCl
(1)请表示反应Ⅰ中电子转移的方向和数目
(2)由反应②可知,氧化性NaClO3
(3)通过反应Ⅱ和Ⅲ分别制备标准状况下2.24LClO2,转移电子物质的量之比为
(4)从氯元素利用率的角度分析,以上三种方法中,制备ClO2的最佳方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)铁元素是构成人体的必不可少的元素之一,缺铁会影响到人体的健康和发育,最大的影响是缺铁性贫血。此类病人需要服用补铁药品。

一个体重50 kg的健康人含铁2 g,这2g铁在人体中以Fe2+和Fe3+的形式存在。以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是________ 。
A.Fe B.Fe2+ C.Fe3+
(2)亚硝酸钠有毒,有传言说亚硝酸钠是致癌物质,但事实上亚硝酸钠并不是致癌物质,致癌的是亚硝酸钠在一定条件下生成的亚硝胺。工业盐的主要成分是NaNO2,曾多次发生过因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,这说明NaNO2具有_______ 性。下列不能实现上述转化的物质是_______ 。
A.Cl2 B.O2 C.FeCl3 D.KMnO4(H+)
(3)在Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了________ 性和________ 性,则生成1分子NO转移电子数为________ ;56g Fe参加反应时,被还原的HNO3为________ g。

一个体重50 kg的健康人含铁2 g,这2g铁在人体中以Fe2+和Fe3+的形式存在。以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是
A.Fe B.Fe2+ C.Fe3+
(2)亚硝酸钠有毒,有传言说亚硝酸钠是致癌物质,但事实上亚硝酸钠并不是致癌物质,致癌的是亚硝酸钠在一定条件下生成的亚硝胺。工业盐的主要成分是NaNO2,曾多次发生过因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,这说明NaNO2具有
A.Cl2 B.O2 C.FeCl3 D.KMnO4(H+)
(3)在Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】今有化合物:
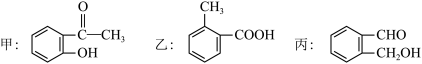
(1)请写出丙中含氧官能团的名称:_____________________ 。
(2)请判别上述哪些化合物互为同分异构体:________________________________ 。
(3)请分别写出鉴别甲的方法。(指明所选 试剂及主要现象即可)鉴别甲的方法:____________________________
(4)请按酸性由强至弱排列甲、乙、丙的顺序:________________ 。

(1)请写出丙中含氧官能团的名称:
(2)请判别上述哪些化合物互为同分异构体:
(3)请分别写出鉴别甲的方法。(指明所选 试剂及主要现象即可)鉴别甲的方法:
(4)请按酸性由强至弱排列甲、乙、丙的顺序:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】 (1)现有5种有机物:①乙烯;②乙醇;③葡萄糖;④乙酸;⑤乙酸乙酯。请分别写出其中含有下列官能团的有机物的结构简式,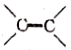
___________ ;—CHO___________ ;—COOH___________ 。在上述5种有机物中,能发生银镜反应的是___________ (填序号,下同);能发生水解反应的___________ ;具有酸性且能发生酯化反应的是___________ ;既能发生加成反应,又能发生加聚反应的是___________ 。
(2)下列说法正确的是___________ (填字母)。
A.含元素种类相同而结构不同的化合物互为同分异构体
B.某有机物完全燃烧后生成二氧化碳和水,说明该有机物中必定含有碳、氢、氧三种元素
C.甲烷与氯气的混合气体在光照条件下反应,生成的是一氯甲烷和氯化氢
D.乙烯与氯气加成反应的产物 ClCH2CH2Cl
(3)请选择合适的试剂除去括号内的杂质。

(2)下列说法正确的是
A.含元素种类相同而结构不同的化合物互为同分异构体
B.某有机物完全燃烧后生成二氧化碳和水,说明该有机物中必定含有碳、氢、氧三种元素
C.甲烷与氯气的混合气体在光照条件下反应,生成的是一氯甲烷和氯化氢
D.乙烯与氯气加成反应的产物 ClCH2CH2Cl
(3)请选择合适的试剂除去括号内的杂质。
| 序号 | 被提纯物(杂质) | 试剂 |
| ① | CH3CH3(CH2=CH2) | |
| ② | CH2=CH2(SO2) | |
| ③ | 乙酸乙酯(乙酸) | |
| ④ | 乙醇(水) |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
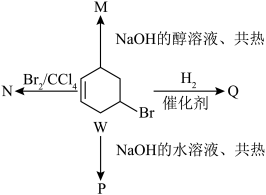
【推荐3】4-溴环己烯(W)在不同条件所发生的相关反应如图:
已知:①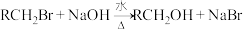 ;
;
②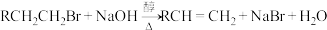 。
。
回答下列问题:
(1)W中所含官能团的名称为___________ 。
(2)M的结构简式可能为___________ 。
(3)Q的核磁共振氢谱中,有___________ 组峰,且峰面积之比为___________ 。
(4)N与NaOH的水溶液在共热条件下发生反应的化学方程式为___________ ,该反应的反应类型为___________ 。
(5)化合物L与P互为同分异构体,同时满足下列条件的L的结构有___________ 种(不包含P和不考虑立体异构)。
①除含一个六元环外不含其他环;
②能使酸性高锰酸钾溶液褪色;
③无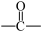 和
和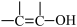 结构。
结构。

已知:①
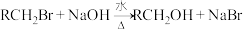 ;
;②
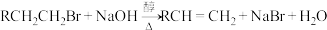 。
。回答下列问题:
(1)W中所含官能团的名称为
(2)M的结构简式可能为
(3)Q的核磁共振氢谱中,有
(4)N与NaOH的水溶液在共热条件下发生反应的化学方程式为
(5)化合物L与P互为同分异构体,同时满足下列条件的L的结构有
①除含一个六元环外不含其他环;
②能使酸性高锰酸钾溶液褪色;
③无
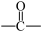 和
和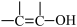 结构。
结构。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)下列分子中若有手性原子,请用“*”标出其手性碳原子_____________ 。
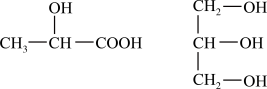
(2)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):H2SO4_______ H2SO3;HClO3_______ HClO4;
(3)根据价层电子对互斥理论判断下列问题:H2S分子的VSEPR构型为____________ ,立体构型为_________________ 。
(4)H2O的沸点(100℃)比H2S的沸点(-61℃)高,这是由于___________________ ;H2O比H2S更稳定,这是由于________________________ 。
(1)下列分子中若有手性原子,请用“*”标出其手性碳原子
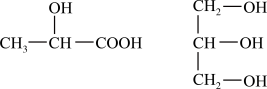
(2)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):H2SO4
(3)根据价层电子对互斥理论判断下列问题:H2S分子的VSEPR构型为
(4)H2O的沸点(100℃)比H2S的沸点(-61℃)高,这是由于
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按要求回答问题:
(1)对下列有机物进行命名_______ 。
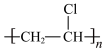
(2) 分子结构中处于同一平面上的原子个数最多有
分子结构中处于同一平面上的原子个数最多有_______ 个。
(3) 中含有的官能团名称为
中含有的官能团名称为_______ 。
(4)在饱和链状烷烃中,含有一个手性C原子且相对分子质量最小的烷烃有_______ 种结构。
(5)分子式为 ,已知其核磁共振氢谱表明只有一种化学环境的氢,则该有机物的结构简式为
,已知其核磁共振氢谱表明只有一种化学环境的氢,则该有机物的结构简式为_______ 。
(6)写出由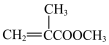 在加热和催化剂作用下发生加聚反应生成有机玻璃的化学方程式
在加热和催化剂作用下发生加聚反应生成有机玻璃的化学方程式_______ 。
(1)对下列有机物进行命名
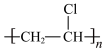
(2)
 分子结构中处于同一平面上的原子个数最多有
分子结构中处于同一平面上的原子个数最多有(3)
 中含有的官能团名称为
中含有的官能团名称为(4)在饱和链状烷烃中,含有一个手性C原子且相对分子质量最小的烷烃有
(5)分子式为
 ,已知其核磁共振氢谱表明只有一种化学环境的氢,则该有机物的结构简式为
,已知其核磁共振氢谱表明只有一种化学环境的氢,则该有机物的结构简式为(6)写出由
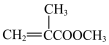 在加热和催化剂作用下发生加聚反应生成有机玻璃的化学方程式
在加热和催化剂作用下发生加聚反应生成有机玻璃的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】学习有机化学,掌握有机物的组成、结构、命名和官能团性质是重中之重。请回答下列问题:
(1) 的分子式为
的分子式为___________ ,所含官能团的名称为___________ 。
(2) 的系统命名为
的系统命名为___________ 。
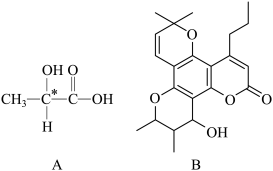
(3)当有机化合物分子中碳原子连有四个不同基团时称为手性碳原子,如A中星号“*”碳原子就是手性碳原子,则B中手性碳原子的个数为___________ ;若使A失去手性,则采取的方法为___________ (用化学方程式表示)。
(1)
 的分子式为
的分子式为(2)
 的系统命名为
的系统命名为(3)当有机化合物分子中碳原子连有四个不同基团时称为手性碳原子,如A中星号“*”碳原子就是手性碳原子,则B中手性碳原子的个数为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】重氮化合物是一类活泼的化合物,在有机合成方面有着重要应用。重氮化合物A在光照及甲醇参与反应的条件下经过一系列活泼中间体转化为F的路线如下:
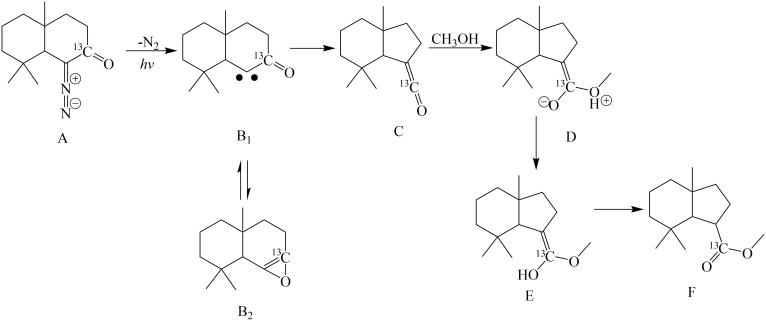
回答下列问题:
(1)为研究反应历程,A中的羰基上的碳原子用13C标记,这种研究方法称为___________ 。
(2)B1中的一个碳原子含有未共用电子对,易与B2相互转化或转化为C,B2的官能团名称为___________ ;上述路线中与B1、B2互为同分异构体的是___________ (填标号)。
(3)从结果上看,C和CH3OH生成E的反应类型为___________ ;写出CH2=C=O与CH3CH2OH反应的化学方程式___________ (不要求写出中间体)。
(4)E不稳定,能自发转化为F,说明稳定性C=O___________ C=C(填“大于”“小于”或“等于”),理由是___________ (从键参数的角度说明)。
(5)X、Y是二十多年前才发现的两种生物碱,在室温下可相互转化:
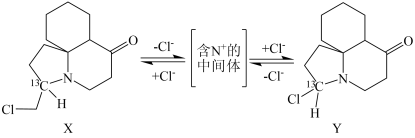
含N+的中间体的结构简式为____________

回答下列问题:
(1)为研究反应历程,A中的羰基上的碳原子用13C标记,这种研究方法称为
(2)B1中的一个碳原子含有未共用电子对,易与B2相互转化或转化为C,B2的官能团名称为
(3)从结果上看,C和CH3OH生成E的反应类型为
(4)E不稳定,能自发转化为F,说明稳定性C=O
(5)X、Y是二十多年前才发现的两种生物碱,在室温下可相互转化:

含N+的中间体的结构简式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】新质生产力的底色是绿色低碳。而化学,在绿色低碳方面当仁不让,新质生产力涵盖的产业链很多与化学化工相关,合成氨是人类科学技术上的一项重大突破,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是固氮的主要来源。
①基态氮原子的价电子轨道表示式为___________ 。
②自然固氮过程中生成的NO 的VSEPR模型名称为
的VSEPR模型名称为___________ 。
(2)铁触媒是普遍使用的人工合成氨的催化剂,以铁为主体通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是___________ 。
②基态铬原子的电子排布式为___________ 。
③下列比较正确的是___________ 。
A.第一电离能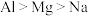 B.熔点:
B.熔点: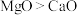
C.离子半径: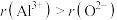 D.键角:
D.键角: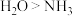
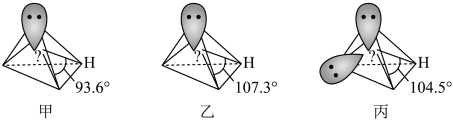
④NH3、H2O和PH3分子的空间结构和相应的键角如图所示,则甲、乙对应的分子分别是___________ 、___________ 。
(1)自然界中的氮元素主要以分子的形式存在于空气中,是固氮的主要来源。
①基态氮原子的价电子轨道表示式为
②自然固氮过程中生成的NO
 的VSEPR模型名称为
的VSEPR模型名称为(2)铁触媒是普遍使用的人工合成氨的催化剂,以铁为主体通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物。
①上述氧化物所涉及的元素中,处于元素周期表中p区的元素是
②基态铬原子的电子排布式为
③下列比较正确的是
A.第一电离能
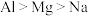 B.熔点:
B.熔点: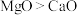
C.离子半径:
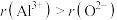 D.键角:
D.键角: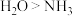
④NH3、H2O和PH3分子的空间结构和相应的键角如图所示,则甲、乙对应的分子分别是
您最近一年使用:0次



