(1)铁元素是构成人体的必不可少的元素之一,缺铁会影响到人体的健康和发育,最大的影响是缺铁性贫血。此类病人需要服用补铁药品。

一个体重50 kg的健康人含铁2 g,这2g铁在人体中以Fe2+和Fe3+的形式存在。以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是________ 。
A.Fe B.Fe2+ C.Fe3+
(2)亚硝酸钠有毒,有传言说亚硝酸钠是致癌物质,但事实上亚硝酸钠并不是致癌物质,致癌的是亚硝酸钠在一定条件下生成的亚硝胺。工业盐的主要成分是NaNO2,曾多次发生过因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,这说明NaNO2具有_______ 性。下列不能实现上述转化的物质是_______ 。
A.Cl2 B.O2 C.FeCl3 D.KMnO4(H+)
(3)在Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了________ 性和________ 性,则生成1分子NO转移电子数为________ ;56g Fe参加反应时,被还原的HNO3为________ g。

一个体重50 kg的健康人含铁2 g,这2g铁在人体中以Fe2+和Fe3+的形式存在。以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是
A.Fe B.Fe2+ C.Fe3+
(2)亚硝酸钠有毒,有传言说亚硝酸钠是致癌物质,但事实上亚硝酸钠并不是致癌物质,致癌的是亚硝酸钠在一定条件下生成的亚硝胺。工业盐的主要成分是NaNO2,曾多次发生过因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,这说明NaNO2具有
A.Cl2 B.O2 C.FeCl3 D.KMnO4(H+)
(3)在Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了
更新时间:2020-01-10 10:14:50
|
相似题推荐
【推荐1】一个完整的氧化还原反应方程式可以拆写成两个“半反应式”,一个是“氧化反应式”,一个是“还原反应式”.如2Fe3++Cu=2Fe2++Cu2+,可拆写为氧化反应式:Cu→Cu2++2e-,还原反应式:2Fe3++2e-→2Fe2+.在稀硫酸中,KMnO4和H2O2能发生氧化还原反应5H2O2+2MnO +6H+===5O2↑+2Mn2++8H2O。
+6H+===5O2↑+2Mn2++8H2O。
(1)将此氧化还原反应拆成半反应式,氧化式:_________ ,还原式:_________ 。
(2)反应中氧化剂是________ ;被氧化元素是__________ ;若有0.5 mol H2O2参加此反应,电子转移个数为____________ 。
(3)若KMnO4的量不足,在Mn2+的催化作用下,H2O2仍能分解,分解反应的化学方程式为________________________ ;这时若有0.5 mol H2O2发生分解,电子转移个数为______ 。
 +6H+===5O2↑+2Mn2++8H2O。
+6H+===5O2↑+2Mn2++8H2O。(1)将此氧化还原反应拆成半反应式,氧化式:
(2)反应中氧化剂是
(3)若KMnO4的量不足,在Mn2+的催化作用下,H2O2仍能分解,分解反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】近几年来关于氮污染的治理倍受关注,根据氮的性质回答以下问题;
(1)Ertl(获2007年诺贝尔化学奖)对合成氨机理进行深入研究,并将研究成果用于汽车尾气处理中,在催化剂存在下可将NO和CO反应转化为两种无色无毒气体,用化学反应方程式 表示这个过程_______ ;
(2)过度排放的氮氧化物易导致硝酸型酸雨,用化学方程式 表示NO2形成酸雨的原因:_______ 。飞机排放的氮氧化物(NO和NO2)会破坏臭氧层,它们和O3和O发生如下反应:O3+NO=NO2+O2;O+NO2=NO+O2,这两个反应反复循环,氮的氧化物在破坏臭氧层的过程中起到了_______ 的作用。
(3)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:

①电极a名称是_______ (填“正极”或“负极”)。
②电解质溶液中OHˉ离子向_______ 移动(填“电极a”或“电极b”)。
③电极a的电极反应式为_______ 。电极b的电极反应式为_______ 。
(1)Ertl(获2007年诺贝尔化学奖)对合成氨机理进行深入研究,并将研究成果用于汽车尾气处理中,在催化剂存在下可将NO和CO反应转化为两种无色无毒气体,用
(2)过度排放的氮氧化物易导致硝酸型酸雨,用
(3)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:

①电极a名称是
②电解质溶液中OHˉ离子向
③电极a的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】化学工业为疫情防控提供了强有力的物质支撑。氯的许多化合物既是重要化工原料,又是高效、广谱的灭菌消毒剂。回答下列问题:
(1)Cl2O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl2反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl2O的化学方程式为_______ 。
(2)ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,每生成1 mol ClO2消耗NaClO2的量为_______ mol;产生“气泡”的化学方程式为_______ 。
(3)向氯水中加入碳酸钙可增大次氯酸的浓度原因是_______ 。
(1)Cl2O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl2反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl2O的化学方程式为
(2)ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,每生成1 mol ClO2消耗NaClO2的量为
(3)向氯水中加入碳酸钙可增大次氯酸的浓度原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】高铁酸钠(Na2FeO4)是一种多功能、高效无毒的新型绿色水处理剂。
(1)Na2FeO4中铁元素的化合价是______ 价,Na2FeO4能给水消毒利用的是________ 性。
(2)用Na2FeO4给水消毒、杀菌时得到的Fe3+可以净水,Fe3+净水原理是______________ (用简要的文字叙述)。
(3)工业上可用FeCl3、NaOH 、NaClO三种物质在一定条件下反应制得Na2FeO4,配平反应的离子方程式:_____Fe3+ +_____OH-+____ClO- =_____FeO42-+ _____ + ______Cl- ,
+ ______Cl- ,____________ 氧化剂为________ ,若反应过程中转移了0.5 mol电子,则还原产物的物质的量为________ mol。
(1)Na2FeO4中铁元素的化合价是
(2)用Na2FeO4给水消毒、杀菌时得到的Fe3+可以净水,Fe3+净水原理是
(3)工业上可用FeCl3、NaOH 、NaClO三种物质在一定条件下反应制得Na2FeO4,配平反应的离子方程式:_____Fe3+ +_____OH-+____ClO- =_____FeO42-+ _____
 + ______Cl- ,
+ ______Cl- ,
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】我国“蓝天保卫战”成果显著,肆虐的雾霾逐渐被遏止。科学家研究发现含氮化合物和含硫化合物在形成雾霾时与大气中的氨有关,转化关系如图所示:
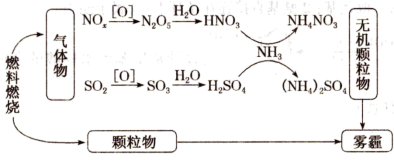
回答下列问题:
(1)从物质分类的角度看,图中的物质属于酸性氧化物的有_______ (写化学式)。
(2)工业上利用氨气制备一氧化氮,反应的化学方程式为_______ 。
(3)下列关于雾霾叙述错误的是_______ 。
A.雾和霾的分散质、分散剂相同 B.雾霾中含有硝酸铵和硫酸铵
C.NH3是形成无机颗粒物的催化剂 D.雾霾的形成与过度施用氮肥有关
(4)化肥、炼油、稀土、钢铁等工业都会排放出高浓度的氨氮废水。氨氮废水是造成河流及湖泊富营养化的主要因素。某氮肥厂产生的氨氮废水中的氮元素多以 和NH3·H2O形式存在,为达到变废为宝回收利用的目的,某团队设计处理流程如下:
和NH3·H2O形式存在,为达到变废为宝回收利用的目的,某团队设计处理流程如下:

①过程II为硝化过程,在微生物的作用下实现 →
→ →
→ 的转化,在碱性条件下
的转化,在碱性条件下 被氧气氧化成
被氧气氧化成 的总反应离子方程式为
的总反应离子方程式为_______ 。
②过程III为反硝化过程,向一定条件下的废水中加入甲醇(CH3OH)实现HNO3→ →N2的转化,将1mol
→N2的转化,将1mol 完全转化为N2,转移的电子数为
完全转化为N2,转移的电子数为_______ 。

回答下列问题:
(1)从物质分类的角度看,图中的物质属于酸性氧化物的有
(2)工业上利用氨气制备一氧化氮,反应的化学方程式为
(3)下列关于雾霾叙述错误的是
A.雾和霾的分散质、分散剂相同 B.雾霾中含有硝酸铵和硫酸铵
C.NH3是形成无机颗粒物的催化剂 D.雾霾的形成与过度施用氮肥有关
(4)化肥、炼油、稀土、钢铁等工业都会排放出高浓度的氨氮废水。氨氮废水是造成河流及湖泊富营养化的主要因素。某氮肥厂产生的氨氮废水中的氮元素多以
 和NH3·H2O形式存在,为达到变废为宝回收利用的目的,某团队设计处理流程如下:
和NH3·H2O形式存在,为达到变废为宝回收利用的目的,某团队设计处理流程如下:
①过程II为硝化过程,在微生物的作用下实现
 →
→ →
→ 的转化,在碱性条件下
的转化,在碱性条件下 被氧气氧化成
被氧气氧化成 的总反应离子方程式为
的总反应离子方程式为②过程III为反硝化过程,向一定条件下的废水中加入甲醇(CH3OH)实现HNO3→
 →N2的转化,将1mol
→N2的转化,将1mol 完全转化为N2,转移的电子数为
完全转化为N2,转移的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】明矾[ ,摩尔质量为:474g/mol]常用于净水,实验室可用废易拉罐(主要含Al,还含有少量的Fe、Mg等杂质)制备明矾,其实验过程为:取12g废易拉罐加入足量NaOH溶液,生成标况下13.44L
,摩尔质量为:474g/mol]常用于净水,实验室可用废易拉罐(主要含Al,还含有少量的Fe、Mg等杂质)制备明矾,其实验过程为:取12g废易拉罐加入足量NaOH溶液,生成标况下13.44L ,充分反应后通入一定量
,充分反应后通入一定量 ,过滤后,在所得固体中加入适量
,过滤后,在所得固体中加入适量 和
和 溶液,再将溶液进行适当操作制得明矾。
溶液,再将溶液进行适当操作制得明矾。
(1)明矾属于复盐,写出 在水中的电离方程式:
在水中的电离方程式:______ 。
(2)废易拉罐溶于NaOH溶液反应的离子方程式:______ ,要使溶液中铝元素完全转化为沉淀,至少通入标况下_____ L 。
。
(3)若要从溶液中得到明矾晶体,请实验操作有:_____ 、______ 、过滤、洗涤、干燥。
(4)若Al在转化过程中转化率为90%,则可生产___ 克含90%明矾粗品?(无解题过程不给分)。
 ,摩尔质量为:474g/mol]常用于净水,实验室可用废易拉罐(主要含Al,还含有少量的Fe、Mg等杂质)制备明矾,其实验过程为:取12g废易拉罐加入足量NaOH溶液,生成标况下13.44L
,摩尔质量为:474g/mol]常用于净水,实验室可用废易拉罐(主要含Al,还含有少量的Fe、Mg等杂质)制备明矾,其实验过程为:取12g废易拉罐加入足量NaOH溶液,生成标况下13.44L ,充分反应后通入一定量
,充分反应后通入一定量 ,过滤后,在所得固体中加入适量
,过滤后,在所得固体中加入适量 和
和 溶液,再将溶液进行适当操作制得明矾。
溶液,再将溶液进行适当操作制得明矾。(1)明矾属于复盐,写出
 在水中的电离方程式:
在水中的电离方程式:(2)废易拉罐溶于NaOH溶液反应的离子方程式:
 。
。(3)若要从溶液中得到明矾晶体,请实验操作有:
(4)若Al在转化过程中转化率为90%,则可生产
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氨气在工农业生产中有重要应用。
(1)①氮气用于工业合成氨,写出氮气的电子式:_______ ;
②NH3的稳定性比PH3_______ (填“强”或“弱”)。
(2)如下图所示,向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象。

①浓盐酸液滴附近会出现白烟,发生反应的化学方程式为_______ 。
②浓硫酸液滴上方没有明显现象,一段时间后浓硫酸的液滴中有白色固体,该固体可能是_______ (写化学式,一种即可)。写出鉴定此物质中阳离子的实验方法和现象:_______ 。
③FeSO4液滴中先出现灰绿色沉淀,过一段时间后变成红褐色,发生的反应包括Fe2++2NH3·H2O=Fe(OH)2↓+2NH 和
和_______ 。
(3)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),反应的化学方程式为_______ ,若反应中有0.3 mol电子发生转移时,生成亚硝酸的质量为_______ g(小数点后保留两位有效数字)。
(1)①氮气用于工业合成氨,写出氮气的电子式:
②NH3的稳定性比PH3
(2)如下图所示,向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象。

①浓盐酸液滴附近会出现白烟,发生反应的化学方程式为
②浓硫酸液滴上方没有明显现象,一段时间后浓硫酸的液滴中有白色固体,该固体可能是
③FeSO4液滴中先出现灰绿色沉淀,过一段时间后变成红褐色,发生的反应包括Fe2++2NH3·H2O=Fe(OH)2↓+2NH
 和
和(3)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)为了防止氯化亚铁溶液氧化变质,常在其中加入____ ,反应的离子方程式是_____ ;
(2)除去铁粉中的铝粉,可用过量的_______ 溶液,然后过滤,反应化学方程式为_________ 。
(2)除去铁粉中的铝粉,可用过量的
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)一个体重50 kg的健康人含铁元素2 g,这2 g铁元素以Fe2+和Fe3+的形式存在。Fe2+易被吸收,所以给贫血者补充铁时,应补充含Fe2+的亚铁盐(如FeSO4)。服用维生素C可使食物中的Fe3+转化成Fe2+,有利于人体对铁的吸收。
①人体中经常进行Fe2+与Fe3+的转化,可表示为Fe2+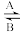 Fe3+。“服用维生素C可使食物中的Fe3+转化为Fe2+”, 由此可以推知维生素C在该过程中作
Fe3+。“服用维生素C可使食物中的Fe3+转化为Fe2+”, 由此可以推知维生素C在该过程中作___________ 剂。
②腌制食品中含有亚硝酸盐,亚硝酸盐能使人体内的铁元素发生A过程,过多食用会发生食物中毒,Fe2+此过程中表现出___________ 性。
③已知下列反应在一定条件下发生:
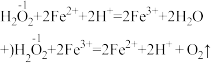
总反应式:2H2O2 2H2O+O2↑
2H2O+O2↑
在以上的反应中,Fe2+实际上起着___________ 的作用。
(2)硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
①下列物质不是硅酸盐材料的是___________
A.陶瓷 B.玻璃 C.水泥 D.生石灰
②SiO2是玻璃的成分之一,SiO2与氢氧化钠溶液反应的离子方程式___________ ,工艺师常用___________ (填物质名称)来雕刻玻璃。
③试管中加入3~5mL Na2SiO3溶液,滴入1~2滴酚酞溶液,再用胶头滴管逐滴加入稀盐酸,边加边振荡,至溶液红色变浅接近消失时停止,静置即得到硅酸胶体,该反应的化学方程式为___________ 。
①人体中经常进行Fe2+与Fe3+的转化,可表示为Fe2+
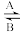 Fe3+。“服用维生素C可使食物中的Fe3+转化为Fe2+”, 由此可以推知维生素C在该过程中作
Fe3+。“服用维生素C可使食物中的Fe3+转化为Fe2+”, 由此可以推知维生素C在该过程中作②腌制食品中含有亚硝酸盐,亚硝酸盐能使人体内的铁元素发生A过程,过多食用会发生食物中毒,Fe2+此过程中表现出
③已知下列反应在一定条件下发生:
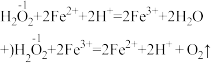
总反应式:2H2O2
 2H2O+O2↑
2H2O+O2↑在以上的反应中,Fe2+实际上起着
(2)硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
①下列物质不是硅酸盐材料的是
A.陶瓷 B.玻璃 C.水泥 D.生石灰
②SiO2是玻璃的成分之一,SiO2与氢氧化钠溶液反应的离子方程式
③试管中加入3~5mL Na2SiO3溶液,滴入1~2滴酚酞溶液,再用胶头滴管逐滴加入稀盐酸,边加边振荡,至溶液红色变浅接近消失时停止,静置即得到硅酸胶体,该反应的化学方程式为
您最近一年使用:0次



