回答下列问题:
(1)下列分子中若有手性原子,请用“*”标出其手性碳原子_____________ 。
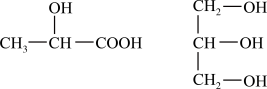
(2)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):H2SO4_______ H2SO3;HClO3_______ HClO4;
(3)根据价层电子对互斥理论判断下列问题:H2S分子的VSEPR构型为____________ ,立体构型为_________________ 。
(4)H2O的沸点(100℃)比H2S的沸点(-61℃)高,这是由于___________________ ;H2O比H2S更稳定,这是由于________________________ 。
(1)下列分子中若有手性原子,请用“*”标出其手性碳原子
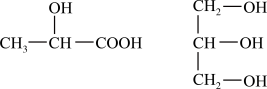
(2)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):H2SO4
(3)根据价层电子对互斥理论判断下列问题:H2S分子的VSEPR构型为
(4)H2O的沸点(100℃)比H2S的沸点(-61℃)高,这是由于
更新时间:2023-04-20 00:02:09
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】乳酸(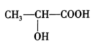 )是人体生理活动中无氧呼吸时的一种代谢产物,它是否存在手性异构体?乳酸分子中可能处于同一平面的原子最多有几个
)是人体生理活动中无氧呼吸时的一种代谢产物,它是否存在手性异构体?乳酸分子中可能处于同一平面的原子最多有几个____ ?
 )是人体生理活动中无氧呼吸时的一种代谢产物,它是否存在手性异构体?乳酸分子中可能处于同一平面的原子最多有几个
)是人体生理活动中无氧呼吸时的一种代谢产物,它是否存在手性异构体?乳酸分子中可能处于同一平面的原子最多有几个
您最近半年使用:0次
【推荐2】已知某些化学键的键能数据如下:
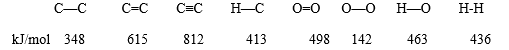
(1)通过比较C—C 和 C=C 的键能大小,简要说明为什么烯烃易发生加成反应而烷烃不能?______ 。
(2)利用键能数据可判断反应 2H2 + O2 → 2 H2O 为 放热反应, 计算每生成 1 mol H2O 所放出的热量为_____________ kJ。
(3)若某有机物的结构简式如下: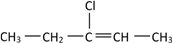 ,一定条件下与HCl发生加成反应后可能生成两种互为同分异构体的物质,写出其中属于手性分子的物质的结构简式:
,一定条件下与HCl发生加成反应后可能生成两种互为同分异构体的物质,写出其中属于手性分子的物质的结构简式:________________
(4)将硫酸铜白色固体溶于水得到蓝色的溶液,原因是生成了一种配合离子,其结构简式为:___________ (标明配位键),向该溶液中加入过量稀氨水得深蓝色溶液,其离子方程式为 _________ 。已知NF3与NH3的结构类似,但NF3不易与Cu2+形成配离子,其主要原因是_________________________________ 。
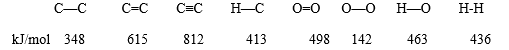
(1)通过比较C—C 和 C=C 的键能大小,简要说明为什么烯烃易发生加成反应而烷烃不能?
(2)利用键能数据可判断反应 2H2 + O2 → 2 H2O 为 放热反应, 计算每生成 1 mol H2O 所放出的热量为
(3)若某有机物的结构简式如下:
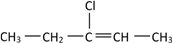 ,一定条件下与HCl发生加成反应后可能生成两种互为同分异构体的物质,写出其中属于手性分子的物质的结构简式:
,一定条件下与HCl发生加成反应后可能生成两种互为同分异构体的物质,写出其中属于手性分子的物质的结构简式:(4)将硫酸铜白色固体溶于水得到蓝色的溶液,原因是生成了一种配合离子,其结构简式为:
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知下列各组有机物:
①CH3—CH2—CH2—CH3和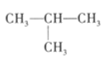 ;②CH2=CH—CH2—CH3和CH3—CH=CH—CH3;③CH3—CH2—OH和CH3—O—CH3;④
;②CH2=CH—CH2—CH3和CH3—CH=CH—CH3;③CH3—CH2—OH和CH3—O—CH3;④ 和
和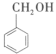 ;⑤
;⑤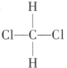 和
和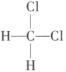 ;⑥CH3—CH2—CH=CH—CH3和
;⑥CH3—CH2—CH=CH—CH3和 (环戊烷);⑦CH2=CH—CH=CH2和CH3—CH2—C≡CH;⑧
(环戊烷);⑦CH2=CH—CH=CH2和CH3—CH2—C≡CH;⑧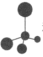 和
和 。
。
(1)其中互为同分异构体的是___ (填序号,下同);
(2)其中属于碳架异构的是___ ;
(3)其中属于位置异构的是___ ;
(4)其中属于官能团异构的是___ ;
(5)其中属于同一种物质的是___ ;
(6)其中属于对映异构的是___ 。
①CH3—CH2—CH2—CH3和
 ;②CH2=CH—CH2—CH3和CH3—CH=CH—CH3;③CH3—CH2—OH和CH3—O—CH3;④
;②CH2=CH—CH2—CH3和CH3—CH=CH—CH3;③CH3—CH2—OH和CH3—O—CH3;④ 和
和 ;⑤
;⑤ 和
和 ;⑥CH3—CH2—CH=CH—CH3和
;⑥CH3—CH2—CH=CH—CH3和 (环戊烷);⑦CH2=CH—CH=CH2和CH3—CH2—C≡CH;⑧
(环戊烷);⑦CH2=CH—CH=CH2和CH3—CH2—C≡CH;⑧ 和
和 。
。(1)其中互为同分异构体的是
(2)其中属于碳架异构的是
(3)其中属于位置异构的是
(4)其中属于官能团异构的是
(5)其中属于同一种物质的是
(6)其中属于对映异构的是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】下表是元素周期表的一部分,请回答:
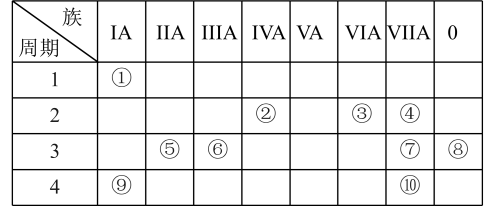
(1)元素⑦的原子结构示意图为___________ ;元素⑩的名称为___________ 。
(2)在这些元素中,化学性质最活泼的金属元素是___________ (填元素符号,下同),最不活泼的元素是___________ ;原子半径最小的元素是___________ 。
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是___________ (填化学式,下同);具有两性的是___________ 。

(1)元素⑦的原子结构示意图为
(2)在这些元素中,化学性质最活泼的金属元素是
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】Na2S 常用作皮革脱毛剂,工业上用反应 Na2SO4 +2C Na2S+2CO2↑ 进行制取。
Na2S+2CO2↑ 进行制取。
完成下列填空:
(1)硫元素在周期表中的位置为______________ 。上述反应中涉及的各元素中原子半径最小的是
__________ (填元素符号)。写出硫化钠的电子式:___________ 。
(2)用上述反应中涉及的元素,写出一个含有非极性键的化合物的化学式。_____________
(3)写出一个能比较 S 和 O 非金属性强弱的化学事实。________________________________
(4)在 2L 的容器内发生上述反应,2 小时内共生成 78 g 硫化钠,则这段时间内用二氧化碳表示的平均反应速率为______________ mol/(L·h) 。
(5)将硫化钠溶液滴入氯化铝溶液中,产生白色沉淀,同时有臭鸡蛋气味的气体生成,用平衡移动原理解
释上述现象。______________________________
 Na2S+2CO2↑ 进行制取。
Na2S+2CO2↑ 进行制取。完成下列填空:
(1)硫元素在周期表中的位置为
(2)用上述反应中涉及的元素,写出一个含有非极性键的化合物的化学式。
(3)写出一个能比较 S 和 O 非金属性强弱的化学事实。
(4)在 2L 的容器内发生上述反应,2 小时内共生成 78 g 硫化钠,则这段时间内用二氧化碳表示的平均反应速率为
(5)将硫化钠溶液滴入氯化铝溶液中,产生白色沉淀,同时有臭鸡蛋气味的气体生成,用平衡移动原理解
释上述现象。
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】有A、B、C、D、E五种短周期主族元素,原子序数由A到E逐渐增大.①A元素最外层电子数是次外层电子数的2倍. ②B的阴离子和C的阳离子与氖原子的电子层结构相同.③在通常状况下,B的单质是气体,0.1molB的气体与足量的氢气完全反应共有0.4mol电子转移.④C的单质在点燃时与B的单质充分反应,生成淡黄色的固体,此淡黄色固体能与AB2反应可生成B的单质.⑤D的气态氢化物与其最高价含氧酸间能发生氧化还原反应.请写出:
(1)A元素的最高价氧化物的电子式_________________________ .
(2)B元素在周期表中的位置_______________________________ .
(3)B单质与C单质在点燃时反应的生成物中所含化学键类型有____________________ .
(4)D元素的低价氧化物与E的单质的水溶液反应的化学方程式为______________________________________________________ .
(5)C与D能形成2:1的化合物,用电子式表示该化合物的形成过程的______________________________________________________ .
(6)元素D与元素E相比,非金属性较强的是______ (用元素符号表示),下列表述中能证明这一事实的是 _______________ (填选项序号).
a.常温下D的单质和E的单质状态不同
b.E的氢化物比D的氢化物稳定
c.一定条件下D和E的单质都能与钠反应
d.D的最高价含氧酸酸性弱于E的最高价含氧酸
e.D的单质能与E的氢化物反应生成E单质
(1)A元素的最高价氧化物的电子式
(2)B元素在周期表中的位置
(3)B单质与C单质在点燃时反应的生成物中所含化学键类型有
(4)D元素的低价氧化物与E的单质的水溶液反应的化学方程式为
(5)C与D能形成2:1的化合物,用电子式表示该化合物的形成过程的
(6)元素D与元素E相比,非金属性较强的是
a.常温下D的单质和E的单质状态不同
b.E的氢化物比D的氢化物稳定
c.一定条件下D和E的单质都能与钠反应
d.D的最高价含氧酸酸性弱于E的最高价含氧酸
e.D的单质能与E的氢化物反应生成E单质
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
(1)磷酸根离子的空间结构为_______________ ,其中P的价层电子对数为_______________ ,杂化轨道类型为_______________ 。
(2) 的晶胞结构示意图如(a)所示。其中O围绕
的晶胞结构示意图如(a)所示。其中O围绕 和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有
和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有 的单元数有
的单元数有_______________ 个。
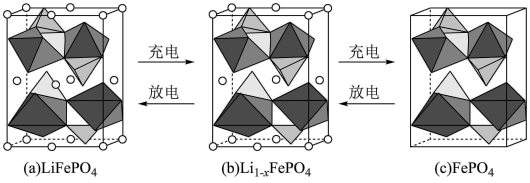
电池充电时, 脱出部分
脱出部分 ,形成
,形成 ,结构示意图如(b)所示,则
,结构示意图如(b)所示,则
_______________ ,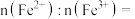
_______________ 。
(1)磷酸根离子的空间结构为
(2)
 的晶胞结构示意图如(a)所示。其中O围绕
的晶胞结构示意图如(a)所示。其中O围绕 和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有
和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有 的单元数有
的单元数有
电池充电时,
 脱出部分
脱出部分 ,形成
,形成 ,结构示意图如(b)所示,则
,结构示意图如(b)所示,则
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)蓝矾(CuSO4•5H2O)的结构如图所示:
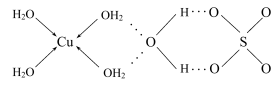
SO 的空间结构是
的空间结构是_____ ,其中S原子的杂化轨道类型是_____ 。
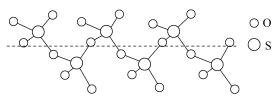
(2)气态SO3分子的空间结构为_____ ;将纯液态SO3冷却到289.8K时凝固得到一种螺旋状单链结构的固体,其结构如图,此固态SO3中S原子的杂化轨道类型是____ 。
(1)蓝矾(CuSO4•5H2O)的结构如图所示:

SO
 的空间结构是
的空间结构是(2)气态SO3分子的空间结构为

您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】请回答下列有关问题。
(1) 元素按周期表分区属于
元素按周期表分区属于________ 区元素
(2)地壳中含量最多的三种元素 、
、 、
、 中,电负性最大的是
中,电负性最大的是______ 。
(3)钠在火焰上灼烧产生的黄光是一种_______ (填字母)
A.吸收光谱 B.发射光谱
(4) 分子的空间构型为
分子的空间构型为_______ 。
(5)钛被称为继铁、铝之后的第三金属,基态钛原子价电子层的电子排布图是______ 。
(6)基态 与
与 离子中未成对的电子数之比为
离子中未成对的电子数之比为________ 。
(7) 分子中所有原子均满足8电子构型,
分子中所有原子均满足8电子构型, 分子中
分子中 键和
键和 键的个数比为
键的个数比为_______ 。
(1)
 元素按周期表分区属于
元素按周期表分区属于(2)地壳中含量最多的三种元素
 、
、 、
、 中,电负性最大的是
中,电负性最大的是(3)钠在火焰上灼烧产生的黄光是一种
A.吸收光谱 B.发射光谱
(4)
 分子的空间构型为
分子的空间构型为(5)钛被称为继铁、铝之后的第三金属,基态钛原子价电子层的电子排布图是
(6)基态
 与
与 离子中未成对的电子数之比为
离子中未成对的电子数之比为(7)
 分子中所有原子均满足8电子构型,
分子中所有原子均满足8电子构型, 分子中
分子中 键和
键和 键的个数比为
键的个数比为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】I.Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
(1)基态Fe2+与Fe3+中未成对的电子数之比为_____ 。
(2)I1(Li)>I1(Na),原因是_____ 。
(3)磷酸根离子的空间构型为____ ,其中P的价层电子对数为____ ,杂化轨道类型为____ 。
II.近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为Fe-Sm-As-F-O组成的化合物。回答下列问题:
(4)元素As与N同族。预测As的氢化物分子的立体结构为____ ,其沸点比NH3的____ (填“高”或“低”),其判断理由是____ 。
(5)Sm的价层电子排布式为4f66s2,Sm3+的价层电子排布式为_____ 。
III.以铁、硫酸、柠檬酸、双氧水、氨水等为原料可制备柠檬酸铁铵。
(6)27gNH 中含电子的物质的量为
中含电子的物质的量为____ mol。
(7)柠檬酸的结构简式为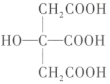 。1mol柠檬酸分子中碳原子与氧原子形成的σ键的数目为
。1mol柠檬酸分子中碳原子与氧原子形成的σ键的数目为____ NA。
(1)基态Fe2+与Fe3+中未成对的电子数之比为
(2)I1(Li)>I1(Na),原因是
(3)磷酸根离子的空间构型为
II.近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为Fe-Sm-As-F-O组成的化合物。回答下列问题:
(4)元素As与N同族。预测As的氢化物分子的立体结构为
(5)Sm的价层电子排布式为4f66s2,Sm3+的价层电子排布式为
III.以铁、硫酸、柠檬酸、双氧水、氨水等为原料可制备柠檬酸铁铵。
(6)27gNH
 中含电子的物质的量为
中含电子的物质的量为(7)柠檬酸的结构简式为
 。1mol柠檬酸分子中碳原子与氧原子形成的σ键的数目为
。1mol柠檬酸分子中碳原子与氧原子形成的σ键的数目为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】 的沸点低于
的沸点低于 ,其原因是
,其原因是_______ 。硒的两种含氧酸的酸性强弱为
_______  (填“>”或“<”)。
(填“>”或“<”)。
 的沸点低于
的沸点低于 ,其原因是
,其原因是
 (填“>”或“<”)。
(填“>”或“<”)。
您最近半年使用:0次




