以钛铁矿(主要成分为 ,还含有MgO、CaO、
,还含有MgO、CaO、 等杂质)为原料合成锂离子电池的电极材料钛酸锂(
等杂质)为原料合成锂离子电池的电极材料钛酸锂( )和磷酸亚铁锂(
)和磷酸亚铁锂( )的工艺流程如图:
)的工艺流程如图:

已知:“溶浸”后的溶液中含金属元素的离子主要包括 、
、 、
、 、
、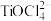 ;富铁元素主要以
;富铁元素主要以 形式存在;富钛渣中钛元素主要以
形式存在;富钛渣中钛元素主要以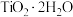 形式存在。
形式存在。
回答下列问题:
(1)“溶浸”时为加快浸取速率,可以采取的措施是___________ (答1条即可);“溶浸”过程 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(2)若在实验室模拟分离富钛渣和富铁液,则检验富钛渣洗涤干净的操作为___________ 。
(3)“沉铁”过程中需控制 ,其目的是
,其目的是___________ (答1条即可)。
(4)“溶钛”过程中Ti元素的浸出率与反应温度的关系如图所示,试分析40℃后Ti元素浸出率呈图像所示变化的原因:___________ 。

(5) 的晶胞结构如图1所示,设该晶胞的边长为a nm,
的晶胞结构如图1所示,设该晶胞的边长为a nm, 为阿伏伽德罗常数的值。Ti的价电子排布式为
为阿伏伽德罗常数的值。Ti的价电子排布式为___________ ,该晶体的密度
___________ (填含a的计算式)g⋅cm-3; 的结构的另一种表示如图2(晶胞中未标出Ti、O原子),画出沿z轴向xy平面投影时氧原子在xy平面的位置:
的结构的另一种表示如图2(晶胞中未标出Ti、O原子),画出沿z轴向xy平面投影时氧原子在xy平面的位置: 。
。________

 ,还含有MgO、CaO、
,还含有MgO、CaO、 等杂质)为原料合成锂离子电池的电极材料钛酸锂(
等杂质)为原料合成锂离子电池的电极材料钛酸锂( )和磷酸亚铁锂(
)和磷酸亚铁锂( )的工艺流程如图:
)的工艺流程如图:
已知:“溶浸”后的溶液中含金属元素的离子主要包括
 、
、 、
、 、
、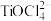 ;富铁元素主要以
;富铁元素主要以 形式存在;富钛渣中钛元素主要以
形式存在;富钛渣中钛元素主要以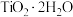 形式存在。
形式存在。回答下列问题:
(1)“溶浸”时为加快浸取速率,可以采取的措施是
 发生反应的离子方程式为
发生反应的离子方程式为(2)若在实验室模拟分离富钛渣和富铁液,则检验富钛渣洗涤干净的操作为
(3)“沉铁”过程中需控制
 ,其目的是
,其目的是(4)“溶钛”过程中Ti元素的浸出率与反应温度的关系如图所示,试分析40℃后Ti元素浸出率呈图像所示变化的原因:

(5)
 的晶胞结构如图1所示,设该晶胞的边长为a nm,
的晶胞结构如图1所示,设该晶胞的边长为a nm, 为阿伏伽德罗常数的值。Ti的价电子排布式为
为阿伏伽德罗常数的值。Ti的价电子排布式为
 的结构的另一种表示如图2(晶胞中未标出Ti、O原子),画出沿z轴向xy平面投影时氧原子在xy平面的位置:
的结构的另一种表示如图2(晶胞中未标出Ti、O原子),画出沿z轴向xy平面投影时氧原子在xy平面的位置: 。
。
更新时间:2023-05-20 19:55:19
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】填空。
(1)写出醋酸与NaOH溶液反应的离子方程式___________ 。
(2)在25℃、101kPa时,4.0g硫粉在氧气中完全燃烧生成二氧化硫气体,放出27kJ的热量,表示硫燃烧的热化学方程式为___________ 。
(3)已知某温度下有如下三个反应: ,
, ,
, 。则该温度下HF、HCN和
。则该温度下HF、HCN和 ,三种弱酸的电离常数由大到小的顺序是
,三种弱酸的电离常数由大到小的顺序是___________ 。
(4)在硫酸工业中,通过下列反应使 氧化为
氧化为 :
: ,在实际生产中,通入过量的空气,原因是
,在实际生产中,通入过量的空气,原因是___________ 。
(1)写出醋酸与NaOH溶液反应的离子方程式
(2)在25℃、101kPa时,4.0g硫粉在氧气中完全燃烧生成二氧化硫气体,放出27kJ的热量,表示硫燃烧的热化学方程式为
(3)已知某温度下有如下三个反应:
 ,
, ,
, 。则该温度下HF、HCN和
。则该温度下HF、HCN和 ,三种弱酸的电离常数由大到小的顺序是
,三种弱酸的电离常数由大到小的顺序是(4)在硫酸工业中,通过下列反应使
 氧化为
氧化为 :
: ,在实际生产中,通入过量的空气,原因是
,在实际生产中,通入过量的空气,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】不同价态氯(或卤素)的归中或歧化反应,试写出下列反应的离子方程式。
(1)次氯酸钠与盐酸反应:________________________ 。
(2)酸化NaIO3和NaI的混合溶液:_____________________ 。
(3)氯气通入热的氢氧化钾溶液(生成物中检测出含有氯酸钾):_____________ 。
(1)次氯酸钠与盐酸反应:
(2)酸化NaIO3和NaI的混合溶液:
(3)氯气通入热的氢氧化钾溶液(生成物中检测出含有氯酸钾):
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某同学利用实验室中几种等浓度溶液:①HCl ②BaCl2 ③Na2CO3,进行以下实验。
(1)将表格补充完整:a._____ ;b._____ 。
(2)除以上试剂外,请任意选择一种能与②反应的试剂,并写出反应的离子方程式。试剂:____ ,离子方程式:____ 。
(3)实验ii中,取100 g含①36.5%的稀溶液与③充分反应,最多可以产生气体多少____ 克?
| 序号 | 操作 | 现象 | 离子方程式 |
| i | 向盛有1 mL的②试管中加入1 mL③ | 产生白色沉淀 | a |
| ii | 向盛有2 mL①的试管中加入1 mL③ | 产生气体 | b |
(2)除以上试剂外,请任意选择一种能与②反应的试剂,并写出反应的离子方程式。试剂:
(3)实验ii中,取100 g含①36.5%的稀溶液与③充分反应,最多可以产生气体多少
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】①~5五种元素在元素周期表中的位置关系如图:
回答下列问题:
(1)①的元素名称是_______ 。
(2)④的基态原子的电子排布式是_______ 。
(3)②和③中,电负性较大的是_______ (填元素符号)。
(4)②和⑤中,第一电离能较大的是_______ (填元素符号)。
(5)②、③、⑤分别与①形成的最简单化合物中,热稳定性最强的是_______ (填化学式)。
| 族周期 | IA | II A | III A | IVA | VA | VIA | VIIA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ |
(1)①的元素名称是
(2)④的基态原子的电子排布式是
(3)②和③中,电负性较大的是
(4)②和⑤中,第一电离能较大的是
(5)②、③、⑤分别与①形成的最简单化合物中,热稳定性最强的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.硒化锌是一种透明半导体,也可作为红外光学材料,熔点是1520℃。
(1)基态锌原子的价电子排布式是_____ 。
(2)根据元素周期律,电负性Se_____ S,Se位于周期表_____ 区。
(3)H2Se的分子构型是_____ ,其中硒原子的杂化轨道类型是_____ 。
(4)H2O的沸点高于H2Se的沸点(-42℃),其原因是_____ 。
Ⅱ.氮及其化合物与人类生产、生活息息相关。回答下列问题:
(5)C、N、O三种元素第一电离能从大到小的顺序是_____ 。
(6)1molN2F2含有_____ molσ键。
(1)基态锌原子的价电子排布式是
(2)根据元素周期律,电负性Se
(3)H2Se的分子构型是
(4)H2O的沸点高于H2Se的沸点(-42℃),其原因是
Ⅱ.氮及其化合物与人类生产、生活息息相关。回答下列问题:
(5)C、N、O三种元素第一电离能从大到小的顺序是
(6)1molN2F2含有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】水是生命之源,它与我们的生活密切相关。在化学实验和科学研究中,水也是一种常用的试剂。
(1)水分子中氧原子在基态时核外电子排布式为______ 。
(2)写出与H2O分子互为等电子体的微粒________________ (填2种)。
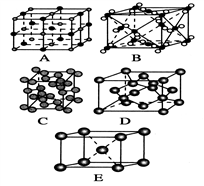
(3)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。其中E图堆积方式的空间利用率为_________ ,与冰的晶体类型相同的是________ (请用相应的编号填写)
(4)高温下,超氧化钾(KO2)晶体呈立方体结构,其晶胞结构与NaCl的相同,则每个晶胞中含有___ 个K+和___ 个O2— ;晶体中K+ 的配位数为___ ,O2— 的配位数为______ 。
(5)60 g 金刚石中的共价键数为_________ 个,60g SiO2晶体中的共价键数为_______ 个。
(1)水分子中氧原子在基态时核外电子排布式为
(2)写出与H2O分子互为等电子体的微粒
(3)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。其中E图堆积方式的空间利用率为

(4)高温下,超氧化钾(KO2)晶体呈立方体结构,其晶胞结构与NaCl的相同,则每个晶胞中含有
(5)60 g 金刚石中的共价键数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】许多金属及其化合物在生活、化工、医药、材料等各个领域有着广泛的应用。
(1)钛由于其稳定的化学性质,良好的耐高温、耐低温、抗强酸、抗强碱以及高强度、低密度,被美誉为“未来钢铁”、“战略金属”。钛基态原子中电子占据最高能级的符号为________ 。与钛同周期的元素中,基态原子的未成对电子数与钛相同的有_______ 种。钛比钢轻、比铝硬,是一种新兴的结构材料。钛硬度比铝大的原因是___________________ 。
(2)有一种氮化钛晶体的晶胞与NaCl晶胞相似,如图所示,该晶胞中N、Ti之间的最近距离为a×10-10 cm,则该氮化钛的密度为______ g·cm-3(NA为阿伏伽德罗常数的值,只列计算式)。

(3)Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能量密度大等优良性能,得到广泛应用。Li2O是离子晶体,其晶格能可通过图(a)的Born-Haber循环计算得到。

Li原子的第一电离能为______ kJ·mol-1,O=O键键能为_____ kJ·mol-1,Li2O晶格能为____ kJ·mol-1。
(1)钛由于其稳定的化学性质,良好的耐高温、耐低温、抗强酸、抗强碱以及高强度、低密度,被美誉为“未来钢铁”、“战略金属”。钛基态原子中电子占据最高能级的符号为
(2)有一种氮化钛晶体的晶胞与NaCl晶胞相似,如图所示,该晶胞中N、Ti之间的最近距离为a×10-10 cm,则该氮化钛的密度为

(3)Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能量密度大等优良性能,得到广泛应用。Li2O是离子晶体,其晶格能可通过图(a)的Born-Haber循环计算得到。

Li原子的第一电离能为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】新型储氢材料是开发利用氢能的重要研究方向.
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得.
①基态Cl原子中,电子占据的最高能层符号为_____ ,该能层具有的原子轨道数为_____ .
②LiBH4由Li+和BH4﹣构成,BH4﹣的立体结构是_____ ,B原子的杂化轨道类型是_____ .
Li、B、H元素的电负性由大到小排列顺序为_____ .
(2)金属氢化物是具有良好发展前景的储氢材料.
①LiH中,离子半径Li+_____ H﹣(填“>”、“=”或“<”).②某储氢材料是第三周期金属元素M的氢化物.M的部分电离能如表所示:
M是_____ (填元素符号).
(3)NaH具有NaCl型晶体结构,已知NaH晶体的晶胞参数a=488pm(棱长),Na+半径为102pm,H﹣的半径为_____ ,NaH的理论密度是___________ g•cm﹣3(只列算式,不必计算出数值,阿伏加德罗常数为NA)
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得.
①基态Cl原子中,电子占据的最高能层符号为
②LiBH4由Li+和BH4﹣构成,BH4﹣的立体结构是
Li、B、H元素的电负性由大到小排列顺序为
(2)金属氢化物是具有良好发展前景的储氢材料.
①LiH中,离子半径Li+
| I1/kJ•mol﹣1 | I2/kJ•mol﹣1 | I3/kJ•mol﹣1 | I4/kJ•mol﹣1 | I5/kJ•mol﹣1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
M是
(3)NaH具有NaCl型晶体结构,已知NaH晶体的晶胞参数a=488pm(棱长),Na+半径为102pm,H﹣的半径为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】下图为几种晶体或晶胞的示意图:
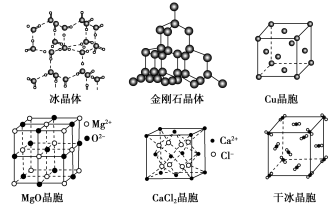
请回答下列问题:
(1)上述晶体中,粒子之间以共价键结合形成的晶体是___________ 。
(2)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为___________ 。
(3)NaCl晶胞与MgO晶胞相同,NaCl晶体的晶格能___________ (填“大于”或“小于”)MgO晶体。
(4)每个Cu晶胞中实际占有___________ 个Cu原子,晶胞中Cu原子配位数为___________ 。
(5)冰的熔点远高于干冰,除H2O是极性分子、CO2是非极性分子外,还有一个重要的原因是___________ 。

请回答下列问题:
(1)上述晶体中,粒子之间以共价键结合形成的晶体是
(2)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为
(3)NaCl晶胞与MgO晶胞相同,NaCl晶体的晶格能
(4)每个Cu晶胞中实际占有
(5)冰的熔点远高于干冰,除H2O是极性分子、CO2是非极性分子外,还有一个重要的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】现有含NaCl、Na2SO4、NaNO3的混合溶液,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、SO 、NO
、NO 的相互分离。相应的实验过程可用下图表示:
的相互分离。相应的实验过程可用下图表示:

(1)写出上述实验过程中所用试剂的名称:试剂1为
(2)控制试剂4的加入量的方法是
(3)加入过量试剂3的目的是
(4)操作①的名称是
(5)写出加入试剂4后发生反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】海洋资源的利用具有广阔前景。
(1)无需经过化学变化就能从海水中获得的物质是( ) (填序号)
A.Cl2 B.淡水 C.烧碱 D.食盐
(2)下图是从海水中提取镁的简单流程。
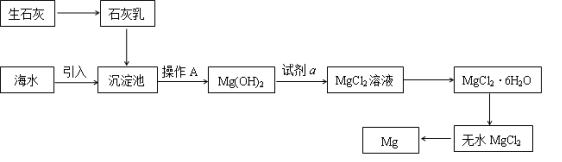
①操作A是_______________________ 。
②无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为____________________________ 。
③海水提镁的过程,为什么要将海水中的氯化镁转变为氢氧化镁,再转变为氯化镁?_____________________________________________ 。
(3)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:

①灼烧海带至灰烬时所用的主要仪器名称是( ) (填序号)
a.坩埚 b.试管 c.蒸发皿 d.烧杯
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式________________________________ 。
③用CCl4提取碘时除了用CCl4还可以选用的试剂是( ) (填字母序号)
a.苯 b.乙醇 c.乙酸
④为检验用CCl4提取碘后的水溶液中是否还含有碘单质。请写出该实验的实验步骤、现象及结论:________ 。
(4)利用海底的“可燃冰”制作的燃料电池的总反应式为CH4+2O2+2KOH = K2CO3+3H2O,则该燃料电池的负极的电极反应为__________________ 。
(5)海底的煤经综合利用开发的副产物CO2能生产甲醇燃料,其反应的方程式为:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。某科学实验将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标。
CH3OH(g)+H2O(g)。某科学实验将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标。
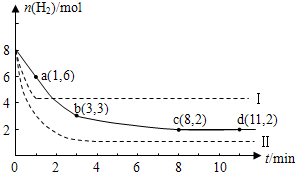
①a点正反应速率_________ (填“大于、等于或小于”)a点逆反应速率。
②平衡时CO2的物质的量浓度是___________ mol/L。
③能够说明该反应达到化学平衡状态的标志是_______ (双选)。
A.单位时间内消耗1molCO2,同时生成3mol H2 B.混合气体的密度不随时间变化
C.CH3OH、H2的浓度不再随时间变化 D.CH3OH和H2O浓度相等
(1)无需经过化学变化就能从海水中获得的物质是
A.Cl2 B.淡水 C.烧碱 D.食盐
(2)下图是从海水中提取镁的简单流程。

①操作A是
②无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为
③海水提镁的过程,为什么要将海水中的氯化镁转变为氢氧化镁,再转变为氯化镁?
(3)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:

①灼烧海带至灰烬时所用的主要仪器名称是
a.坩埚 b.试管 c.蒸发皿 d.烧杯
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式
③用CCl4提取碘时除了用CCl4还可以选用的试剂是
a.苯 b.乙醇 c.乙酸
④为检验用CCl4提取碘后的水溶液中是否还含有碘单质。请写出该实验的实验步骤、现象及结论:
(4)利用海底的“可燃冰”制作的燃料电池的总反应式为CH4+2O2+2KOH = K2CO3+3H2O,则该燃料电池的负极的电极反应为
(5)海底的煤经综合利用开发的副产物CO2能生产甲醇燃料,其反应的方程式为:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。某科学实验将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标。
CH3OH(g)+H2O(g)。某科学实验将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标。
①a点正反应速率
②平衡时CO2的物质的量浓度是
③能够说明该反应达到化学平衡状态的标志是
A.单位时间内消耗1molCO2,同时生成3mol H2 B.混合气体的密度不随时间变化
C.CH3OH、H2的浓度不再随时间变化 D.CH3OH和H2O浓度相等
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】自古至今,铁及其化合物在人类生产生活中的使用发挥了巨大的作用。
(1)四大发明之一的司南是由天然磁石制成的,其主要成分是___________ (填化学式) 。
(2)由于Fe(OH)2易被氧化,所以制备时常隔绝空气制备,写出Fe(OH)2露置在空气中被氧化的化学方程式___________ 。
(3)某工业废渣wg (主要含二氧化硅、氧化铁、氧化镁)中提取氧化铁的工业流程如图(部分操作和条件略):
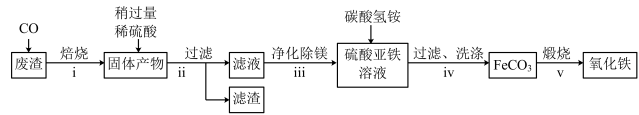
提示:二氧化硅不溶于稀硫酸。
①验证硫酸亚铁溶液中是否存在Fe3+的常用的试剂是___________ (填化学式)。
②步骤Ⅴ中,发生反应的化学方程式为___________ 。
③若提取过程中铁元素的损耗忽略不计,最终获得n g的氧化铁。则废渣中铁元素的质量分数为___________ 。
(1)四大发明之一的司南是由天然磁石制成的,其主要成分是
(2)由于Fe(OH)2易被氧化,所以制备时常隔绝空气制备,写出Fe(OH)2露置在空气中被氧化的化学方程式
(3)某工业废渣wg (主要含二氧化硅、氧化铁、氧化镁)中提取氧化铁的工业流程如图(部分操作和条件略):

提示:二氧化硅不溶于稀硫酸。
①验证硫酸亚铁溶液中是否存在Fe3+的常用的试剂是
②步骤Ⅴ中,发生反应的化学方程式为
③若提取过程中铁元素的损耗忽略不计,最终获得n g的氧化铁。则废渣中铁元素的质量分数为
您最近一年使用:0次



