自古至今,铁及其化合物在人类生产生活中的使用发挥了巨大的作用。
(1)四大发明之一的司南是由天然磁石制成的,其主要成分是___________ (填化学式) 。
(2)由于Fe(OH)2易被氧化,所以制备时常隔绝空气制备,写出Fe(OH)2露置在空气中被氧化的化学方程式___________ 。
(3)某工业废渣wg (主要含二氧化硅、氧化铁、氧化镁)中提取氧化铁的工业流程如图(部分操作和条件略):
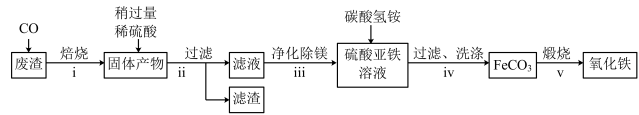
提示:二氧化硅不溶于稀硫酸。
①验证硫酸亚铁溶液中是否存在Fe3+的常用的试剂是___________ (填化学式)。
②步骤Ⅴ中,发生反应的化学方程式为___________ 。
③若提取过程中铁元素的损耗忽略不计,最终获得n g的氧化铁。则废渣中铁元素的质量分数为___________ 。
(1)四大发明之一的司南是由天然磁石制成的,其主要成分是
(2)由于Fe(OH)2易被氧化,所以制备时常隔绝空气制备,写出Fe(OH)2露置在空气中被氧化的化学方程式
(3)某工业废渣wg (主要含二氧化硅、氧化铁、氧化镁)中提取氧化铁的工业流程如图(部分操作和条件略):

提示:二氧化硅不溶于稀硫酸。
①验证硫酸亚铁溶液中是否存在Fe3+的常用的试剂是
②步骤Ⅴ中,发生反应的化学方程式为
③若提取过程中铁元素的损耗忽略不计,最终获得n g的氧化铁。则废渣中铁元素的质量分数为
更新时间:2023-07-10 13:11:26
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】某化学兴趣小组在探究次氯酸钠溶液的性质时发现:往过量 FeSO4溶液中滴入几滴NaClO溶液,并加入适量硫酸,溶液立即变黄。请你协助他们完成该反应还原产物的部分探究过程。
(1)溶液变黄,说明反应生成了_________ (离子符号),可以通过加入____________ (试剂名称)进行检验。
(2)甲同学推测该反应的还原产物为Cl2;乙同学推测该反应的还原产物为________ (填微粒)。
(3)你认为甲同学的推测是否正确?____________ (填“正确”或“不正确”).
(4)假设乙同学的推测是正确。写出过量 FeSO4溶液中,滴入几滴NaClO溶液,并加入适量硫酸的离子方程式:___________________________________________________ 。
(1)溶液变黄,说明反应生成了
(2)甲同学推测该反应的还原产物为Cl2;乙同学推测该反应的还原产物为
(3)你认为甲同学的推测是否正确?
(4)假设乙同学的推测是正确。写出
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】磷酸亚铁锂 电池是新能源汽车的动力电池之一,采用湿法冶金工艺回收该废电池正极片(除
电池是新能源汽车的动力电池之一,采用湿法冶金工艺回收该废电池正极片(除 外,还含有
外,还含有 箔、少量其他不溶物)得到
箔、少量其他不溶物)得到 晶体等资源。
晶体等资源。
(1) 中铁元素的化合价为
中铁元素的化合价为_________ 。
(2) 与
与 溶液反应的离子方程式为
溶液反应的离子方程式为________________________________________ 。
(3)能将 氧化为
氧化为 的试剂是
的试剂是_________ (填序号)。
A. B.稀硫酸 C.铜
B.稀硫酸 C.铜
(4)若溶液中含有 ,加入试剂
,加入试剂________________ (填化学式)时溶液变为红色。
 电池是新能源汽车的动力电池之一,采用湿法冶金工艺回收该废电池正极片(除
电池是新能源汽车的动力电池之一,采用湿法冶金工艺回收该废电池正极片(除 外,还含有
外,还含有 箔、少量其他不溶物)得到
箔、少量其他不溶物)得到 晶体等资源。
晶体等资源。(1)
 中铁元素的化合价为
中铁元素的化合价为(2)
 与
与 溶液反应的离子方程式为
溶液反应的离子方程式为(3)能将
 氧化为
氧化为 的试剂是
的试剂是A.
 B.稀硫酸 C.铜
B.稀硫酸 C.铜(4)若溶液中含有
 ,加入试剂
,加入试剂
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氯化铁是常见的水处理剂,无水晶FeCl3易升华。工业上制备无水的FeCl3的一种工艺如图所示:

(1)加入吸收塔的吸收剂X应是______ (填字母编号)。
a. NaOH溶液 b. 饱和食盐水 c. FeCl2溶液 d. 淀粉KI溶液
(2)取0.5mL饱和FeCl3溶液滴入50mL沸水中,得红褐色氢氧化铁胶体,则发生反应的离子方程式为_________________ ,区分胶体和溶液的方法是_________________ 。
(3)实验室中从FeCl3溶液制得FeCl3·6H2O晶体的过程中,需先加入盐酸且保持过量,然后进行的操作依次为________ 、冷却结晶、过滤。
(4)将H2S气体通入FeCl3溶液中会出现浑浊,则其反应的离子方程式为_________ 。
(5)铁铬氯化还原液流电池是一种低成本的储能电池,电池结构如右图所示(电极材料为石墨),工作原理为: ,则电池放电时,Cl-将移向
,则电池放电时,Cl-将移向_______ 极(填“正”或“负”)。


(1)加入吸收塔的吸收剂X应是
a. NaOH溶液 b. 饱和食盐水 c. FeCl2溶液 d. 淀粉KI溶液
(2)取0.5mL饱和FeCl3溶液滴入50mL沸水中,得红褐色氢氧化铁胶体,则发生反应的离子方程式为
(3)实验室中从FeCl3溶液制得FeCl3·6H2O晶体的过程中,需先加入盐酸且保持过量,然后进行的操作依次为
(4)将H2S气体通入FeCl3溶液中会出现浑浊,则其反应的离子方程式为
(5)铁铬氯化还原液流电池是一种低成本的储能电池,电池结构如右图所示(电极材料为石墨),工作原理为:
 ,则电池放电时,Cl-将移向
,则电池放电时,Cl-将移向
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】为了除去下列物质中的少量杂质(括号内为杂质)。请在空白处填入适当的试剂:
| 物质 | 试剂 | 物质 | 试剂 |
| CuO(Al2O3) | | FeCl3溶液(FeCl2) | |
| NaHCO3溶液(Na2CO3) | | Fe(Al) | |
| CO2(HCl) | | Cu(Zn) | |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)完成下列基本计算:
①3.6 g H2O的物质的量为______ mol;
②分子数为3.01×1023的H2的物质的量为______ mol;
③标准状况下,8.96 L N2的物质的量为______ mol;
④75 mL 2.0 mol·L-1 CaCl2溶液中含CaCl2______ mol。
(2)选出下列各小题物质分离或提纯所依据的物理性质和分离方法______ 。
性质差异:A、溶解度随温度变化差异 B、在不同溶剂中的溶解度差异
C、沸点差异 D、互不相溶 E、在水中的溶解度差异
分离方法:a、蒸馏 b、过滤 c、分液 d、萃取 e、结晶
(3)工业电解食盐水制取氯气的化学方程式:_____________________________________ 。
①3.6 g H2O的物质的量为
②分子数为3.01×1023的H2的物质的量为
③标准状况下,8.96 L N2的物质的量为
④75 mL 2.0 mol·L-1 CaCl2溶液中含CaCl2
(2)选出下列各小题物质分离或提纯所依据的物理性质和分离方法
| 性质差异 | 分离方法 | |
| ①除去氯化钠溶液中的泥沙 | ||
| ②用四氯化碳提取溴水中的溴单质 | ||
| ③分离乙酸(沸点1180C)与乙酸乙酯(沸点77.10C) | ||
| ④分离汽油和水 | ||
| ⑤从含有少量NaCl的KNO3溶液中提取KNO3 |
性质差异:A、溶解度随温度变化差异 B、在不同溶剂中的溶解度差异
C、沸点差异 D、互不相溶 E、在水中的溶解度差异
分离方法:a、蒸馏 b、过滤 c、分液 d、萃取 e、结晶
(3)工业电解食盐水制取氯气的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.某校化学一兴趣小组在社会实践活动中,考察了当地某工厂的废水(无色)处理流程,并取该厂未经处理的废水样品进行实验分析。

已知: 固体难溶于硝酸。
固体难溶于硝酸。
(1)取少量废水,向其中滴入紫色石蕊试液,溶液变红,该废水呈_______ (填“酸性”或“碱性”),说明废水中含有较大量的_______ (填离子符号),建议该厂用_______ (填化学式)处理废水。
(2)另取少量废水,滴加适量 溶液,有白色沉淀产生,说明该废水中一定含有的离子是
溶液,有白色沉淀产生,说明该废水中一定含有的离子是_______ ,其离子反应方程式为_______ 。
(3)已知该工厂废水中除含有以上离子外,还含有较多的 。该兴趣小组另取少量废水进行如图所示实验。开始时,试管中无明显现象,原因是
。该兴趣小组另取少量废水进行如图所示实验。开始时,试管中无明显现象,原因是_______ ;随试剂的滴加,试管中出现的现象是_______ ,该反应的离子方程式为_______ 。
Ⅱ.另一兴趣小组在实验室中尝试制备氢氧化铁胶体并探究它的性质。
(4)判断胶体的制备是否成功,可利用胶体的_______
(5)向 胶体中逐滴加入了稀
胶体中逐滴加入了稀 溶液,结果出现了一系列变化:
溶液,结果出现了一系列变化:
①先出现红褐色沉淀,原因是_______ 。
②随后沉淀溶解,此反应的离子方程式是_______ 。

已知:
 固体难溶于硝酸。
固体难溶于硝酸。(1)取少量废水,向其中滴入紫色石蕊试液,溶液变红,该废水呈
(2)另取少量废水,滴加适量
 溶液,有白色沉淀产生,说明该废水中一定含有的离子是
溶液,有白色沉淀产生,说明该废水中一定含有的离子是(3)已知该工厂废水中除含有以上离子外,还含有较多的
 。该兴趣小组另取少量废水进行如图所示实验。开始时,试管中无明显现象,原因是
。该兴趣小组另取少量废水进行如图所示实验。开始时,试管中无明显现象,原因是Ⅱ.另一兴趣小组在实验室中尝试制备氢氧化铁胶体并探究它的性质。
(4)判断胶体的制备是否成功,可利用胶体的
(5)向
 胶体中逐滴加入了稀
胶体中逐滴加入了稀 溶液,结果出现了一系列变化:
溶液,结果出现了一系列变化:①先出现红褐色沉淀,原因是
②随后沉淀溶解,此反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】工业上利用硫铁矿烧渣(主要成分为Fe2O3、FeO、SiO2等)为原料制备高档颜料铁红(Fe2O3),具体生产流程如下:

试回答下列问题:
(1)滤液X中含有的金属阳离子是_________ (填离子符号)。
(2)步骤Ⅲ中可选用________ 调节溶液的pH(填选项字母)。
(3)步骤Ⅳ中,FeCO3沉淀完全后,溶液中含有少量Fe2+,检验Fe2+的方法是________ 。
(4)步骤Ⅳ的反应温度一般需控制在35℃以下,其目的是_________ ,_______ 。
(5)在空气中煅烧FeCO3生成产品氧化铁的化学方程式为______________________ 。

试回答下列问题:
(1)滤液X中含有的金属阳离子是
(2)步骤Ⅲ中可选用
| A.稀硝酸 | B.氨水 | C.氢氧化钠溶液 | D.高锰酸钾溶液 |
(3)步骤Ⅳ中,FeCO3沉淀完全后,溶液中含有少量Fe2+,检验Fe2+的方法是
(4)步骤Ⅳ的反应温度一般需控制在35℃以下,其目的是
(5)在空气中煅烧FeCO3生成产品氧化铁的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】金属钛性能优越,被称为继铁、铝之后的“第三金属”,工业上用钛矿石(主要成分: FeO、TiO2、SiO2等)为原料制取钛并得到副产物绿矾(FeSO4·7H2O),工艺流程如下,回答下列问题:
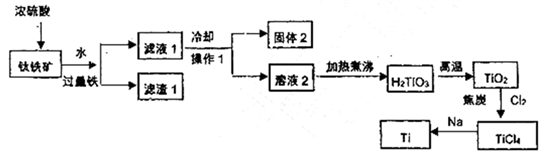
已知: ①TiO2(s)+H2SO4(aq)=TiOSO4(aq)+H2O(l)
②TiO2+易水解,只能存在于强酸性溶液中
(1)钛矿石在加入浓硫酸酸溶前要先粉碎,其目的是_____________ 。
(2)加入过量铁粉的目的是_____________ 。
(3)固体2 的主要成分是_____________ 。
(4)请用化学平衡移动原理解释溶液2 加热煮沸的目的_____________ 。
(5)在高温下,TiO2和焦炭的混合物中通入Cl2得到TiC14和一种可燃性气体,请写出反应的化学方程式_____________ 。

已知: ①TiO2(s)+H2SO4(aq)=TiOSO4(aq)+H2O(l)
②TiO2+易水解,只能存在于强酸性溶液中
(1)钛矿石在加入浓硫酸酸溶前要先粉碎,其目的是
(2)加入过量铁粉的目的是
(3)固体2 的主要成分是
(4)请用化学平衡移动原理解释溶液2 加热煮沸的目的
(5)在高温下,TiO2和焦炭的混合物中通入Cl2得到TiC14和一种可燃性气体,请写出反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】以硅藻土(主要成分为SiO2,含有少量的Fe2O3、 Al2O3) 为载体的V2O5-K2SO4常用作接触法制硫酸的催化剂。以下是一种废钒催化剂综合回收利用的工艺路线。
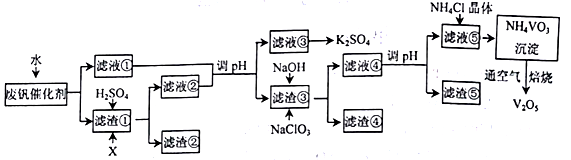
已知: 废钒催化剂中钒元素主要以VOSO4和V2O5形式存在;
V2O5是两性氧化物,不溶于水,溶于酸生成VO2+,溶于碱生成VO3-;
VOSO4是强电解质,溶于水电离出VO2+。
回答下列问题:
(1)VOSO4中V 元素的化合价为___________ 。
(2)滤渣①酸溶后加入的最佳试剂X 为_________ 。
a.NaClO b.Na2SO3c.K2SO3d.K2S
(3)从滤液③中得到产品K2SO4的操作为_________ 。滤渣③除含有V2O2(OH)4,还含有_________ 。
(4)若滤液⑤中c(VO3-)=0.1mol·L-1,为使钒元素的沉淀率达到98%,至少应调节c(NH4+)为_________ [Ksp(NH4VO3)=1.6×10-3]。
(5)“焙烧”时通入足量的空气,反应后的尾气可以直接排放。该反应的化学方程式为____________ 。
(6) V2O5纯度测定原理: 称取V2O5产品ag,先加入硫酸将V2O5转化为VO2+,再加入V1 mLc1mol·L-1(NH4) 2Fe(SO4) 2溶液将VO2+转 化为VO2+,最 后 用c2mol·L-1KMnO4 溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗KMnO4溶液V2mL。假设杂质不参与反应,实验测得某V2O5产品的纯度为91%,则理论上加入(NH4)2Fe(SO4)2溶液的体积V1至少_________ mL (用相关字母表示)。

已知: 废钒催化剂中钒元素主要以VOSO4和V2O5形式存在;
V2O5是两性氧化物,不溶于水,溶于酸生成VO2+,溶于碱生成VO3-;
VOSO4是强电解质,溶于水电离出VO2+。
回答下列问题:
(1)VOSO4中V 元素的化合价为
(2)滤渣①酸溶后加入的最佳试剂X 为
a.NaClO b.Na2SO3c.K2SO3d.K2S
(3)从滤液③中得到产品K2SO4的操作为
(4)若滤液⑤中c(VO3-)=0.1mol·L-1,为使钒元素的沉淀率达到98%,至少应调节c(NH4+)为
(5)“焙烧”时通入足量的空气,反应后的尾气可以直接排放。该反应的化学方程式为
(6) V2O5纯度测定原理: 称取V2O5产品ag,先加入硫酸将V2O5转化为VO2+,再加入V1 mLc1mol·L-1(NH4) 2Fe(SO4) 2溶液将VO2+转 化为VO2+,最 后 用c2mol·L-1KMnO4 溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗KMnO4溶液V2mL。假设杂质不参与反应,实验测得某V2O5产品的纯度为91%,则理论上加入(NH4)2Fe(SO4)2溶液的体积V1至少
您最近一年使用:0次



