I.某校化学一兴趣小组在社会实践活动中,考察了当地某工厂的废水(无色)处理流程,并取该厂未经处理的废水样品进行实验分析。

已知: 固体难溶于硝酸。
固体难溶于硝酸。
(1)取少量废水,向其中滴入紫色石蕊试液,溶液变红,该废水呈_______ (填“酸性”或“碱性”),说明废水中含有较大量的_______ (填离子符号),建议该厂用_______ (填化学式)处理废水。
(2)另取少量废水,滴加适量 溶液,有白色沉淀产生,说明该废水中一定含有的离子是
溶液,有白色沉淀产生,说明该废水中一定含有的离子是_______ ,其离子反应方程式为_______ 。
(3)已知该工厂废水中除含有以上离子外,还含有较多的 。该兴趣小组另取少量废水进行如图所示实验。开始时,试管中无明显现象,原因是
。该兴趣小组另取少量废水进行如图所示实验。开始时,试管中无明显现象,原因是_______ ;随试剂的滴加,试管中出现的现象是_______ ,该反应的离子方程式为_______ 。
Ⅱ.另一兴趣小组在实验室中尝试制备氢氧化铁胶体并探究它的性质。
(4)判断胶体的制备是否成功,可利用胶体的_______
(5)向 胶体中逐滴加入了稀
胶体中逐滴加入了稀 溶液,结果出现了一系列变化:
溶液,结果出现了一系列变化:
①先出现红褐色沉淀,原因是_______ 。
②随后沉淀溶解,此反应的离子方程式是_______ 。

已知:
 固体难溶于硝酸。
固体难溶于硝酸。(1)取少量废水,向其中滴入紫色石蕊试液,溶液变红,该废水呈
(2)另取少量废水,滴加适量
 溶液,有白色沉淀产生,说明该废水中一定含有的离子是
溶液,有白色沉淀产生,说明该废水中一定含有的离子是(3)已知该工厂废水中除含有以上离子外,还含有较多的
 。该兴趣小组另取少量废水进行如图所示实验。开始时,试管中无明显现象,原因是
。该兴趣小组另取少量废水进行如图所示实验。开始时,试管中无明显现象,原因是Ⅱ.另一兴趣小组在实验室中尝试制备氢氧化铁胶体并探究它的性质。
(4)判断胶体的制备是否成功,可利用胶体的
(5)向
 胶体中逐滴加入了稀
胶体中逐滴加入了稀 溶液,结果出现了一系列变化:
溶液,结果出现了一系列变化:①先出现红褐色沉淀,原因是
②随后沉淀溶解,此反应的离子方程式是
更新时间:2023-10-17 09:17:45
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】利用如图所示的“价-类”二维图,可以从物质类别、化合价角度认识含氯元素的物质的性质及其转化关系,图中甲~辛均为含氯元素的物质。回答下列问题:
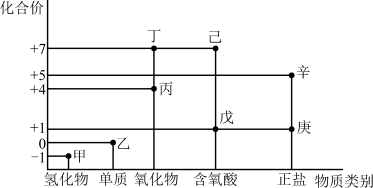
(1)戊的化学式为_______ 。
(2)甲、乙、丙中,属于非电解质的是_______ (填化学式)。根据氯元素的化合价判断乙_______ (填序号)。
a.只有氧化性 b.只有还原性 c.既有氧化性又有还原性
(3)庚是“84”消毒液的有效成分,能有效灭菌,某化学社团模拟生产厂家配制了 “84消毒液”,并在瓶体贴上标签,如图所示,回答下列问题:
“84消毒液”,并在瓶体贴上标签,如图所示,回答下列问题:
①写出氯气和 溶液生产此消毒液的离子方程式
溶液生产此消毒液的离子方程式_______ 。该“84消毒液”有效成分的物质的量浓度为_______ 。
②“84消毒液”与稀硫酸混合使用可增强消毒能力,该社团成员用 的浓硫酸配制
的浓硫酸配制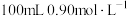 的稀硫酸用于增强“84消毒液”的消毒能力。若所配制的稀硫酸浓度偏高,则可能的原因是
的稀硫酸用于增强“84消毒液”的消毒能力。若所配制的稀硫酸浓度偏高,则可能的原因是_______ 。
A.配制前,容量瓶中有少量蒸馏水
B.量取浓硫酸时,仰视液体的凹液面
C.未冷却,立即转移至容量瓶定容
D.未洗涤烧杯和玻璃棒

(1)戊的化学式为
(2)甲、乙、丙中,属于非电解质的是
a.只有氧化性 b.只有还原性 c.既有氧化性又有还原性
(3)庚是“84”消毒液的有效成分,能有效灭菌,某化学社团模拟生产厂家配制了
 “84消毒液”,并在瓶体贴上标签,如图所示,回答下列问题:
“84消毒液”,并在瓶体贴上标签,如图所示,回答下列问题:| 84消毒液 |
(有效成分) (规格)  (质量分数) 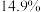 (密度)  |
 溶液生产此消毒液的离子方程式
溶液生产此消毒液的离子方程式②“84消毒液”与稀硫酸混合使用可增强消毒能力,该社团成员用
 的浓硫酸配制
的浓硫酸配制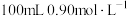 的稀硫酸用于增强“84消毒液”的消毒能力。若所配制的稀硫酸浓度偏高,则可能的原因是
的稀硫酸用于增强“84消毒液”的消毒能力。若所配制的稀硫酸浓度偏高,则可能的原因是A.配制前,容量瓶中有少量蒸馏水
B.量取浓硫酸时,仰视液体的凹液面
C.未冷却,立即转移至容量瓶定容
D.未洗涤烧杯和玻璃棒
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按要求填空:
(1)碳酸钡和足量的稀硝酸反应(写出离子方程式)___________________________ 。
(2)氢氧化钡溶液和硫酸镁溶液(写出离子方程式)___________________________ 。
(3)在澄清石灰水中加入过量碳酸氢钠溶液(写出离子方程式)_______________________ 。
(4)用双线桥标出下述反应中电子转移的方向和数目:_______________________ 。
C + 4HNO3(浓) CO2↑ + 4NO2↑+2H2O
CO2↑ + 4NO2↑+2H2O
(1)碳酸钡和足量的稀硝酸反应(写出离子方程式)
(2)氢氧化钡溶液和硫酸镁溶液(写出离子方程式)
(3)在澄清石灰水中加入过量碳酸氢钠溶液(写出离子方程式)
(4)用双线桥标出下述反应中电子转移的方向和数目:
C + 4HNO3(浓)
 CO2↑ + 4NO2↑+2H2O
CO2↑ + 4NO2↑+2H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】铝和铝合金是一类重要的金属材料。回答下列问题:
(1)除去镁粉中混有少量铝粉,应加入的试剂为_______ ,发生反应的离子方程式为_______ ,然后经过滤、洗涤、干燥。
(2)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得 在同温同压下的体积之比是
在同温同压下的体积之比是_______ 。
(3)氢氧化亚铁在空气中会逐渐被氧化为氢氧化铁,其化学方程式为_______ 。
(4)某同学在实验室用铝土矿(含有 和
和 ,不考虑其他杂质)制取金属铝的流程如下:
,不考虑其他杂质)制取金属铝的流程如下:_______ 。
② 与稀硫酸反应的离子方程式为
与稀硫酸反应的离子方程式为_______ 。
③滤液II中溶质的用途之一是_______ 。
(1)除去镁粉中混有少量铝粉,应加入的试剂为
(2)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得
 在同温同压下的体积之比是
在同温同压下的体积之比是(3)氢氧化亚铁在空气中会逐渐被氧化为氢氧化铁,其化学方程式为
(4)某同学在实验室用铝土矿(含有
 和
和 ,不考虑其他杂质)制取金属铝的流程如下:
,不考虑其他杂质)制取金属铝的流程如下:
②
 与稀硫酸反应的离子方程式为
与稀硫酸反应的离子方程式为③滤液II中溶质的用途之一是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】判断下列各组离子在指定溶液里能否共存。
(1)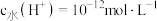 的溶液:
的溶液:
________
(2)使酚酞变红色的溶液:
________
(3)常温下, 的溶液:
的溶液:
________
(4) 的溶液:
的溶液:
________
(5)使 试纸显蓝色的溶液:
试纸显蓝色的溶液: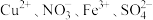
________
(6)与铝粉反应放出 的无色溶液:
的无色溶液: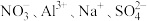
________
(7)使红色石蕊试纸变蓝的溶液:
________
(8)常温下,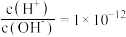 的溶液:
的溶液: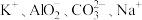
________
(9)中性溶液:
________
(10)使甲基橙变红色的溶液:
________
(1)
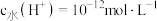 的溶液:
的溶液:
(2)使酚酞变红色的溶液:

(3)常温下,
 的溶液:
的溶液:
(4)
 的溶液:
的溶液:
(5)使
 试纸显蓝色的溶液:
试纸显蓝色的溶液: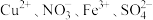
(6)与铝粉反应放出
 的无色溶液:
的无色溶液: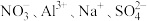
(7)使红色石蕊试纸变蓝的溶液:

(8)常温下,
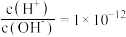 的溶液:
的溶液: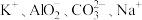
(9)中性溶液:

(10)使甲基橙变红色的溶液:

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)写出下列反应的化学方程式,并且①用单线桥、②用双线桥法标出反应中电子转移的情况,并按要求填空
①实验室用高锰酸钾制取氧气:___________ ;还原产物是___________
②在呼吸面具中二氧化碳与过氧化钠反应___________ ;还原剂是___________
(2)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为:3ClO-+2Fe3++10OH-=2FeO2-+3Cl-+5H2O
①分析元素化合价的变化(填“升高”或“降低”或“不变”)
Cl___________ O___________ Fe___________ H___________
②分析该氧化还原反应,其中氧化剂为___________ 还原剂为___________ 氧化产物为___________ 还原产物为___________
(3)将下列离子K+、Na+、Cu2+、H+、NO 、Cl-、CO
、Cl-、CO 、OH-按可能大量共存于同一溶液的情况,把它们分成A、B两组,每组中均含两种阳离子和两种阴离子。若在A中滴入石蕊溶液,可观察到溶液从无色变为红色;若向B中滴入酚酞试剂,可观察到溶液从无色变为红色。则:A组所含离子为
、OH-按可能大量共存于同一溶液的情况,把它们分成A、B两组,每组中均含两种阳离子和两种阴离子。若在A中滴入石蕊溶液,可观察到溶液从无色变为红色;若向B中滴入酚酞试剂,可观察到溶液从无色变为红色。则:A组所含离子为___________ ;B组所含离子为___________ 。
(1)写出下列反应的化学方程式,并且①用单线桥、②用双线桥法标出反应中电子转移的情况,并按要求填空
①实验室用高锰酸钾制取氧气:
②在呼吸面具中二氧化碳与过氧化钠反应
(2)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为:3ClO-+2Fe3++10OH-=2FeO2-+3Cl-+5H2O
①分析元素化合价的变化(填“升高”或“降低”或“不变”)
Cl
②分析该氧化还原反应,其中氧化剂为
(3)将下列离子K+、Na+、Cu2+、H+、NO
 、Cl-、CO
、Cl-、CO 、OH-按可能大量共存于同一溶液的情况,把它们分成A、B两组,每组中均含两种阳离子和两种阴离子。若在A中滴入石蕊溶液,可观察到溶液从无色变为红色;若向B中滴入酚酞试剂,可观察到溶液从无色变为红色。则:A组所含离子为
、OH-按可能大量共存于同一溶液的情况,把它们分成A、B两组,每组中均含两种阳离子和两种阴离子。若在A中滴入石蕊溶液,可观察到溶液从无色变为红色;若向B中滴入酚酞试剂,可观察到溶液从无色变为红色。则:A组所含离子为
您最近一年使用:0次
填空题
|
适中
(0.65)
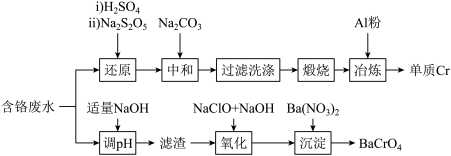
【推荐1】铬元素是一种重金属元素,工业上处理含铬废水并将其资源化的工艺有多种,其中两种工艺如下图所示: 和
和 两种价态,
两种价态, 价铬在酸性环境中氧化性更强。
价铬在酸性环境中氧化性更强。
② 。
。
回答下列问题:
(1)“还原”时,先加入 酸化,再加入
酸化,再加入 固体,其发生反应的离子方程式为
固体,其发生反应的离子方程式为_____ ,
(2)“中和”过程中,有大量气泡生成,写出中和时产生 的离子方程式:
的离子方程式:_____ 。
(3)“氧化”时,发生反应的化学方程式为:_____ 。
 和
和 两种价态,
两种价态, 价铬在酸性环境中氧化性更强。
价铬在酸性环境中氧化性更强。②
 。
。回答下列问题:
(1)“还原”时,先加入
 酸化,再加入
酸化,再加入 固体,其发生反应的离子方程式为
固体,其发生反应的离子方程式为(2)“中和”过程中,有大量气泡生成,写出中和时产生
 的离子方程式:
的离子方程式:(3)“氧化”时,发生反应的化学方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】用化学方法除去下列物质中混有的少量杂质,其中括号内为杂质,写出除杂需加入的试剂(用化学式表示)以及发生反应的离子方程式。
(1)固体Na2CO3(NaHCO3)除杂发生反应的化学方程式___ ;
(2)固体Fe(OH)3(Al(OH)3)除杂发生反应的离子方程式____ ;
(3)溶液FeCl2(CuCl2)除杂发生反应的离子方程式____ ;
(4)气体CO2(HCl)除杂发生反应的离子方程式___ 。
(1)固体Na2CO3(NaHCO3)除杂发生反应的化学方程式
(2)固体Fe(OH)3(Al(OH)3)除杂发生反应的离子方程式
(3)溶液FeCl2(CuCl2)除杂发生反应的离子方程式
(4)气体CO2(HCl)除杂发生反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】溴元素和碘元素在工农业生产和日常生活中有着广泛应用。根据信息,完成下列填空。
Ⅰ.下图是从海水中提取粗溴的主要流程

(1)步骤①中,海水通过___________ (操作名称)、趁热过滤,得到苦卤;步骤②选用 作氧化剂,请写出发生反应的离子方程式
作氧化剂,请写出发生反应的离子方程式______ 。
(2)可用热空气吹出溴是因为溴的___________(选填编号)
(3)下列关于含溴化合物的用途说法错误的是___________(选填编号)
Ⅱ.实验小组从海带中提取碘
(4)将干海带经过浸泡、_____ (操作名称),得到滤液
(5)用如图所示的仪器提取碘水中的碘。该仪器名称为___________ ,该步操作的名称为___________ ;图示的提取剂可以是___________ (选填编号)。
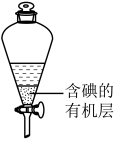
a.酒精b.苯c.四氯化碳d.醋酸
碘在该溶剂中显___________ 色
Ⅰ.下图是从海水中提取粗溴的主要流程

(1)步骤①中,海水通过
 作氧化剂,请写出发生反应的离子方程式
作氧化剂,请写出发生反应的离子方程式(2)可用热空气吹出溴是因为溴的___________(选填编号)
| A.熔点较低 | B.熔点较高 | C.沸点较低 | D.沸点较高 |
| A.食盐添加剂 | B.杀虫剂 | C.镇静剂 | D.感光材料 |
Ⅱ.实验小组从海带中提取碘
(4)将干海带经过浸泡、
(5)用如图所示的仪器提取碘水中的碘。该仪器名称为

a.酒精b.苯c.四氯化碳d.醋酸
碘在该溶剂中显
您最近一年使用:0次

 、
、 、Cl-、OH-中的一种或几种。
、Cl-、OH-中的一种或几种。

