用化学方法除去下列物质中混有的少量杂质,其中括号内为杂质,写出除杂需加入的试剂(用化学式表示)以及发生反应的离子方程式。
(1)固体Na2CO3(NaHCO3)除杂发生反应的化学方程式___ ;
(2)固体Fe(OH)3(Al(OH)3)除杂发生反应的离子方程式____ ;
(3)溶液FeCl2(CuCl2)除杂发生反应的离子方程式____ ;
(4)气体CO2(HCl)除杂发生反应的离子方程式___ 。
(1)固体Na2CO3(NaHCO3)除杂发生反应的化学方程式
(2)固体Fe(OH)3(Al(OH)3)除杂发生反应的离子方程式
(3)溶液FeCl2(CuCl2)除杂发生反应的离子方程式
(4)气体CO2(HCl)除杂发生反应的离子方程式
更新时间:2020-01-14 15:11:34
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氧化还原反应在高中化学中是一类重要的反应类型。KMnO4、FeCl3是中学化学中常用的氧化剂。回答下列问题:
(1)下列基本反应类型中一定属于氧化还原反应的是_______(填字母)。
(2)实验室迅速制备少量氯气可利用如下反应:KMnO4+HCl(浓)→KCl+MnCl2+Cl2↑+H2O(未配平)。
①上述反应中被还原的元素为_______ (填元素符号)。
② 与Fe2+反应生成Mn2+,Fe2+发生
与Fe2+反应生成Mn2+,Fe2+发生_______ 反应(填“氧化”或“还原”。)
③配平以下化学方程式并用双线桥标出电子转移的方向和数目:_______ 。 。
。
(3)FeCl3溶液能与Cu反应制作印刷电路板。其制作原理可用 表示。
表示。
①上式中X的化学式为_______ 。
②该反应的离子方程式为_______ 。
(1)下列基本反应类型中一定属于氧化还原反应的是_______(填字母)。
| A.化合反应 | B.分解反应 | C.置换反应 | D.复分解反应 |
①上述反应中被还原的元素为
②
 与Fe2+反应生成Mn2+,Fe2+发生
与Fe2+反应生成Mn2+,Fe2+发生③配平以下化学方程式并用双线桥标出电子转移的方向和数目:
 。
。(3)FeCl3溶液能与Cu反应制作印刷电路板。其制作原理可用
 表示。
表示。①上式中X的化学式为
②该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】写出下列反应离子方程式
(1)NaHCO3溶液与NaHSO4溶液反应:______________________________________ 。
(2)NaHCO3溶液与NaOH溶液反应:______________________________________ 。
(1)NaHCO3溶液与NaHSO4溶液反应:
(2)NaHCO3溶液与NaOH溶液反应:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.现有下列九种物质:① ②
② 溶液 ③
溶液 ③ ④盐酸 ⑤熔融
④盐酸 ⑤熔融 ⑥铜 ⑦苯 ⑧纯醋酸 ⑨硫酸氢钠
⑥铜 ⑦苯 ⑧纯醋酸 ⑨硫酸氢钠
(1)上述物质中属于电解质且能导电的是_______ (填序号,下同),属于非电解质的是_______ 。
(2)写出②在水中的电离方程式:_______ 。
(3)写出溶液②和⑨的溶液反应的离子方程式_______ 。
(4)写出向④中加入①的反应的离子方程式_______ 。
Ⅱ.写出下列反应的离子反应方程式
(5)实验室制备 :
:_______ 。
(6)实验室用 制备
制备 :
:_______ 。
(7)向氯化镁溶液滴加氨水:_______ 。
(8)等浓度、等体积的 溶液和
溶液和 溶液混合:
溶液混合:_______ 。
(9)用 溶液处理水垢中的
溶液处理水垢中的 :
:_______ 。
 ②
② 溶液 ③
溶液 ③ ④盐酸 ⑤熔融
④盐酸 ⑤熔融 ⑥铜 ⑦苯 ⑧纯醋酸 ⑨硫酸氢钠
⑥铜 ⑦苯 ⑧纯醋酸 ⑨硫酸氢钠(1)上述物质中属于电解质且能导电的是
(2)写出②在水中的电离方程式:
(3)写出溶液②和⑨的溶液反应的离子方程式
(4)写出向④中加入①的反应的离子方程式
Ⅱ.写出下列反应的离子反应方程式
(5)实验室制备
 :
:(6)实验室用
 制备
制备 :
:(7)向氯化镁溶液滴加氨水:
(8)等浓度、等体积的
 溶液和
溶液和 溶液混合:
溶液混合:(9)用
 溶液处理水垢中的
溶液处理水垢中的 :
:
您最近一年使用:0次
【推荐1】回答下列问题:
(1)现有NaOH、Na2CO3、Ba(OH)2三种无色溶液,选用一种试剂把他们鉴别出来,并写出反应的离子方程式。
①鉴别试剂____________ ;
②反应的离子方程式__________________ 、________________ 、________________ 。
(2)某工厂的废水中含有大量的FeSO4、较多的Cu2+和少量Na+。为了减少污染并变废为宝,工厂计划从该废水中回收FeSO4和Cu。请根据流程图,在方框和括号内填写物质的名称(或主要成分的化学式)或操作方法,完成回收FeSO4和Cu的简单实验方案。_____________ 、_____________ 、_____________ 、_____________ 、_____________ 、_____________ 、_____________ ,

(1)现有NaOH、Na2CO3、Ba(OH)2三种无色溶液,选用一种试剂把他们鉴别出来,并写出反应的离子方程式。
①鉴别试剂
②反应的离子方程式
(2)某工厂的废水中含有大量的FeSO4、较多的Cu2+和少量Na+。为了减少污染并变废为宝,工厂计划从该废水中回收FeSO4和Cu。请根据流程图,在方框和括号内填写物质的名称(或主要成分的化学式)或操作方法,完成回收FeSO4和Cu的简单实验方案。

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某溶液含Cl-、SO42-、CO32-三种阴离子,欲依次检验出此三种阴离子且只取用一次该溶液,则:
(1)最先检出的离子是____ ,需加入稍过量的试剂是____________ (写化学式);
(2)最后检出的离子是____ ,反应的离子方程式为___________________________ 。
(1)最先检出的离子是
(2)最后检出的离子是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】实验步骤
(1)除去不溶性杂质
①将粗盐倒入烧杯中,加适量水溶解,用玻璃棒搅拌;
②在过滤器上将粗盐水过滤,弃去沉淀,保留_______ 。
(2)去除杂质离子
①向烧杯中加入_______ ,边加边搅拌,直至______ 产生;
②再依次加入______ 和________ 溶液,边加边搅拌,直至______ 产生;
③将混合物在过滤器上过滤,弃去沉淀,保留_______ 。
(3)提纯
①向滤液中加入适量______ ,边加边搅拌,直至___________ 产生,用pH试纸测量溶液的pH,使溶液的pH_______ 7;
②将溶液转移至________ 中,用酒精灯加热蒸干。
(1)除去不溶性杂质
①将粗盐倒入烧杯中,加适量水溶解,用玻璃棒搅拌;
②在过滤器上将粗盐水过滤,弃去沉淀,保留
(2)去除杂质离子
①向烧杯中加入
②再依次加入
③将混合物在过滤器上过滤,弃去沉淀,保留
(3)提纯
①向滤液中加入适量
②将溶液转移至
您最近一年使用:0次
【推荐1】为达到下表中的实验目的,请选择合适的试剂及实验方法,将其标号填入对应的空格。
供选择的化学试剂及实验方法:
A.加热升华
B.向溶液中通入足量的CO2气体
C.分别通入品红溶液中,观察现象
D.取样,加盐酸酸化的BaCl2溶液,观察现象
| 序号 | 实验目的 | 试剂及方法 |
| (1) | 鉴别CO2和SO2气体 | |
| (2) | 除去食盐中混有的少量碘 | |
| (3) | 检验Na2SO3溶液中是否含有Na2SO4 | |
| (4) | 除去NaHCO3溶液中混有的Na2CO3 |
供选择的化学试剂及实验方法:
A.加热升华
B.向溶液中通入足量的CO2气体
C.分别通入品红溶液中,观察现象
D.取样,加盐酸酸化的BaCl2溶液,观察现象
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】除去下表内各物质中含有的少量杂质,写出除杂试剂,并填写分离方法。
| 序号 | 物质 | 杂质 | 所加试剂 | 分离方法 |
| (1) | NO | NO2 | ||
| (2) | Fe粉 | Al粉 | ||
| (3) | 氯化钠固体 | 氯化铵固体 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】N2O、NO和NO2等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
(1)N2O的处理。N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式为____ 。
(2)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH溶液吸收,吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是____ (填化学式);吸收后排放的尾气中含量较高的氮氧化物是____ (填化学式)
(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
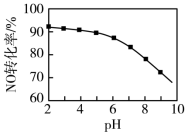
①在酸性NaClO溶液中,HClO氧化NO生成Cl-和NO ,其离子方程式为
,其离子方程式为____ 。
②NaClO溶液的初始pH越小,NO转化率越高,其原因是____ 。
(1)N2O的处理。N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式为
(2)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH溶液吸收,吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是
(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。

①在酸性NaClO溶液中,HClO氧化NO生成Cl-和NO
 ,其离子方程式为
,其离子方程式为②NaClO溶液的初始pH越小,NO转化率越高,其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)滑石是一种硅酸盐矿物,其化学式为 ,用氧化物的形式表示为
,用氧化物的形式表示为__________ 。
(2)除去下列物质中所含杂质(括号内为杂质),写出除去杂质的试剂。
①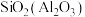
_____________
②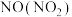
_____________
③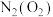
______________
④
___________
⑤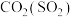
_____________
 ,用氧化物的形式表示为
,用氧化物的形式表示为(2)除去下列物质中所含杂质(括号内为杂质),写出除去杂质的试剂。
①
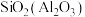
②
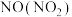
③
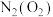
④

⑤
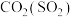
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】【化学---选修2:化学与技术】
南海某小岛上,可利用的淡水资源相当匮乏,解放军战士为了寻找合适的饮用水源,对岛上山泉水进行分析化验,结果显示山泉水属于硬水。
(1)硬水是指含有较多______________ 的水,硬水加热后产生沉淀的离子方程式为:________________________________ (写出生成一种沉淀物的即可) 。
(2)硬度为1°的水是指每升水含10 mg CaO或与之相当的物质(如7.1 mg MgO),已知水的硬度在8°以下的称为软水,在8°以上的称为硬水。已知岛上山泉水中c( Ca2+)=1.2×10-3 mol/L,c(Mg2+) =6×l0-4mol/L,那么此水______ (填“是”或“否”)属于硬水。
(3)离子交换法是软化水的常用方法。聚丙烯酸钠是一种离子交换树脂,写出聚丙烯酸钠单体的结构简式__________________ 。
(4)解放军战士通常向水中加入明矾净水,请用离子方程式解释其净水原理:______________ 。
(5)岛上还可以用海水淡化来获得淡水。下面是海水利用电渗析法获得淡水的原理图,已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极。请分析下列问题:

①阳离子交换膜是指___________ (填A或B)。
②写出通电后阳极区的电极反应式____________ ,阴极区的现象是:_______________ 。
南海某小岛上,可利用的淡水资源相当匮乏,解放军战士为了寻找合适的饮用水源,对岛上山泉水进行分析化验,结果显示山泉水属于硬水。
(1)硬水是指含有较多
(2)硬度为1°的水是指每升水含10 mg CaO或与之相当的物质(如7.1 mg MgO),已知水的硬度在8°以下的称为软水,在8°以上的称为硬水。已知岛上山泉水中c( Ca2+)=1.2×10-3 mol/L,c(Mg2+) =6×l0-4mol/L,那么此水
(3)离子交换法是软化水的常用方法。聚丙烯酸钠是一种离子交换树脂,写出聚丙烯酸钠单体的结构简式
(4)解放军战士通常向水中加入明矾净水,请用离子方程式解释其净水原理:
(5)岛上还可以用海水淡化来获得淡水。下面是海水利用电渗析法获得淡水的原理图,已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极。请分析下列问题:

①阳离子交换膜是指
②写出通电后阳极区的电极反应式
您最近一年使用:0次

 溶液的浓度,甲、乙两同学设计了两个方案。回答下列问题:
溶液的浓度,甲、乙两同学设计了两个方案。回答下列问题:

 沉淀完全的操作为
沉淀完全的操作为

