【化学---选修2:化学与技术】
南海某小岛上,可利用的淡水资源相当匮乏,解放军战士为了寻找合适的饮用水源,对岛上山泉水进行分析化验,结果显示山泉水属于硬水。
(1)硬水是指含有较多______________ 的水,硬水加热后产生沉淀的离子方程式为:________________________________ (写出生成一种沉淀物的即可) 。
(2)硬度为1°的水是指每升水含10 mg CaO或与之相当的物质(如7.1 mg MgO),已知水的硬度在8°以下的称为软水,在8°以上的称为硬水。已知岛上山泉水中c( Ca2+)=1.2×10-3 mol/L,c(Mg2+) =6×l0-4mol/L,那么此水______ (填“是”或“否”)属于硬水。
(3)离子交换法是软化水的常用方法。聚丙烯酸钠是一种离子交换树脂,写出聚丙烯酸钠单体的结构简式__________________ 。
(4)解放军战士通常向水中加入明矾净水,请用离子方程式解释其净水原理:______________ 。
(5)岛上还可以用海水淡化来获得淡水。下面是海水利用电渗析法获得淡水的原理图,已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极。请分析下列问题:

①阳离子交换膜是指___________ (填A或B)。
②写出通电后阳极区的电极反应式____________ ,阴极区的现象是:_______________ 。
南海某小岛上,可利用的淡水资源相当匮乏,解放军战士为了寻找合适的饮用水源,对岛上山泉水进行分析化验,结果显示山泉水属于硬水。
(1)硬水是指含有较多
(2)硬度为1°的水是指每升水含10 mg CaO或与之相当的物质(如7.1 mg MgO),已知水的硬度在8°以下的称为软水,在8°以上的称为硬水。已知岛上山泉水中c( Ca2+)=1.2×10-3 mol/L,c(Mg2+) =6×l0-4mol/L,那么此水
(3)离子交换法是软化水的常用方法。聚丙烯酸钠是一种离子交换树脂,写出聚丙烯酸钠单体的结构简式
(4)解放军战士通常向水中加入明矾净水,请用离子方程式解释其净水原理:
(5)岛上还可以用海水淡化来获得淡水。下面是海水利用电渗析法获得淡水的原理图,已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极。请分析下列问题:

①阳离子交换膜是指
②写出通电后阳极区的电极反应式
更新时间:2016-12-09 10:00:40
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】现有下列几种物质:
①Al2O3、②CuO、③NaHSO4、④FeCl3、⑤Cl2、⑥NaOH、⑦稀硫酸。回答下列问题:
(1)上述物质中属于碱性氧化物的是___________ (填序号,下同),属于两性氧化物的是___________ ,属于混合物的是___________ 。
(2)上述物质在水中能电离出三种离子的是___________ (填序号);写出④的电离方程式:___________ 。
(3)写出①与⑦反应的离子方程式:___________ 。
①Al2O3、②CuO、③NaHSO4、④FeCl3、⑤Cl2、⑥NaOH、⑦稀硫酸。回答下列问题:
(1)上述物质中属于碱性氧化物的是
(2)上述物质在水中能电离出三种离子的是
(3)写出①与⑦反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在抗击新冠肺炎疫情的战役中,病毒在不断发生变异,现有疫苗对变异病毒的有效性有待进一步的验证,因此民众的防疫意识不能松懈。
(1)口罩作为基础防疫物资,可以有效防止飞沫的传播。最新的研究表明新冠病毒可能通过气溶胶传播。气溶胶属于________ (填“胶体”或“溶液”);常利用________ 区分溶液和胶体。
(2)为有效防止新冠病毒的传播,除了戴口罩,还需加强对隔离场所的消毒。常用的消毒剂有双氧水、医用酒精以及含氯消毒剂。其中含氯消毒剂的家族最庞大、应用最广泛。实验室制备 有三种常用方法:
有三种常用方法:
a.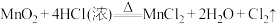
b.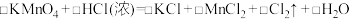
c.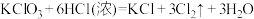
①常温下,医用酒精、 、
、 、
、 、浓盐酸中属于混合物的是
、浓盐酸中属于混合物的是________ ;属于电解质的是________ 。
②写出反应a对应的离子方程式________ 。
③配平反应b的方程式________ 。
④当三个反应中参与反应的HCl的质量相同时,得到 的质量最多的是反应
的质量最多的是反应________ (填“a”、“b”、“c”)。
(1)口罩作为基础防疫物资,可以有效防止飞沫的传播。最新的研究表明新冠病毒可能通过气溶胶传播。气溶胶属于
(2)为有效防止新冠病毒的传播,除了戴口罩,还需加强对隔离场所的消毒。常用的消毒剂有双氧水、医用酒精以及含氯消毒剂。其中含氯消毒剂的家族最庞大、应用最广泛。实验室制备
 有三种常用方法:
有三种常用方法:a.
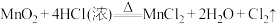
b.
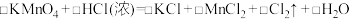
c.
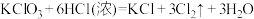
①常温下,医用酒精、
 、
、 、
、 、浓盐酸中属于混合物的是
、浓盐酸中属于混合物的是②写出反应a对应的离子方程式
③配平反应b的方程式
④当三个反应中参与反应的HCl的质量相同时,得到
 的质量最多的是反应
的质量最多的是反应
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)BiCl3的水解产物中有BiOCl生成。
①写出BiCl3水解反应的方程式:_________________________ 。
②医药上将BiOCl称为次氯酸铋,该名称____________ (填“正确”或“不正确”)。
③如何配制BiCl3溶液?_________________________________ 。
(2)将pH=2的某酸HnA与pH=12的某碱B(OH)m等体积混合后溶液的pH=8。
①若生成的盐中只有一种离子水解,该离子水解的离子方程式为_____________________ 。
②简述该混合液呈碱性的原因______________________ 。
①写出BiCl3水解反应的方程式:
②医药上将BiOCl称为次氯酸铋,该名称
③如何配制BiCl3溶液?
(2)将pH=2的某酸HnA与pH=12的某碱B(OH)m等体积混合后溶液的pH=8。
①若生成的盐中只有一种离子水解,该离子水解的离子方程式为
②简述该混合液呈碱性的原因
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题
学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理 请回答下列问题:
请回答下列问题:
(1)常温下,某纯碱溶液中滴入酚酞,溶液呈红色,则该溶液呈______ 性,原因是________________ ; 用离子方程式表示
用离子方程式表示
(2)在常温下将pH=2的盐酸10mL加水稀释到1L,则稀释后的溶液的pH值等于______________ ;
(3)已知在H2S溶液中存在下列平衡: H2S H++HS-
H++HS-
向H2S溶液中加入NaOH固体时, 不考虑温度变化
不考虑温度变化 电离平衡向
电离平衡向______ 移动, 填“左”或“右”),c(H+)
填“左”或“右”),c(H+)______ 。(填“增大”、“减小”或“不变”
向H2S溶液中加入NaHS固体时,电离平衡向______ 移动, 填“左”或“右”)c(S2—)
填“左”或“右”)c(S2—)______ 。(填“增大”、“减小”或“不变”)

(4)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示。则图中表示醋酸溶液中pH变化曲线的是______  填“A”或“B”
填“A”或“B” ;设盐酸中加入的Zn质量为m1,醋酸溶液中加入的Zn质量为m2,则m1
;设盐酸中加入的Zn质量为m1,醋酸溶液中加入的Zn质量为m2,则m1______ m2。 (选填“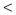 ”、“
”、“ ”、“
”、“ ”
”
学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理
 请回答下列问题:
请回答下列问题: (1)常温下,某纯碱溶液中滴入酚酞,溶液呈红色,则该溶液呈
 用离子方程式表示
用离子方程式表示
(2)在常温下将pH=2的盐酸10mL加水稀释到1L,则稀释后的溶液的pH值等于
(3)已知在H2S溶液中存在下列平衡: H2S
 H++HS-
H++HS-向H2S溶液中加入NaOH固体时,
 不考虑温度变化
不考虑温度变化 电离平衡向
电离平衡向 填“左”或“右”),c(H+)
填“左”或“右”),c(H+)
向H2S溶液中加入NaHS固体时,电离平衡向
 填“左”或“右”)c(S2—)
填“左”或“右”)c(S2—)
(4)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示。则图中表示醋酸溶液中pH变化曲线的是
 填“A”或“B”
填“A”或“B” ;设盐酸中加入的Zn质量为m1,醋酸溶液中加入的Zn质量为m2,则m1
;设盐酸中加入的Zn质量为m1,醋酸溶液中加入的Zn质量为m2,则m1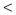 ”、“
”、“ ”、“
”、“ ”
”
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】镁的化合物具有广泛用途,请回答有关镁的下列问题:
(1)单质镁在空气中燃烧的主要产物是________ ,还生成少量的________ (填化学式)。
(2)物质的量为0.10mol的镁条在只含有CO2和O2混合气体的容器中燃烧(产物不含碳酸镁),反应后容器内固体物质的质量不可能为_____________
A.3.2g B.4.0g C.4.2g D.4.6g
(3)镁作为一种强还原剂,还用于钛和铀的生产,写出镁与TiCl4在高温条件下制取钛的化学方程式_______________ 。
(4)氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。Mg2Cu是一种储氢合金。350℃时,Mg2Cu与H2反应,生成MgCu2和仅含一种金属元素的氢化物(其中氢的质量分数为0.077),Mg2Cu与H2反应的化学方程式为___________ 。
(5)CH3MgCl是一种重要的有机合成剂,其中镁的化合价是__________ ,该化合物水解时生成甲烷、氯化镁和氢氧化镁,请写出该反应的化学方程式______________________ 。
(1)单质镁在空气中燃烧的主要产物是
(2)物质的量为0.10mol的镁条在只含有CO2和O2混合气体的容器中燃烧(产物不含碳酸镁),反应后容器内固体物质的质量不可能为
A.3.2g B.4.0g C.4.2g D.4.6g
(3)镁作为一种强还原剂,还用于钛和铀的生产,写出镁与TiCl4在高温条件下制取钛的化学方程式
(4)氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。Mg2Cu是一种储氢合金。350℃时,Mg2Cu与H2反应,生成MgCu2和仅含一种金属元素的氢化物(其中氢的质量分数为0.077),Mg2Cu与H2反应的化学方程式为
(5)CH3MgCl是一种重要的有机合成剂,其中镁的化合价是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】完成下列问题:
(1)某温度时,纯水的pH=6。该温度下0.01 mol/LNaOH溶液的pH=________ 。
(2)25℃时,已知:HB为一元酸, 0.1mol·L-1的 HB溶液的pH值为3,关于该溶液下列说法正确的是_________ 。
A.此溶液中不存在HB分子 B.升温,pH增大
C.加水稀释,c(OH-)增大. D.NaB溶液中c(H+)<c(OH-)
(3)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH3COO-)-c(Na+)=________ (填准确数值)。
(4)明矾能净水,其原理为:______________________ (用离子方程式解释)。
(5)氢氧化铜悬浊液中存在如下平衡:Cu(OH)2(s) Cu2+(aq)+2OH-(aq),常温下其Ksp=2×10-20。某硫酸铜溶液里c(Cu2+)=0.02 mol·L
Cu2+(aq)+2OH-(aq),常温下其Ksp=2×10-20。某硫酸铜溶液里c(Cu2+)=0.02 mol·L ,如要生成Cu(OH)2沉淀,应调整溶液使之pH>
,如要生成Cu(OH)2沉淀,应调整溶液使之pH>_______ 。
(1)某温度时,纯水的pH=6。该温度下0.01 mol/LNaOH溶液的pH=
(2)25℃时,已知:HB为一元酸, 0.1mol·L-1的 HB溶液的pH值为3,关于该溶液下列说法正确的是
A.此溶液中不存在HB分子 B.升温,pH增大
C.加水稀释,c(OH-)增大. D.NaB溶液中c(H+)<c(OH-)
(3)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH3COO-)-c(Na+)=
(4)明矾能净水,其原理为:
(5)氢氧化铜悬浊液中存在如下平衡:Cu(OH)2(s)
 Cu2+(aq)+2OH-(aq),常温下其Ksp=2×10-20。某硫酸铜溶液里c(Cu2+)=0.02 mol·L
Cu2+(aq)+2OH-(aq),常温下其Ksp=2×10-20。某硫酸铜溶液里c(Cu2+)=0.02 mol·L ,如要生成Cu(OH)2沉淀,应调整溶液使之pH>
,如要生成Cu(OH)2沉淀,应调整溶液使之pH>
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】电化学原理广泛应用于日常生活、生产和科学技术等方面,以满足不同的需要。根据如图所示装置,分别回答下列问题:
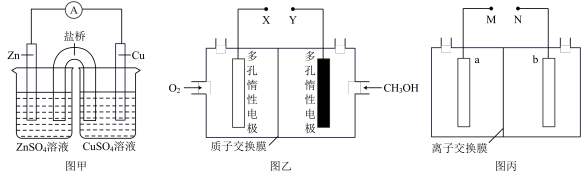
(1)图甲中电极电势Zn______ Cu(填“高于”、“低于”);盐桥中装有KCl饱和溶液,电池工作时盐桥中 将
将______
A.移向 溶液 B.移向
溶液 B.移向 溶液 C.不移动
溶液 C.不移动
(2)图乙为使用酸性电解液的甲醇燃料电池的工作原理示意图,其负极电极反应式为___________ ,工作时若消耗32g甲醇,则理论上左室溶液质量变化值为______ g
(3)图丙为模拟离子交换膜法电解饱和食盐水原理示意图,若以图乙装置为电源,a电极区得到烧碱溶液,则N应与图乙中______ 相连(填“X”、“Y”),图丙中用到______ 离子交换膜(填“阴”、“阳”),电解总反应离子方程式为__________________
(4)若将图丙中a、b电极换成Fe电极电解处理含 的废水,阳极电极反应式为
的废水,阳极电极反应式为______ ;25℃时,阳极区产生的离子将 转化为
转化为 后调节pH为5时,
后调节pH为5时, 完全沉淀(离子浓度为
完全沉淀(离子浓度为 ),调节溶液pH为7时,溶液中
),调节溶液pH为7时,溶液中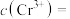
______ 

(1)图甲中电极电势Zn
 将
将A.移向
 溶液 B.移向
溶液 B.移向 溶液 C.不移动
溶液 C.不移动(2)图乙为使用酸性电解液的甲醇燃料电池的工作原理示意图,其负极电极反应式为
(3)图丙为模拟离子交换膜法电解饱和食盐水原理示意图,若以图乙装置为电源,a电极区得到烧碱溶液,则N应与图乙中
(4)若将图丙中a、b电极换成Fe电极电解处理含
 的废水,阳极电极反应式为
的废水,阳极电极反应式为 转化为
转化为 后调节pH为5时,
后调节pH为5时, 完全沉淀(离子浓度为
完全沉淀(离子浓度为 ),调节溶液pH为7时,溶液中
),调节溶液pH为7时,溶液中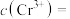

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
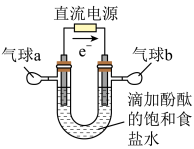
【推荐2】知识的梳理和感悟是有效学习的方法之一。某学习小组将有关“电解饱和食盐水”的相关内容进行梳理,形成如下问题(显示的电极均为石墨)。
(1)图中,电解一段时间后,气球b中的气体是_____ (填化学式),U形管_____ (填“左”或“右”)边的溶液变红。
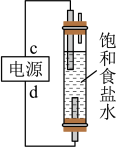
(2)利用图制作一种环保型消毒液发生器,可制备“84”消毒液的有效成分,则c为电源的_____ 极;该发生器中反应的总离子方程式为_____ 。
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。该工艺的相关物质运输与转化关系如图所示(其中的电极未标出,所用的离子膜都只允许阳离子通过)。

①燃料电池B中的电极反应式分别为
负极:_____ ,
正极:_____ 。
②分析图3可知,氢氧化钠的质量分数为a%、b%、c%,由大到小的顺序为_____ 。
(1)图中,电解一段时间后,气球b中的气体是

(2)利用图制作一种环保型消毒液发生器,可制备“84”消毒液的有效成分,则c为电源的

(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。该工艺的相关物质运输与转化关系如图所示(其中的电极未标出,所用的离子膜都只允许阳离子通过)。

①燃料电池B中的电极反应式分别为
负极:
正极:
②分析图3可知,氢氧化钠的质量分数为a%、b%、c%,由大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某化工厂的废液中,含有大量 溶液,但当中掺杂有一些
溶液,但当中掺杂有一些 、
、 ,为实现变废为宝,选择适当的试剂设计实验除去杂质,从而得到纯净的
,为实现变废为宝,选择适当的试剂设计实验除去杂质,从而得到纯净的 晶体,相应的实验流程如图所示。
晶体,相应的实验流程如图所示。

请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X_______ 。
(2)上述实验流程中加入过量 溶液后发生反应的离子方程式:
溶液后发生反应的离子方程式:_______ 、_______ 。
(3)上述实验流程中,其他不变,①②两步的试剂可否交换,请说明原因_______ 。
(4)(本小题两空均填化学式)按此实验方案得到的溶液3中肯定含有_______ 杂质。为了解决这个问题,可以向溶液3中加入适量的_______ 。
(5)在①步操作中如何证明加的 溶液已过量?
溶液已过量?_______ 。
 溶液,但当中掺杂有一些
溶液,但当中掺杂有一些 、
、 ,为实现变废为宝,选择适当的试剂设计实验除去杂质,从而得到纯净的
,为实现变废为宝,选择适当的试剂设计实验除去杂质,从而得到纯净的 晶体,相应的实验流程如图所示。
晶体,相应的实验流程如图所示。
请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X
(2)上述实验流程中加入过量
 溶液后发生反应的离子方程式:
溶液后发生反应的离子方程式:(3)上述实验流程中,其他不变,①②两步的试剂可否交换,请说明原因
(4)(本小题两空均填化学式)按此实验方案得到的溶液3中肯定含有
(5)在①步操作中如何证明加的
 溶液已过量?
溶液已过量?
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】海水是巨大的资源宝库。下图是从海水中提取食盐和溴的主要流程。

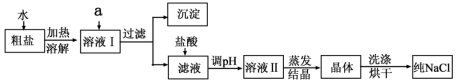
(1)粗盐除含NaCl外,还含有少量MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是粗盐提纯的操作流程。
提供的试剂:Na2CO3溶液、K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、饱和NaCl溶液。
①除去溶液I中的MgCl2、CaCl2、Na2SO4,从提供的试剂中选出a所代表的试剂,按滴加顺序依次为:过量的NaOH溶液、_____________ 、_____________ ;
②如何证明操作①中NaOH溶液已经过量?_______________________________________
③蒸发过程所用的主要仪器有:铁架台、酒精灯、_______________________ ;
(2)某同学欲用四氯化碳萃取较高浓度的溴水中的溴,经振荡并在铁架台上静置分层后,
①分离出四氯化碳层的具体操作 是:______ 。②分离碘的四氯化碳溶液的操作方法 是:________ 。
(3)工业上将较高浓度的溴水经进一步处理得到工业溴。某研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为 59℃,微溶于水,有毒性和强腐蚀性。水的沸点为100℃。他们参观生产过程后,设计了如下装置简图:

①图中仪器B的名称:__________ 。
②用热水浴加热的优点是:________ 。
③实验装置气密性良好,要达到提纯溴的目的,收集溴时温度计应控制的温度为:____ 。

(1)粗盐除含NaCl外,还含有少量MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是粗盐提纯的操作流程。

提供的试剂:Na2CO3溶液、K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、饱和NaCl溶液。
①除去溶液I中的MgCl2、CaCl2、Na2SO4,从提供的试剂中选出a所代表的试剂,按滴加顺序依次为:过量的NaOH溶液、
②如何证明操作①中NaOH溶液已经过量?
③蒸发过程所用的主要仪器有:铁架台、酒精灯、
(2)某同学欲用四氯化碳萃取较高浓度的溴水中的溴,经振荡并在铁架台上静置分层后,
①分离出四氯化碳层的
(3)工业上将较高浓度的溴水经进一步处理得到工业溴。某研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为 59℃,微溶于水,有毒性和强腐蚀性。水的沸点为100℃。他们参观生产过程后,设计了如下装置简图:

①图中仪器B的名称:
②用热水浴加热的优点是:
③实验装置气密性良好,要达到提纯溴的目的,收集溴时温度计应控制的温度为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】为除去粗盐中的 、
、 、
、 及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(提示:用于沉淀的试剂稍过量):
及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(提示:用于沉淀的试剂稍过量):
称取粗盐


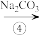
 滤液
滤液
 精盐
精盐
(1)第①步中,操作A是___________ ,第⑤步中,操作B是___________ 。
(2)第④步中,写出相应的化学方程式(设粗盐溶液中 的主要存在形式为氯化钙)
的主要存在形式为氯化钙)___________ 。
(3)若先用盐酸调溶液至中性,再过滤,将对实验结果产生影响,其原因是___________ 。
(4)设计实验检验得到精盐是否含有 。
。___________ 。
 、
、 、
、 及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(提示:用于沉淀的试剂稍过量):
及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(提示:用于沉淀的试剂稍过量):称取粗盐



 滤液
滤液
 精盐
精盐(1)第①步中,操作A是
(2)第④步中,写出相应的化学方程式(设粗盐溶液中
 的主要存在形式为氯化钙)
的主要存在形式为氯化钙)(3)若先用盐酸调溶液至中性,再过滤,将对实验结果产生影响,其原因是
(4)设计实验检验得到精盐是否含有
 。
。
您最近一年使用:0次