2015届湖北省八校高三二次联考理综化学试卷
湖北
高三
阶段练习
2017-07-26
858次
整体难度:
适中
考查范围:
化学与STSE、认识化学科学、化学反应原理、物质结构与性质、化学实验基础、常见无机物及其应用、有机化学基础
2015届湖北省八校高三二次联考理综化学试卷
湖北
高三
阶段练习
2017-07-26
858次
整体难度:
适中
考查范围:
化学与STSE、认识化学科学、化学反应原理、物质结构与性质、化学实验基础、常见无机物及其应用、有机化学基础
一、单选题 添加题型下试题
单选题
|
较易(0.85)
1. 下列说法错误的是
| A.氧化钙用作儿童食品的干燥剂存在安全隐患 |
| B.聚乙烯、聚氯乙烯、聚苯乙烯都是通过加聚反应制得的 |
| C.雾霾天气对人的健康造成危害,“雾”和“霾”的分散质微粒不相同 |
| D.绿色化学的核心是利用化学原理对环境污染进行治理 |
您最近一年使用:0次
单选题
|
适中(0.64)
2. 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.1 L 1 mol·L-1的NaClO溶液中含有ClO-的数目为NA |
| B.78 g苯含有C=C键的数目为3 NA |
| C.常温常压下,14 g由N2和CO组成的混合气体含有的电子总数为7 NA |
| D.1 mol FeI2与足量氯气反应时转移的电子数为2 NA |
您最近一年使用:0次
单选题
|
较难(0.4)
解题方法
3. 根据表中八种短周期元素的有关信息判断,下列说法错误的是
| 元素编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径/nm | 0.037 | 0.074 | 0.082 | 0.099 | 0.102 | 0.143 | 0.152 | 0.186 |
| 最高化合价或 最低化合价 | +1 | -2 | +3 | -1 | -2 | +3 | +1 | +1 |
| A.元素②⑥形成的化合物具有两性 |
| B.元素②气态氢化物的沸点小于元素⑤气态氢化物的沸点 |
| C.元素⑤对应的离子半径大于元素⑦对应的离子半径 |
| D.元素④的最高价氧化物的水化物比元素⑤的最高价氧化物的水化物酸性强 |
您最近一年使用:0次
2019-01-30更新
|
385次组卷
|
3卷引用:2015届湖北省八校高三二次联考理综化学试卷
单选题
|
适中(0.64)
名校
您最近一年使用:0次
2015-05-11更新
|
530次组卷
|
4卷引用:2015届湖北省八校高三二次联考理综化学试卷
单选题
|
适中(0.64)
5. 下列有关说法正确的是
| A.2,2-二甲基丁烷与2,4-二甲基戊烷的一氯代物种类数相同 |
| B.乙烷、苯、裂化汽油溶液均不能使酸性高锰酸钾溶液褪色 |
| C.苯的密度比水小,但由苯反应制得的溴苯、硝基苯、环己烷的密度都比水大 |
| D.乙酸乙酯在碱性条件下的水解反应称为皂化反应 |
您最近一年使用:0次
单选题
|
较难(0.4)
6. 能正确表示下列反应的离子方程式的是
2Ba2++4OH-+Al3++2SO42-=2BaSO4↓+AlO2-+2H2O
2Ba2++4OH-+Al3++2SO42-=2BaSO4↓+AlO2-+2H2O
A.用惰性电极电解MgCl2溶液:2Cl-+2H2O Cl2↑+H2↑+2OH- Cl2↑+H2↑+2OH- |
| B.向石灰水中滴加少量Ca(HCO3)2溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
| C.过氧化钠与水反应:2O22-+2H2O=4OH-+O2↑ |
| D.一定量明矾溶液中滴加Ba(OH)2溶液至沉淀的质量最大时: |
【知识点】 离子反应的发生及书写 电解池
您最近一年使用:0次
2016-12-09更新
|
373次组卷
|
2卷引用:2015届湖北省八校高三二次联考理综化学试卷
单选题
|
适中(0.65)
解题方法
7. 氯在饮用水处理中常用作杀菌剂,且HClO的杀菌能力比ClO-强。25℃时氯气-氯水体系中存在以下平衡关系:
Cl2(g) Cl2(aq)K1=10-1.2
Cl2(aq)K1=10-1.2
Cl2(aq)+H2O HClO+H++Cl-K2=10-3.4
HClO+H++Cl-K2=10-3.4
HClO H++ClO-Ka=?
H++ClO-Ka=?
其中,Cl2(aq)、HClO和ClO-分别在三者中所占的物质的量分数(α)随pH变化的关系如图所示。

下列表述正确的是
Cl2(g)
 Cl2(aq)K1=10-1.2
Cl2(aq)K1=10-1.2Cl2(aq)+H2O
 HClO+H++Cl-K2=10-3.4
HClO+H++Cl-K2=10-3.4HClO
 H++ClO-Ka=?
H++ClO-Ka=?其中,Cl2(aq)、HClO和ClO-分别在三者中所占的物质的量分数(α)随pH变化的关系如图所示。

下列表述正确的是
A.Cl2(g)+H2O 2H++ClO-+Cl-,K=10-10.9 2H++ClO-+Cl-,K=10-10.9 |
| B.pH=7.5时,用氯处理饮用水体系中,c(Cl-)+c(HClO)=c(H+)-c(OH-) |
| C.用氯处理饮用水时,pH=6.5时杀菌效果比pH=4.5时好 |
| D.氯处理饮用水时,在夏季的杀菌效果比在冬季好 |
您最近一年使用:0次
2016-12-09更新
|
1398次组卷
|
3卷引用:2015届湖北省八校高三二次联考理综化学试卷
二、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
名校
8. 水杨酸甲酯又叫冬青油,是一种重要的有机合成原料。某化学小组用水杨酸( )和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率。
)和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率。
实验步骤:
Ⅰ.如图,在三颈烧瓶中加入6.9 g (0.05 mol)水杨酸和24 g(30 mL,0.75 mol)甲醇,向混合物中加入约10 mL甲苯(甲苯与水形成的共沸物,沸点为85℃,该实验中加入甲苯,易将水蒸出),再小心地加入5 mL浓硫酸,摇动混匀,加入1~2粒沸石,组装好实验装置,在85~95℃下恒温加热反应1.5小时;

Ⅱ.待装置冷却后,分离出甲醇,然后转移至分液漏斗,依次用少量水、5%NaHCO3 溶液和水洗涤;分出的产物加入少量无水MgSO4固体,过滤得到粗酯;
Ⅲ.将粗酯进行蒸馏,收集221℃~224℃的馏分,得水杨酸甲酯4.5g。
常用物理常数:
请根据以上信息回答下列问题:
(1)仪器A的名称是___________ ,制备水杨酸甲酯时,最合适的加热方法是__________ 。
(2)实验中加入甲苯对合成水杨酸甲酯的作用是_____________________ 。
(3)反应结束后,分离甲醇的操作是_____________ 。
(4)洗涤操作中,第一次水洗的主要目的是__________ ,第二次水洗的主要目的是________ 。
(5)检验产品中是否含有水杨酸的化学方法是________________________ 。
(6)本实验的产率为___________ (保留两位有效数字)。
 )和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率。
)和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率。实验步骤:
Ⅰ.如图,在三颈烧瓶中加入6.9 g (0.05 mol)水杨酸和24 g(30 mL,0.75 mol)甲醇,向混合物中加入约10 mL甲苯(甲苯与水形成的共沸物,沸点为85℃,该实验中加入甲苯,易将水蒸出),再小心地加入5 mL浓硫酸,摇动混匀,加入1~2粒沸石,组装好实验装置,在85~95℃下恒温加热反应1.5小时;

Ⅱ.待装置冷却后,分离出甲醇,然后转移至分液漏斗,依次用少量水、5%NaHCO3 溶液和水洗涤;分出的产物加入少量无水MgSO4固体,过滤得到粗酯;
Ⅲ.将粗酯进行蒸馏,收集221℃~224℃的馏分,得水杨酸甲酯4.5g。
常用物理常数:
名称 | 分子量 | 颜色状态 | 相对密度 | 熔点(℃) | 沸点(℃) |
水杨酸甲酯 | 152 | 无色液体 | 1.18 | -8.6 | 224 |
水杨酸 | 138 | 白色晶体 | 1.44 | 158 | 210 |
甲醇 | 32 | 无色液体 | 0.792 | -97 | 64.7 |
(1)仪器A的名称是
(2)实验中加入甲苯对合成水杨酸甲酯的作用是
(3)反应结束后,分离甲醇的操作是
(4)洗涤操作中,第一次水洗的主要目的是
(5)检验产品中是否含有水杨酸的化学方法是
(6)本实验的产率为
您最近一年使用:0次
2018-03-29更新
|
61次组卷
|
4卷引用:2015届湖北省八校高三二次联考理综化学试卷
2015届湖北省八校高三二次联考理综化学试卷2015届甘肃省西北师大附中高三校四诊模拟化学试卷(已下线)精做02 研究有机化合物的一般步骤和方法—《大题精做》2017-2018学年高二化学人教选修5【全国百强校】山东省济南市历城第二中学2019届高三上学期11月月考理科综合化学试题
三、填空题 添加题型下试题
填空题
|
较难(0.4)
9. I.已知碳酸锂在水中的溶解度很小且随温度升高而减小,现用Na2CO3溶液和Li2SO4溶液制Li2CO3。
(1)Na2CO3溶液中离子浓度由大到小的顺序为________________________________________ 。
(2)写出制备Li2CO3的化学方程式_________________________________________________ 。
(3)获得Li2CO3的最佳方法是将反应后的物质_____ 。
a.静置、过滤 b.加热后,趁热过滤 c.蒸发浓缩、冷却结晶
II.可逆反应①A(g)+2B(g) 2C(g) ②2E(g)
2C(g) ②2E(g) F(g)+G(g)分别在密闭容器的两个反应室中进行,反应室之间有可滑动、无摩擦的密封隔板。反应开始和达到平衡时有关物理量变化如图所示:
F(g)+G(g)分别在密闭容器的两个反应室中进行,反应室之间有可滑动、无摩擦的密封隔板。反应开始和达到平衡时有关物理量变化如图所示:

(4)反应①是__________ 反应(填“放热”或“吸热”)。
(5)达到平衡I时,体系压强与反应开始时体系压强之比为_________ 。
(6)平衡I和平衡II中,E的体积分数________ (填“相等”、“不相等”、“无法确定”)。
(7)达平衡I时,计算A的转化率___________ (用分数表示)。
(1)Na2CO3溶液中离子浓度由大到小的顺序为
(2)写出制备Li2CO3的化学方程式
(3)获得Li2CO3的最佳方法是将反应后的物质
a.静置、过滤 b.加热后,趁热过滤 c.蒸发浓缩、冷却结晶
II.可逆反应①A(g)+2B(g)
 2C(g) ②2E(g)
2C(g) ②2E(g) F(g)+G(g)分别在密闭容器的两个反应室中进行,反应室之间有可滑动、无摩擦的密封隔板。反应开始和达到平衡时有关物理量变化如图所示:
F(g)+G(g)分别在密闭容器的两个反应室中进行,反应室之间有可滑动、无摩擦的密封隔板。反应开始和达到平衡时有关物理量变化如图所示:
(4)反应①是
(5)达到平衡I时,体系压强与反应开始时体系压强之比为
(6)平衡I和平衡II中,E的体积分数
(7)达平衡I时,计算A的转化率
您最近一年使用:0次
四、解答题 添加题型下试题
解答题-工业流程题
|
困难(0.15)
解题方法
10. (1)美国麻省理工学院(MIT)近年来设计出镁锑液态金属电池,其工作原理如图所示,负极金属失去电子,并通过外电路做功,而负极金属离子化后通过熔盐迁移到正极并与正极金属合金化;充电则执行相反的过程。

写出电池放电时的正极反应式为_________________________________ 。
(2)我国锑的蕴藏量占世界第一位,辉锑矿(Sb2S3)是其主要矿物。某冶金课题组进行三氯化锑水溶液的电解研究,然后利用电解过程中阳极生成的五氯化锑作为浸出剂,对辉锑矿进行酸性浸出;从而实现浸出-电解的闭路循环,解决了传统炼锑过程中工业三废排放量大的问题。流程如图:

①写出锑元素在周期表中的位置__________________ 。
②工业三废指的是__________________________ 。
③电解过程中阳极主要是Sb3+被氧化成Sb5+。请写出阴极的电极反应式___________ 。
④根据流程图写出浸出步骤发生反应的化学方程式________ 。
⑤已知浸出液中除Sb3+外,还有Cu2+、Pb2+等重金属离子,其中c(Cu2+)=1.6×10-3mol·L-1,向浸出液中加入硫化钠至溶液中的Cu2+刚好完全沉淀,则c(S2-)=______ 。(已知Ksp(CuS)=8×10-45 Ksp(PbS)=3.4×10-28)
⑥还原除砷的原理是:在大于4mol·L-1的HCl溶液中,以次磷酸钠(Na3PO2)做还原剂,保持微沸温度,使AsCl3被还原为棕色单质砷沉淀,请配平该反应的化学方程式:__
AsCl3 + __Na3PO2 + __HCl + __H2O = __As ↓+ __H3PO3 + __NaCl

写出电池放电时的正极反应式为
(2)我国锑的蕴藏量占世界第一位,辉锑矿(Sb2S3)是其主要矿物。某冶金课题组进行三氯化锑水溶液的电解研究,然后利用电解过程中阳极生成的五氯化锑作为浸出剂,对辉锑矿进行酸性浸出;从而实现浸出-电解的闭路循环,解决了传统炼锑过程中工业三废排放量大的问题。流程如图:

①写出锑元素在周期表中的位置
②工业三废指的是
③电解过程中阳极主要是Sb3+被氧化成Sb5+。请写出阴极的电极反应式
④根据流程图写出浸出步骤发生反应的化学方程式
⑤已知浸出液中除Sb3+外,还有Cu2+、Pb2+等重金属离子,其中c(Cu2+)=1.6×10-3mol·L-1,向浸出液中加入硫化钠至溶液中的Cu2+刚好完全沉淀,则c(S2-)=
⑥还原除砷的原理是:在大于4mol·L-1的HCl溶液中,以次磷酸钠(Na3PO2)做还原剂,保持微沸温度,使AsCl3被还原为棕色单质砷沉淀,请配平该反应的化学方程式:
AsCl3 + __Na3PO2 + __HCl + __H2O = __As ↓+ __H3PO3 + __NaCl
您最近一年使用:0次
五、填空题 添加题型下试题
填空题
|
适中(0.65)
解题方法
11. 【化学---选修2:化学与技术】
南海某小岛上,可利用的淡水资源相当匮乏,解放军战士为了寻找合适的饮用水源,对岛上山泉水进行分析化验,结果显示山泉水属于硬水。
(1)硬水是指含有较多______________ 的水,硬水加热后产生沉淀的离子方程式为:________________________________ (写出生成一种沉淀物的即可) 。
(2)硬度为1°的水是指每升水含10 mg CaO或与之相当的物质(如7.1 mg MgO),已知水的硬度在8°以下的称为软水,在8°以上的称为硬水。已知岛上山泉水中c( Ca2+)=1.2×10-3 mol/L,c(Mg2+) =6×l0-4mol/L,那么此水______ (填“是”或“否”)属于硬水。
(3)离子交换法是软化水的常用方法。聚丙烯酸钠是一种离子交换树脂,写出聚丙烯酸钠单体的结构简式__________________ 。
(4)解放军战士通常向水中加入明矾净水,请用离子方程式解释其净水原理:______________ 。
(5)岛上还可以用海水淡化来获得淡水。下面是海水利用电渗析法获得淡水的原理图,已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极。请分析下列问题:

①阳离子交换膜是指___________ (填A或B)。
②写出通电后阳极区的电极反应式____________ ,阴极区的现象是:_______________ 。
南海某小岛上,可利用的淡水资源相当匮乏,解放军战士为了寻找合适的饮用水源,对岛上山泉水进行分析化验,结果显示山泉水属于硬水。
(1)硬水是指含有较多
(2)硬度为1°的水是指每升水含10 mg CaO或与之相当的物质(如7.1 mg MgO),已知水的硬度在8°以下的称为软水,在8°以上的称为硬水。已知岛上山泉水中c( Ca2+)=1.2×10-3 mol/L,c(Mg2+) =6×l0-4mol/L,那么此水
(3)离子交换法是软化水的常用方法。聚丙烯酸钠是一种离子交换树脂,写出聚丙烯酸钠单体的结构简式
(4)解放军战士通常向水中加入明矾净水,请用离子方程式解释其净水原理:
(5)岛上还可以用海水淡化来获得淡水。下面是海水利用电渗析法获得淡水的原理图,已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极。请分析下列问题:

①阳离子交换膜是指
②写出通电后阳极区的电极反应式
您最近一年使用:0次
2016-12-09更新
|
104次组卷
|
5卷引用:2015届湖北省八校高三二次联考理综化学试卷
填空题
|
较难(0.4)
12. [化学—选修3:物质结构与性质]有X、Y、Z、W、P、Q六种前两周期的主族元素,原子序数依次增大,价电子数之和为26,原子半径依Y、Z、W、P、Q、X依次减小。围绕上述元素,回答下列问题:
(1)Q的电子排布图为____________ ,YQ3中心原子的杂化类型为________ ,除X外,其余元素的第一电离能由小到大顺序为_______________ (元素符号回答)。
(2)X2P和ZP2固态时均为分子晶体,但熔点X2P比ZP2高得多,原因是___________________ 。
(3)固体A是离子晶体,结构类似于CsCl,组成中含W的质量分数为73.7%,它的所有原子的最外层都符合相应的稀有气体原子的最外层电子结构,该物质适当加热就分解成两种单质气体。该物质的电子式_________ ,其与水反应的化学方程式为__________________________ 。
(4)Z单质有三类异形体,其中一种骨架型原子晶体的立方晶胞如图

计算晶体中Z原子的空间利用率为________________ ( )。
)。
(1)Q的电子排布图为
(2)X2P和ZP2固态时均为分子晶体,但熔点X2P比ZP2高得多,原因是
(3)固体A是离子晶体,结构类似于CsCl,组成中含W的质量分数为73.7%,它的所有原子的最外层都符合相应的稀有气体原子的最外层电子结构,该物质适当加热就分解成两种单质气体。该物质的电子式
(4)Z单质有三类异形体,其中一种骨架型原子晶体的立方晶胞如图

计算晶体中Z原子的空间利用率为
 )。
)。
【知识点】 物质结构与性质
您最近一年使用:0次
2016-12-09更新
|
168次组卷
|
2卷引用:2015届湖北省八校高三二次联考理综化学试卷
六、解答题 添加题型下试题
解答题-有机推断题
|
较难(0.4)
13. [化学—选修5:有机化学基础]已知B和E分别是生产酚醛树脂和有机玻璃的重要原料。工业上生产B和E的一种途径是:
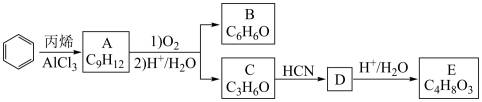
①A为苯的同系物,其一氯代物有5种;
②C、D、E的核磁共振氢谱图中,峰的个数分别为1,2,3;
③等量的E分别与足量的Na和足量的NaHCO3溶液反应,在相同条件下,生成的气体气体相同。
回答下列问题:
(1)C分子中所含官能团的名称是____________________ 。
(2)C→D的反应类型是______________ 。
(3)A的结构简式为_____________ ,A的含有苯环的同分异构体(除A外)有_____ 种。
(4)糠醛(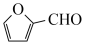 )是一种重要的化工原料,如同甲醛与苯酚反应生成酚醛树脂,它也可与苯酚反应生成糠醛树脂,写出该反应的化学方程式
)是一种重要的化工原料,如同甲醛与苯酚反应生成酚醛树脂,它也可与苯酚反应生成糠醛树脂,写出该反应的化学方程式_____________________________________ 。
(5)E有多种脱水产物,其中F具有六元环状结构,G是一种聚酯高分子材料,写出F和G的结构简式。
F:__________________________ G:_________________________

①A为苯的同系物,其一氯代物有5种;
②C、D、E的核磁共振氢谱图中,峰的个数分别为1,2,3;
③等量的E分别与足量的Na和足量的NaHCO3溶液反应,在相同条件下,生成的气体气体相同。
回答下列问题:
(1)C分子中所含官能团的名称是
(2)C→D的反应类型是
(3)A的结构简式为
(4)糠醛(
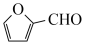 )是一种重要的化工原料,如同甲醛与苯酚反应生成酚醛树脂,它也可与苯酚反应生成糠醛树脂,写出该反应的化学方程式
)是一种重要的化工原料,如同甲醛与苯酚反应生成酚醛树脂,它也可与苯酚反应生成糠醛树脂,写出该反应的化学方程式(5)E有多种脱水产物,其中F具有六元环状结构,G是一种聚酯高分子材料,写出F和G的结构简式。
F:
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:化学与STSE、认识化学科学、化学反应原理、物质结构与性质、化学实验基础、常见无机物及其应用、有机化学基础
试卷题型(共 13题)
题型
数量
单选题
7
解答题
3
填空题
3
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 化学与健康 化学与环境保护 | |
| 2 | 0.64 | 化学计量 盐类的水解 | |
| 3 | 0.4 | 元素非金属性强弱的比较方法 微粒半径大小的比较方法 根据原子结构进行元素种类推断 氢键概念及特征 | |
| 4 | 0.64 | 化学实验基础 钠及其化合物 | |
| 5 | 0.64 | 烃 有机物的结构特点 | |
| 6 | 0.4 | 离子反应的发生及书写 电解池 | |
| 7 | 0.65 | 次氯酸及其性质 电离平衡常数及影响因素 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 | |
| 二、解答题 | |||
| 8 | 0.65 | 常见有机物的制备 | 实验探究题 |
| 10 | 0.15 | 氧化还原反应方程式的配平 溶度积常数相关计算 电解池电极反应式及化学方程式的书写与判断 物质分离、提纯综合应用 | 工业流程题 |
| 13 | 0.4 | 根据要求书写同分异构体 同分异构体的数目的确定 加成反应 有机推断综合考查 | 有机推断题 |
| 三、填空题 | |||
| 9 | 0.4 | 化学平衡 盐类的水解 | |
| 11 | 0.65 | 离子反应的发生及书写 盐类水解在生活、生产中的应用 电解原理的应用 物质分离、提纯综合应用 | |
| 12 | 0.4 | 物质结构与性质 | |