名校
解题方法
1 . 近日,武汉市第十二中学的“化学妙妙屋”社团以黄铁矿FeS2(杂质为石英)为原料,设计了如下工艺流程:
(1)在空气中焙烧黄铁矿的化学方程式为:________ 。
(2)研究发现,pH和温度对石灰石浆液的脱硫效率有一定影响。当烟气通入速度一定时,石灰石浆液的脱硫率与浆液pH的关系如图所示(pH=-lgc(H+))。下列有关说法正确的是_____ 。
b.反应时需鼓入足量的空气以保证SO2被充分氧化生成CaSO4
c.将脱硫后的气体通入KMnO4溶液,可粗略判断烟气脱硫效率
d.石灰石浆液pH>5.7烟气脱硫效果降低,是因为石灰石的溶解程度增大
(3)检验反应Ⅱ所得的滤液中所含阴离子的方法是_______ 。
(4)向红渣酸浸得到的滤液中加入适量铁粉还原,再由还原后的滤液制得FeSO4·7H2O的操作为:_____ 、_____ 、过滤、洗涤、干燥。
(5)粗盐水精制过程中,为有效除去 、
、 、
、 等杂质,下列加入溶液的顺序错误的是
等杂质,下列加入溶液的顺序错误的是_____ (填选项)过滤后再向滤液中加_____ (填化学式)调节pH。
a.NaOH b.Na2CO3 c.BaCl2
A.cba B.acb C.cab D.abc
(6)工业制备出的硫酸中还含有少量 尾气,为防止污染需净化尾气。已知我国
尾气,为防止污染需净化尾气。已知我国 排放标准限值为100mg/m3,工业常用氨水接触法吸收
排放标准限值为100mg/m3,工业常用氨水接触法吸收 生成一种酸式盐,若尾气中
生成一种酸式盐,若尾气中 的含量为Xmg/m3( X>100 ),则处理每立方米尾气至少需要
的含量为Xmg/m3( X>100 ),则处理每立方米尾气至少需要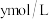 的氨水
的氨水_____ L。
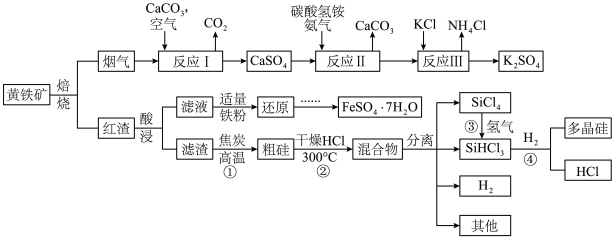
(1)在空气中焙烧黄铁矿的化学方程式为:
(2)研究发现,pH和温度对石灰石浆液的脱硫效率有一定影响。当烟气通入速度一定时,石灰石浆液的脱硫率与浆液pH的关系如图所示(pH=-lgc(H+))。下列有关说法正确的是

b.反应时需鼓入足量的空气以保证SO2被充分氧化生成CaSO4
c.将脱硫后的气体通入KMnO4溶液,可粗略判断烟气脱硫效率
d.石灰石浆液pH>5.7烟气脱硫效果降低,是因为石灰石的溶解程度增大
(3)检验反应Ⅱ所得的滤液中所含阴离子的方法是
(4)向红渣酸浸得到的滤液中加入适量铁粉还原,再由还原后的滤液制得FeSO4·7H2O的操作为:
(5)粗盐水精制过程中,为有效除去
 、
、 、
、 等杂质,下列加入溶液的顺序错误的是
等杂质,下列加入溶液的顺序错误的是a.NaOH b.Na2CO3 c.BaCl2
A.cba B.acb C.cab D.abc
(6)工业制备出的硫酸中还含有少量
 尾气,为防止污染需净化尾气。已知我国
尾气,为防止污染需净化尾气。已知我国 排放标准限值为100mg/m3,工业常用氨水接触法吸收
排放标准限值为100mg/m3,工业常用氨水接触法吸收 生成一种酸式盐,若尾气中
生成一种酸式盐,若尾气中 的含量为Xmg/m3( X>100 ),则处理每立方米尾气至少需要
的含量为Xmg/m3( X>100 ),则处理每立方米尾气至少需要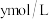 的氨水
的氨水
您最近半年使用:0次
名校
解题方法
2 . LiH是制备有机合成的重要还原剂LiAlH4的反应物,氢化锂遇水蒸气剧烈反应。某小组设计如图所示装置制备LiH:
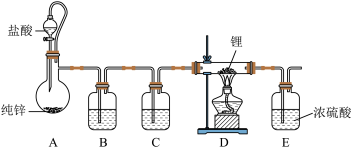
| A.装置B中盛装浓硫酸 |
| B.装置A中加入少量硫酸铜,可加快反应速率 |
| C.装置E用于吸收尾气,避免污染环境 |
| D.实验中,先点燃酒精灯,再通入H2 |
您最近半年使用:0次
名校
解题方法
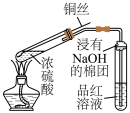
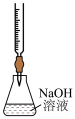
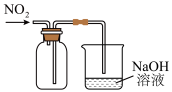
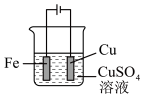
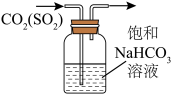
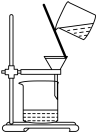
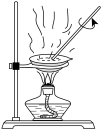
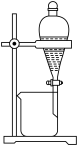
3 . 下列实验装置(夹持装置略)及操作正确的是
|
|
|
|
| A.检验浓硫酸与铜反应产生的二氧化硫 | B.酸碱中和滴定 | C.收集 气体 气体 | D.铁上镀铜 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
4 . 工业废水中常含有一定量的 ,利用滴定原理测定
,利用滴定原理测定 含量的方法如下:
含量的方法如下:
步骤Ⅰ:量取30.00 mL废水于锥形瓶中,加入适量稀硫酸酸化。
步骤Ⅱ:加入过量的碘化钾溶液并放于暗处充分反应,其中 转化为
转化为 。
。
步骤Ⅲ:向锥形瓶中滴加几滴淀粉溶液。用滴定管量取0.1 000 mol·L-1 溶液进行滴定,数据记录如下:(
溶液进行滴定,数据记录如下:( )
)
(1)步骤Ⅰ量取30.00 mL废水,选择的仪器是_______ 。
(2)滴定达到终点时的实验现象是_______ 。
(3)以下操作会造成废水中 含量测定值偏小的是
含量测定值偏小的是_______ (填字母)。
A.滴定终点读数时,俯视滴定管的刻度
B.盛装待测液的锥形瓶用蒸馏水洗过,未用待测液润洗
C.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
D.量取 溶液的滴定管用蒸馏水洗后未用标准液润洗
溶液的滴定管用蒸馏水洗后未用标准液润洗
E.步骤Ⅱ中“放于暗处反应”,若未放于暗处
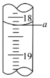
(4)步骤Ⅲ中a的读数如下图所示,则 的含量为
的含量为_______ g·L (写出计算过程)。
(写出计算过程)。
 ,利用滴定原理测定
,利用滴定原理测定 含量的方法如下:
含量的方法如下:步骤Ⅰ:量取30.00 mL废水于锥形瓶中,加入适量稀硫酸酸化。
步骤Ⅱ:加入过量的碘化钾溶液并放于暗处充分反应,其中
 转化为
转化为 。
。步骤Ⅲ:向锥形瓶中滴加几滴淀粉溶液。用滴定管量取0.1 000 mol·L-1
 溶液进行滴定,数据记录如下:(
溶液进行滴定,数据记录如下:( )
)| 实验次数 | 第一次(mL) | 第二次(mL) | 第三次(mL) |
 溶液原始读数 溶液原始读数 | 1.02 | 2.00 | 0.20 |
 溶液终点读数 溶液终点读数 | 19.03 | 19.99 | a |
(1)步骤Ⅰ量取30.00 mL废水,选择的仪器是
(2)滴定达到终点时的实验现象是
(3)以下操作会造成废水中
 含量测定值偏小的是
含量测定值偏小的是A.滴定终点读数时,俯视滴定管的刻度
B.盛装待测液的锥形瓶用蒸馏水洗过,未用待测液润洗
C.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
D.量取
 溶液的滴定管用蒸馏水洗后未用标准液润洗
溶液的滴定管用蒸馏水洗后未用标准液润洗E.步骤Ⅱ中“放于暗处反应”,若未放于暗处
(4)步骤Ⅲ中a的读数如下图所示,则
 的含量为
的含量为 (写出计算过程)。
(写出计算过程)。
您最近半年使用:0次
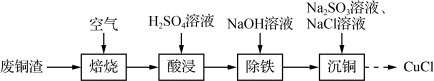
5 . 以工业废铜渣(主要含CuO,还含有CuS、Fe2O3等)为原料制备CuCl,并测定其纯度。其制备过程可表示为
(1)焙烧。将废铜渣放在空气中加热至300℃充分焙烧,反应中CuS转化成CuO,其反应的化学方程式为_______ 。
(2)酸浸。将焙烧后的产物与一定浓度的硫酸溶液放入反应器中,以一定的速率搅拌进行反应。在该过程中,还可以提高铜元素浸出效率的措施是_______ 。
(3)除铁。酸浸后,测得溶液中c(Fe3+)=0.1 mol·L-1,c(Cu2+)=2 mol·L-1.向其中滴加NaOH溶液调节溶液pH除去Fe3+,则需调节溶液pH范围为____ 。已知:Fe3+完全沉淀后其浓度应小于1×10-6 mol·L-1。
(4)沉铜。除铁后,过滤,向滤液中加入Na2SO3溶液、NaCl溶液, 搅拌下充分反应,过滤,洗涤,干燥得到CuCl。
①得到CuCl沉淀的离子方程式为_______ 。
②相同条件下,CuCl沉淀率随 的变化如下图所示。
的变化如下图所示。 大于2.5,CuCl沉淀率几乎不变的原因
大于2.5,CuCl沉淀率几乎不变的原因_______ 。
(1)焙烧。将废铜渣放在空气中加热至300℃充分焙烧,反应中CuS转化成CuO,其反应的化学方程式为
(2)酸浸。将焙烧后的产物与一定浓度的硫酸溶液放入反应器中,以一定的速率搅拌进行反应。在该过程中,还可以提高铜元素浸出效率的措施是
(3)除铁。酸浸后,测得溶液中c(Fe3+)=0.1 mol·L-1,c(Cu2+)=2 mol·L-1.向其中滴加NaOH溶液调节溶液pH除去Fe3+,则需调节溶液pH范围为
(4)沉铜。除铁后,过滤,向滤液中加入Na2SO3溶液、NaCl溶液, 搅拌下充分反应,过滤,洗涤,干燥得到CuCl。
①得到CuCl沉淀的离子方程式为
②相同条件下,CuCl沉淀率随
 的变化如下图所示。
的变化如下图所示。 大于2.5,CuCl沉淀率几乎不变的原因
大于2.5,CuCl沉淀率几乎不变的原因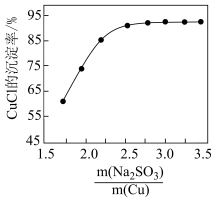
您最近半年使用:0次
名校
6 . 对下列图示实验的描述正确的是
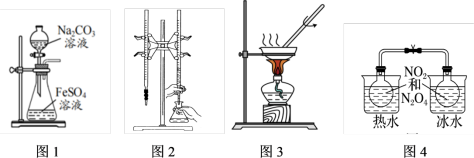
| A.图1所示的实验:制取FeCO3 |
| B.图2所示的实验:用NaOH溶液滴定盐酸 |
| C.图3所示的实验:用装置丁将FeCl3溶液蒸干制得无水FeCl3 |
| D.图4所示的实验:根据两烧瓶中气体颜色的变化(热水中变深、冰水中变浅)可以判断2NO2(g) ⇌N2O4(g)的正反应是吸热反应 |
您最近半年使用:0次
名校
解题方法
7 . 用铜阳极泥进行金银提取,精炼过程产生的金精炼尾渣中含有多种贵金属,一种从金精炼尾渣中回收金(Au)、铂(Pt)、钯(Pd)的工艺流程如下: 、
、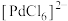 、
、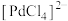 、
、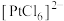 。
。
回答下列问题:
(1)“浸出”时,为提高金精炼尾渣的浸出速率,可采取的措施有___________ (任写两条)。
(2)“浸出”时,所用王水的组成及体积比为___________ 。
(3)“分金”时,生成金单质的离子方程式为___________ ;金位于元素周期表的第六周期第ⅠB族,则基态金原子的价层电子轨道表示式为___________ 。
(4)“沉铂”时,得到的 经煅烧后可得到海绵铂。工业上会将海绵铂反复“浸出—分金—沉铂—煅烧”2~3次,其目的为
经煅烧后可得到海绵铂。工业上会将海绵铂反复“浸出—分金—沉铂—煅烧”2~3次,其目的为___________ 。
(5)“沉钯”时,加入氯酸钠的目的为___________ 。
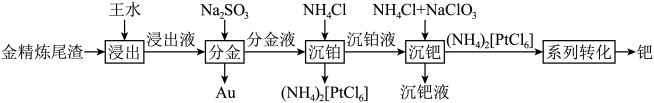
(6)“系列转化”涉及的部分转化如下:
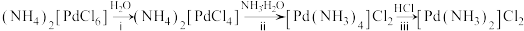
该过程中Pd有___________ 种不同的配位数,配位能力
___________  (填“>”或“<”);ⅲ中发生反应的化学方程式为
(填“>”或“<”);ⅲ中发生反应的化学方程式为___________ 。
 、
、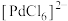 、
、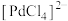 、
、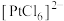 。
。回答下列问题:
(1)“浸出”时,为提高金精炼尾渣的浸出速率,可采取的措施有
(2)“浸出”时,所用王水的组成及体积比为
(3)“分金”时,生成金单质的离子方程式为
(4)“沉铂”时,得到的
 经煅烧后可得到海绵铂。工业上会将海绵铂反复“浸出—分金—沉铂—煅烧”2~3次,其目的为
经煅烧后可得到海绵铂。工业上会将海绵铂反复“浸出—分金—沉铂—煅烧”2~3次,其目的为(5)“沉钯”时,加入氯酸钠的目的为
(6)“系列转化”涉及的部分转化如下:
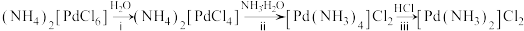
该过程中Pd有

 (填“>”或“<”);ⅲ中发生反应的化学方程式为
(填“>”或“<”);ⅲ中发生反应的化学方程式为
您最近半年使用:0次
名校
8 . 下列实验操作及现象均正确,且能得出相应结论的是
| 选项 | 实验操作和现象 | 结论 |
| A | 用pH计测定氯化铵溶液的pH,温度升高后,pH降低 | 温度升高促进 水解 水解 |
| B | 密闭容器中发生反应 ,缩小容器体积,气体颜色变深 ,缩小容器体积,气体颜色变深 | 缩小体积,平衡逆向移动 |
| C | 向溶液X中滴加盐酸酸化的 溶液,产生白色沉淀 溶液,产生白色沉淀 | 溶液X中存在 |
| D | 向FeS和CuS的混合物中加入足量稀硫酸,FeS完全溶解,CuS未溶解 |  (FeS)> (FeS)> (CuS) (CuS) |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
9 . 下列装置和试剂均合理且能达到实验目的的是
| 装置 |
|
|
| 目的 | 除去 中混有的 中混有的 | 除去 胶体中的 胶体中的 、 、 |
| 选项 | A | B |
| 装置 |
|
|
| 目的 | 蒸发 溶液获得 溶液获得 晶体 晶体 | 分离乙酸和乙酸乙酯的混合物 |
| 选项 | C | D |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次