解题方法
1 . 实验室用苯和液溴制取溴苯并验证其反应类型的实验装置图(夹持装置略)及有关数据如下,按下列步骤回答有关问题。
_______ 。
(2)在a中加入15mL无水苯和少量铁屑,在b中小心加入4mL液态溴,向a中滴入液溴,有白雾生成,a中发生反应的化学方程式为_______ 。
(3)d中CCl4的作用是_______ ;e中出现_______ ,则说明苯与液溴发生了取代反应。
(4)充分反应后,经过下列步骤分离提纯。
①反应后a瓶中的溴苯因溶有溴而显褐色,提纯溴苯的过程中,除去溴苯中的溴依次用水、_______ 溶液、水洗涤。
②向分离出的粗溴苯中加入少量无水氯化钙,静置、过滤。加入氯化钙的目的是_______ 。
③已知苯与溴还可能发生副反应生成对二溴苯(沸点 和邻二溴苯(沸点
和邻二溴苯(沸点 要进一步提纯,再进行
要进一步提纯,再进行_______ (填操作名称)即可得到较纯净的溴苯,该过程中为了受热均匀和易于控制温度,可采用_______ (填“水浴”或“油浴”)加热。
| 苯 | 溴 | 溴苯 | |
| 密度/(g·cm⁻³) | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解性 | 微溶 | 微溶 | 微溶 |

(2)在a中加入15mL无水苯和少量铁屑,在b中小心加入4mL液态溴,向a中滴入液溴,有白雾生成,a中发生反应的化学方程式为
(3)d中CCl4的作用是
(4)充分反应后,经过下列步骤分离提纯。
①反应后a瓶中的溴苯因溶有溴而显褐色,提纯溴苯的过程中,除去溴苯中的溴依次用水、
②向分离出的粗溴苯中加入少量无水氯化钙,静置、过滤。加入氯化钙的目的是
③已知苯与溴还可能发生副反应生成对二溴苯(沸点
 和邻二溴苯(沸点
和邻二溴苯(沸点 要进一步提纯,再进行
要进一步提纯,再进行
您最近半年使用:0次
2 . 阅读下列材料,按要求回答问题。
材料1 酒精、苯、CCl4都是有机溶剂,有机溶剂之间大多能互溶;
材料2 碘(I2)易溶于有机溶剂;
材料3 溴微溶于水,易溶于有机溶剂,其溶液呈橙红色。
在酒精、苯、CCl4、蒸馏水四种试剂中:
(1)能把碘单质从碘水中萃取出来的是___________ ,进行分液之后___________ (填“能”或“不能”)得到纯净的碘单质。
(2)能把溴从溴水中萃取出来,并在分液时使含溴液体从分液漏斗下口流出的是___________ 。
(3)CCl4___________ (填“能”或“不能”)把碘酒中的碘萃取出来,原因是___________ 。
材料1 酒精、苯、CCl4都是有机溶剂,有机溶剂之间大多能互溶;
材料2 碘(I2)易溶于有机溶剂;
材料3 溴微溶于水,易溶于有机溶剂,其溶液呈橙红色。
在酒精、苯、CCl4、蒸馏水四种试剂中:
(1)能把碘单质从碘水中萃取出来的是
(2)能把溴从溴水中萃取出来,并在分液时使含溴液体从分液漏斗下口流出的是
(3)CCl4
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
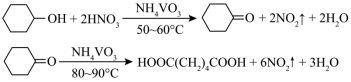
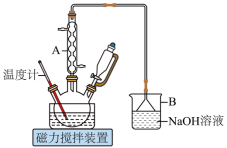
3 . 1,6己二酸是常用的化工原料,在高分子材料、医药、润滑剂的制造等方面都有重要作用。实验室利用图中的装置(夹持装置已省略),以环己醇和硝酸为反应物制备1,6己二酸。反应原理为:
实验步骤如下:
Ⅰ.向三颈烧瓶中加入0.03gNH4VO3固体和18mL浓HNO3(略过量),向恒压滴液漏斗中加入6mL环己醇
Ⅱ.将三颈烧瓶放入水浴中,电磁搅拌并加热至50℃。移去水浴,打开恒压滴液漏斗活塞滴加5~6滴环己醇,观察到三颈烧瓶中产生红棕色气体时,开始慢慢加入余下的环己醇。调节滴加环己醇的速度,使三颈烧瓶内温度维持在50~60℃之间,直至环己醇全部滴加完毕
Ⅲ.将三颈烧瓶放入80~90℃水浴中加热10min,至几乎无红棕色气体导出为止。然后迅速将三颈烧瓶中混合液倒入100mL烧杯中,冷却至室温后,有白色晶体析出,减压过滤,___________,干燥,得到粗产品
Ⅳ.1,6-己二酸粗产品的提纯
(1)将步骤Ⅲ补充完整:_______ 。步骤Ⅳ提纯方法的名称为_______ 。如图为1,6己二酸在水中的溶解度曲线,80℃时1,6-己二酸水溶液的密度为ρg·mL-1;该溶液的物质的量浓度为_______ 。
| 试剂 | 相对分子质量 | 密度/(g·mL-1) | 熔点/℃ | 沸点/℃ | 溶解性 |
| 环己醇 | 100 | 0.962 | 25.9 | 161.8 | 可溶于水、乙醇、乙醚 |
| 1,6-己二酸 | 146 | 1.360 | 152 | 330.5 | 微溶于冷水,易溶于乙醇 |
| NH4VO3 | 117 | 2.326 | 210(分解) | — | 微溶于冷水,易溶于热水 |
Ⅰ.向三颈烧瓶中加入0.03gNH4VO3固体和18mL浓HNO3(略过量),向恒压滴液漏斗中加入6mL环己醇
Ⅱ.将三颈烧瓶放入水浴中,电磁搅拌并加热至50℃。移去水浴,打开恒压滴液漏斗活塞滴加5~6滴环己醇,观察到三颈烧瓶中产生红棕色气体时,开始慢慢加入余下的环己醇。调节滴加环己醇的速度,使三颈烧瓶内温度维持在50~60℃之间,直至环己醇全部滴加完毕
Ⅲ.将三颈烧瓶放入80~90℃水浴中加热10min,至几乎无红棕色气体导出为止。然后迅速将三颈烧瓶中混合液倒入100mL烧杯中,冷却至室温后,有白色晶体析出,减压过滤,___________,干燥,得到粗产品
Ⅳ.1,6-己二酸粗产品的提纯
(1)将步骤Ⅲ补充完整:

| A.46.07% | B.57.08% | C.63.03% | D.74.61% |
您最近半年使用:0次
4 . 下列实验操作、现象及结论都正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将铁锈溶于浓盐酸,再滴入KMnO4溶液 | 紫色褪去 | 铁锈中含有二价铁 |
| B | 向淀粉溶液中加入稀硫酸,加热一段时间后,再滴加银氨溶液,水浴加热 | 未产生银镜 | 淀粉未发生水解 |
| C | 向盛有10滴0.1mol/L AgNO3溶液的试管中滴加15滴0.1mol/L NaCl溶液,观察现象,再滴加2滴0.1mol/L KI溶液 | 先产生白色沉淀,后产生黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| D | 向一体积可变的密闭容器中充入NO2,发生反应:2NO2(g) N2O4(g),将容器体积压缩至原来的一半 N2O4(g),将容器体积压缩至原来的一半 | 相比压缩体积之前,气体颜色变浅 | 增大压强,平衡向气体分子数减小的方向移动 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
7日内更新
|
411次组卷
|
3卷引用:2024届内蒙古自治区赤峰市高三下学期三模理科综合试题-高中化学
2024届内蒙古自治区赤峰市高三下学期三模理科综合试题-高中化学(已下线)押题卷02(15+4题型) -2024高考化学考点必杀300题(新高考通用)内蒙古赤峰市2024届高三4月模拟考试(二模)理综-化学试题
名校
5 . 实验室用浓硫酸和乙醇制乙烯的装置如图所示,对下列操作或现象描述正确的是
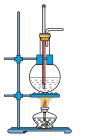
| A.为控制反应温度,温度计的量程为0~150℃ |
| B.实验得到的气体能使溴水褪色说明有乙烯生成 |
| C.反应中圆底烧瓶内会产生黑色固体 |
| D.用排水法或向下排空气法收集乙烯 |
您最近半年使用:0次
7日内更新
|
113次组卷
|
2卷引用:上海市晋元高级中学2023-2024学年高二下学期期中考试 化学学科(等级考)试卷
6 . 间苯三酚可用于合成重要的有机合成中间体3,5-二甲氧基苯酚,反应如图:
下列说法不正确的是

| 物质 | 沸点/ | 熔点/ | 溶解性 |
| 甲醇 | 64.7 | 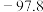 | 易溶于水 |
| 3,5-二甲氧基苯酚 | 172~175 | 33~36 | 易溶于甲醇、乙醚,微溶于水 |
| A.该反应属于取代反应 |
| B.分离出甲醇的操作是蒸馏 |
C.洗涤时,可用饱和 溶液除去有机层中的氯化氢 溶液除去有机层中的氯化氢 |
D.间苯三酚与3,5-二甲氧基苯酚均可与 溶液发生显色反应 溶液发生显色反应 |
您最近半年使用:0次
7日内更新
|
128次组卷
|
2卷引用:北京一零一中学2023-2024学年高二下学期期中考试化学试题
7 . 废弃电脑的CPU中含有贵重金属Cu、Ag、Au,可回收利用,部分流程如下:

(1)铜元素在周期表中位于______ ,基态铜原子的核外电子排布式为______ 。
(2)电脑CPU在使用时会涂抹一层散热硅脂(一种液体橡胶,主要成分为聚二甲基硅氧烷和聚甲基硅氧烷),可用______洗去;
(3)用Zn粉还原 的化学反应方程式为
的化学反应方程式为______ ;
(4)试剂1为______ (填名称,下同),试剂2为______ ;
(5)加入过其铁粉的原因是______ ;
(6)滤渣2溶于试剂2的原因是______ ;(用离子反应方程式表示)
(7)金属铜的晶胞结构如图所示,铜原子之间的最小距离为apm,则铜晶胞的密度为______  (
( 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。

(1)铜元素在周期表中位于
(2)电脑CPU在使用时会涂抹一层散热硅脂(一种液体橡胶,主要成分为聚二甲基硅氧烷和聚甲基硅氧烷),可用______洗去;
| A.NaOH溶液 | B.纯碱溶液 | C.稀硫酸 | D.酒精 |
(3)用Zn粉还原
 的化学反应方程式为
的化学反应方程式为(4)试剂1为
(5)加入过其铁粉的原因是
(6)滤渣2溶于试剂2的原因是
(7)金属铜的晶胞结构如图所示,铜原子之间的最小距离为apm,则铜晶胞的密度为
 (
( 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。
您最近半年使用:0次
22-23高一下·全国·单元测试
8 . 污水的处理方法
(1)常用的污水处理方法有_______ 、_______ 、和_______ 等。
(2)污水处理常用化学方法:_______ 、_______ 、沉淀法等。
(3)污水处理的流程
①一级处理:通常采用_______ 方法,即用格栅间、沉淀池等除去污水中不溶解的污染物。
②二级处理:采用_______ 方法(又称_______ 法)及某些化学方法,除去水中的可降解有机物等污染物。
③三级处理:主要采用_______ 、_______ 、离子交换法和_______ 等,对污水进行深度处理和净化。经过三级处理后的水可用于_______ 和_______ 用水等。
(1)常用的污水处理方法有
(2)污水处理常用化学方法:
(3)污水处理的流程
①一级处理:通常采用
②二级处理:采用
③三级处理:主要采用
您最近半年使用:0次
2024高三·全国·专题练习
解题方法
9 . 碳酸锰(MnCO3)是制造高性能磁性材料的主要原料。实验室以KMnO4为原料制备少量MnCO3并研究其性质,制备MnCO3的装置如图1所示。已知: MnCO3难溶于水、乙醇,100 ℃开始分解,在潮湿环境下易被氧化。
(1)选用仪器B、C的目的是___________ 。
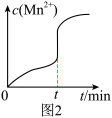
(2)在烧瓶中加入一定量的KMnO4固体,滴加硫酸酸化的H2C2O4溶液,其反应的离子方程式为___________ 。 反应过程中c(Mn2+)随时间的变化曲线如图2所示,则t min时,c(Mn2+)迅速增大的原因是___________ 。___________ 。
(4)实验结束后,将装置A中的混合物过滤,用乙醇洗涤滤渣,再___________ ,即得到干燥的MnCO3固体。用乙醇洗涤的优点是___________ 。
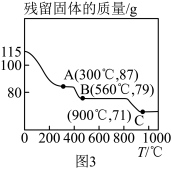
(5)在空气中加热MnCO3固体,随着温度的升高,残留固体的质量变化如图3所示。则A点的成分为___________ (填化学式);B→C反应的化学方程式为___________ 。
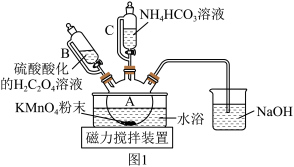
(1)选用仪器B、C的目的是
(2)在烧瓶中加入一定量的KMnO4固体,滴加硫酸酸化的H2C2O4溶液,其反应的离子方程式为
(4)实验结束后,将装置A中的混合物过滤,用乙醇洗涤滤渣,再
(5)在空气中加热MnCO3固体,随着温度的升高,残留固体的质量变化如图3所示。则A点的成分为
您最近半年使用:0次
2024高三·全国·专题练习
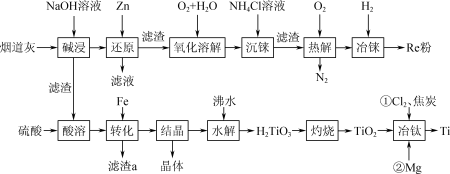
10 . 稀有金属元素铼(Re)和锰同族,铼和钛是航天工程不可缺少的材料。某烟道灰的主要成分为Re2O7、TiO2、SiO2、CuO、 Fe2O3,从中提取铼粉和钛的流程如图所示: 被Zn还原为+4价的铼。ZnO为两性氧化物,溶于碱生成ZnO
被Zn还原为+4价的铼。ZnO为两性氧化物,溶于碱生成ZnO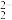 。
。
回答下列问题:
(1)“碱浸”过程Re2O7、SiO2分别发生反应的离子方程式为___________ 、___________ 。
(2)“氧化溶解”过程中Re(OH)4转化为ReO ,该反应中还原剂与氧化剂的物质的量之比为
,该反应中还原剂与氧化剂的物质的量之比为___________ 。
(3)“酸溶”过程得到的钛在溶液中以TiO2+形式存在,其“水解”反应的离子方程式为___________ 。
(4)“转化”过程中加入Fe的作用是___________ ;所得晶体主要成分的化学式中含有7个结晶水,其化学式是___________ 。
(5)“冶钛”过程中将TiO2先转化为TiCl4,再用Mg进行还原,写出高温条件下用Mg还原TiCl4的化学方程式:___________ 。
 被Zn还原为+4价的铼。ZnO为两性氧化物,溶于碱生成ZnO
被Zn还原为+4价的铼。ZnO为两性氧化物,溶于碱生成ZnO 。
。回答下列问题:
(1)“碱浸”过程Re2O7、SiO2分别发生反应的离子方程式为
(2)“氧化溶解”过程中Re(OH)4转化为ReO
 ,该反应中还原剂与氧化剂的物质的量之比为
,该反应中还原剂与氧化剂的物质的量之比为(3)“酸溶”过程得到的钛在溶液中以TiO2+形式存在,其“水解”反应的离子方程式为
(4)“转化”过程中加入Fe的作用是
(5)“冶钛”过程中将TiO2先转化为TiCl4,再用Mg进行还原,写出高温条件下用Mg还原TiCl4的化学方程式:
您最近半年使用:0次



