废弃电脑的CPU中含有贵重金属Cu、Ag、Au,可回收利用,部分流程如下:

(1)铜元素在周期表中位于______ ,基态铜原子的核外电子排布式为______ 。
(2)电脑CPU在使用时会涂抹一层散热硅脂(一种液体橡胶,主要成分为聚二甲基硅氧烷和聚甲基硅氧烷),可用______洗去;
(3)用Zn粉还原 的化学反应方程式为
的化学反应方程式为______ ;
(4)试剂1为______ (填名称,下同),试剂2为______ ;
(5)加入过其铁粉的原因是______ ;
(6)滤渣2溶于试剂2的原因是______ ;(用离子反应方程式表示)
(7)金属铜的晶胞结构如图所示,铜原子之间的最小距离为apm,则铜晶胞的密度为______  (
( 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。

(1)铜元素在周期表中位于
(2)电脑CPU在使用时会涂抹一层散热硅脂(一种液体橡胶,主要成分为聚二甲基硅氧烷和聚甲基硅氧烷),可用______洗去;
| A.NaOH溶液 | B.纯碱溶液 | C.稀硫酸 | D.酒精 |
(3)用Zn粉还原
 的化学反应方程式为
的化学反应方程式为(4)试剂1为
(5)加入过其铁粉的原因是
(6)滤渣2溶于试剂2的原因是
(7)金属铜的晶胞结构如图所示,铜原子之间的最小距离为apm,则铜晶胞的密度为
 (
( 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。
2024·云南曲靖·一模 查看更多[2]
更新时间:2024-05-07 19:30:14
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
【推荐1】1998年,LiW,Dhandapani B等制备了一种具有良好加氢脱氮性质的催化剂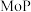 ,开辟了一类全新的催化材料。近年来,过渡金属磷化物(
,开辟了一类全新的催化材料。近年来,过渡金属磷化物(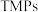 )作为一种新型催化材料,开始广泛应用在电化学、生物学、光学、催化等方面。常见的过渡金属磷化物有
)作为一种新型催化材料,开始广泛应用在电化学、生物学、光学、催化等方面。常见的过渡金属磷化物有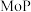 、
、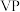 、
、 、
、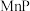 、
、 、
、 等,在金属磷化物中金属原子围绕着非金属原子形成正三棱柱,非金属原子位于正三棱柱的中心。请回答下列问题:
等,在金属磷化物中金属原子围绕着非金属原子形成正三棱柱,非金属原子位于正三棱柱的中心。请回答下列问题:
(1)基态磷原子的价电子排布式为_______ 。基态 与
与 中未成对电子数之比为
中未成对电子数之比为_______ 。
(2) 、P、S三种元素的第一电离能由大到小的顺序是
、P、S三种元素的第一电离能由大到小的顺序是_______ 。电负性:P_______ As(填“>、=或<”),原因是_______ 。
(3) 分子的空间构型为
分子的空间构型为_______ ,其中P的杂化轨道类型为_______ 杂化。
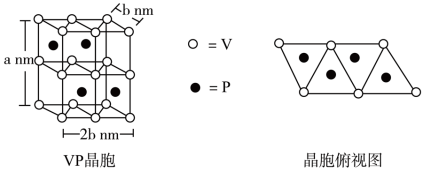
(4)磷化钒(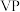 )的晶胞结构如图所示,V作简单六方棱柱体排列,P交替地填入一半的V的正三棱柱中心空隙。与V原子距离相等且最近的P原子有
)的晶胞结构如图所示,V作简单六方棱柱体排列,P交替地填入一半的V的正三棱柱中心空隙。与V原子距离相等且最近的P原子有_______ 个,晶胞的各参数见下图,设阿伏加德罗常数为 ,则
,则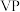 晶体的密度为
晶体的密度为_______  。(列出计算式)
。(列出计算式)
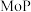 ,开辟了一类全新的催化材料。近年来,过渡金属磷化物(
,开辟了一类全新的催化材料。近年来,过渡金属磷化物(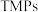 )作为一种新型催化材料,开始广泛应用在电化学、生物学、光学、催化等方面。常见的过渡金属磷化物有
)作为一种新型催化材料,开始广泛应用在电化学、生物学、光学、催化等方面。常见的过渡金属磷化物有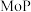 、
、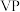 、
、 、
、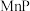 、
、 、
、 等,在金属磷化物中金属原子围绕着非金属原子形成正三棱柱,非金属原子位于正三棱柱的中心。请回答下列问题:
等,在金属磷化物中金属原子围绕着非金属原子形成正三棱柱,非金属原子位于正三棱柱的中心。请回答下列问题:(1)基态磷原子的价电子排布式为
 与
与 中未成对电子数之比为
中未成对电子数之比为(2)
 、P、S三种元素的第一电离能由大到小的顺序是
、P、S三种元素的第一电离能由大到小的顺序是(3)
 分子的空间构型为
分子的空间构型为(4)磷化钒(
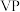 )的晶胞结构如图所示,V作简单六方棱柱体排列,P交替地填入一半的V的正三棱柱中心空隙。与V原子距离相等且最近的P原子有
)的晶胞结构如图所示,V作简单六方棱柱体排列,P交替地填入一半的V的正三棱柱中心空隙。与V原子距离相等且最近的P原子有 ,则
,则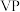 晶体的密度为
晶体的密度为 。(列出计算式)
。(列出计算式)
您最近一年使用:0次
【推荐2】有A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20。其中A为非金属元素;A和E属同一族,它们的原子最外层电子排布为ns1,B和D也属同一族,它们的原子最外层的p能级电子数均是s能级电子数的两倍。C原子最外层电子数等于D原子最外层电子数的一半。请回答下列问题:
(1)C是_______ ,D是_______ ,E是_______ 。
(2)由这五种元素组成的一种化合物是_______ (写化学式)。写出该物质的一种主要用途:_______ 。
(3)写出C元素基态原子的电子排布式:_______ 。
(4)用电子排布图表示D元素原子的价电子排布为_______ 。
(5)元素B与D的电负性的大小关系是B_______ D,C与E的第一电离能的大小关系是C_______ E(填“>”“<”或“=”)。
(1)C是
(2)由这五种元素组成的一种化合物是
(3)写出C元素基态原子的电子排布式:
(4)用电子排布图表示D元素原子的价电子排布为
(5)元素B与D的电负性的大小关系是B
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】工业中可利用生产钛白的副产物 和硫铁矿
和硫铁矿 联合制备铁精粉(
联合制备铁精粉( )和硫酸,实现能源及资源的有效利用。
)和硫酸,实现能源及资源的有效利用。
(1) 结构示意图如图。
结构示意图如图。

①铁元素常见的化合价有+2和+3价, 比
比 稳定的因:
稳定的因:________ 。
②下列粒子的中心原子杂化方式与 中S的杂化方式相同的是:
中S的杂化方式相同的是:
A.HCN B. C.
C. D.
D.
③ 中Fe(Ⅱ)的配位数是
中Fe(Ⅱ)的配位数是_______ , 与
与 的作用力类型是
的作用力类型是_________ 。
(2) 晶体的晶胞形状为立方体,结构如图。
晶体的晶胞形状为立方体,结构如图。
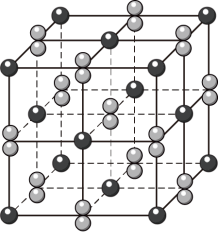
①距离 最近的阳离子有
最近的阳离子有___________ 个, 位于
位于 所形成的
所形成的___________ (填“正四面体”或“正八面体”)空隙。
② 晶体的晶胞参数为a nm,密度为
晶体的晶胞参数为a nm,密度为 ,
, 的摩尔质量为M
的摩尔质量为M  ,则阿伏加德罗常数的值
,则阿伏加德罗常数的值
___________ (用含a、ρ、M的代数式表示)。
(3) 加热脱水后生成
加热脱水后生成 ,再与
,再与 在氧气中掺烧可联合制备铁精粉和硫酸。硫酸工业中,用98%的浓硫酸a吨吸收
在氧气中掺烧可联合制备铁精粉和硫酸。硫酸工业中,用98%的浓硫酸a吨吸收 制得发烟硫酸(化学组成可表示为
制得发烟硫酸(化学组成可表示为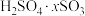 ),可生产
),可生产 质量分数为40%的发烟硫酸
质量分数为40%的发烟硫酸___________ 吨。
 和硫铁矿
和硫铁矿 联合制备铁精粉(
联合制备铁精粉( )和硫酸,实现能源及资源的有效利用。
)和硫酸,实现能源及资源的有效利用。(1)
 结构示意图如图。
结构示意图如图。
①铁元素常见的化合价有+2和+3价,
 比
比 稳定的因:
稳定的因:②下列粒子的中心原子杂化方式与
 中S的杂化方式相同的是:
中S的杂化方式相同的是:A.HCN B.
 C.
C. D.
D.
③
 中Fe(Ⅱ)的配位数是
中Fe(Ⅱ)的配位数是 与
与 的作用力类型是
的作用力类型是(2)
 晶体的晶胞形状为立方体,结构如图。
晶体的晶胞形状为立方体,结构如图。
①距离
 最近的阳离子有
最近的阳离子有 位于
位于 所形成的
所形成的②
 晶体的晶胞参数为a nm,密度为
晶体的晶胞参数为a nm,密度为 ,
, 的摩尔质量为M
的摩尔质量为M  ,则阿伏加德罗常数的值
,则阿伏加德罗常数的值
(3)
 加热脱水后生成
加热脱水后生成 ,再与
,再与 在氧气中掺烧可联合制备铁精粉和硫酸。硫酸工业中,用98%的浓硫酸a吨吸收
在氧气中掺烧可联合制备铁精粉和硫酸。硫酸工业中,用98%的浓硫酸a吨吸收 制得发烟硫酸(化学组成可表示为
制得发烟硫酸(化学组成可表示为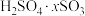 ),可生产
),可生产 质量分数为40%的发烟硫酸
质量分数为40%的发烟硫酸
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】化合物X不含结晶水,由五种常见的元素组成,某实验小组按如下流程进行相关实验:
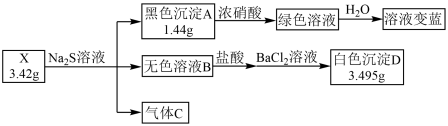
已知:①气体C有刺激性气味,遇 产生白烟;②所加试剂均过量
产生白烟;②所加试剂均过量
请回答:
(1)组成 的五种元素为
的五种元素为 和
和_____________ (填元素符号):气体C的VSEPR模型名称为_____________ 。
(2)化合物 与
与 的反应为非氧化还原反应,写出该反应的化学方程式
的反应为非氧化还原反应,写出该反应的化学方程式_____________ 。
(3)写出黑色固体 溶于浓
溶于浓 得到绿色溶液,发生反应的离子方程式为
得到绿色溶液,发生反应的离子方程式为_____________ 。
(4) 及气体
及气体 与化合物
与化合物 中的金属阳离子结合能力由弱到强的顺序为
中的金属阳离子结合能力由弱到强的顺序为_____________ ,设计实验证明_____________ 。

已知:①气体C有刺激性气味,遇
 产生白烟;②所加试剂均过量
产生白烟;②所加试剂均过量请回答:
(1)组成
 的五种元素为
的五种元素为 和
和(2)化合物
 与
与 的反应为非氧化还原反应,写出该反应的化学方程式
的反应为非氧化还原反应,写出该反应的化学方程式(3)写出黑色固体
 溶于浓
溶于浓 得到绿色溶液,发生反应的离子方程式为
得到绿色溶液,发生反应的离子方程式为(4)
 及气体
及气体 与化合物
与化合物 中的金属阳离子结合能力由弱到强的顺序为
中的金属阳离子结合能力由弱到强的顺序为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上用黄铜矿(主要成分是 ,还含有少量
,还含有少量 )制备CuCl的工艺流程如图:
)制备CuCl的工艺流程如图:
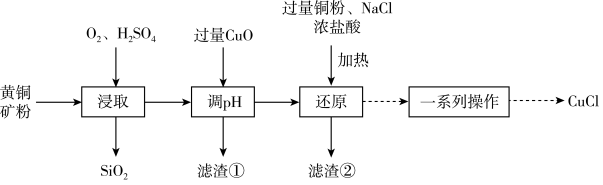
(1)已知在水溶液中存在平衡: (无色)。“还原”的离子方程式为
(无色)。“还原”的离子方程式为_____ 。
(2)关于该工艺流程,下列说法正确的是_____。
(3)CuCl是一种难溶于水和乙醇的白色固体,但其易溶于氨水的原因是_____ 。
(4)滤渣①的主要成分是_____ (填写化学式)。设计实验验证滤渣①中的阳离子_____ 。
 ,还含有少量
,还含有少量 )制备CuCl的工艺流程如图:
)制备CuCl的工艺流程如图:
(1)已知在水溶液中存在平衡:
 (无色)。“还原”的离子方程式为
(无色)。“还原”的离子方程式为(2)关于该工艺流程,下列说法正确的是_____。
A.“浸取”时离子方程式为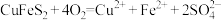 |
| B.“一系列操作”是加入大量的水、过滤、用无水乙醇洗涤、真空干燥 |
| C.“滤渣②”主要成分是CuCl |
| D.“还原”时当溶液变为无色时,表明“还原”进行完全 |
(3)CuCl是一种难溶于水和乙醇的白色固体,但其易溶于氨水的原因是
(4)滤渣①的主要成分是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】固态化合物M的组成为CuSi2O5,以M为原料实现如下转化:
(1)①固体D的成分为_______ ,溶液E中含氮微粒有_______ 。
②写出反应Ⅱ的化学反应方程式_______ 。
③溶液F加热可得纳米 ,过程中pH会明显下降,原因是
,过程中pH会明显下降,原因是_______ 。
(2)下列说法正确的是_______。
(3)已知 能溶于较浓强碱溶液,蓝色溶液C中可能存在铝元素,请设计实验方案进行检验
能溶于较浓强碱溶液,蓝色溶液C中可能存在铝元素,请设计实验方案进行检验_______ 。

(1)①固体D的成分为
②写出反应Ⅱ的化学反应方程式
③溶液F加热可得纳米
 ,过程中pH会明显下降,原因是
,过程中pH会明显下降,原因是(2)下列说法正确的是_______。
| A.反应Ⅰ不能在陶瓷坩埚中进行 |
| B.固体X可溶于浓氨水 |
| C.溶液A经净化处理后可用于工业粘合剂 |
D.反应Ⅲ中发生的离子反应有: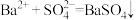 |
 能溶于较浓强碱溶液,蓝色溶液C中可能存在铝元素,请设计实验方案进行检验
能溶于较浓强碱溶液,蓝色溶液C中可能存在铝元素,请设计实验方案进行检验
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】锂离子二次电池正极材料磷酸亚铁锂是应用广泛的正极材料之一。一种制备磷酸亚铁锂的化学方法为:C+4FePO4+2Li2CO3 4LiFePO4+3CO2↑.回答下列问题:
4LiFePO4+3CO2↑.回答下列问题:
(1)Fe失去电子变成为阳离子时首先失去______ 轨道的电子。
(2)C、O、Li原子的第一电离能由大到小的顺序是______ ;PO43-的空间构型为______ 。
(3)C与Si同主族,CO2在高温高压下所形成的晶体结构与SiO2相似,该晶体的熔点比SiO2晶体______ (填“高”或“低”)。硅酸盐和SiO2一样,都是以硅氧四面体作为基本结构单元,下图表示一种含n个硅原子的单链式多硅酸根的结构(投影如图1所示),Si原子的杂化类型为______ ,其化学式可表示为______ 。

(4)图2表示普鲁士蓝的晶体结构( 个晶胞,K+未标出,每隔一个立方体在立方体体心有一个钾离子)。
个晶胞,K+未标出,每隔一个立方体在立方体体心有一个钾离子)。
①普鲁士蓝晶体中每个Fe3+周围最近且等距离的Fe2+数目为______ 个。
②晶体中该立方体的边长为a nm,设阿伏加 德罗常数为NA,其晶体密度为______ g•cm-3。
 4LiFePO4+3CO2↑.回答下列问题:
4LiFePO4+3CO2↑.回答下列问题:(1)Fe失去电子变成为阳离子时首先失去
(2)C、O、Li原子的第一电离能由大到小的顺序是
(3)C与Si同主族,CO2在高温高压下所形成的晶体结构与SiO2相似,该晶体的熔点比SiO2晶体

(4)图2表示普鲁士蓝的晶体结构(
 个晶胞,K+未标出,每隔一个立方体在立方体体心有一个钾离子)。
个晶胞,K+未标出,每隔一个立方体在立方体体心有一个钾离子)。①普鲁士蓝晶体中每个Fe3+周围最近且等距离的Fe2+数目为
②晶体中该立方体的边长为a nm,设阿伏加 德罗常数为NA,其晶体密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】中国是全球最大的锰矿石和锰系材料生产、消费大国,请回答下列问题:
(1)基态锰原子的价层电子排布式为_______ 。
(2)铜锰氧化物(CuMn2O4)能在常温下催化氧化一氧化碳和甲醛(HCHO)。
①CO和N2互为等电于体。CO分子中σ键和π键数目之比为_______ 。
②HCHO分子的H—C—H键角_______ (填“大于”“小于”或“等于”)CO2的键角,理由是_______ 。
③向一定物质的量浓度的Cu(NO3)2和Mn(NO3)2溶液中加入Na2CO3溶液,所得沉淀经高温灼烧,可制得CuMn2O4。CO 的立体构型是
的立体构型是_______ 。
(3)晶体熔点:Fe2O3晶体_______ (填“>”“<”或“=”)Al2O3晶体,理由是_______ 。
(4)锰、铁的第三电离能(I3)较大的是_______ (填元素符号)。
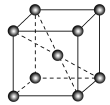
(5)锰晶胞如图所示。已知锰晶胞参数为a nm。设锰晶胞中两个锰原子核之间最短距离为d nm,则d=_______ 。锰晶胞中Mn的空间利用率=_______ 。
(1)基态锰原子的价层电子排布式为
(2)铜锰氧化物(CuMn2O4)能在常温下催化氧化一氧化碳和甲醛(HCHO)。
①CO和N2互为等电于体。CO分子中σ键和π键数目之比为
②HCHO分子的H—C—H键角
③向一定物质的量浓度的Cu(NO3)2和Mn(NO3)2溶液中加入Na2CO3溶液,所得沉淀经高温灼烧,可制得CuMn2O4。CO
 的立体构型是
的立体构型是(3)晶体熔点:Fe2O3晶体
(4)锰、铁的第三电离能(I3)较大的是
(5)锰晶胞如图所示。已知锰晶胞参数为a nm。设锰晶胞中两个锰原子核之间最短距离为d nm,则d=

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】含硼化合物由于其特殊的结构和性质在生产、生活和科研中应用广泛。回答下列问题:
(1)基态硼原子的核外电子的空间运动状态有_______ 种;B、N、H的电负性由大到小的顺序为_______ 。
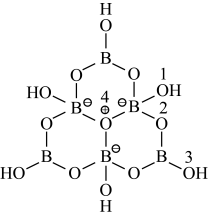
(2)含硼阴离子[B6O7(OH)6]2-的结构如图所示。其中硼原子的杂化方式为_______ ,该结构中共有_______ 种不同化学环境的氧原子。
(3)BF3与H2O结合形成固态化合物BF3·OH2…OH2,该物质在6.2℃时熔化电离出H3O+和一种含硼阴离子_______ (填离子符号),该熔化电离过程破坏的作用力为_______ ,H3O+的空间构型为_______ 。
(4)金属硼氢化物可用作储氢材料。如图是一种金属硼氢化物氨合物的晶体结构示意图。图中八面体的中心代表金属M原子,顶点代表氨分子:四面体的中心代表硼原子,顶点代表氢原子。该晶体属立方晶系,晶胞棱边夹角均为90°,棱长为apm,密度为ρg·cm-3,阿伏加德罗常数的值为NA。
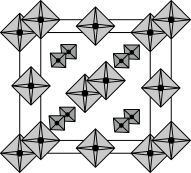
①该晶体的化学式为_______ 。
②金属M原子与硼原子间最短距离为_______ pm。
③金属M的相对原子质量为_______ (列出表达式)
(1)基态硼原子的核外电子的空间运动状态有
(2)含硼阴离子[B6O7(OH)6]2-的结构如图所示。其中硼原子的杂化方式为

(3)BF3与H2O结合形成固态化合物BF3·OH2…OH2,该物质在6.2℃时熔化电离出H3O+和一种含硼阴离子
(4)金属硼氢化物可用作储氢材料。如图是一种金属硼氢化物氨合物的晶体结构示意图。图中八面体的中心代表金属M原子,顶点代表氨分子:四面体的中心代表硼原子,顶点代表氢原子。该晶体属立方晶系,晶胞棱边夹角均为90°,棱长为apm,密度为ρg·cm-3,阿伏加德罗常数的值为NA。

①该晶体的化学式为
②金属M原子与硼原子间最短距离为
③金属M的相对原子质量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】CoCl2 • 6H2O可用作油漆干燥剂,工艺上可用含钴废料(主要为Co,含少量Fe、Al,有机杂质)为原料来制取CoCl2• 6H2O,以下是制备该物质的一种新工艺流程:

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
请回答下列问题:
(1)“焙烧”的目的是___________ 。
(2)①试剂a可选用___________ ;
②“酸浸”时Co转化为Co2+,反应的离子方程式为___________ 。
(3)“氧化”过程中,H2O2的作用:___________ 。
(4)①加入碳酸钠调节pH至b,b的范围是___________ ;
②“滤渣”中所含沉淀成分的化学式为___________ ;
③滤渣经洗涤后,洗涤液与滤液合并,检验滤渣洗涤干净的操作是___________ 。
(5)滤液需加盐酸,其目的是___________ 。
(6)操作I为___________ 、___________ ,过滤,洗涤,干燥。

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.7 | 7.5 | 7.6 | 3.8 |
| 完全沉淀 | 3.2 | 9.7 | 9.2 | 5.2 |
(1)“焙烧”的目的是
(2)①试剂a可选用
②“酸浸”时Co转化为Co2+,反应的离子方程式为
(3)“氧化”过程中,H2O2的作用:
(4)①加入碳酸钠调节pH至b,b的范围是
②“滤渣”中所含沉淀成分的化学式为
③滤渣经洗涤后,洗涤液与滤液合并,检验滤渣洗涤干净的操作是
(5)滤液需加盐酸,其目的是
(6)操作I为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】钛铁矿的主要成分为FeTiO3(可表示为FeO·TiO2),含有少量MgO、SiO2等杂质。利用钛铁矿制备二氧化钛,进一步制备钛单质,流程如图:

已知:FeTiO3+4H+=Fe2++TiO2++2H2O,草酸(H2C2O4)具有很强还原性,易被氧化成二氧化碳。
(1)化合物FeTiO3中铁元素的化合价是___________ 。
(2)钛铁矿加入过量H2SO4后,得到的滤渣A为_________________ (填化学式)。
(3)含TiO2+ 溶液乙转化生成TiO2的离子方程式是________________________________ 。
(4)由滤液丙制备LiFePO4的过程中,所需17%双氧水与H2C2O4的质量比是______________ 。
(5)用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。滴定分析时,称取TiO2(摩尔质量为Mg/mol)试样wg,消耗c mol/L NH4Fe(SO4)2标准溶液VmL,则TiO2质量分数为________ (用代数式表示)。
(6)TiO2制取单质Ti,涉及到的步骤如下: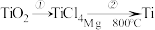
反应②的方程式是_________________ 。由TiCl4→Ti需要在Ar气中进行的理由是__________ 。反应后得到Mg、MgCl2、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据表中信息,需加热的温度略高于_________ ℃即可。

已知:FeTiO3+4H+=Fe2++TiO2++2H2O,草酸(H2C2O4)具有很强还原性,易被氧化成二氧化碳。
(1)化合物FeTiO3中铁元素的化合价是
(2)钛铁矿加入过量H2SO4后,得到的滤渣A为
(3)含TiO2+ 溶液乙转化生成TiO2的离子方程式是
(4)由滤液丙制备LiFePO4的过程中,所需17%双氧水与H2C2O4的质量比是
(5)用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。滴定分析时,称取TiO2(摩尔质量为Mg/mol)试样wg,消耗c mol/L NH4Fe(SO4)2标准溶液VmL,则TiO2质量分数为
(6)TiO2制取单质Ti,涉及到的步骤如下:
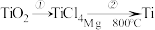
| TiCl4 | Mg | MgCl2 | Ti | |
| 熔点/℃ | -25.0 | 648.8 | 714 | 1667 |
| 沸点/℃ | 136.4 | 1090 | 1412 | 3287 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】无水氯化钴( )可用作彩色水泥的添加剂、催化剂、饲料等,以钴渣(主要成分是CoO,含少量NiO、CuO、FeO和
)可用作彩色水泥的添加剂、催化剂、饲料等,以钴渣(主要成分是CoO,含少量NiO、CuO、FeO和 等)为原料制备无水氯化钴的流程如下:
等)为原料制备无水氯化钴的流程如下:
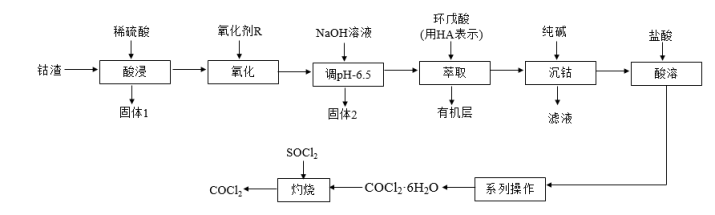
已知:几种金属离子沉淀的pH如下表所示:
请回答下列问题:
(1)“酸浸”时,用稀硝酸代替稀硫酸,缺点是___________ 。
(2)“氧化剂R”的作用是___________ 。
(3)“固体2”的主要成分是___________ 。(填化学式)
(4)M代表被萃取的离子,萃取过程简化为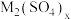 (水层)+2xHA (有机层)
(水层)+2xHA (有机层) 2MAx(有机层)+xH2SO4 (水层)。在萃取过程中加入适量氨水,其作用是
2MAx(有机层)+xH2SO4 (水层)。在萃取过程中加入适量氨水,其作用是___________ 。
(5)室温下,“沉钴”时,当溶液中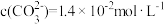 时,
时,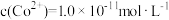 ,
,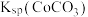 =
=___________ 。
(6) 与水反应生成SO2和HCl。“灼烧”时发生反应的化学方程式为
与水反应生成SO2和HCl。“灼烧”时发生反应的化学方程式为___________ 。
(7)测定CoCl2产品纯度:准确称取mg CoCl2产品溶于蒸馏水配制成250mL溶液,量取25.00mL所配制溶液于锥形瓶中,滴几滴K2CrO4溶液,用cmol/L的AgNO3溶液滴定至终点,消耗AgNO3溶液的体积为xmL。该产品纯度为___________ (用含m、c和x的代数式表示)。
 )可用作彩色水泥的添加剂、催化剂、饲料等,以钴渣(主要成分是CoO,含少量NiO、CuO、FeO和
)可用作彩色水泥的添加剂、催化剂、饲料等,以钴渣(主要成分是CoO,含少量NiO、CuO、FeO和 等)为原料制备无水氯化钴的流程如下:
等)为原料制备无水氯化钴的流程如下:
已知:几种金属离子沉淀的pH如下表所示:
| 金属离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Co2+ | 7.6 | 9.2 |
| Cu2+ | 4.4 | 6.4 |
| Ni2+ | 6.8 | 8.4 |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.5 | 9.5 |
请回答下列问题:
(1)“酸浸”时,用稀硝酸代替稀硫酸,缺点是
(2)“氧化剂R”的作用是
(3)“固体2”的主要成分是
(4)M代表被萃取的离子,萃取过程简化为
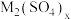 (水层)+2xHA (有机层)
(水层)+2xHA (有机层) 2MAx(有机层)+xH2SO4 (水层)。在萃取过程中加入适量氨水,其作用是
2MAx(有机层)+xH2SO4 (水层)。在萃取过程中加入适量氨水,其作用是(5)室温下,“沉钴”时,当溶液中
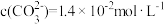 时,
时,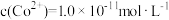 ,
,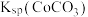 =
=(6)
 与水反应生成SO2和HCl。“灼烧”时发生反应的化学方程式为
与水反应生成SO2和HCl。“灼烧”时发生反应的化学方程式为(7)测定CoCl2产品纯度:准确称取mg CoCl2产品溶于蒸馏水配制成250mL溶液,量取25.00mL所配制溶液于锥形瓶中,滴几滴K2CrO4溶液,用cmol/L的AgNO3溶液滴定至终点,消耗AgNO3溶液的体积为xmL。该产品纯度为
您最近一年使用:0次



