解题方法
1 . 科研工作者合成了低温超导化合物M,再利用低温去插层法,获得了一个新化合物N。二者的晶体结构如图所示,下列说法正确的是
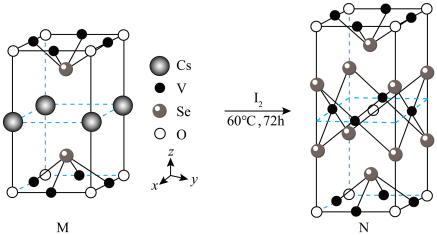
| A.去插层过程中Cs元素均转化为Cs单质 | B.N的化学式为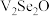 |
| C.M中与Cs原子最临近的Se原子有2个 | D.N中V原子填充了Se原子构成的正八面体空隙 |
您最近半年使用:0次
解题方法
2 . 一定条件下,K、CuCl2和F2反应生成KCl和化合物X,化合物 X 的晶胞结构如图所示(晶胞参数a≠c,α=β=γ=90°), 其中灰球代表 Cu、黑球代表 K、白球代表F。若阿伏加德罗常数的值为NA。下列说法错误的是
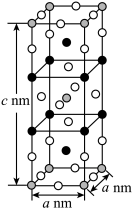
| A.上述反应中 CuCl2与F2的物质的量之比为1:2 |
| B.基态F原子核外电子有5 种空间运动状态 |
| C.Cu原子填充在由 F原子构成的八面体空隙中 |
D.化合物X的密度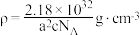 |
您最近半年使用:0次
名校
解题方法
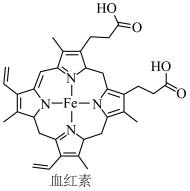
3 . 铁被誉为“工业之母”,铁也是人体必须的痕量元素之一。人体血液中血红蛋白中血红素结构如图 的最外层电子排布式是
的最外层电子排布式是___________ 。
(2)血红素结构中含有吡咯(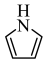 )单元。吡咯能与盐酸反应,从结构角度解释原因
)单元。吡咯能与盐酸反应,从结构角度解释原因 ___________ 。吡咯(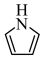 )的沸点高于噻吩(
)的沸点高于噻吩(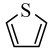 )的原因是
)的原因是 ___________ 。
(3)CO的中毒是由于CO与血红蛋白(Hb)发生配位反应,其反应方程式可表示为:CO (aq) +Hb (aq) ⇌Hb•CO(aq)。已知CO、O₂与血红素(Hb) 的配位常数如下表:
①写出两种与CO互为等电子体的微粒的化学式 ___________ 。
②反应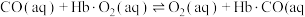 )的平衡常数K=
)的平衡常数K=___________ 。
(4)某FeₓNy的晶胞如图1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物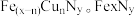 转化为两种Cu替代型产物的能量变化如图2 所示,其中更稳定的Cu替代型产物的化学式为
转化为两种Cu替代型产物的能量变化如图2 所示,其中更稳定的Cu替代型产物的化学式为 ___________ 。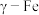 晶胞结构如图3,平均7个晶胞含有 1个碳原子,则奥氏体中碳的质量分数约为
晶胞结构如图3,平均7个晶胞含有 1个碳原子,则奥氏体中碳的质量分数约为 ___________ (列计算式)。
 的最外层电子排布式是
的最外层电子排布式是(2)血红素结构中含有吡咯(
 )单元。吡咯能与盐酸反应,从结构角度解释原因
)单元。吡咯能与盐酸反应,从结构角度解释原因  )的沸点高于噻吩(
)的沸点高于噻吩( )的原因是
)的原因是 (3)CO的中毒是由于CO与血红蛋白(Hb)发生配位反应,其反应方程式可表示为:CO (aq) +Hb (aq) ⇌Hb•CO(aq)。已知CO、O₂与血红素(Hb) 的配位常数如下表:
| CO | O2 | |
| 配位常数 K | 2×107 | 5×104 |
②反应
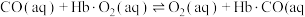 )的平衡常数K=
)的平衡常数K=(4)某FeₓNy的晶胞如图1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物
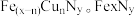 转化为两种Cu替代型产物的能量变化如图2 所示,其中更稳定的Cu替代型产物的化学式为
转化为两种Cu替代型产物的能量变化如图2 所示,其中更稳定的Cu替代型产物的化学式为 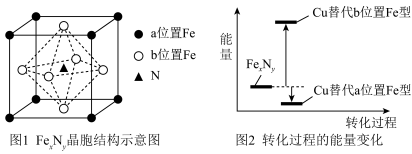
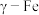 晶胞结构如图3,平均7个晶胞含有 1个碳原子,则奥氏体中碳的质量分数约为
晶胞结构如图3,平均7个晶胞含有 1个碳原子,则奥氏体中碳的质量分数约为 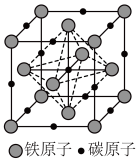
您最近半年使用:0次
名校
4 . 华东理工大学某研究团队自主研发了一种钙钛矿单晶生长技术,大大缩短了晶体生长周期,实现了多种金属卤化物钙钛矿半导体的低温、快速、可控制备,为新一代高性能光电子器件提供了丰富材料库。钙钛矿的主要成分为 。
。
(1)基态 原子的价层电子排布式为
原子的价层电子排布式为___________ 。
(2)为鉴别某一固体样品是否为晶体,或对某一晶体样品的结构进行精确测定,可选用的实验仪器为___________ (填序号)。
 原子光谱仪
原子光谱仪  红外光谱仪
红外光谱仪  射线衍射仪
射线衍射仪
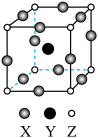
(3) 的晶胞如图所示,X表示的是
的晶胞如图所示,X表示的是___________ (填“ ”、“
”、“ ”或“O”)元素的离子,晶胞中金属离子与氧离子间的化学键类型为
”或“O”)元素的离子,晶胞中金属离子与氧离子间的化学键类型为___________ 。已知:该晶胞棱长为 ,阿伏加德罗常数为
,阿伏加德罗常数为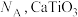 的摩尔质量为
的摩尔质量为 ,则该晶体的密度为ρ=
,则该晶体的密度为ρ=___________  。
。 的四卤化物熔点如下表所示,
的四卤化物熔点如下表所示,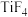 熔点高于其他三种卤化物,自
熔点高于其他三种卤化物,自 至
至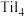 熔点依次升高,原因是
熔点依次升高,原因是___________ 。
(5)单晶硅也是一种常见的半导体材料,常用于太阳能电池板,单晶硅的晶体类型为___________ 晶体。单晶硅熔点___________ 金刚石熔点(填“高于”或“低于”),原因是___________ 。
 。
。(1)基态
 原子的价层电子排布式为
原子的价层电子排布式为(2)为鉴别某一固体样品是否为晶体,或对某一晶体样品的结构进行精确测定,可选用的实验仪器为
 原子光谱仪
原子光谱仪  红外光谱仪
红外光谱仪 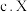 射线衍射仪
射线衍射仪(3)
 的晶胞如图所示,X表示的是
的晶胞如图所示,X表示的是 ”、“
”、“ ”或“O”)元素的离子,晶胞中金属离子与氧离子间的化学键类型为
”或“O”)元素的离子,晶胞中金属离子与氧离子间的化学键类型为 ,阿伏加德罗常数为
,阿伏加德罗常数为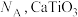 的摩尔质量为
的摩尔质量为 ,则该晶体的密度为ρ=
,则该晶体的密度为ρ= 。
。
 的四卤化物熔点如下表所示,
的四卤化物熔点如下表所示,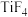 熔点高于其他三种卤化物,自
熔点高于其他三种卤化物,自 至
至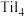 熔点依次升高,原因是
熔点依次升高,原因是| 化合物 | 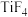 |  | 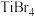 | 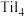 |
熔点 | 377 | 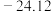 | 38.3 | 155 |
(5)单晶硅也是一种常见的半导体材料,常用于太阳能电池板,单晶硅的晶体类型为
您最近半年使用:0次
5 . I.按构成晶体的粒子和粒子间作用力的不同,将以下晶体进行分类:
①氯化钡、②石英、③金刚砂、④水、⑤乙醇、⑥铜、⑦氯酸钾、⑧高锰酸钾、⑨稀有气体的晶体、⑩干冰
(1)属于共价晶体的有:___________ ;属于分子晶体的有:___________ ;属于离子晶体的有:___________ ;属于金属晶体的有:___________ 。
Ⅱ.比较:
(2)熔点:金刚石___________ 干冰(填“>”或“<”),原因是___________ 。
(3)键角:CH4___________ H2O(填“>”或“<”),原因是___________ 。
Ⅲ.请回答:
(4)黄铜合金采取面心立方堆积,其晶胞结构如图所示:___________ 。
②与Cu原子等距离且最近的Cu原子有___________ 个。
(5)甲醛与新制Cu(OH)2悬浊液加热可得砖红色沉淀Cu2O,已知Cu2O晶胞的结构如图所示:___________ 。
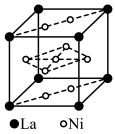
(6)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构如图。___________ 。
①氯化钡、②石英、③金刚砂、④水、⑤乙醇、⑥铜、⑦氯酸钾、⑧高锰酸钾、⑨稀有气体的晶体、⑩干冰
(1)属于共价晶体的有:
Ⅱ.比较:
(2)熔点:金刚石
(3)键角:CH4
Ⅲ.请回答:
(4)黄铜合金采取面心立方堆积,其晶胞结构如图所示:

②与Cu原子等距离且最近的Cu原子有
(5)甲醛与新制Cu(OH)2悬浊液加热可得砖红色沉淀Cu2O,已知Cu2O晶胞的结构如图所示:
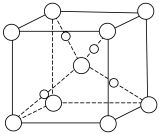
(6)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构如图。
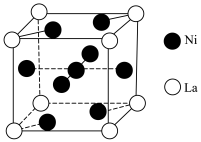
您最近半年使用:0次
名校
解题方法
6 . 下列说法错误的是
| A.MgO的离子键的键能大于CaO的 | B.BF3键角为120°,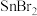 的键角大于120° 的键角大于120° |
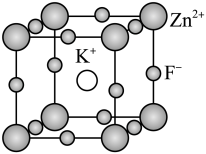
C.如图所示的晶胞的化学式为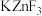 | D.DNA双螺旋的两个螺旋链通过氢键相互结合 |
您最近半年使用:0次
名校
7 . 硫化物含硫量的测定、脱硫是极具价值的重要课题。
(1)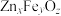 是一种复合脱硫剂,可用于脱除煤气中的
是一种复合脱硫剂,可用于脱除煤气中的 。
。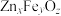 晶胞结构如图1所示(A、B交替排列,且A、B分别为晶胞的
晶胞结构如图1所示(A、B交替排列,且A、B分别为晶胞的 的结构),其化学式为
的结构),其化学式为__________ 。
②一定温度下将一定比例 和
和 的混合气体以一定流速通过装有上述脱硫剂的反应器,一段时间后,出口处检测到
的混合气体以一定流速通过装有上述脱硫剂的反应器,一段时间后,出口处检测到 。研究表明
。研究表明 参与了
参与了 与
与 生成
生成 的反应,反应机理如图2所示,反应前后
的反应,反应机理如图2所示,反应前后 的质量不变,该反应过程可描述为
的质量不变,该反应过程可描述为__________ 。
(2)稀土硫化物中硫含量的测定对其生产和质量控制具有重要意义。用如下方法对稀土硫化物中具有代表性的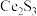 (
( 基态原子核外电子排布式为
基态原子核外电子排布式为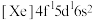 )样品硫含量进行测定。实验检测原理为
)样品硫含量进行测定。实验检测原理为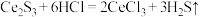
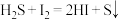

步骤1:称取0.1600g样品于反应瓶中,再准确滴加20.00mL 碘溶液;
碘溶液;
步骤2:缓慢滴加稍过量的稀盐酸(边滴加边摇动反应瓶),盖上瓶塞,剧烈摇动2min;
步骤3:滴入
 溶液至恰好完全反应,消耗
溶液至恰好完全反应,消耗 溶液20.00mL。
溶液20.00mL。
① 元素最高正化合价为
元素最高正化合价为__________ 。
②步骤1中不能使用稀硝酸的原因是__________ 。
③该样品中硫的质量分数为__________ (写出计算过程)。
(1)
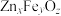 是一种复合脱硫剂,可用于脱除煤气中的
是一种复合脱硫剂,可用于脱除煤气中的 。
。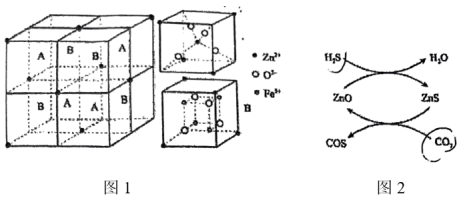
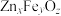 晶胞结构如图1所示(A、B交替排列,且A、B分别为晶胞的
晶胞结构如图1所示(A、B交替排列,且A、B分别为晶胞的 的结构),其化学式为
的结构),其化学式为②一定温度下将一定比例
 和
和 的混合气体以一定流速通过装有上述脱硫剂的反应器,一段时间后,出口处检测到
的混合气体以一定流速通过装有上述脱硫剂的反应器,一段时间后,出口处检测到 。研究表明
。研究表明 参与了
参与了 与
与 生成
生成 的反应,反应机理如图2所示,反应前后
的反应,反应机理如图2所示,反应前后 的质量不变,该反应过程可描述为
的质量不变,该反应过程可描述为(2)稀土硫化物中硫含量的测定对其生产和质量控制具有重要意义。用如下方法对稀土硫化物中具有代表性的
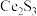 (
( 基态原子核外电子排布式为
基态原子核外电子排布式为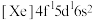 )样品硫含量进行测定。实验检测原理为
)样品硫含量进行测定。实验检测原理为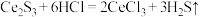
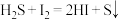

步骤1:称取0.1600g样品于反应瓶中,再准确滴加20.00mL
 碘溶液;
碘溶液;步骤2:缓慢滴加稍过量的稀盐酸(边滴加边摇动反应瓶),盖上瓶塞,剧烈摇动2min;
步骤3:滴入

 溶液至恰好完全反应,消耗
溶液至恰好完全反应,消耗 溶液20.00mL。
溶液20.00mL。①
 元素最高正化合价为
元素最高正化合价为②步骤1中不能使用稀硝酸的原因是
③该样品中硫的质量分数为
您最近半年使用:0次
名校
解题方法
8 .  是一种常见催化剂,能催化臭氧(
是一种常见催化剂,能催化臭氧( )与烟气(
)与烟气( 、
、 )的反应。回答下列问题:
)的反应。回答下列问题:
(1)写出 和
和 原子基态价电子排布式:
原子基态价电子排布式:___________ 、___________ 。
(2) 和
和 的中心原子轨道的杂化类型为
的中心原子轨道的杂化类型为___________ 、___________ 。
(3) 和
和 中所含元素的第一电离能由大到小的顺序是
中所含元素的第一电离能由大到小的顺序是___________ 。两种微粒的空间构型分别为___________ 、___________ 。
(4) 与
与 生成的
生成的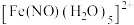 ,画出生成的
,画出生成的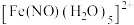 的结构简式,并用“
的结构简式,并用“ ”标出所有配位键:
”标出所有配位键:___________ 。
(5)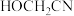 分子中含有的
分子中含有的 键和
键和 键的数目之比为
键的数目之比为___________ 。
(6)一种可吸收甲醛材料,其化学式为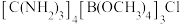 ,部分晶体结构如下图所示:
,部分晶体结构如下图所示: 为平面结构。
为平面结构。
①该材料包含的化学键类型有___________ 。
②组成该材料的 三元素的电负性由大到小的顺序是
三元素的电负性由大到小的顺序是___________ 。
(7)某高温超导材料,其晶胞结构如图所示,该立方晶胞参数为apm。阿伏加德罗常数的值为 。
。___________ 。
②该晶体的密度为___________  。
。
 是一种常见催化剂,能催化臭氧(
是一种常见催化剂,能催化臭氧( )与烟气(
)与烟气( 、
、 )的反应。回答下列问题:
)的反应。回答下列问题:(1)写出
 和
和 原子基态价电子排布式:
原子基态价电子排布式:(2)
 和
和 的中心原子轨道的杂化类型为
的中心原子轨道的杂化类型为(3)
 和
和 中所含元素的第一电离能由大到小的顺序是
中所含元素的第一电离能由大到小的顺序是(4)
 与
与 生成的
生成的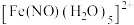 ,画出生成的
,画出生成的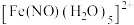 的结构简式,并用“
的结构简式,并用“ ”标出所有配位键:
”标出所有配位键:(5)
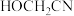 分子中含有的
分子中含有的 键和
键和 键的数目之比为
键的数目之比为(6)一种可吸收甲醛材料,其化学式为
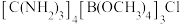 ,部分晶体结构如下图所示:
,部分晶体结构如下图所示: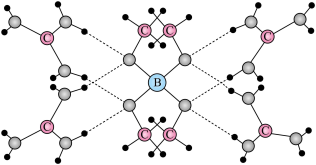
 为平面结构。
为平面结构。①该材料包含的化学键类型有
②组成该材料的
 三元素的电负性由大到小的顺序是
三元素的电负性由大到小的顺序是(7)某高温超导材料,其晶胞结构如图所示,该立方晶胞参数为apm。阿伏加德罗常数的值为
 。
。
②该晶体的密度为
 。
。
您最近半年使用:0次
名校
解题方法
9 . 超高硬度生物材料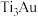 合金是理想的人工髋关节和膝关节材料,其晶体有
合金是理想的人工髋关节和膝关节材料,其晶体有 (图甲)、
(图甲)、 (图乙)两种结构,如下图所示。下列说法错误的是
(图乙)两种结构,如下图所示。下列说法错误的是
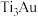 合金是理想的人工髋关节和膝关节材料,其晶体有
合金是理想的人工髋关节和膝关节材料,其晶体有 (图甲)、
(图甲)、 (图乙)两种结构,如下图所示。下列说法错误的是
(图乙)两种结构,如下图所示。下列说法错误的是
| A.图甲中,Ti原子距离最近且等距的Ti原子有8个 |
| B.图乙中,Ti原子位于Au原子构成的四面体空隙中 |
C.图乙中,若M的坐标为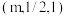 ,则N的坐标为 ,则N的坐标为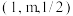 |
D.图乙中,晶胞边长为dpm,晶体的密度为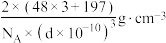 |
您最近半年使用:0次
10 . 目前,全世界镍(Ni)的消费量仅次于铜、铝、铅、锌,居有色金属第五位,镍行业发展蕴藏着巨大的潜力。
(1)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于___________ 晶体;基态Ni原子的电子排布式为___________ 。
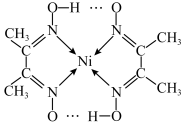
(2)某配合物结构如图所示,分子内含有的作用力有___________ (填编号)。
A.氢键 B.离子键 C.共价键 D.金属键 E.配位键___________ 。
(1)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于
(2)某配合物结构如图所示,分子内含有的作用力有
A.氢键 B.离子键 C.共价键 D.金属键 E.配位键
您最近半年使用:0次



