名校
解题方法
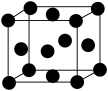
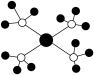
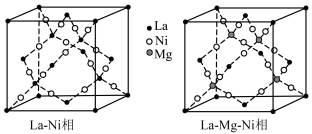
1 . La-Ni相及La-Mg-Ni相均用作贮氢合金材料,以下为二者晶胞结构:
(1)金属镧La位于周期表的____________ 区; 的价电子排布图为
的价电子排布图为____________ ; 与同周期且相邻的元素第一电离能从大到小的顺序为
与同周期且相邻的元素第一电离能从大到小的顺序为____________ .
(2)La-Mg-Ni相的化学式为____________ ,其晶体中与 等距且最近的
等距且最近的 有
有____________ 个;La-Ni相中原子空间利用率为____________ (已知: 原子半径分别为
原子半径分别为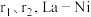 相晶胞参数为a)。
相晶胞参数为a)。
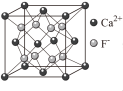
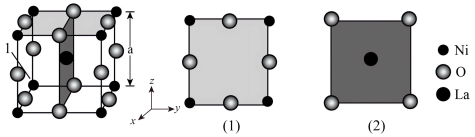
(3)镍酸镧电催化剂立方晶胞如图所示,晶胞参数为a,图(1)和图(2)是晶胞的不同切面。 和
和 的最短距离为
的最短距离为____________ .
②若原子1的分数坐标为 ,则
,则 的分数坐标为
的分数坐标为____________ 。
(1)金属镧La位于周期表的
 的价电子排布图为
的价电子排布图为 与同周期且相邻的元素第一电离能从大到小的顺序为
与同周期且相邻的元素第一电离能从大到小的顺序为(2)La-Mg-Ni相的化学式为
 等距且最近的
等距且最近的 有
有 原子半径分别为
原子半径分别为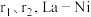 相晶胞参数为a)。
相晶胞参数为a)。(3)镍酸镧电催化剂立方晶胞如图所示,晶胞参数为a,图(1)和图(2)是晶胞的不同切面。
 和
和 的最短距离为
的最短距离为②若原子1的分数坐标为
 ,则
,则 的分数坐标为
的分数坐标为
您最近半年使用:0次
名校
2 . 下列有关说法正确 的是
|
|
| A.电子云密度大的区域电子数目多 | B.晶胞中每个Cu原子周围有12个紧邻的原子 |
|
 晶胞结构 晶胞结构 |
| C.铜离子与氨分子之间形成离子键 | D.每个 晶胞平均占有8个 晶胞平均占有8个 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
3 . 晶体按其几何形态的对称程度可分为七类,其中四方晶系是非常重要的一类。
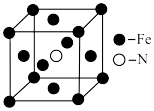
(1)铁和氨在640℃时可发生置换反应,一种产物的晶胞结构如图所示,该反应的化学方程式为_______ 。 晶体具有优异的非线性光学性能。分别用○、●表示
晶体具有优异的非线性光学性能。分别用○、●表示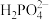 和
和 ,
, 晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是
晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是 、
、 在晶胞xz面、yz面上的位置:
在晶胞xz面、yz面上的位置:_______ (填标号)。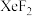 晶体也属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有
晶体也属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有_______ 个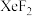 分子。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点原子的分数坐标为
分子。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点原子的分数坐标为 。已知
。已知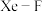 键键长为rpm,则B点原子的分数坐标为
键键长为rpm,则B点原子的分数坐标为_______ 。 在棱上,两端均与Fe相连,立方体中心空隙可容纳
在棱上,两端均与Fe相连,立方体中心空隙可容纳 ,如图所示(
,如图所示( 在图中省略)。
在图中省略)。 与
与 之间最近距离为
之间最近距离为_______ pm,设阿伏加德罗常数的值为NA,则该晶体的密度为_______ g/cm3。
(1)铁和氨在640℃时可发生置换反应,一种产物的晶胞结构如图所示,该反应的化学方程式为
 晶体具有优异的非线性光学性能。分别用○、●表示
晶体具有优异的非线性光学性能。分别用○、●表示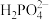 和
和 ,
, 晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是
晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是 、
、 在晶胞xz面、yz面上的位置:
在晶胞xz面、yz面上的位置: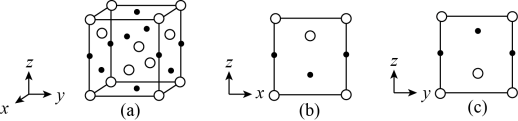
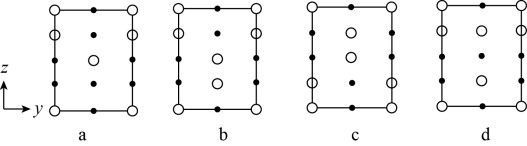
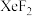 晶体也属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有
晶体也属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有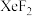 分子。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点原子的分数坐标为
分子。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点原子的分数坐标为 。已知
。已知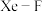 键键长为rpm,则B点原子的分数坐标为
键键长为rpm,则B点原子的分数坐标为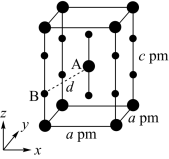
 在棱上,两端均与Fe相连,立方体中心空隙可容纳
在棱上,两端均与Fe相连,立方体中心空隙可容纳 ,如图所示(
,如图所示( 在图中省略)。
在图中省略)。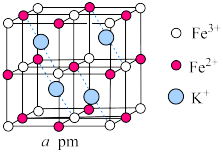
 与
与 之间最近距离为
之间最近距离为
您最近半年使用:0次
名校
解题方法
4 . 六方硫化锌的结构是S原子作六方最密堆积,其晶胞如图所示,图中A点分数坐标为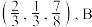 点分数坐标为
点分数坐标为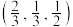 ;底
;底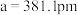 ,高
,高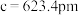 。设
。设 为阿伏加德罗常数的值。下列说法
为阿伏加德罗常数的值。下列说法错误 的是
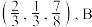 点分数坐标为
点分数坐标为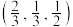 ;底
;底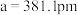 ,高
,高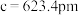 。设
。设 为阿伏加德罗常数的值。下列说法
为阿伏加德罗常数的值。下列说法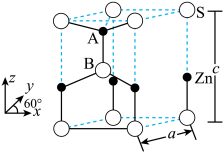
A.晶胞中, 填充空隙类型为正四面体空隙 填充空隙类型为正四面体空隙 | B.图中S原子的配位数为6 |
C.图中 的核间距约为 的核间距约为 | D.该晶体的化学式为 |
您最近半年使用:0次
昨日更新
|
458次组卷
|
4卷引用:贵州省贵阳市第六中学2024届高三下学期一模考试化学试题
贵州省贵阳市第六中学2024届高三下学期一模考试化学试题浙江省舟山中学2023-2024学年高二下学期4月月考化学试题(已下线)题型5 物质结构与性质 有机物的结构与性质(25题)-2024年高考化学常考点必杀300题(新高考通用)河南省焦作市博爱县第一中2023-2024学年高二下学期4月期中考试化学试题
名校
解题方法
5 . 钛,铬,铁,镍、铜等金属及其化合物在工业上有重要用途。
(1)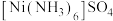 中
中 的键角
的键角_______ (填“>”或“<”) 中
中 的键角,原因是
的键角,原因是_______
(2)元素铜与镍的第二电离能分别为: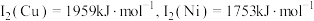 ,则
,则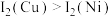 的原因是
的原因是_______
(3)某含铁物质的结构如图所示,图中“Fe”代表 ,则
,则 与氮原子之间形成的化学键的类型是
与氮原子之间形成的化学键的类型是_______ (填“配位键”或“离子键”)。基态 和
和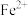 中未成对电子数之比为
中未成对电子数之比为_______ 。 )具有很强的储氢能力,其晶胞结构如图,其中
)具有很强的储氢能力,其晶胞结构如图,其中
_______ 。已知晶胞体积为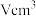 ,若储氢后形成
,若储氢后形成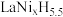 (H进入晶胞空隙,晶胞体积不变),
(H进入晶胞空隙,晶胞体积不变), 为阿伏加德罗常数的值,则氢元素在合金中的密度为
为阿伏加德罗常数的值,则氢元素在合金中的密度为_______ 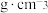 (用含V、
(用含V、 的代数式表示)。
的代数式表示)。
(1)
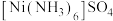 中
中 的键角
的键角 中
中 的键角,原因是
的键角,原因是(2)元素铜与镍的第二电离能分别为:
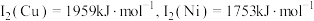 ,则
,则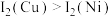 的原因是
的原因是(3)某含铁物质的结构如图所示,图中“Fe”代表
 ,则
,则 与氮原子之间形成的化学键的类型是
与氮原子之间形成的化学键的类型是 和
和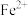 中未成对电子数之比为
中未成对电子数之比为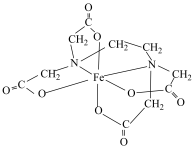
 )具有很强的储氢能力,其晶胞结构如图,其中
)具有很强的储氢能力,其晶胞结构如图,其中
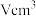 ,若储氢后形成
,若储氢后形成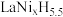 (H进入晶胞空隙,晶胞体积不变),
(H进入晶胞空隙,晶胞体积不变), 为阿伏加德罗常数的值,则氢元素在合金中的密度为
为阿伏加德罗常数的值,则氢元素在合金中的密度为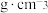 (用含V、
(用含V、 的代数式表示)。
的代数式表示)。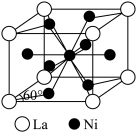
您最近半年使用:0次
名校
6 . 锆(Zr)是重要的战略金属,可从其氧化物中提取。下图是某种锆的氧化物晶体的立方晶胞,NA为阿伏加德罗常数的值。下列说法错误的是
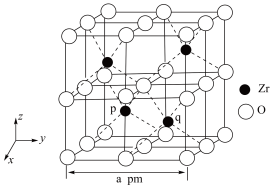
| A.该氧化物的化学式为ZrO2 |
B.该氧化物的密度为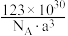 g·cm-3 g·cm-3 |
C.Zr原子之间的最短距离为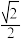 apm apm |
D.q点原子分数坐标为( , , , , ) ) |
您最近半年使用:0次
解题方法
7 . 过渡金属的氮化物和碳化物都表现了较好的催化性能,由碳(C)、钨(W)两种元素形成的两种碳化物甲(晶胞边长为 )和乙(晶胞边长为
)和乙(晶胞边长为 )的立方晶胞结构如图所示。下列说法正确的是
)的立方晶胞结构如图所示。下列说法正确的是
 )和乙(晶胞边长为
)和乙(晶胞边长为 )的立方晶胞结构如图所示。下列说法正确的是
)的立方晶胞结构如图所示。下列说法正确的是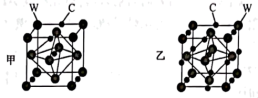
A.晶胞乙中两个 原子最近距离为 原子最近距离为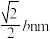 | B.晶体甲中与 原子距离最近的 原子距离最近的 原子有8个 原子有8个 |
C.甲、乙两种晶胞的密度比为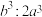 | D.碳化物甲的化学式为WC |
您最近半年使用:0次
8 . 金属铁因生产工艺和温度不同,会有不同的晶体结构。α-Fe和γ-Fe的晶体结构如图所示,下列说法正确的是
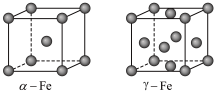
| A.金属铁因为有自由移动的离子而具有导电性 | B.1个γ-Fe晶胞的质量约为(4×56)g |
| C.γ-Fe中铁原子的配位数为12 | D.α-Fe与γ-Fe的性质相同 |
您最近半年使用:0次
名校
9 . 铜及其合金是人类最早使用的金属材料,铜的化合物在现代生活和生产中有着广泛的应用。
(1)铜的熔点比钙的高,其原因是_____ 。
(2)下图是铜的某种氧化物的晶胞结构示意图,该氧化物的化学式为_____ 。_____ ,阴离子的空间结构为_____ 。
(4)铜与Cl原子构成晶体的晶胞结构如下图所示,该晶体的化学式为_____ ,已知该晶体的密度为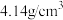 ,则该晶胞的边长为
,则该晶胞的边长为_____ pm(写计算式)。将该物质气化后实验测定其蒸汽的相对分子质量为199,则其气体的分子式为_____ 。
(1)铜的熔点比钙的高,其原因是
(2)下图是铜的某种氧化物的晶胞结构示意图,该氧化物的化学式为
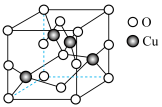
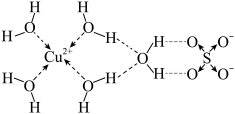
(4)铜与Cl原子构成晶体的晶胞结构如下图所示,该晶体的化学式为
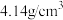 ,则该晶胞的边长为
,则该晶胞的边长为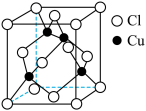
您最近半年使用:0次
名校
解题方法
10 . 硒( )是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光(
)是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光( )效应以来,
)效应以来, 在发光材料、生物医学等领域引起广泛关注。一种含
在发光材料、生物医学等领域引起广泛关注。一种含 的新型
的新型 分子Ⅳ的合成路线如下:
分子Ⅳ的合成路线如下: 与S同是O族,基态硒原子价电子排布式为
与S同是O族,基态硒原子价电子排布式为_______ 。
(2) 的沸点低于
的沸点低于 ,其原因是
,其原因是_______ 。
(3)关于I~Ⅲ三种反应物,下列说法正确的有_______ 。
A.I中仅有 键
键
B.I中的 键为非极性共价键
键为非极性共价键
C.Ⅱ易溶于水
D.Ⅱ中原子的杂化轨道类型只有 与
与
E.I~Ⅲ含有的元素中,O电负性最大
(4)Ⅳ中具有孤对电子的原子有_______ 。
(5)硒的两种含氧酸的酸性强弱为
_______  (填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠(
(填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠( )可减轻重金属铊引起的中毒。
)可减轻重金属铊引起的中毒。 的立体构型为
的立体构型为_______ 。
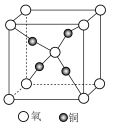
(6)铜和氧形成的一种离子化合物的晶体结构如图,其分子式是_______ 。
 )是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光(
)是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光( )效应以来,
)效应以来, 在发光材料、生物医学等领域引起广泛关注。一种含
在发光材料、生物医学等领域引起广泛关注。一种含 的新型
的新型 分子Ⅳ的合成路线如下:
分子Ⅳ的合成路线如下: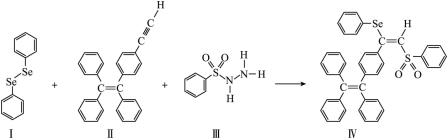
 与S同是O族,基态硒原子价电子排布式为
与S同是O族,基态硒原子价电子排布式为(2)
 的沸点低于
的沸点低于 ,其原因是
,其原因是(3)关于I~Ⅲ三种反应物,下列说法正确的有
A.I中仅有
 键
键B.I中的
 键为非极性共价键
键为非极性共价键C.Ⅱ易溶于水
D.Ⅱ中原子的杂化轨道类型只有
 与
与
E.I~Ⅲ含有的元素中,O电负性最大
(4)Ⅳ中具有孤对电子的原子有
(5)硒的两种含氧酸的酸性强弱为

 (填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠(
(填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠( )可减轻重金属铊引起的中毒。
)可减轻重金属铊引起的中毒。 的立体构型为
的立体构型为(6)铜和氧形成的一种离子化合物的晶体结构如图,其分子式是
您最近半年使用:0次