1 . 铈(Ce,镧系元素)的氧化物是常用的催化剂,能用于汽车尾气的净化。两种铈的氧化物的晶胞结构(晶胞参数均为anm)如图a和图b所示。图b晶胞中存在O缺陷,其中Ce的化合价有 和+4。已知
和+4。已知 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 和+4。已知
和+4。已知 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
| A.Ce位于元素周期表的ds区 |
| B.图a晶胞中Ce的配位数为4 |
C.图a表示的晶体的摩尔体积为 |
| D.图b晶胞中化合价为+3 的Ce的数目为2 |
您最近一年使用:0次
2 . 钒的某种氧化物的立方晶胞结构如图所示。已知: 为阿伏加德罗常数的值,晶体密度为d
为阿伏加德罗常数的值,晶体密度为d  。下列叙述正确的是
。下列叙述正确的是
 为阿伏加德罗常数的值,晶体密度为d
为阿伏加德罗常数的值,晶体密度为d  。下列叙述正确的是
。下列叙述正确的是
| A.基态V的电子占11个能级 | B.该晶体的化学式为 |
| C.1个晶胞含2个钒离子 | D.晶胞参数a为 |
您最近一年使用:0次
名校
3 . 铊中毒的特效药普鲁士蓝的部分结构如图1所示,记为Ⅰ型立方结构。将Ⅰ型立方结构平移、旋转、并置,可得到晶体的晶胞(如图2,记为Ⅱ型立方结构,下层左后的小立方体g未标出)。下列说法正确的是
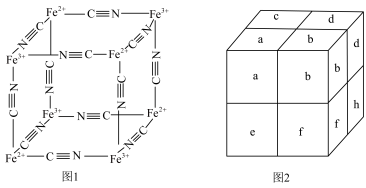
A.若 位于Ⅱ型立方结构的棱心和体心,则 位于Ⅱ型立方结构的棱心和体心,则 位于Ⅱ型立方结构的顶点和面心 位于Ⅱ型立方结构的顶点和面心 |
| B.每个普鲁士蓝晶胞中含6个π键 |
C.从结构上分析,基态 比基态 比基态 相对更稳定 相对更稳定 |
D.若 的摩尔质量为 的摩尔质量为 ,该蓝色晶体密度为 ,该蓝色晶体密度为 ,Ⅱ型立方结构的边长为 ,Ⅱ型立方结构的边长为 ,则阿伏加德罗常数的值可表示为 ,则阿伏加德罗常数的值可表示为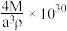 |
您最近一年使用:0次
4 . 某低温超导材料晶胞结构如图所示,下列说法中错误的是

| A.Sn位于周期表d区 | B.化学式为SnNb3 |
| C.该晶体内部有自由电子,是电的良导体 | D.Sn的配位数为12 |
您最近一年使用:0次
5 . 食盐是厨房中的调味品,其主要成分为NaCl(晶胞结构如图1所示),设NA为阿伏加德罗常数的值。下列说法错误的是 apm。
apm。

 apm。
apm。A.由图2可知: |
B.该晶体的密度为 ×1030g/cm3 ×1030g/cm3 |
C.在熔融状态下,反应KCl+Na NaCl+K↑能发生,是因为K的熔沸点比Na的熔沸点高 NaCl+K↑能发生,是因为K的熔沸点比Na的熔沸点高 |
| D.该晶胞中,每个Cl-周围距离最近且相等的Cl-有12个 |
您最近一年使用:0次
名校
解题方法
6 . 萤石是自然界中常见的含氟矿物,其晶胞结构如图所示,下列说法错误的是 ×100%;
×100%;
②该晶胞的参数为 anm;
anm;
③F-的半径为r1nm,Ca2+的半径为r2nm。

 ×100%;
×100%;②该晶胞的参数为
 anm;
anm;③F-的半径为r1nm,Ca2+的半径为r2nm。
A.Ca2+的空间利用率为 ×100% ×100% |
| B.a和b之间距离为r1+r2nm |
| C.该物质的分子式为CaF2 |
| D.CaF2中Ca2+采取面心立方最密堆积,每个Ca2+周围距离最近且相等的F-有8个 |
您最近一年使用:0次
名校
解题方法
7 .  是一种常见催化剂,能催化臭氧(
是一种常见催化剂,能催化臭氧( )与烟气(
)与烟气( 、
、 )的反应。回答下列问题:
)的反应。回答下列问题:
(1)写出 和
和 原子基态价电子排布式:
原子基态价电子排布式:___________ 、___________ 。
(2) 和
和 的中心原子轨道的杂化类型为
的中心原子轨道的杂化类型为___________ 、___________ 。
(3) 和
和 中所含元素的第一电离能由大到小的顺序是
中所含元素的第一电离能由大到小的顺序是___________ 。两种微粒的空间构型分别为___________ 、___________ 。
(4) 与
与 生成的
生成的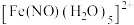 ,画出生成的
,画出生成的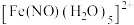 的结构简式,并用“
的结构简式,并用“ ”标出所有配位键:
”标出所有配位键:___________ 。
(5)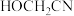 分子中含有的
分子中含有的 键和
键和 键的数目之比为
键的数目之比为___________ 。
(6)一种可吸收甲醛材料,其化学式为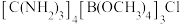 ,部分晶体结构如下图所示:
,部分晶体结构如下图所示: 为平面结构。
为平面结构。
①该材料包含的化学键类型有___________ 。
②组成该材料的 三元素的电负性由大到小的顺序是
三元素的电负性由大到小的顺序是___________ 。
(7)某高温超导材料,其晶胞结构如图所示,该立方晶胞参数为apm。阿伏加德罗常数的值为 。
。___________ 。
②该晶体的密度为___________  。
。
 是一种常见催化剂,能催化臭氧(
是一种常见催化剂,能催化臭氧( )与烟气(
)与烟气( 、
、 )的反应。回答下列问题:
)的反应。回答下列问题:(1)写出
 和
和 原子基态价电子排布式:
原子基态价电子排布式:(2)
 和
和 的中心原子轨道的杂化类型为
的中心原子轨道的杂化类型为(3)
 和
和 中所含元素的第一电离能由大到小的顺序是
中所含元素的第一电离能由大到小的顺序是(4)
 与
与 生成的
生成的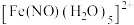 ,画出生成的
,画出生成的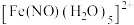 的结构简式,并用“
的结构简式,并用“ ”标出所有配位键:
”标出所有配位键:(5)
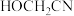 分子中含有的
分子中含有的 键和
键和 键的数目之比为
键的数目之比为(6)一种可吸收甲醛材料,其化学式为
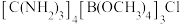 ,部分晶体结构如下图所示:
,部分晶体结构如下图所示: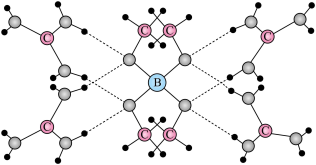
 为平面结构。
为平面结构。①该材料包含的化学键类型有
②组成该材料的
 三元素的电负性由大到小的顺序是
三元素的电负性由大到小的顺序是(7)某高温超导材料,其晶胞结构如图所示,该立方晶胞参数为apm。阿伏加德罗常数的值为
 。
。
②该晶体的密度为
 。
。
您最近一年使用:0次
8 .  (摩尔质量为
(摩尔质量为 )的晶胞形状为长方体,边长分别为a nm、b nm、c nm,结构如图所示。下列说法正确的是
)的晶胞形状为长方体,边长分别为a nm、b nm、c nm,结构如图所示。下列说法正确的是
 (摩尔质量为
(摩尔质量为 )的晶胞形状为长方体,边长分别为a nm、b nm、c nm,结构如图所示。下列说法正确的是
)的晶胞形状为长方体,边长分别为a nm、b nm、c nm,结构如图所示。下列说法正确的是
A. 的配位数为4 的配位数为4 |
B. 的空间结构为正四面体形 的空间结构为正四面体形 |
C. 的密度为 的密度为 |
D.配离子 中配体的中心原子价层电子对数为6 中配体的中心原子价层电子对数为6 |
您最近一年使用:0次
7日内更新
|
25次组卷
|
2卷引用:安徽省芜湖市2024届高三毕业班下学期5月教学质量统测化学试卷
9 . 金属铁因生产工艺和温度不同,会有不同的晶体结构。α-Fe和γ-Fe的晶体结构如图所示,下列说法正确的是
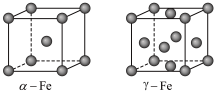
| A.金属铁因为有自由移动的离子而具有导电性 | B.1个γ-Fe晶胞的质量约为(4×56)g |
| C.γ-Fe中铁原子的配位数为12 | D.α-Fe与γ-Fe的性质相同 |
您最近一年使用:0次
10 . 由Sc、Sn、V组成的晶体晶胞如图1所示(晶胞底边边长为anm,高为cnm,a≠c),图2显示的是三种原子在xz面、yz面上的位置,图3显示的是Sc、Sn原子在xy面上的位置。已知:Sc原子半径为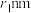 ,Sn原子半径为
,Sn原子半径为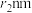 ,V原子半径为
,V原子半径为 。下列说法错误的是
。下列说法错误的是
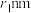 ,Sn原子半径为
,Sn原子半径为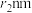 ,V原子半径为
,V原子半径为 。下列说法错误的是
。下列说法错误的是
| A.Sc、Sn、V三种元素的基态原子所含的价层电子个数:V>Sn>Sc |
| B.与Sc距离最近的Sc原子数为6 |
C.该合金的化学式为 |
D.该晶体的空间占有率: |
您最近一年使用:0次



