解题方法
1 . 某锂电池的负极材料由锂原子嵌入石墨烯层间形成,其晶胞结构如图甲,下列说法错误的是
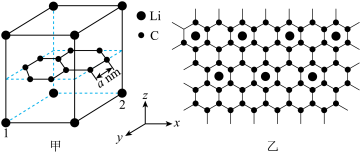

| A.该晶体的化学式为LiC6 |
B.1号、2号Li之间的距离为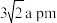 |
| C.图乙可表示该化合物沿z轴的局部投影图 |
| D.利用X射线衍射实验可测得晶胞参数α、β、γ |
您最近一年使用:0次
2 . 一种镁铜合金的晶胞拉维斯结构如图(a),该晶胞可看成由8个小立方体构成,其中4个小立方体体心填入Mg,另外4个小立方体的体心填入以四面体方式排列的Cu,其余Mg占据晶胞的顶点和面心。图(b)是对图(a)沿立方格子对角面取得的截图。设阿伏加德罗常数的值为 ,下列说法错误的是
,下列说法错误的是
 ,下列说法错误的是
,下列说法错误的是

| A.基态Mg原子核外电子有12种不同的运动状态 |
B. |
| C.上述合金的组成可表示为MgCu2 |
D.上述合金晶体的密度为 |
您最近一年使用:0次
3 . 过渡元素锰能形成很多重要的化合物。回答下列问题:
(1)三醋酸锰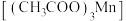 是一种有机反应氧化剂。Mn在元素周期表中的位置为
是一种有机反应氧化剂。Mn在元素周期表中的位置为___________ 。下列表示锰原子处于激发态的有___________ (填标号,下同),其中能量较高的是___________ 。
a.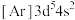 b.
b.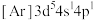 c.
c.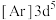 d.
d.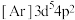
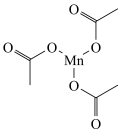
(2)三醋酸锰是一种配合物,其结构如图所示,所含 键和
键和 键个数之比为
键个数之比为___________ 。羧酸可表示为A―H, 、
、 和
和 酸性随A―H间的电子云密度增大而减弱,其中酸性最弱的是
酸性随A―H间的电子云密度增大而减弱,其中酸性最弱的是___________ 。
(3)锰酸锂( )可作为锂离子电池的正极材料,通过
)可作为锂离子电池的正极材料,通过 嵌入或脱嵌实现充放电。
嵌入或脱嵌实现充放电。
①锰酸锂可充电电池的总反应为: 。
。 从锰酸锂中脱嵌的过程为
从锰酸锂中脱嵌的过程为___________ 。(填“放电”或“充电”)过程,对应的电极反应式为___________ 。
② 晶胞可看成由图1中A、B单元按图2方式构成。图1中“
晶胞可看成由图1中A、B单元按图2方式构成。图1中“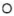 ”表示
”表示 ,则“
,则“ ”表示的微粒是
”表示的微粒是___________ 。(填离子符号)。

(1)三醋酸锰
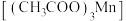 是一种有机反应氧化剂。Mn在元素周期表中的位置为
是一种有机反应氧化剂。Mn在元素周期表中的位置为a.
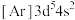 b.
b.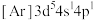 c.
c.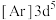 d.
d.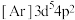
(2)三醋酸锰是一种配合物,其结构如图所示,所含
 键和
键和 键个数之比为
键个数之比为 、
、 和
和 酸性随A―H间的电子云密度增大而减弱,其中酸性最弱的是
酸性随A―H间的电子云密度增大而减弱,其中酸性最弱的是
(3)锰酸锂(
 )可作为锂离子电池的正极材料,通过
)可作为锂离子电池的正极材料,通过 嵌入或脱嵌实现充放电。
嵌入或脱嵌实现充放电。①锰酸锂可充电电池的总反应为:
 。
。 从锰酸锂中脱嵌的过程为
从锰酸锂中脱嵌的过程为②
 晶胞可看成由图1中A、B单元按图2方式构成。图1中“
晶胞可看成由图1中A、B单元按图2方式构成。图1中“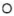 ”表示
”表示 ,则“
,则“ ”表示的微粒是
”表示的微粒是
您最近一年使用:0次
4 .  可用于防蛀牙膏的添加剂,其晶胞结构如图所示,晶胞参数为
可用于防蛀牙膏的添加剂,其晶胞结构如图所示,晶胞参数为 ,下列说法正确的是
,下列说法正确的是

 可用于防蛀牙膏的添加剂,其晶胞结构如图所示,晶胞参数为
可用于防蛀牙膏的添加剂,其晶胞结构如图所示,晶胞参数为 ,下列说法正确的是
,下列说法正确的是
A.含 添加剂的牙膏可以在酸性条件下保持很好的效果 添加剂的牙膏可以在酸性条件下保持很好的效果 |
B.图中黑色的球●代表 |
C.每个 周围紧邻且等距离的 周围紧邻且等距离的 个数为4 个数为4 |
D. 与 与 最小核心距为 最小核心距为 |
您最近一年使用:0次
名校
解题方法
5 . 某种铁的氧化物的立方体结构如图所示,白球为 ,其余代表铁的离子,
,其余代表铁的离子, 表示阿伏加德罗常数的值。下列有关说法错误的是
表示阿伏加德罗常数的值。下列有关说法错误的是
 ,其余代表铁的离子,
,其余代表铁的离子, 表示阿伏加德罗常数的值。下列有关说法错误的是
表示阿伏加德罗常数的值。下列有关说法错误的是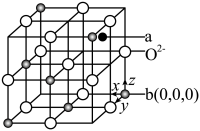
A. 的离子均位于 的离子均位于 构成的正八面体空隙中 构成的正八面体空隙中 |
B.该铁的氧化物的化学式为 |
C.设立方体的棱长为1,则 点的坐标为 点的坐标为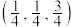 |
D.若立方体棱长为 ,则晶体密度计算式为 ,则晶体密度计算式为 |
您最近一年使用:0次
2024-02-26更新
|
397次组卷
|
3卷引用:河北省2023-2024学年高三上学期质量监测期末联考化学试题
名校
解题方法
6 . X、Y、R、Q为前四周期元素且原子序数依次增大,X的单质与氢气可以化合生成气体G,其水溶液呈碱性;Y的一种单质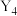 中分子为正四面体结构;R基态原子的核外有6个单电子;Q的基态原子M层电子全充满,N层只有一个电子。请回答下列问题:
中分子为正四面体结构;R基态原子的核外有6个单电子;Q的基态原子M层电子全充满,N层只有一个电子。请回答下列问题:
(1)Q元素在周期表中的位置是______ 。
(2) 价层的轨道表示式是
价层的轨道表示式是______ 。
(3)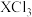 与
与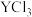 的键角大小为:
的键角大小为: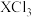
______  (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。
(4)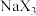 可用于安全气囊的产气药剂,
可用于安全气囊的产气药剂, 离子中中心原子的杂化方式为
离子中中心原子的杂化方式为______ 杂化。
(5)如下图所示Y可形成多种含氧酸根:
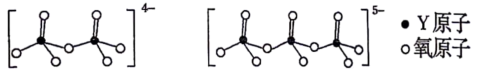
这类酸根离子的化学式可用通式表示为______ (用n代表Y原子数)。
(6)已知R元素形成的配合物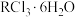 中心原子
中心原子 配位数为6,向含
配位数为6,向含 的溶液中滴加
的溶液中滴加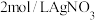 溶液,反应完全后消耗
溶液,反应完全后消耗 溶液
溶液 ,则该配离子的化学式为
,则该配离子的化学式为______ 。
(7)已知 晶体结构单元如下图所示,离H最近且等距的H的个数为
晶体结构单元如下图所示,离H最近且等距的H的个数为______ 。

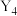 中分子为正四面体结构;R基态原子的核外有6个单电子;Q的基态原子M层电子全充满,N层只有一个电子。请回答下列问题:
中分子为正四面体结构;R基态原子的核外有6个单电子;Q的基态原子M层电子全充满,N层只有一个电子。请回答下列问题:(1)Q元素在周期表中的位置是
(2)
 价层的轨道表示式是
价层的轨道表示式是(3)
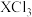 与
与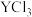 的键角大小为:
的键角大小为: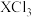
 (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。(4)
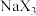 可用于安全气囊的产气药剂,
可用于安全气囊的产气药剂, 离子中中心原子的杂化方式为
离子中中心原子的杂化方式为(5)如下图所示Y可形成多种含氧酸根:

这类酸根离子的化学式可用通式表示为
(6)已知R元素形成的配合物
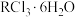 中心原子
中心原子 配位数为6,向含
配位数为6,向含 的溶液中滴加
的溶液中滴加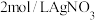 溶液,反应完全后消耗
溶液,反应完全后消耗 溶液
溶液 ,则该配离子的化学式为
,则该配离子的化学式为(7)已知
 晶体结构单元如下图所示,离H最近且等距的H的个数为
晶体结构单元如下图所示,离H最近且等距的H的个数为
您最近一年使用:0次
解题方法
7 . 某种新型储氢材料(摩尔质量为188g∙mol–1)的立方晶胞如图,该晶胞可储存6个氢原子。已知M核内中子数比质子数多4,标准状况下氢气的密度为ρg∙cm–3,NA表示阿伏加德罗常数的值。下列说法正确的是
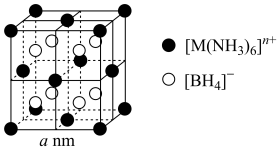

| A.晶胞中[M(NH3)6]n+和[BH4]–的配位数相同 |
| B.M离子最外层电子排布式为3s23p63d6 |
C.在晶胞体对角线的一维空间上会出现 的排布规律 的排布规律 |
D.该材料的储氢能力[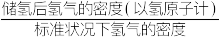 ]为 ]为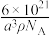 |
您最近一年使用:0次
名校
8 . 砷化镓是当代国际公认的继“硅”之后最成熟的半导体材料,是光电子和微电子工业最重要的支撑材料之一、砷化镓晶胞如图所示。(设 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
| A.晶体的熔点:砷化镓<氮化镓 | B.晶胞中 的键长为 的键长为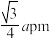 |
| C.砷化镓晶体中存在非极性共价键 | D.该晶体的理论密度为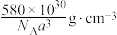 |
您最近一年使用:0次
名校
9 . 因生产金属铁的工艺和温度不同,产生的铁单质的晶体结构、密度和性质均不同,铁的晶体中铁原子有三种堆积方式,其中两种立方晶胞结构如图所示。下列关于铁或其晶胞的说法中正确的是
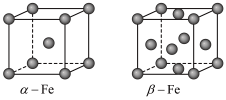

| A.铁在周期表中位于第四周期第VIIIB族,是过渡元素也是副族元素 |
| B.在两种晶胞中,每个Fe原子周围均有8个与之距离相等且最近的Fe原子 |
C.若ɑ-Fe晶胞边长为bpm,则Fe原子半径r= bpm bpm |
D.若β-Fe晶胞中最近的两个Fe原子核间距为apm,阿伏加德罗常数为NA,晶胞的密度表达式是 |
您最近一年使用:0次
解题方法
10 . 甲为碳单质的一种晶体,其二维结构图如图,乙为C、K原子构成的一种晶体,其二维结构图如图。下列叙述错误的是


| A.甲、乙的二维材料都具有良好的导电性 |
B.甲、乙中碳原子都是 杂化 杂化 |
C.乙的化学式为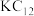 |
D.甲中碳原子数与 键数之比为2:3 键数之比为2:3 |
您最近一年使用:0次



