名校
解题方法
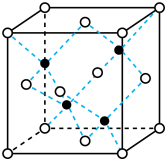
1 . Cu的化合物种类繁多,在人类的生产生活中有着广泛的应用,实验测得一种Cu与Br形成的化合物沸点为1345℃,晶胞结构如图所示(黑球代表铜,晶胞的密度为ρ g·cm-3,设 为阿伏加德罗常数的值),下列说法正确的是
为阿伏加德罗常数的值),下列说法正确的是
 为阿伏加德罗常数的值),下列说法正确的是
为阿伏加德罗常数的值),下列说法正确的是
| A.晶体的化学式为CuBr2 |
| B.晶体中与Br最近且距离相等的Br有6个 |
C.Cu与Br之间的最短距离为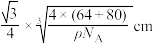 |
| D.该化合物为共价晶体 |
您最近一年使用:0次
名校
解题方法
2 . 自然界中,纯粹的典型晶体是不多的,大多数晶体是分子晶体、共价晶体、金属晶体和离子晶体之间的过渡晶体。以下列出了第三周期几种氧化物晶体中离子键的百分数。
提示:离子键的百分数是通过电负性的差值计算出来的,电负性的差值越大,离子键的百分数越大。
(1)从原子结构角度解释,为什么一般认为氧化镁属于离子晶体,而二氧化硅属于共价晶体:___________ 。
(2)硅元素位于元素周期表的___________ 区。基态硅原子的价层电子排布式为___________ 。
(3)一种硼镁化合物具有超导性能,晶体结构属于六方晶系,其晶体结构、晶胞沿c轴的投影图如下所示,已知该晶体中晶胞各边长度分别为apm、apm和cpm,两条底边夹角为120°,距离最近的两个B原子之间距离为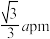 。
。
①该物质化学式为___________ ;
②距离每个B原子最近的Mg原子有___________ 个;
③该晶体密度为___________  。
。 含量。
含量。
(ⅰ)称取m克硅酸钠样品加热溶解后,配置为250mL待测液。
(ⅱ)移取50mL待测液至250mL锥形瓶中,加入10滴甲基红指示剂【HIn(红色) (黄色)】,摇匀后用0.2000mol/L HCl标准溶液滴定至体系为玫瑰红色,消耗盐酸体积为
(黄色)】,摇匀后用0.2000mol/L HCl标准溶液滴定至体系为玫瑰红色,消耗盐酸体积为 ,体系中有沉淀。
,体系中有沉淀。
(ⅲ)加入3.0g氟化钠固体,充分反应。
(ⅳ)用0.5000mol/L HCl标准溶液滴定至溶液为玫瑰红色并继续加入至过量,共加入 。
。
(ⅴ)用0.5000mol/L NaOH标准溶液滴定至溶液变为亮黄色,消耗NaOH溶液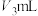 。
。
已知: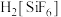 为强电解质,回答问题:
为强电解质,回答问题:
①步骤(ⅲ)中加入NaF后发生化学反应的离子方程式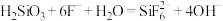 ,则加入NaF后的实验现象为
,则加入NaF后的实验现象为___________ 。
②样品中硅酸钠的纯度为___________ (用质量分数表示)。
| 氧化物 |  | MgO |  |  |
| 离子键百分数 | 62 | 50 | 41 | 33 |
(1)从原子结构角度解释,为什么一般认为氧化镁属于离子晶体,而二氧化硅属于共价晶体:
(2)硅元素位于元素周期表的
(3)一种硼镁化合物具有超导性能,晶体结构属于六方晶系,其晶体结构、晶胞沿c轴的投影图如下所示,已知该晶体中晶胞各边长度分别为apm、apm和cpm,两条底边夹角为120°,距离最近的两个B原子之间距离为
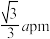 。
。①该物质化学式为
②距离每个B原子最近的Mg原子有
③该晶体密度为
 。
。
 含量。
含量。(ⅰ)称取m克硅酸钠样品加热溶解后,配置为250mL待测液。
(ⅱ)移取50mL待测液至250mL锥形瓶中,加入10滴甲基红指示剂【HIn(红色)
 (黄色)】,摇匀后用0.2000mol/L HCl标准溶液滴定至体系为玫瑰红色,消耗盐酸体积为
(黄色)】,摇匀后用0.2000mol/L HCl标准溶液滴定至体系为玫瑰红色,消耗盐酸体积为 ,体系中有沉淀。
,体系中有沉淀。(ⅲ)加入3.0g氟化钠固体,充分反应。
(ⅳ)用0.5000mol/L HCl标准溶液滴定至溶液为玫瑰红色并继续加入至过量,共加入
 。
。(ⅴ)用0.5000mol/L NaOH标准溶液滴定至溶液变为亮黄色,消耗NaOH溶液
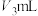 。
。已知:
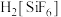 为强电解质,回答问题:
为强电解质,回答问题:①步骤(ⅲ)中加入NaF后发生化学反应的离子方程式
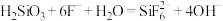 ,则加入NaF后的实验现象为
,则加入NaF后的实验现象为②样品中硅酸钠的纯度为
您最近一年使用:0次
解题方法
3 .  是人体必需微量元素之一、研究表明硒代蛋氨酸(结构简式如下图)有抗氧化作用,对肿瘤细胞增殖有显著抑制作用。
是人体必需微量元素之一、研究表明硒代蛋氨酸(结构简式如下图)有抗氧化作用,对肿瘤细胞增殖有显著抑制作用。_______ 。
(2)N、O、 的第一电离能由大到小的顺序为
的第一电离能由大到小的顺序为_______ , 的空间结构为
的空间结构为_______ 。
(3)固态硒代蛋氨酸晶体类型为_______ ,硒代蛋氨酸分子中 的杂化方式为
的杂化方式为_______ 。
(4)比较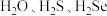 的沸点大小:
的沸点大小:_______ ,原因是_______ 。
(5)某种具有氧原子缺陷的超导材料的长方体晶胞结构如图所示。晶胞参数分别为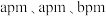 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。已知该晶体中
。已知该晶体中 为
为 价,Y为
价,Y为 价,O为
价,O为 价,则
价,则
_______ ,该晶体的密度为_______  。
。
 是人体必需微量元素之一、研究表明硒代蛋氨酸(结构简式如下图)有抗氧化作用,对肿瘤细胞增殖有显著抑制作用。
是人体必需微量元素之一、研究表明硒代蛋氨酸(结构简式如下图)有抗氧化作用,对肿瘤细胞增殖有显著抑制作用。
(2)N、O、
 的第一电离能由大到小的顺序为
的第一电离能由大到小的顺序为 的空间结构为
的空间结构为(3)固态硒代蛋氨酸晶体类型为
 的杂化方式为
的杂化方式为(4)比较
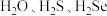 的沸点大小:
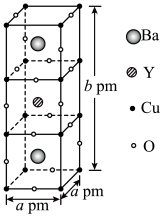
的沸点大小:(5)某种具有氧原子缺陷的超导材料的长方体晶胞结构如图所示。晶胞参数分别为
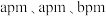 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。已知该晶体中
。已知该晶体中 为
为 价,Y为
价,Y为 价,O为
价,O为 价,则
价,则
 。
。
您最近一年使用:0次
名校
解题方法
4 . 一种含钒的锑化物 在超导方面具有潜在的应用前景,
在超导方面具有潜在的应用前景, 的晶胞结构如图甲所示,晶胞高度
的晶胞结构如图甲所示,晶胞高度 处水平截面如图乙所示:
处水平截面如图乙所示:
 在超导方面具有潜在的应用前景,
在超导方面具有潜在的应用前景, 的晶胞结构如图甲所示,晶胞高度
的晶胞结构如图甲所示,晶胞高度 处水平截面如图乙所示:
处水平截面如图乙所示:
A.M的化学式为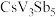 |
| B.M中V的化合价为+4和+5 |
| C.V原子周围紧邻的Sb原子数为6 |
| D.M晶体不导电,熔融状态可导电 |
您最近一年使用:0次
2024-06-04更新
|
111次组卷
|
2卷引用:河北省张家口市2024届高三下学期第三次模拟考试化学试卷
名校
5 . 氮的某种氧化物晶胞结构如图所示,由两种离子构成,下列说法错误的是

| A.晶胞中阴阳离子中N原子杂化类型不同 |
B.晶体密度: |
| C.阳离子中N—O键长<阴离子中N—O键长 |
| D.该氧化物发生水解反应的产物只有一种 |
您最近一年使用:0次
2024-05-31更新
|
163次组卷
|
2卷引用:2024届山东省日照市五莲县第一中学高三下学期模拟预测化学试题
解题方法
6 . 氰氨化钙是无公害农产品生产中极具使用价值的一种土壤改良剂,其晶胞结构如图所示,下列有关说法错误的是
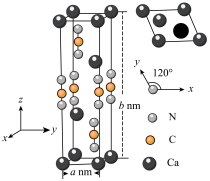
| A.该化合物的焰色试验为砖红色 | B.氰氨化钙的化学式为 |
| C.每个阴离子团的配位数为12 | D.该晶体的密度为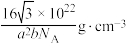 |
您最近一年使用:0次
名校
7 . 如图所示,Ti和Au可以形成 和
和 两种不同类型的合金。在
两种不同类型的合金。在 类型晶胞(
类型晶胞( ,
,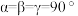 )中,Au原子位于顶点,Ti原子位于面心。在
)中,Au原子位于顶点,Ti原子位于面心。在 型晶胞(
型晶胞(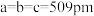 ,
, )中,Au原子位于顶点和体心,每个晶胞面上有两个Ti原子,它们之间的连线平行于晶胞的棱且连线中点为面心,它们之间的距离恰好是晶胞棱长的一半。
)中,Au原子位于顶点和体心,每个晶胞面上有两个Ti原子,它们之间的连线平行于晶胞的棱且连线中点为面心,它们之间的距离恰好是晶胞棱长的一半。
 和
和 两种不同类型的合金。在
两种不同类型的合金。在 类型晶胞(
类型晶胞( ,
,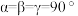 )中,Au原子位于顶点,Ti原子位于面心。在
)中,Au原子位于顶点,Ti原子位于面心。在 型晶胞(
型晶胞(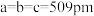 ,
, )中,Au原子位于顶点和体心,每个晶胞面上有两个Ti原子,它们之间的连线平行于晶胞的棱且连线中点为面心,它们之间的距离恰好是晶胞棱长的一半。
)中,Au原子位于顶点和体心,每个晶胞面上有两个Ti原子,它们之间的连线平行于晶胞的棱且连线中点为面心,它们之间的距离恰好是晶胞棱长的一半。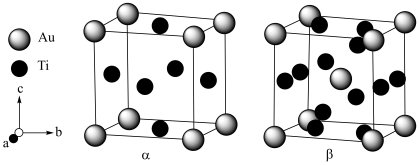
A. 和 和 两种合金的化学式都是 两种合金的化学式都是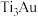 |
B. 和 和 两种晶胞中Ti的配位数均为6 两种晶胞中Ti的配位数均为6 |
C. 晶体的密度为 晶体的密度为 |
D. 型的合金硬度更高 型的合金硬度更高 |
您最近一年使用:0次
解题方法
8 . 威尔逊氏病是一种遗传性疾病,铜元素会在肝脏和其他组织内积聚。二巯基丙醇(Ⅰ: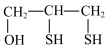 )能和铜结合成化合物Ⅱ:
)能和铜结合成化合物Ⅱ: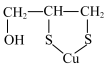 ,并通过尿液排出体外,故可用于治疗威尔逊氏病。
,并通过尿液排出体外,故可用于治疗威尔逊氏病。
(2)金属铜的化合物应用也十分广泛。如铜的某种氧化物广泛应用于太阳能电池领域。其晶胞如图所示:

②该晶胞为立方体,边长为anm,设
 为阿伏加德罗常数的值,则该晶胞的密度为
为阿伏加德罗常数的值,则该晶胞的密度为 。
。③下列说法正确的是
A.
 中的S原子均采取sp杂化
中的S原子均采取sp杂化B.
 中所有元素中S的电负性最大
中所有元素中S的电负性最大C.
 在水溶液中以
在水溶液中以 形式存在,
形式存在, 的配位原子为O
的配位原子为OD.
 和铜结合成
和铜结合成 ,是因为S的电负性比O小,更易与铜离子形成配位键
,是因为S的电负性比O小,更易与铜离子形成配位键(3)①水、②甲醇、③甲硫醇(
 )的沸点从大到小的顺序为
)的沸点从大到小的顺序为
您最近一年使用:0次
9 . 磷化硼是一种超硬耐磨涂层材料,结构与金刚石相似,其晶胞结构如图所示。请回答下列问题:___________ ,基态磷原子中电子的运动状态有___________ 种,与硼同主族的第四周期元素的基态原子价层电子的轨道表示式为___________ 。
(2) 为一元弱酸,
为一元弱酸, 分子中
分子中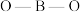 的键角
的键角___________ (填“ ”“
”“ ”或“
”或“ ”)
”) (中的
(中的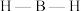 的键角,原因为
的键角,原因为___________ 。
(3)磷化硼晶体属于___________ 晶体,其中硼原子的配位数为___________ 。
(4)磷化硼的化学式为___________ ,该晶体的密度为___________  (用含a、
(用含a、 的代数式表示,阿伏加德罗常数的值为
的代数式表示,阿伏加德罗常数的值为 )。
)。

(2)
 为一元弱酸,
为一元弱酸, 分子中
分子中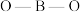 的键角
的键角 ”“
”“ ”或“
”或“ ”)
”) (中的
(中的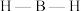 的键角,原因为
的键角,原因为(3)磷化硼晶体属于
(4)磷化硼的化学式为
 (用含a、
(用含a、 的代数式表示,阿伏加德罗常数的值为
的代数式表示,阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
10 . 二氧化铈(CeO2)作为一种脱硝催化剂,能在Ce4+和Ce3+之间改变氧化状态,将NO氧化为NO2,并引起氧空位的形成,得到新的铈氧化物[Cex(Ⅲ)Cey(Ⅳ)Oz]。当二氧化铈晶胞发生如下图变化时,有关说法错误的是
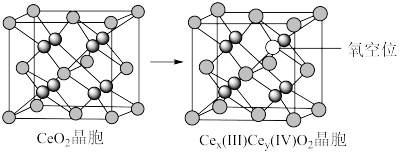
| A.铈位于氧原子形成的八面体空隙中 |
| B.生成新的铈氧化物中x、y、z的最简整数比为2:2:7,当1 mol CeO2发生变化时,可吸收标况下NO的体积为5.6 L |
C.晶胞的俯视图为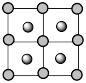 |
D.若晶胞边长为a pm,则CeO2晶体的密度为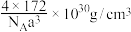 (NA表示阿伏加德罗常数的值) (NA表示阿伏加德罗常数的值) |
您最近一年使用:0次



