名校
解题方法
1 . 2024年3月上海交大韩礼元教授团队再发 论文,在钙钛矿太阳能电池稳定性领域获得新进展。钙钛可矿晶体晶胞结构如图所示,设晶体的密度为
论文,在钙钛矿太阳能电池稳定性领域获得新进展。钙钛可矿晶体晶胞结构如图所示,设晶体的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,下列说法错误的是
,下列说法错误的是
 论文,在钙钛矿太阳能电池稳定性领域获得新进展。钙钛可矿晶体晶胞结构如图所示,设晶体的密度为
论文,在钙钛矿太阳能电池稳定性领域获得新进展。钙钛可矿晶体晶胞结构如图所示,设晶体的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,下列说法错误的是
,下列说法错误的是
A.晶体的化学式为 |
| B.晶体中钛离子位于氧离子所形成的八面体空隙中 |
C.若图中A的原子分数坐标为 ,则B的原子分数坐标为 ,则B的原子分数坐标为 |
D.晶胞中钛离子与钙离子之间的距离为 |
您最近一年使用:0次
2 . 二氧化铈(CeO2)晶体属于立方CaF2型晶体结构(如图所示),其中晶胞参数为apm,下列说法正确的是
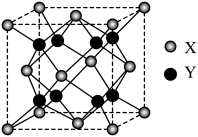
| A.Y代表O2- |
| B.Ce4+与O2-的核间距离最小为0.5apm |
C.该晶体的摩尔体积为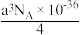 m3/mol m3/mol |
| D.离Ce4+等距离最近的Ce4+有8个 |
您最近一年使用:0次
3 . 二氧化铈(CeO2)作为一种脱硝催化剂,能在Ce4+和Ce3+之间改变氧化状态,将NO氧化为NO2,并引起氧空位的形成,得到新的铈氧化物[Cex(Ⅲ)Cey(Ⅳ)Oz]。当二氧化铈晶胞发生如下图变化时,有关说法错误的是
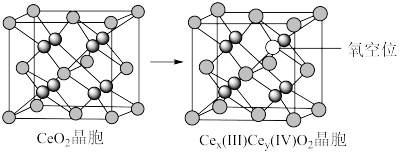
| A.铈位于氧原子形成的八面体空隙中 |
| B.生成新的铈氧化物中x、y、z的最简整数比为2:2:7,当1 mol CeO2发生变化时,可吸收标况下NO的体积为5.6 L |
C.晶胞的俯视图为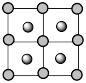 |
D.若晶胞边长为a pm,则CeO2晶体的密度为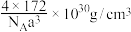 (NA表示阿伏加德罗常数的值) (NA表示阿伏加德罗常数的值) |
您最近一年使用:0次
名校
4 . 大力发展光伏产业对我国新能源体系建设具有重要作用。目前,对光伏材料中钙钛矿半导体材料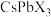 (
(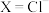 ,
, ,
, )、甲脒铅碘基钙钛矿
)、甲脒铅碘基钙钛矿 (
( )和双钙钛矿(
)和双钙钛矿( )性能的研究正不断深入。回答下列问题:
)性能的研究正不断深入。回答下列问题:
(1)Cs和Pb分别为第6周期ⅠA和ⅣA元素,基态Pb原子的价电子排布式为___________ ,两种元素原子第一电离能的大小顺序为___________ 。
(2)甲脒{ }中三种元素的电负性大小顺序为
}中三种元素的电负性大小顺序为___________ 。1mol甲脒中存在___________ mol  键。解释
键。解释 中∠NCH键角大于
中∠NCH键角大于 中∠NCH键角的原因:
中∠NCH键角的原因:___________ 。
(3)某种双钙钛矿( )晶体的一种结构单元(晶胞的
)晶体的一种结构单元(晶胞的 )如下图所示。
)如下图所示。___________ ;
②晶体中与 最近且距离相等的
最近且距离相等的 数目为
数目为___________ 个。 周围的
周围的 构成
构成___________ (填空间构型);
③该晶体的密度是___________  (列出表达式,阿伏加德罗常数为
(列出表达式,阿伏加德罗常数为 )。
)。
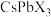 (
(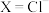 ,
, ,
, )、甲脒铅碘基钙钛矿
)、甲脒铅碘基钙钛矿 (
( )和双钙钛矿(
)和双钙钛矿( )性能的研究正不断深入。回答下列问题:
)性能的研究正不断深入。回答下列问题:(1)Cs和Pb分别为第6周期ⅠA和ⅣA元素,基态Pb原子的价电子排布式为
(2)甲脒{
 }中三种元素的电负性大小顺序为
}中三种元素的电负性大小顺序为 键。解释
键。解释 中∠NCH键角大于
中∠NCH键角大于 中∠NCH键角的原因:
中∠NCH键角的原因:(3)某种双钙钛矿(
 )晶体的一种结构单元(晶胞的
)晶体的一种结构单元(晶胞的 )如下图所示。
)如下图所示。
②晶体中与
 最近且距离相等的
最近且距离相等的 数目为
数目为 周围的
周围的 构成
构成③该晶体的密度是
 (列出表达式,阿伏加德罗常数为
(列出表达式,阿伏加德罗常数为 )。
)。
您最近一年使用:0次
名校
解题方法
5 . 科学家研发出一种新型储氢材料,晶胞结构如下图所示,晶胞参数为apm,下列说法正确的是
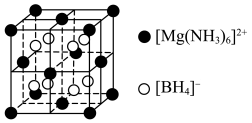
| A.所含非金属元素的电负性N>B>H |
B.该晶体的化学式为 |
C.阴、阳离子的最小距离为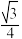 apm apm |
| D.若晶胞以[BH4]-为顶点,所得晶胞结构与NaCl晶胞相同 |
您最近一年使用:0次
解题方法
6 . 钛酸钙是一种典型的钙钛矿型半导体材料,其晶胞结构如图所示。下列关于钛酸钙说法不正确的是

| A.每个晶胞中含有3个O2﹣ |
| B.化学式为CaTiO3 |
| C.含有离子键 |
| D.晶体具有良好的导电性和延展性 |
您最近一年使用:0次
7 . 由 、
、 、
、 等元素组成的钒基笼目金属在超导电性方面有广阔的应用前景,其晶胞结构如下图所示。下列说法错误的是
等元素组成的钒基笼目金属在超导电性方面有广阔的应用前景,其晶胞结构如下图所示。下列说法错误的是
 、
、 、
、 等元素组成的钒基笼目金属在超导电性方面有广阔的应用前景,其晶胞结构如下图所示。下列说法错误的是
等元素组成的钒基笼目金属在超导电性方面有广阔的应用前景,其晶胞结构如下图所示。下列说法错误的是
A.钒基笼目金属的化学式为 | B. 分布在由 分布在由 构成的八面体空隙中 构成的八面体空隙中 |
C.可以通过 射线衍射实验测定晶体结构 射线衍射实验测定晶体结构 | D.1号、2号 原子间的距离为 原子间的距离为 |
您最近一年使用:0次
8 .  的晶胞示意图如图甲所示。存在“缺陷”的氧化镍晶体
的晶胞示意图如图甲所示。存在“缺陷”的氧化镍晶体 如图乙所示(一个
如图乙所示(一个 空缺,另有两个
空缺,另有两个 被两个
被两个 所取代,其晶体仍呈电中性)。下列说法正确的是
所取代,其晶体仍呈电中性)。下列说法正确的是
 的晶胞示意图如图甲所示。存在“缺陷”的氧化镍晶体
的晶胞示意图如图甲所示。存在“缺陷”的氧化镍晶体 如图乙所示(一个
如图乙所示(一个 空缺,另有两个
空缺,另有两个 被两个
被两个 所取代,其晶体仍呈电中性)。下列说法正确的是
所取代,其晶体仍呈电中性)。下列说法正确的是
A. 元素位于元素周期表的 元素位于元素周期表的 区 区 |
B. 晶体中每个 晶体中每个 周围与它距离相等且最近的 周围与它距离相等且最近的 有6个 有6个 |
C.某氧化镍 晶体中 晶体中 与 与 的个数比为 的个数比为 ,则 ,则 |
D. 晶体中与一个 晶体中与一个 距离相等且最近的 距离相等且最近的 构成的空间几何形状为正四面体 构成的空间几何形状为正四面体 |
您最近一年使用:0次
9 . 硫元素化合物非常丰富,应用广泛。
请回答:
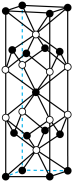
(1)由钾、镍、硫三种元素组成的某电极材料的晶胞如图,已知钾离子位于晶胞顶点及体心,其化学式是___________ ,与钾离子直接相邻的元素是___________ (填元素符号)。
(3)①硫酰卤( ):
):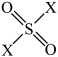 ,分子中S原子的杂化方式为:
,分子中S原子的杂化方式为:___________ ;比较键角
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
请回答:
(1)由钾、镍、硫三种元素组成的某电极材料的晶胞如图,已知钾离子位于晶胞顶点及体心,其化学式是
A.基态S原子的价层电子排布图: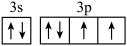 |
B.第一电离能: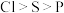 |
| C.K、Ni同为第四周期金属元素,都处于元素周期表d区 |
D.离子半径: |
(3)①硫酰卤(
 ):
): ,分子中S原子的杂化方式为:
,分子中S原子的杂化方式为:
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。②氟磺酸(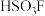 )属于超酸,可看作
)属于超酸,可看作 部分水解形成的产物。氟磺酸酸性比硫酸强。请从分子结构上说明氟磺酸酸性强的原因:
部分水解形成的产物。氟磺酸酸性比硫酸强。请从分子结构上说明氟磺酸酸性强的原因: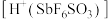 ,由
,由 (
(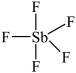 )与
)与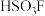 等物质的量化合生成。写出其中阴离子的结构式:
等物质的量化合生成。写出其中阴离子的结构式:
您最近一年使用:0次
10 . 钒的某种氧化物的立方晶胞结构如图所示。已知: 为阿伏加德罗常数的值,晶体密度为d
为阿伏加德罗常数的值,晶体密度为d  。下列叙述正确的是
。下列叙述正确的是
 为阿伏加德罗常数的值,晶体密度为d
为阿伏加德罗常数的值,晶体密度为d  。下列叙述正确的是
。下列叙述正确的是
| A.基态V的电子占11个能级 | B.该晶体的化学式为 |
| C.1个晶胞含2个钒离子 | D.晶胞参数a为 |
您最近一年使用:0次



