解题方法
1 . 已知镁铁氢化物的结构如图所示(氢未画出),晶胞参数 原子间的最近距离为晶胞参数的一半,
原子间的最近距离为晶胞参数的一半, 原子以正八面体的配位模式有序分布在
原子以正八面体的配位模式有序分布在 原子周围。设阿伏加德罗常数的值为
原子周围。设阿伏加德罗常数的值为 ,下列说法正确的是
,下列说法正确的是
 原子间的最近距离为晶胞参数的一半,
原子间的最近距离为晶胞参数的一半, 原子以正八面体的配位模式有序分布在
原子以正八面体的配位模式有序分布在 原子周围。设阿伏加德罗常数的值为
原子周围。设阿伏加德罗常数的值为 ,下列说法正确的是
,下列说法正确的是
A.该镁铁氢化物的化学式为 |
B.所含元素的第一电离能: |
C.晶胞中与 原子距离最近且等距的 原子距离最近且等距的 原子有4个 原子有4个 |
D.镁铁氢化物中氢的密度是标准状况下的氢气密度的 倍 倍 |
您最近一年使用:0次
解题方法
2 . 铜的化合物可用于制造催化剂,铜和氧形成的一种离子化合物的晶体结构如图。下列有关说法正确的是

A.化学式为 | B.阳离子的配位数3 |
C.该物质的密度为 | D.基态O原子电子排布图 |
您最近一年使用:0次
2024-05-17更新
|
147次组卷
|
2卷引用:贵州省毕节市2024届高三下学期三模考试化学试题
解题方法
3 . 过渡元素在材料和化工生产中占有重要地位。
(1) 中的化学键具有明显的共价性,蒸气状态下以双聚分子存在(
中的化学键具有明显的共价性,蒸气状态下以双聚分子存在(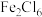 ),写出氯化铁双聚分子的结构式
),写出氯化铁双聚分子的结构式___________ 。
(2)元素Mn和Fe的部分电离能如下表所示,发现Mn元素的第三电离能( )要大于Fe元素的第三电离能,原因是
)要大于Fe元素的第三电离能,原因是___________ 。
(3)Mn的一种配合物化学式为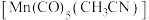 ,下列说法正确的是___________。
,下列说法正确的是___________。
(4)某晶体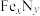 的晶胞如图1所示,Cu可以完全取代该晶体中a位置Fe或b位置Fe,
的晶胞如图1所示,Cu可以完全取代该晶体中a位置Fe或b位置Fe,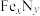 转化为两种Cu替代型产物的能量变化如图2所示。
转化为两种Cu替代型产物的能量变化如图2所示。___________ 。
②下列关于晶体的说法正确的是___________ 。
A.晶体的形成与晶体的自范性有关
B.测定某一固体是否属于晶体可以用X-射线衍射仪进行实验
C.晶体和非晶体的根本区别在于固体是否有规则的几何外形
D.由玻璃制成规则的玻璃球体现了晶体的自范性
E.晶胞是晶体结构中最小的重复单元
(1)
 中的化学键具有明显的共价性,蒸气状态下以双聚分子存在(
中的化学键具有明显的共价性,蒸气状态下以双聚分子存在(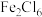 ),写出氯化铁双聚分子的结构式
),写出氯化铁双聚分子的结构式(2)元素Mn和Fe的部分电离能如下表所示,发现Mn元素的第三电离能(
 )要大于Fe元素的第三电离能,原因是
)要大于Fe元素的第三电离能,原因是| 元素 | Mn | Fe | |
| 电离能 (  ) ) |  | 717 | 759 |
 | 1509 | 1561 | |
 | 3248 | 2957 | |
(3)Mn的一种配合物化学式为
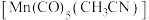 ,下列说法正确的是___________。
,下列说法正确的是___________。A. 与Mn原子配位时,提供孤电子对的是C原子 与Mn原子配位时,提供孤电子对的是C原子 |
| B.电负性:H<C<N<O |
C. 中两个C原子的杂化类型均为 中两个C原子的杂化类型均为 |
D. 中σ键与π键数目之比为5:2 中σ键与π键数目之比为5:2 |
(4)某晶体
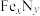 的晶胞如图1所示,Cu可以完全取代该晶体中a位置Fe或b位置Fe,
的晶胞如图1所示,Cu可以完全取代该晶体中a位置Fe或b位置Fe,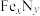 转化为两种Cu替代型产物的能量变化如图2所示。
转化为两种Cu替代型产物的能量变化如图2所示。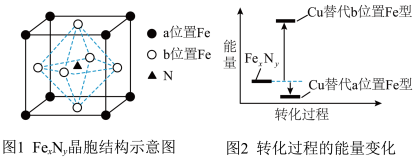
②下列关于晶体的说法正确的是
A.晶体的形成与晶体的自范性有关
B.测定某一固体是否属于晶体可以用X-射线衍射仪进行实验
C.晶体和非晶体的根本区别在于固体是否有规则的几何外形
D.由玻璃制成规则的玻璃球体现了晶体的自范性
E.晶胞是晶体结构中最小的重复单元
您最近一年使用:0次
名校
解题方法
4 . 半导体光催化可以将太阳能直接转化为化学能,在解决能源危机方面具有广阔的发展前景。GaN材料属于新兴的第三代半导体,其晶体存在六方纤锌矿型(图1)和立方闪锌矿型(图2)两种不同的晶体结构,下列说法错误的是( )

A.两种晶体结构中, 原子的配位数均为4 原子的配位数均为4 |
B.在图1中,设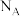 为阿伏加德罗常数的数值,则晶胞密度为 为阿伏加德罗常数的数值,则晶胞密度为 |
C.在图2中,若①号原子坐标为 ,则②号原子坐标为 ,则②号原子坐标为 |
D.在图2中,相邻的两个 原子之间距离为 原子之间距离为 |
您最近一年使用:0次
5 . 金属合金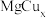 的结构可看作以
的结构可看作以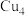 四面体(相互共用顶点)替换立方金刚石结构中的碳原子,形成三维骨架,在晶胞空隙处,有序地放置
四面体(相互共用顶点)替换立方金刚石结构中的碳原子,形成三维骨架,在晶胞空隙处,有序地放置 原子(四面体的4个顶点代表
原子(四面体的4个顶点代表 原子,圆球代表
原子,圆球代表 原子),结构如图所示.下列说法错误的是
原子),结构如图所示.下列说法错误的是
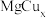 的结构可看作以
的结构可看作以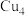 四面体(相互共用顶点)替换立方金刚石结构中的碳原子,形成三维骨架,在晶胞空隙处,有序地放置
四面体(相互共用顶点)替换立方金刚石结构中的碳原子,形成三维骨架,在晶胞空隙处,有序地放置 原子(四面体的4个顶点代表
原子(四面体的4个顶点代表 原子,圆球代表
原子,圆球代表 原子),结构如图所示.下列说法错误的是
原子),结构如图所示.下列说法错误的是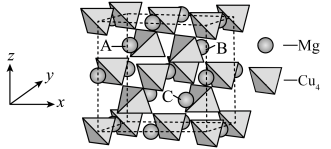
A. |
| B.该晶体在高温时导电能力变弱 |
C.晶胞参数为 ,则 ,则 原子之间的距离为 原子之间的距离为 |
D.若A的原子坐标为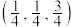 ,则C的原子坐标为 ,则C的原子坐标为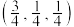 |
您最近一年使用:0次
名校
解题方法
6 . 超高硬度生物材料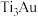 合金是理想的人工髋关节和膝关节材料,其晶体有
合金是理想的人工髋关节和膝关节材料,其晶体有 (图甲)、
(图甲)、 (图乙)两种结构,如下图所示。下列说法错误的是
(图乙)两种结构,如下图所示。下列说法错误的是
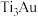 合金是理想的人工髋关节和膝关节材料,其晶体有
合金是理想的人工髋关节和膝关节材料,其晶体有 (图甲)、
(图甲)、 (图乙)两种结构,如下图所示。下列说法错误的是
(图乙)两种结构,如下图所示。下列说法错误的是
| A.图甲中,Ti原子距离最近且等距的Ti原子有8个 |
| B.图乙中,Ti原子位于Au原子构成的四面体空隙中 |
C.图乙中,若M的坐标为 ,则N的坐标为 ,则N的坐标为 |
D.图乙中,晶胞边长为dpm,晶体的密度为 |
您最近一年使用:0次
解题方法
7 . 氮族元素与镓能形成氮化镓、砷化镓等材料,广泛应用于雷达等行业中。回答下列问题:
(1)基态氮原子的价层电子排布图为______ 。基态N原子核外电子的运动状态有_____ 种。
(2) 、
、 、
、 的沸点由高到低的顺序为
的沸点由高到低的顺序为_______ (填化学式,下同),还原性由强到弱的顺序为______ 。
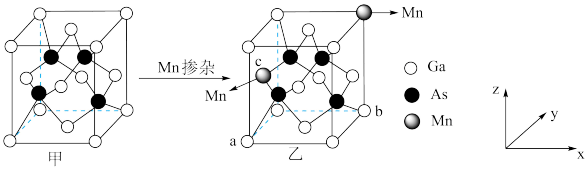
(3) 的晶胞结构如图甲所示,将Mn掺杂到
的晶胞结构如图甲所示,将Mn掺杂到 的晶体中得到稀磁性半导体材料,其结构如图乙所示。a、b点的原子分数坐标分别为
的晶体中得到稀磁性半导体材料,其结构如图乙所示。a、b点的原子分数坐标分别为 和
和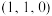 。
。______ 。
②晶体乙中Mn、Ga、As的原子个数比为_______ (填最简整数比)。
③若 晶胞参数为1nm,则Ga和As之间的最短距离为
晶胞参数为1nm,则Ga和As之间的最短距离为____ 。
(4)Li、Fe、As可组成一种新型材料,其立方晶胞结构和z轴方向投影图如图所示。该物质的化学式为____ ;若晶胞参数为 , A、B处的两个As原子之间的距离为
, A、B处的两个As原子之间的距离为____ nm。 ,则晶体的密度为
,则晶体的密度为_____  (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(1)基态氮原子的价层电子排布图为
(2)
 、
、 、
、 的沸点由高到低的顺序为
的沸点由高到低的顺序为(3)
 的晶胞结构如图甲所示,将Mn掺杂到
的晶胞结构如图甲所示,将Mn掺杂到 的晶体中得到稀磁性半导体材料,其结构如图乙所示。a、b点的原子分数坐标分别为
的晶体中得到稀磁性半导体材料,其结构如图乙所示。a、b点的原子分数坐标分别为 和
和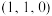 。
。
②晶体乙中Mn、Ga、As的原子个数比为
③若
 晶胞参数为1nm,则Ga和As之间的最短距离为
晶胞参数为1nm,则Ga和As之间的最短距离为(4)Li、Fe、As可组成一种新型材料,其立方晶胞结构和z轴方向投影图如图所示。该物质的化学式为
 , A、B处的两个As原子之间的距离为
, A、B处的两个As原子之间的距离为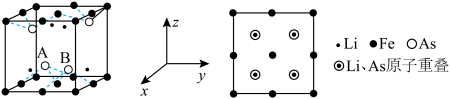
 ,则晶体的密度为
,则晶体的密度为 (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。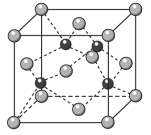
您最近一年使用:0次
名校
8 . 全固态氟离子电池中的固态电解质晶胞如图。电池工作时, 发生迁移。晶胞参数越大,可供离子迁移的空间越大,越有利于离子传输。F位点空缺也可使离子传输更加高效。下列说法
发生迁移。晶胞参数越大,可供离子迁移的空间越大,越有利于离子传输。F位点空缺也可使离子传输更加高效。下列说法不正确 的是
 发生迁移。晶胞参数越大,可供离子迁移的空间越大,越有利于离子传输。F位点空缺也可使离子传输更加高效。下列说法
发生迁移。晶胞参数越大,可供离子迁移的空间越大,越有利于离子传输。F位点空缺也可使离子传输更加高效。下列说法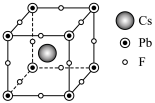
| A.晶体中与Cs距离最近且相等的F有12个 |
B.该固态电解质的化学式为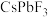 |
| C.在Pb位点掺杂K,F位点将出现空缺 |
| D.随Pb位点掺杂K含量的增大,离子传输效率一定提高 |
您最近一年使用:0次
2024-05-12更新
|
481次组卷
|
3卷引用:2024届福建省部分地市高三下学期三模化学试题
名校
解题方法
9 . 回答下列问题:
(1)氮和铁能形成一种磁性材料,其晶胞如图所示,该晶胞中Fe原子的个数为___________ ,该该磁性材料的化学式为___________ 。___________ 个氯离子,阴离子与阳离子的个数比是___________ 。___________ 。 )的沸点为65℃,甲醛HCHO(
)的沸点为65℃,甲醛HCHO( )沸点为-19℃。两者的相对分子质量接近,但甲醇的沸点比甲醛高,主要原因是
)沸点为-19℃。两者的相对分子质量接近,但甲醇的沸点比甲醛高,主要原因是___________ 。
(5)NH3、CH4、HF、H2O分子中,价键的极性由强到弱的顺序是___________ 。
(6)F、Cl、Br、I、At等简称卤素,(CN)2称为“拟卤素”,在性质上与卤素相似,(CN)2里各原子均满足8电子稳定结构。写出(CN)2的电子式___________ 。
(1)氮和铁能形成一种磁性材料,其晶胞如图所示,该晶胞中Fe原子的个数为



 )的沸点为65℃,甲醛HCHO(
)的沸点为65℃,甲醛HCHO( )沸点为-19℃。两者的相对分子质量接近,但甲醇的沸点比甲醛高,主要原因是
)沸点为-19℃。两者的相对分子质量接近,但甲醇的沸点比甲醛高,主要原因是(5)NH3、CH4、HF、H2O分子中,价键的极性由强到弱的顺序是
(6)F、Cl、Br、I、At等简称卤素,(CN)2称为“拟卤素”,在性质上与卤素相似,(CN)2里各原子均满足8电子稳定结构。写出(CN)2的电子式
您最近一年使用:0次
10 . CaTiO3可以制成未来量子计算机的元件。CaTiO3的晶胞结构如图。下列说法正确的是
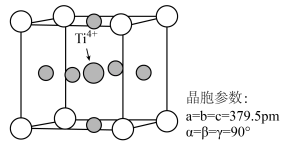
| A.晶胞中O2-占据面心、Ca2+占据顶点 |
B.晶胞中O2-之间最近距离为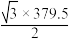 pm pm |
| C.每个Ca2+周围距离最近的Ti4+有6个 |
D.晶体密度为 g∙cm-3 g∙cm-3 |
您最近一年使用:0次



