名校
解题方法
1 . 自然界中,纯粹的典型晶体是不多的,大多数晶体是分子晶体、共价晶体、金属晶体和离子晶体之间的过渡晶体。以下列出了第三周期几种氧化物晶体中离子键的百分数。
提示:离子键的百分数是通过电负性的差值计算出来的,电负性的差值越大,离子键的百分数越大。
(1)从原子结构角度解释,为什么一般认为氧化镁属于离子晶体,而二氧化硅属于共价晶体:___________ 。
(2)硅元素位于元素周期表的___________ 区。基态硅原子的价层电子排布式为___________ 。
(3)一种硼镁化合物具有超导性能,晶体结构属于六方晶系,其晶体结构、晶胞沿c轴的投影图如下所示,已知该晶体中晶胞各边长度分别为apm、apm和cpm,两条底边夹角为120°,距离最近的两个B原子之间距离为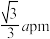 。
。
①该物质化学式为___________ ;
②距离每个B原子最近的Mg原子有___________ 个;
③该晶体密度为___________  。
。 含量。
含量。
(ⅰ)称取m克硅酸钠样品加热溶解后,配置为250mL待测液。
(ⅱ)移取50mL待测液至250mL锥形瓶中,加入10滴甲基红指示剂【HIn(红色) (黄色)】,摇匀后用0.2000mol/L HCl标准溶液滴定至体系为玫瑰红色,消耗盐酸体积为
(黄色)】,摇匀后用0.2000mol/L HCl标准溶液滴定至体系为玫瑰红色,消耗盐酸体积为 ,体系中有沉淀。
,体系中有沉淀。
(ⅲ)加入3.0g氟化钠固体,充分反应。
(ⅳ)用0.5000mol/L HCl标准溶液滴定至溶液为玫瑰红色并继续加入至过量,共加入 。
。
(ⅴ)用0.5000mol/L NaOH标准溶液滴定至溶液变为亮黄色,消耗NaOH溶液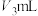 。
。
已知: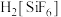 为强电解质,回答问题:
为强电解质,回答问题:
①步骤(ⅲ)中加入NaF后发生化学反应的离子方程式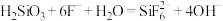 ,则加入NaF后的实验现象为
,则加入NaF后的实验现象为___________ 。
②样品中硅酸钠的纯度为___________ (用质量分数表示)。
| 氧化物 |  | MgO |  |  |
| 离子键百分数 | 62 | 50 | 41 | 33 |
(1)从原子结构角度解释,为什么一般认为氧化镁属于离子晶体,而二氧化硅属于共价晶体:
(2)硅元素位于元素周期表的
(3)一种硼镁化合物具有超导性能,晶体结构属于六方晶系,其晶体结构、晶胞沿c轴的投影图如下所示,已知该晶体中晶胞各边长度分别为apm、apm和cpm,两条底边夹角为120°,距离最近的两个B原子之间距离为
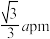 。
。①该物质化学式为
②距离每个B原子最近的Mg原子有
③该晶体密度为
 。
。
 含量。
含量。(ⅰ)称取m克硅酸钠样品加热溶解后,配置为250mL待测液。
(ⅱ)移取50mL待测液至250mL锥形瓶中,加入10滴甲基红指示剂【HIn(红色)
 (黄色)】,摇匀后用0.2000mol/L HCl标准溶液滴定至体系为玫瑰红色,消耗盐酸体积为
(黄色)】,摇匀后用0.2000mol/L HCl标准溶液滴定至体系为玫瑰红色,消耗盐酸体积为 ,体系中有沉淀。
,体系中有沉淀。(ⅲ)加入3.0g氟化钠固体,充分反应。
(ⅳ)用0.5000mol/L HCl标准溶液滴定至溶液为玫瑰红色并继续加入至过量,共加入
 。
。(ⅴ)用0.5000mol/L NaOH标准溶液滴定至溶液变为亮黄色,消耗NaOH溶液
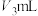 。
。已知:
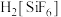 为强电解质,回答问题:
为强电解质,回答问题:①步骤(ⅲ)中加入NaF后发生化学反应的离子方程式
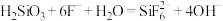 ,则加入NaF后的实验现象为
,则加入NaF后的实验现象为②样品中硅酸钠的纯度为
您最近一年使用:0次
名校
2 . 硫化物含硫量的测定、脱硫是极具价值的重要课题。
(1)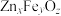 是一种复合脱硫剂,可用于脱除煤气中的
是一种复合脱硫剂,可用于脱除煤气中的 。
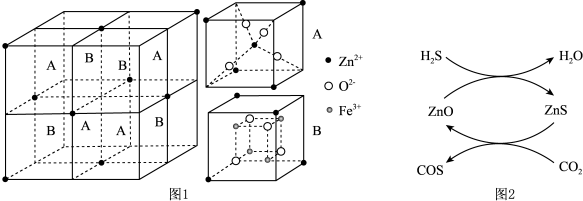
。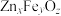 晶胞结构如图1所示(A、B交替排列,且A、B分别为晶胞的
晶胞结构如图1所示(A、B交替排列,且A、B分别为晶胞的 的结构),其化学式为
的结构),其化学式为__________ 。
②一定温度下将一定比例 和
和 的混合气体以一定流速通过装有上述脱硫剂的反应器,一段时间后,出口处检测到
的混合气体以一定流速通过装有上述脱硫剂的反应器,一段时间后,出口处检测到 。研究表明
。研究表明 参与了
参与了 与
与 生成
生成 的反应,反应机理如图2所示,反应前后
的反应,反应机理如图2所示,反应前后 的质量不变,该反应过程可描述为
的质量不变,该反应过程可描述为__________ 。
(2)稀土硫化物中硫含量的测定对其生产和质量控制具有重要意义。用如下方法对稀土硫化物中具有代表性的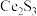 (
( 基态原子核外电子排布式为
基态原子核外电子排布式为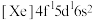 )样品硫含量进行测定。实验检测原理为
)样品硫含量进行测定。实验检测原理为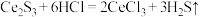
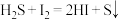

步骤1:称取0.1600g样品于反应瓶中,再准确滴加20.00mL 碘溶液;
碘溶液;
步骤2:缓慢滴加稍过量的稀盐酸(边滴加边摇动反应瓶),盖上瓶塞,剧烈摇动2min;
步骤3:滴入
 溶液至恰好完全反应,消耗
溶液至恰好完全反应,消耗 溶液20.00mL。
溶液20.00mL。
① 元素最高正化合价为
元素最高正化合价为__________ 。
②步骤1中不能使用稀硝酸的原因是__________ 。
③该样品中硫的质量分数为__________ (写出计算过程)。
(1)
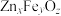 是一种复合脱硫剂,可用于脱除煤气中的
是一种复合脱硫剂,可用于脱除煤气中的 。
。 
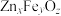 晶胞结构如图1所示(A、B交替排列,且A、B分别为晶胞的
晶胞结构如图1所示(A、B交替排列,且A、B分别为晶胞的 的结构),其化学式为
的结构),其化学式为②一定温度下将一定比例
 和
和 的混合气体以一定流速通过装有上述脱硫剂的反应器,一段时间后,出口处检测到
的混合气体以一定流速通过装有上述脱硫剂的反应器,一段时间后,出口处检测到 。研究表明
。研究表明 参与了
参与了 与
与 生成
生成 的反应,反应机理如图2所示,反应前后
的反应,反应机理如图2所示,反应前后 的质量不变,该反应过程可描述为
的质量不变,该反应过程可描述为(2)稀土硫化物中硫含量的测定对其生产和质量控制具有重要意义。用如下方法对稀土硫化物中具有代表性的
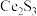 (
( 基态原子核外电子排布式为
基态原子核外电子排布式为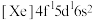 )样品硫含量进行测定。实验检测原理为
)样品硫含量进行测定。实验检测原理为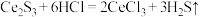
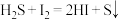

步骤1:称取0.1600g样品于反应瓶中,再准确滴加20.00mL
 碘溶液;
碘溶液;步骤2:缓慢滴加稍过量的稀盐酸(边滴加边摇动反应瓶),盖上瓶塞,剧烈摇动2min;
步骤3:滴入

 溶液至恰好完全反应,消耗
溶液至恰好完全反应,消耗 溶液20.00mL。
溶液20.00mL。①
 元素最高正化合价为
元素最高正化合价为②步骤1中不能使用稀硝酸的原因是
③该样品中硫的质量分数为
您最近一年使用:0次
3 . 白云石的主要成分为 ,还含有少量的
,还含有少量的 和
和 。利用白云石制备碳酸钙和氧化镁,其主要流程的示意图如下。
。利用白云石制备碳酸钙和氧化镁,其主要流程的示意图如下。
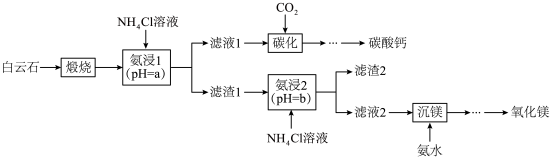
已知: 。
。
(1)组成 的四种元素,电负性由大到小的顺序是
的四种元素,电负性由大到小的顺序是___________ 。
(2)“氨浸1”在室温下进行,写出氯化铵浸取氧化钙总反应的离子方程式___________ 。
(3)两次“氨浸”的pH比较;a___________ b(填“>”“=”或“<”)。
(4)“碳化”时,测得碳酸钙的产率及碳酸钙中镁元素的含量随溶液pH的变化如图所示。
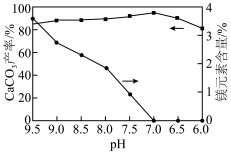

___________ 时,碳化效果最佳。低于该pH,碳酸钙的产率下降,其原因用离子方程式表示:___________ 。
(5)“沉镁”发生反应: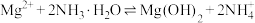 ,其平衡常数
,其平衡常数
___________ (用含氢氧化的 和
和 的
的 的代数式表示)。
的代数式表示)。
(6)制备过程除了充分利用 ,还可以循环利用的1种物质是
,还可以循环利用的1种物质是___________ (填化学式)。
(7)称取 试样置于烧杯中,加蒸馏水数滴润湿,盖一表面皿,滴加盐酸至固体完全溶解,定容在
试样置于烧杯中,加蒸馏水数滴润湿,盖一表面皿,滴加盐酸至固体完全溶解,定容在 的容量瓶内,用移液管吸取
的容量瓶内,用移液管吸取 待测液于锥形瓶中,加入相关试剂,摇匀后用
待测液于锥形瓶中,加入相关试剂,摇匀后用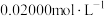 EDTA溶液滴定至终点(
EDTA溶液滴定至终点( 与EDTA以等物质的量比反应)。进行平行实验,测得平均消耗EDTA溶液
与EDTA以等物质的量比反应)。进行平行实验,测得平均消耗EDTA溶液 。产品中碳酸钙质量分数为
。产品中碳酸钙质量分数为___________ (列出计算式)。
(8)碳酸钙的某种晶胞结构如下图所示。

①每个晶胞中含有___________ 个“ ”单元。
”单元。
②每个阴离子团的配位数(紧邻的阳离子数)为___________ 。
 ,还含有少量的
,还含有少量的 和
和 。利用白云石制备碳酸钙和氧化镁,其主要流程的示意图如下。
。利用白云石制备碳酸钙和氧化镁,其主要流程的示意图如下。
已知:
 。
。(1)组成
 的四种元素,电负性由大到小的顺序是
的四种元素,电负性由大到小的顺序是(2)“氨浸1”在室温下进行,写出氯化铵浸取氧化钙总反应的离子方程式
(3)两次“氨浸”的pH比较;a
(4)“碳化”时,测得碳酸钙的产率及碳酸钙中镁元素的含量随溶液pH的变化如图所示。


(5)“沉镁”发生反应:
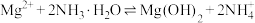 ,其平衡常数
,其平衡常数
 和
和 的
的 的代数式表示)。
的代数式表示)。(6)制备过程除了充分利用
 ,还可以循环利用的1种物质是
,还可以循环利用的1种物质是(7)称取
 试样置于烧杯中,加蒸馏水数滴润湿,盖一表面皿,滴加盐酸至固体完全溶解,定容在
试样置于烧杯中,加蒸馏水数滴润湿,盖一表面皿,滴加盐酸至固体完全溶解,定容在 的容量瓶内,用移液管吸取
的容量瓶内,用移液管吸取 待测液于锥形瓶中,加入相关试剂,摇匀后用
待测液于锥形瓶中,加入相关试剂,摇匀后用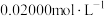 EDTA溶液滴定至终点(
EDTA溶液滴定至终点( 与EDTA以等物质的量比反应)。进行平行实验,测得平均消耗EDTA溶液
与EDTA以等物质的量比反应)。进行平行实验,测得平均消耗EDTA溶液 。产品中碳酸钙质量分数为
。产品中碳酸钙质量分数为(8)碳酸钙的某种晶胞结构如下图所示。

①每个晶胞中含有
 ”单元。
”单元。②每个阴离子团的配位数(紧邻的阳离子数)为
您最近一年使用:0次
名校
解题方法
4 . “天问一号”着陆火星,“嫦娥五号”采回月壤,探索宇宙奥秘离不开化学。镍铼合金是制造喷气发动机的燃烧室、涡轮叶片及排气喷嘴的重要材料。元素铼( )的熔点仅次于钨,是稀有金属之一,地壳中铼的含量极低,多伴生于铜、锌、铅等矿物中。工业上,常从冶炼铜的富铼渣(含
)的熔点仅次于钨,是稀有金属之一,地壳中铼的含量极低,多伴生于铜、锌、铅等矿物中。工业上,常从冶炼铜的富铼渣(含 )中提取铼,其工艺流程如图所示:
)中提取铼,其工艺流程如图所示:
(1)矿样粒度与浸出率关系如下图所示,则“浸出”时应将富铼渣粉碎至___________目(填字母)。
(2)已知“浸出”时反应中 转化为两种强酸,写出富铼渣“浸出”时发生反应的离子方程式:
转化为两种强酸,写出富铼渣“浸出”时发生反应的离子方程式:__________________ 。
(3)实验室中,操作Ⅲ所用装置应选用___________(填字母)。
(4)“一系列操作”包括①________ (填操作名称,下同)、冷却结晶、过滤、洗涤和②____________ ;从下列仪器中选出①②中需使用的仪器,依次为______ (填字母)。___________ 法提纯;“热还原”反应中氧化剂与还原剂的物质的量之比为___________ 。
(6)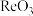 晶胞结构如下图所示,其中氧原子配位数为
晶胞结构如下图所示,其中氧原子配位数为___________ ,铼原子填在了氧原子围成的___________ (填“四面体”“立方体”或“八面体”)空隙中。
 )的熔点仅次于钨,是稀有金属之一,地壳中铼的含量极低,多伴生于铜、锌、铅等矿物中。工业上,常从冶炼铜的富铼渣(含
)的熔点仅次于钨,是稀有金属之一,地壳中铼的含量极低,多伴生于铜、锌、铅等矿物中。工业上,常从冶炼铜的富铼渣(含 )中提取铼,其工艺流程如图所示:
)中提取铼,其工艺流程如图所示: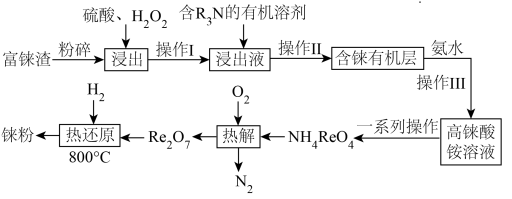
(1)矿样粒度与浸出率关系如下图所示,则“浸出”时应将富铼渣粉碎至___________目(填字母)。
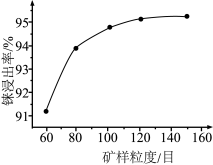
| A.60 | B.80 | C.100 | D.120 |
(2)已知“浸出”时反应中
 转化为两种强酸,写出富铼渣“浸出”时发生反应的离子方程式:
转化为两种强酸,写出富铼渣“浸出”时发生反应的离子方程式:(3)实验室中,操作Ⅲ所用装置应选用___________(填字母)。
A.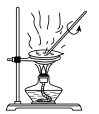 | B.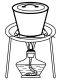 | C.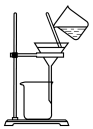 | D.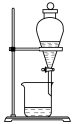 |
(4)“一系列操作”包括①
A.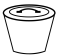 B.
B.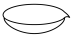 C.
C. D.
D.
(6)
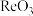 晶胞结构如下图所示,其中氧原子配位数为
晶胞结构如下图所示,其中氧原子配位数为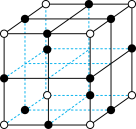
您最近一年使用:0次
2024-03-26更新
|
170次组卷
|
2卷引用:2024届黑龙江省绥化市高三下学期3月联考模拟检测化学试卷
名校
5 . 苯酚化学式为C6H5OH,是具有特殊气味的无色针状晶体,有毒,是生产某些树脂、杀菌剂、防腐剂以及药物(如阿司匹林)的重要原料,苯酚遇三氯化铁溶液显紫色。
(1)苯酚的降解
方法1:已知: 具有强氧化性,Fe2+浓度较高时会导致
具有强氧化性,Fe2+浓度较高时会导致 猝灭。
猝灭。 可将苯酚氧化为CO2,但反应速率较慢。加入Fe2+可加快反应,过程为:
可将苯酚氧化为CO2,但反应速率较慢。加入Fe2+可加快反应,过程为:
ⅰ.
ⅱ. 将苯酚氧化
将苯酚氧化
① 氧化苯酚的离子方程式是
氧化苯酚的离子方程式是________ 。
②将电解得到的含 溶液稀释后加入苯酚处理器,调节溶液总体积为1L,pH=1,测得在相同时间内,不同条件下苯酚的降解率如图。
溶液稀释后加入苯酚处理器,调节溶液总体积为1L,pH=1,测得在相同时间内,不同条件下苯酚的降解率如图。________ 。
方法2:H2O2在Fe3O4催化剂表面产生 除去废水中的苯酚的原理如图所示。
除去废水中的苯酚的原理如图所示。
③在不同初始pH条件下,研究苯酚的去除率随时间的变化,结果表明:在反应开始时,初始pH=6的溶液中苯酚的去除率明显低于初始pH=3的溶液,但一段时间后两者接近,原因是________ 。
已知:电解中转移1mol电子所消耗的电量为F库仑。
取处理后的水样100mL,酸化后加入KBr溶液,通电。电解产生的Br2全部与苯酚反应,当苯酚完全反应时,消耗的电量为a库仑,则样品中苯酚的含量为________ g/L。(写出计算过程)
(3)铁化合物的结构
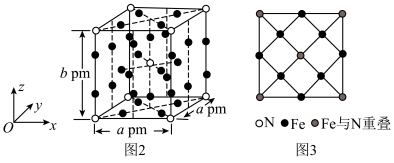
磁性氮化铁的晶胞结构如图2所示,沿z轴方向的投影如图3所示,则该化合物的化学式为________ 。
(1)苯酚的降解
方法1:已知:
 具有强氧化性,Fe2+浓度较高时会导致
具有强氧化性,Fe2+浓度较高时会导致 猝灭。
猝灭。 可将苯酚氧化为CO2,但反应速率较慢。加入Fe2+可加快反应,过程为:
可将苯酚氧化为CO2,但反应速率较慢。加入Fe2+可加快反应,过程为:ⅰ.

ⅱ.
 将苯酚氧化
将苯酚氧化①
 氧化苯酚的离子方程式是
氧化苯酚的离子方程式是②将电解得到的含
 溶液稀释后加入苯酚处理器,调节溶液总体积为1L,pH=1,测得在相同时间内,不同条件下苯酚的降解率如图。
溶液稀释后加入苯酚处理器,调节溶液总体积为1L,pH=1,测得在相同时间内,不同条件下苯酚的降解率如图。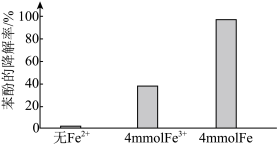
方法2:H2O2在Fe3O4催化剂表面产生
 除去废水中的苯酚的原理如图所示。
除去废水中的苯酚的原理如图所示。③在不同初始pH条件下,研究苯酚的去除率随时间的变化,结果表明:在反应开始时,初始pH=6的溶液中苯酚的去除率明显低于初始pH=3的溶液,但一段时间后两者接近,原因是

已知:电解中转移1mol电子所消耗的电量为F库仑。
取处理后的水样100mL,酸化后加入KBr溶液,通电。电解产生的Br2全部与苯酚反应,当苯酚完全反应时,消耗的电量为a库仑,则样品中苯酚的含量为
(3)铁化合物的结构
磁性氮化铁的晶胞结构如图2所示,沿z轴方向的投影如图3所示,则该化合物的化学式为
您最近一年使用:0次
2024-04-29更新
|
409次组卷
|
2卷引用:江苏省东台市安丰中学等六校2024届高三下学期4月联考模拟化学试题
6 . 铜锈中含有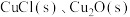 和
和 。有人提出腐蚀途径如下:
。有人提出腐蚀途径如下:
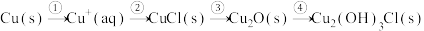
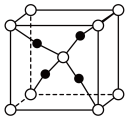
(1)上图所示晶体结构表示铜锈中___________ 物质(填写化学式)。
(2)过程①是典型的电化学腐蚀,其负极反应为___________
(3)过程③、④涉及的反应方程式包括:
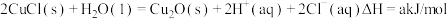
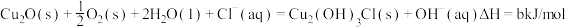
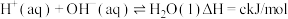
则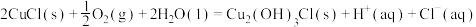 的
的
_______  。
。
(4)环境越潮湿、氧气含量越___________ 、气温越___________ ,铜的腐蚀越严重。
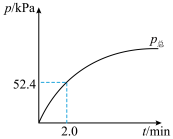
(5)铜锈还含有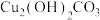 ,其分解方程式为:
,其分解方程式为: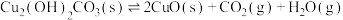 。该反应的
。该反应的 随温度的变化关系如图所示,
随温度的变化关系如图所示,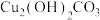 分解的最低温度为
分解的最低温度为___________ K,当温度从 升高到
升高到 时,平衡向
时,平衡向___________ 移动,判定理由是___________ 。

(6)某温度下,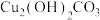 在恒容密闭容器中的分解达平衡时,容器内压强为
在恒容密闭容器中的分解达平衡时,容器内压强为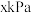 ,则反应平衡常数
,则反应平衡常数
_______ 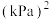 。
。
(7)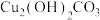 分解过程中总压强随时间的变化关系如图所示,则在
分解过程中总压强随时间的变化关系如图所示,则在 内,
内, 的平均生成速率
的平均生成速率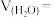
_______ 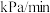 。
。
 和
和 。有人提出腐蚀途径如下:
。有人提出腐蚀途径如下: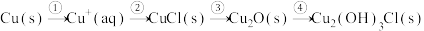

(1)上图所示晶体结构表示铜锈中
(2)过程①是典型的电化学腐蚀,其负极反应为
(3)过程③、④涉及的反应方程式包括:
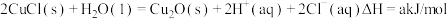
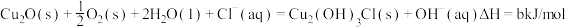
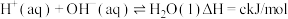
则
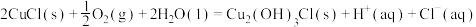 的
的
 。
。(4)环境越潮湿、氧气含量越
(5)铜锈还含有
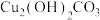 ,其分解方程式为:
,其分解方程式为: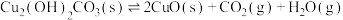 。该反应的
。该反应的 随温度的变化关系如图所示,
随温度的变化关系如图所示,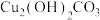 分解的最低温度为
分解的最低温度为 升高到
升高到 时,平衡向
时,平衡向
(6)某温度下,
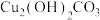 在恒容密闭容器中的分解达平衡时,容器内压强为
在恒容密闭容器中的分解达平衡时,容器内压强为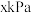 ,则反应平衡常数
,则反应平衡常数
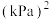 。
。(7)
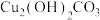 分解过程中总压强随时间的变化关系如图所示,则在
分解过程中总压强随时间的变化关系如图所示,则在 内,
内, 的平均生成速率
的平均生成速率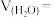
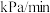 。
。
您最近一年使用:0次



