1 . 四氯化锡在有机合成、染料工业中有广泛的应用,其极易水解,熔点为 、沸点为
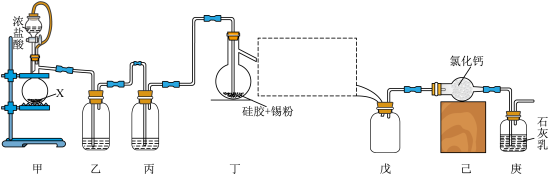
、沸点为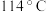 。某同学查阅资料后设计了如图所示的装置(部分夹持装置及装置丁处热源省略)制备
。某同学查阅资料后设计了如图所示的装置(部分夹持装置及装置丁处热源省略)制备 。
。
(1)试剂 是
是______ (填化学式);装置丙的作用是______ ;方框中仪器的名称是______ 。
(2)当______ (填现象)时,点燃装置丁处的酒精灯。
(3)写出装置庚中反应的化学方程式:______ 。
(4)制得的产品中含少量 ,利用如下方法测定其纯度:取
,利用如下方法测定其纯度:取 产品于锥形瓶中,加入稀盐酸溶解,用
产品于锥形瓶中,加入稀盐酸溶解,用 碘酸钾标准溶液滴定至终点,消耗标准溶液的体积为
碘酸钾标准溶液滴定至终点,消耗标准溶液的体积为 ,反应原理为
,反应原理为 ,
,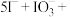
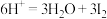 ,
, 。
。
①实验中必须使用______ (填“酸”或“碱”)式滴定管;若滴定时未用标准液润洗滴定管,则测得 的纯度
的纯度______ (填“偏高”或“偏低”)。
②滴定时应选用的指示剂为______ ; 的纯度为
的纯度为______ 。
 、沸点为
、沸点为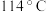 。某同学查阅资料后设计了如图所示的装置(部分夹持装置及装置丁处热源省略)制备
。某同学查阅资料后设计了如图所示的装置(部分夹持装置及装置丁处热源省略)制备 。
。
(1)试剂
 是
是(2)当
(3)写出装置庚中反应的化学方程式:
(4)制得的产品中含少量
 ,利用如下方法测定其纯度:取
,利用如下方法测定其纯度:取 产品于锥形瓶中,加入稀盐酸溶解,用
产品于锥形瓶中,加入稀盐酸溶解,用 碘酸钾标准溶液滴定至终点,消耗标准溶液的体积为
碘酸钾标准溶液滴定至终点,消耗标准溶液的体积为 ,反应原理为
,反应原理为 ,
,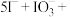
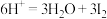 ,
, 。
。①实验中必须使用
 的纯度
的纯度②滴定时应选用的指示剂为
 的纯度为
的纯度为
您最近一年使用:0次
2 . 某实验小组进行酯化反应的改进,创新性地利用草酸(乙二酸)的自催化而不需外加浓硫酸即可实现草酸和1—丁醇合成草酸二丁酯。主要实验步骤如下: 三颈烧瓶中依次加入
三颈烧瓶中依次加入 草酸、
草酸、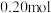 1—丁醇和
1—丁醇和 环己烷、三颗沸石。在三颈烧瓶中间瓶口连接分水器及仪器A,搭建如图甲所示的装置(部分装置已省略)。
环己烷、三颗沸石。在三颈烧瓶中间瓶口连接分水器及仪器A,搭建如图甲所示的装置(部分装置已省略)。
②回流反应:加热,升温至溶液沸腾并回流,将温度稳定在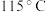 ,待分水器全部被水充满后继续回流
,待分水器全部被水充满后继续回流 ,即可停止反应。
,即可停止反应。
③后处理:移去热源,待温度降至 左右时,将反应液缓慢转移至烧杯中,边搅拌边加入溶液B直至无气泡产生,水洗,将上层油状液体转移至锥形瓶中,加入无水硫酸镁,
左右时,将反应液缓慢转移至烧杯中,边搅拌边加入溶液B直至无气泡产生,水洗,将上层油状液体转移至锥形瓶中,加入无水硫酸镁, 后,用短颈漏斗快速滤入
后,用短颈漏斗快速滤入 圆底烧瓶中进行蒸馏,获得纯净的草酸二丁酯,并称重收集产物
圆底烧瓶中进行蒸馏,获得纯净的草酸二丁酯,并称重收集产物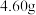 。
。
请回答下列问题:
(1)仪器 的名称为
的名称为_______ 。
(2)写出该合成反应的化学方程式:_______ 。
(3)后处理环节中,溶液B为_______ ,加入无水硫酸镁的作用是_______ 。
(4)该实验制得的草酸二丁酯的产率为_______ (保留3位有效数字)。
(5)该实验小组分别深入探究反应温度、带水剂(环己烷)用量对草酸二丁酯产率的影响。实验设计与结果如下。
Ⅰ.温度:在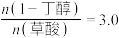 、反应时间为
、反应时间为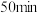 条件下,反应温度对酯产率的影响如图乙所示。
条件下,反应温度对酯产率的影响如图乙所示。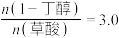 、反应时间为
、反应时间为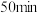 、反应温度在
、反应温度在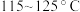 内,带水剂(环己烷)用量对酯产率的影响如图丙所示。
内,带水剂(环己烷)用量对酯产率的影响如图丙所示。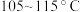 内,酯产率随温度升高而升高的主要原因是
内,酯产率随温度升高而升高的主要原因是_______ 。
②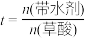 ,当
,当 在
在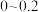 内,酯产率随着带水剂(环己烷)用量的增加而增加的原因是
内,酯产率随着带水剂(环己烷)用量的增加而增加的原因是_______ 。
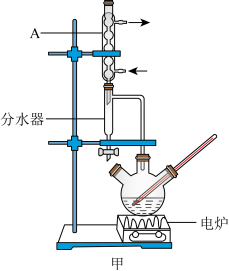
 三颈烧瓶中依次加入
三颈烧瓶中依次加入 草酸、
草酸、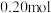 1—丁醇和
1—丁醇和 环己烷、三颗沸石。在三颈烧瓶中间瓶口连接分水器及仪器A,搭建如图甲所示的装置(部分装置已省略)。
环己烷、三颗沸石。在三颈烧瓶中间瓶口连接分水器及仪器A,搭建如图甲所示的装置(部分装置已省略)。②回流反应:加热,升温至溶液沸腾并回流,将温度稳定在
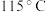 ,待分水器全部被水充满后继续回流
,待分水器全部被水充满后继续回流 ,即可停止反应。
,即可停止反应。③后处理:移去热源,待温度降至
 左右时,将反应液缓慢转移至烧杯中,边搅拌边加入溶液B直至无气泡产生,水洗,将上层油状液体转移至锥形瓶中,加入无水硫酸镁,
左右时,将反应液缓慢转移至烧杯中,边搅拌边加入溶液B直至无气泡产生,水洗,将上层油状液体转移至锥形瓶中,加入无水硫酸镁, 后,用短颈漏斗快速滤入
后,用短颈漏斗快速滤入 圆底烧瓶中进行蒸馏,获得纯净的草酸二丁酯,并称重收集产物
圆底烧瓶中进行蒸馏,获得纯净的草酸二丁酯,并称重收集产物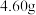 。
。请回答下列问题:
(1)仪器
 的名称为
的名称为(2)写出该合成反应的化学方程式:
(3)后处理环节中,溶液B为
(4)该实验制得的草酸二丁酯的产率为
(5)该实验小组分别深入探究反应温度、带水剂(环己烷)用量对草酸二丁酯产率的影响。实验设计与结果如下。
Ⅰ.温度:在
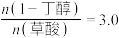 、反应时间为
、反应时间为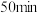 条件下,反应温度对酯产率的影响如图乙所示。
条件下,反应温度对酯产率的影响如图乙所示。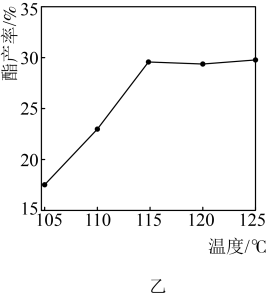
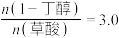 、反应时间为
、反应时间为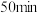 、反应温度在
、反应温度在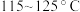 内,带水剂(环己烷)用量对酯产率的影响如图丙所示。
内,带水剂(环己烷)用量对酯产率的影响如图丙所示。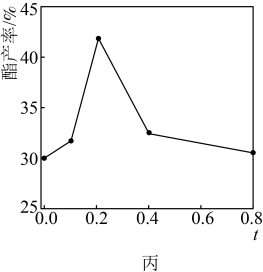
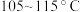 内,酯产率随温度升高而升高的主要原因是
内,酯产率随温度升高而升高的主要原因是②
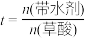 ,当
,当 在
在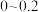 内,酯产率随着带水剂(环己烷)用量的增加而增加的原因是
内,酯产率随着带水剂(环己烷)用量的增加而增加的原因是
您最近一年使用:0次
3 . 某试样含有 、
、 及㤢性物质。称取试样
及㤢性物质。称取试样 ,溶解后配制到
,溶解后配制到 容量瓶中。吸取
容量瓶中。吸取 ,在
,在 介质中用
介质中用 将
将 还原为
还原为 ,除去过量的
,除去过量的 后调至中性测定
后调至中性测定 ,消耗
,消耗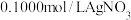 溶液
溶液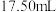 。另吸取
。另吸取 试液用
试液用 酸化后加热除去
酸化后加热除去 ,再调至中性,滴定过剩
,再调至中性,滴定过剩 时消耗了上述
时消耗了上述 溶液
溶液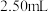 。计算试样中
。计算试样中 、
、 的质量分数
的质量分数_______ 、_______ 。
 、
、 及㤢性物质。称取试样
及㤢性物质。称取试样 ,溶解后配制到
,溶解后配制到 容量瓶中。吸取
容量瓶中。吸取 ,在
,在 介质中用
介质中用 将
将 还原为
还原为 ,除去过量的
,除去过量的 后调至中性测定
后调至中性测定 ,消耗
,消耗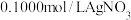 溶液
溶液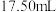 。另吸取
。另吸取 试液用
试液用 酸化后加热除去
酸化后加热除去 ,再调至中性,滴定过剩
,再调至中性,滴定过剩 时消耗了上述
时消耗了上述 溶液
溶液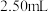 。计算试样中
。计算试样中 、
、 的质量分数
的质量分数
您最近一年使用:0次
4 . 对下列实验现象或操作解释正确的是
| 选项 | 现象或操作 | 解释 |
| A | 淀粉-KI溶液中滴入氯水变蓝,再通入 ,蓝色褪去 ,蓝色褪去 |  具有漂白性 具有漂白性 |
| B | 配制 溶液时,先将 溶液时,先将 溶于适量盐酸,再用蒸馏水稀释,最后在试剂瓶中加入少量的锡粒 溶于适量盐酸,再用蒸馏水稀释,最后在试剂瓶中加入少量的锡粒 | 抑制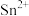 水解,并防止 水解,并防止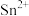 被氧化为 被氧化为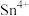 |
| C | 某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成 | 该溶液中含有 |
| D | 向钾盐固体中滴加浓盐酸,将产生的气体通入品红溶液,品红溶液褪色 | 钾盐为亚硫酸钾 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-05-12更新
|
293次组卷
|
2卷引用:2024届河南省九师联盟2023-2024学年高三下学期4月联考理综试题-高中化学
5 . 间苯三酚可用于合成重要的有机合成中间体3,5-二甲氧基苯酚,反应如图:
下列说法不正确的是

| 物质 | 沸点/ | 熔点/ | 溶解性 |
| 甲醇 | 64.7 | 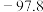 | 易溶于水 |
| 3,5-二甲氧基苯酚 | 172~175 | 33~36 | 易溶于甲醇、乙醚,微溶于水 |
| A.该反应属于取代反应 |
| B.分离出甲醇的操作是蒸馏 |
C.洗涤时,可用饱和 溶液除去有机层中的氯化氢 溶液除去有机层中的氯化氢 |
D.间苯三酚与3,5-二甲氧基苯酚均可与 溶液发生显色反应 溶液发生显色反应 |
您最近一年使用:0次
2024-05-08更新
|
172次组卷
|
2卷引用:北京一零一中学2023-2024学年高二下学期期中考试化学试题
6 . 废弃电脑的CPU中含有贵重金属Cu、Ag、Au,可回收利用,部分流程如下:

(1)铜元素在周期表中位于______ ,基态铜原子的核外电子排布式为______ 。
(2)电脑CPU在使用时会涂抹一层散热硅脂(一种液体橡胶,主要成分为聚二甲基硅氧烷和聚甲基硅氧烷),可用______洗去;
(3)用Zn粉还原 的化学反应方程式为
的化学反应方程式为______ ;
(4)试剂1为______ (填名称,下同),试剂2为______ ;
(5)加入过其铁粉的原因是______ ;
(6)滤渣2溶于试剂2的原因是______ ;(用离子反应方程式表示)
(7)金属铜的晶胞结构如图所示,铜原子之间的最小距离为apm,则铜晶胞的密度为______  (
( 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。

(1)铜元素在周期表中位于
(2)电脑CPU在使用时会涂抹一层散热硅脂(一种液体橡胶,主要成分为聚二甲基硅氧烷和聚甲基硅氧烷),可用______洗去;
| A.NaOH溶液 | B.纯碱溶液 | C.稀硫酸 | D.酒精 |
(3)用Zn粉还原
 的化学反应方程式为
的化学反应方程式为(4)试剂1为
(5)加入过其铁粉的原因是
(6)滤渣2溶于试剂2的原因是
(7)金属铜的晶胞结构如图所示,铜原子之间的最小距离为apm,则铜晶胞的密度为
 (
( 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。
您最近一年使用:0次
2024高三·全国·专题练习
解题方法
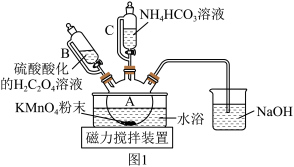
7 . 碳酸锰(MnCO3)是制造高性能磁性材料的主要原料。实验室以KMnO4为原料制备少量MnCO3并研究其性质,制备MnCO3的装置如图1所示。已知: MnCO3难溶于水、乙醇,100 ℃开始分解,在潮湿环境下易被氧化。
(1)选用仪器B、C的目的是___________ 。
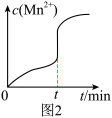
(2)在烧瓶中加入一定量的KMnO4固体,滴加硫酸酸化的H2C2O4溶液,其反应的离子方程式为___________ 。 反应过程中c(Mn2+)随时间的变化曲线如图2所示,则t min时,c(Mn2+)迅速增大的原因是___________ 。___________ 。
(4)实验结束后,将装置A中的混合物过滤,用乙醇洗涤滤渣,再___________ ,即得到干燥的MnCO3固体。用乙醇洗涤的优点是___________ 。
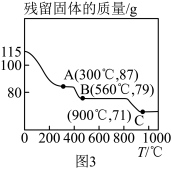
(5)在空气中加热MnCO3固体,随着温度的升高,残留固体的质量变化如图3所示。则A点的成分为___________ (填化学式);B→C反应的化学方程式为___________ 。
(1)选用仪器B、C的目的是
(2)在烧瓶中加入一定量的KMnO4固体,滴加硫酸酸化的H2C2O4溶液,其反应的离子方程式为
(4)实验结束后,将装置A中的混合物过滤,用乙醇洗涤滤渣,再
(5)在空气中加热MnCO3固体,随着温度的升高,残留固体的质量变化如图3所示。则A点的成分为
您最近一年使用:0次
2024高三·全国·专题练习
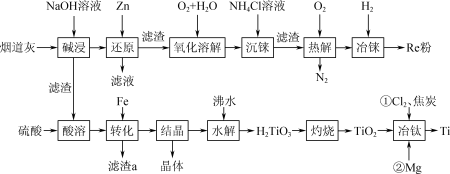
8 . 稀有金属元素铼(Re)和锰同族,铼和钛是航天工程不可缺少的材料。某烟道灰的主要成分为Re2O7、TiO2、SiO2、CuO、 Fe2O3,从中提取铼粉和钛的流程如图所示: 被Zn还原为+4价的铼。ZnO为两性氧化物,溶于碱生成ZnO
被Zn还原为+4价的铼。ZnO为两性氧化物,溶于碱生成ZnO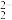 。
。
回答下列问题:
(1)“碱浸”过程Re2O7、SiO2分别发生反应的离子方程式为___________ 、___________ 。
(2)“氧化溶解”过程中Re(OH)4转化为ReO ,该反应中还原剂与氧化剂的物质的量之比为
,该反应中还原剂与氧化剂的物质的量之比为___________ 。
(3)“酸溶”过程得到的钛在溶液中以TiO2+形式存在,其“水解”反应的离子方程式为___________ 。
(4)“转化”过程中加入Fe的作用是___________ ;所得晶体主要成分的化学式中含有7个结晶水,其化学式是___________ 。
(5)“冶钛”过程中将TiO2先转化为TiCl4,再用Mg进行还原,写出高温条件下用Mg还原TiCl4的化学方程式:___________ 。
 被Zn还原为+4价的铼。ZnO为两性氧化物,溶于碱生成ZnO
被Zn还原为+4价的铼。ZnO为两性氧化物,溶于碱生成ZnO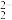 。
。回答下列问题:
(1)“碱浸”过程Re2O7、SiO2分别发生反应的离子方程式为
(2)“氧化溶解”过程中Re(OH)4转化为ReO
 ,该反应中还原剂与氧化剂的物质的量之比为
,该反应中还原剂与氧化剂的物质的量之比为(3)“酸溶”过程得到的钛在溶液中以TiO2+形式存在,其“水解”反应的离子方程式为
(4)“转化”过程中加入Fe的作用是
(5)“冶钛”过程中将TiO2先转化为TiCl4,再用Mg进行还原,写出高温条件下用Mg还原TiCl4的化学方程式:
您最近一年使用:0次
2024高三·全国·专题练习
9 . 下列实验装置及操作正确的是

| A.图甲:实验室里制取少量的Fe(OH)3胶体 |
| B.图乙:配置一定物质的量浓度的H2SO4溶液 |
| C.图丙:检测待测液中是否含有K+ |
| D.图丁:比较硫、碳、硅三种元素的非金属性强弱 |
您最近一年使用:0次
2024高三·全国·专题练习
解题方法
10 . 通过下列实验操作和实验现象,得到的结论正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 用pH试纸测溶液pH | NaHCO3显蓝色,NaHSO3显红色 | H2CO3、H2SO3均是弱酸 |
| B | 向钾盐溶液中滴加浓盐酸 | 产生的无色气体使品红溶液褪色 | 该钾盐一定是K2SO3或KHSO3 |
| C | 向含有等量KBr、KI混合溶液中依次加入少量新制氯水和CCl4,振荡、静置 | 溶液分层,下层呈紫红色 | 氧化性:Cl2>Br2>I2 |
| D | 在火焰上灼烧搅拌过某无色溶液的玻璃棒 | 火焰出现黄色 | 不能确定溶液中含有Na元素 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



