四氯化锡在有机合成、染料工业中有广泛的应用,其极易水解,熔点为 、沸点为
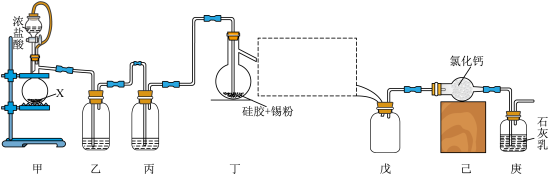
、沸点为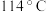 。某同学查阅资料后设计了如图所示的装置(部分夹持装置及装置丁处热源省略)制备
。某同学查阅资料后设计了如图所示的装置(部分夹持装置及装置丁处热源省略)制备 。
。
(1)试剂 是
是______ (填化学式);装置丙的作用是______ ;方框中仪器的名称是______ 。
(2)当______ (填现象)时,点燃装置丁处的酒精灯。
(3)写出装置庚中反应的化学方程式:______ 。
(4)制得的产品中含少量 ,利用如下方法测定其纯度:取
,利用如下方法测定其纯度:取 产品于锥形瓶中,加入稀盐酸溶解,用
产品于锥形瓶中,加入稀盐酸溶解,用 碘酸钾标准溶液滴定至终点,消耗标准溶液的体积为
碘酸钾标准溶液滴定至终点,消耗标准溶液的体积为 ,反应原理为
,反应原理为 ,
,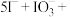
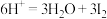 ,
, 。
。
①实验中必须使用______ (填“酸”或“碱”)式滴定管;若滴定时未用标准液润洗滴定管,则测得 的纯度
的纯度______ (填“偏高”或“偏低”)。
②滴定时应选用的指示剂为______ ; 的纯度为
的纯度为______ 。
 、沸点为
、沸点为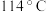 。某同学查阅资料后设计了如图所示的装置(部分夹持装置及装置丁处热源省略)制备
。某同学查阅资料后设计了如图所示的装置(部分夹持装置及装置丁处热源省略)制备 。
。
(1)试剂
 是
是(2)当
(3)写出装置庚中反应的化学方程式:
(4)制得的产品中含少量
 ,利用如下方法测定其纯度:取
,利用如下方法测定其纯度:取 产品于锥形瓶中,加入稀盐酸溶解,用
产品于锥形瓶中,加入稀盐酸溶解,用 碘酸钾标准溶液滴定至终点,消耗标准溶液的体积为
碘酸钾标准溶液滴定至终点,消耗标准溶液的体积为 ,反应原理为
,反应原理为 ,
,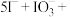
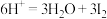 ,
, 。
。①实验中必须使用
 的纯度
的纯度②滴定时应选用的指示剂为
 的纯度为
的纯度为
更新时间:2024-05-26 08:04:41
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】如图是实验室制备氯气并进行一系列相关实验的装置。请回答下列问题:

(1)仪器a的名称是_______ 。
(2)按图组装好装置后,首先应进行的操作是_______ 。
(3)实验开始后,Ⅰ、Ⅱ处的有色布条褪色的是_______ 处(填“Ⅰ”或“Ⅱ”)
(4)装置A的烧瓶中发生反应的化学方程式_______ 。
(5)D中发生反应的离子方程式为_______ 。
(6)装置B中长颈漏斗的作用是_______ 。
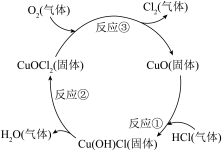
(7)近年来,随着化学工业快速发展,氯气的需求迅速增加。如图是某制备氯气的原理示意图。CuO的作用是_______ ,总反应方程式为_______ 。

(1)仪器a的名称是
(2)按图组装好装置后,首先应进行的操作是
(3)实验开始后,Ⅰ、Ⅱ处的有色布条褪色的是
(4)装置A的烧瓶中发生反应的化学方程式
(5)D中发生反应的离子方程式为
(6)装置B中长颈漏斗的作用是
(7)近年来,随着化学工业快速发展,氯气的需求迅速增加。如图是某制备氯气的原理示意图。CuO的作用是

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】碘化钠在医疗及食品方面有重要的作用,实验室以 、单质碘和水合肼
、单质碘和水合肼 (有还原性)为原料制备碘化钠。回答下列有关问题:
(有还原性)为原料制备碘化钠。回答下列有关问题:
(1)利用下列实验装置制取次氯酸钠和氢氧化钠混合液。
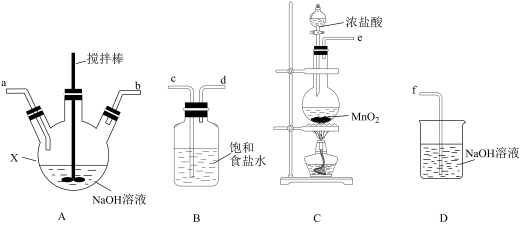
①仪器X的名称是_______ ,导管口连接顺序为________ (按气流方向,用小写字母表示)。
②写出A中反应的化学方程式___________ 。
(2)制备水合肼:
反应原理为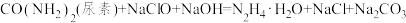 。
。
①将次氯酸钠和氢氧化钠混合液缓慢滴加到尿素溶液中,边加边搅拌。该操作需严格控制试剂的滴加顺序和滴加速度,原因是________ 。
② 一级电离方程式为
一级电离方程式为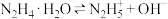 ,其二级电离方程式为
,其二级电离方程式为______ 。
(3)碘化钠的制备:采用水合肼还原法制取碘化钠固体,其制备流程如图所示。

①“还原”过程主要消耗“合成”中生成的副产物 ,反应的离子方程式是
,反应的离子方程式是________ 。
②工业上也可用硫化钠或铁屑还原碘酸钠制备碘化钠,“水合肼还原法”的优点是________ 。
 、单质碘和水合肼
、单质碘和水合肼 (有还原性)为原料制备碘化钠。回答下列有关问题:
(有还原性)为原料制备碘化钠。回答下列有关问题:(1)利用下列实验装置制取次氯酸钠和氢氧化钠混合液。

①仪器X的名称是
②写出A中反应的化学方程式
(2)制备水合肼:
反应原理为
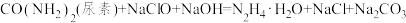 。
。①将次氯酸钠和氢氧化钠混合液缓慢滴加到尿素溶液中,边加边搅拌。该操作需严格控制试剂的滴加顺序和滴加速度,原因是
②
 一级电离方程式为
一级电离方程式为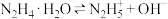 ,其二级电离方程式为
,其二级电离方程式为(3)碘化钠的制备:采用水合肼还原法制取碘化钠固体,其制备流程如图所示。

①“还原”过程主要消耗“合成”中生成的副产物
 ,反应的离子方程式是
,反应的离子方程式是②工业上也可用硫化钠或铁屑还原碘酸钠制备碘化钠,“水合肼还原法”的优点是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某化学兴趣小组设计了如图装置,该装置能制取Cl2,并进行相关性质实验。(提示:氯气几乎不溶于饱和食盐水,氧化性:Cl2>I2)。

回答下列问题:
(1)仪器a的名称为___________ 。
(2)关闭活塞K后,装置G可以储存多余的Cl2,对装置的基本要求是___________ ,储气瓶b内盛放的试剂是___________ 。
(3)A中发生反应的离子方程式为___________ 。
(4)实验开始时,先打开分液漏斗旋塞和活塞K,点燃A处酒精灯,让氯气充满整个装置,然后再点燃E处酒精灯。
①在装置E的硬质玻璃管内盛有炭粉,发生氧化还原反应,产物为CO2和HC,则E中发生反应的化学方程式为___________ 。
②装置F中球形干燥管的作用是___________ 。
③先点燃A处酒精灯,让氯气充满整个装置,然后再点燃E处酒精灯的目的是_______ 。
(5)淀粉溶液遇I2变蓝,故C中颜色最终变为___________ 。

回答下列问题:
(1)仪器a的名称为
(2)关闭活塞K后,装置G可以储存多余的Cl2,对装置的基本要求是
(3)A中发生反应的离子方程式为
(4)实验开始时,先打开分液漏斗旋塞和活塞K,点燃A处酒精灯,让氯气充满整个装置,然后再点燃E处酒精灯。
①在装置E的硬质玻璃管内盛有炭粉,发生氧化还原反应,产物为CO2和HC,则E中发生反应的化学方程式为
②装置F中球形干燥管的作用是
③先点燃A处酒精灯,让氯气充满整个装置,然后再点燃E处酒精灯的目的是
(5)淀粉溶液遇I2变蓝,故C中颜色最终变为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用如图装置(部分装置省略)制备 和
和 ,探究其氧化还原性质。
,探究其氧化还原性质。

回答下列问题:
(1)盛放 粉末的仪器名称是
粉末的仪器名称是_______ ,a中的试剂为_______ 。
(2)b中采用的加热方式是_______ ,d的作用是_______ ,d可选用试剂_______ (填标号)。
A. B.
B. C.
C. D.
D.
(3)图中制取标准状况下22.4L 时,被氧化的盐酸为
时,被氧化的盐酸为_______  ,c中化学反应的离子方程式是
,c中化学反应的离子方程式是_______ 。
(4)实验室还可以用 和浓盐酸反应来制取氯气,当消耗15.8g
和浓盐酸反应来制取氯气,当消耗15.8g 时,标准状况下产生的氯气的体积是
时,标准状况下产生的氯气的体积是_______ L。
 和
和 ,探究其氧化还原性质。
,探究其氧化还原性质。
回答下列问题:
(1)盛放
 粉末的仪器名称是
粉末的仪器名称是(2)b中采用的加热方式是
A.
 B.
B. C.
C. D.
D.
(3)图中制取标准状况下22.4L
 时,被氧化的盐酸为
时,被氧化的盐酸为 ,c中化学反应的离子方程式是
,c中化学反应的离子方程式是(4)实验室还可以用
 和浓盐酸反应来制取氯气,当消耗15.8g
和浓盐酸反应来制取氯气,当消耗15.8g 时,标准状况下产生的氯气的体积是
时,标准状况下产生的氯气的体积是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备KClO3和NaClO,并探究其氧化还原性质。
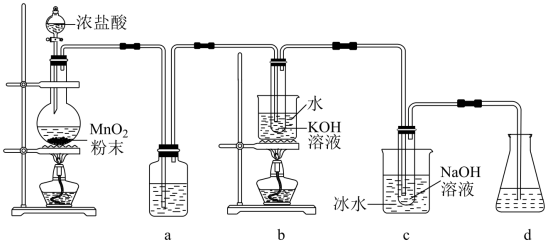
回答下列问题:
(1)盛放MnO2粉末的仪器名称是_______ ,a中的试剂为_______ 。
(2)b中反应的化学方程式为_______ 。
(3)c中反应的离子方程式是_______ ,采用冰水浴冷却的目的是_______ 。
(4)d中可选用试剂_______ (填标号)。

回答下列问题:
(1)盛放MnO2粉末的仪器名称是
(2)b中反应的化学方程式为
(3)c中反应的离子方程式是
(4)d中可选用试剂_______ (填标号)。
| A.Na2S溶液 | B.NaCl 溶液 | C.NaOH溶液 | D.H2SO4溶液 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】铋酸钠(NaBiO3)是分析化学中的重要试剂,在水中缓慢分解,遇沸水或酸则迅速分解。某兴趣小组设计实验制取铋酸钠并探究其应用。回答下列问题:
Ⅰ.制取铋酸钠
制取装置如图(加热和夹持仪器已略去),部分物质性质如表:

(1)B装置用于除去HCl,盛放的试剂是____ 。
(2)C中盛放Bi(OH)3与NaOH混合物,与Cl2反应生成NaBiO3,反应的离子方程式为____ 。
(3)当观察到____ (填现象)时,可以初步判断C中反应已经完成。
(4)拆除装置前必须先除去烧瓶中残留Cl2以免污染空气。除去Cl2的操作是____ 。
(5)反应结束后,为从装置C中获得尽可能多的产品,需要的操作有____ 。
Ⅱ.铋酸钠的应用——检验Mn2+
(6)往待测液中加入铋酸钠晶体,加硫酸酸化,溶液变为紫红色,证明待测液中存在Mn2+。但某同学在较浓的MnSO4溶液中加入铋酸钠晶体,加硫酸酸化,结果没有紫红色出现,但观察到黑色固体(MnO2)生成。产生此现象的离子反应方程式为____ 。
Ⅲ.产品纯度的测定
(7)取上述NaBiO3产品wg,加入足量稀硫酸和MnSO4稀溶液使其完全反应,再用cmol·L-1的H2C2O4标准溶液滴定生成的MnO (已知:H2C2O4+MnO
(已知:H2C2O4+MnO ——CO2+Mn2++H2O,未配平),当溶液紫红色恰好褪去时,消耗vmL标准溶液。该产品的纯度为
——CO2+Mn2++H2O,未配平),当溶液紫红色恰好褪去时,消耗vmL标准溶液。该产品的纯度为____ (用含w、c、v的代数式表示)。
Ⅰ.制取铋酸钠
制取装置如图(加热和夹持仪器已略去),部分物质性质如表:

| 物质 | NaBiO3 | Bi(OH)3 |
| 性质 | 不溶于冷水,浅黄色 | 难溶于水;白色 |
(2)C中盛放Bi(OH)3与NaOH混合物,与Cl2反应生成NaBiO3,反应的离子方程式为
(3)当观察到
(4)拆除装置前必须先除去烧瓶中残留Cl2以免污染空气。除去Cl2的操作是
(5)反应结束后,为从装置C中获得尽可能多的产品,需要的操作有
Ⅱ.铋酸钠的应用——检验Mn2+
(6)往待测液中加入铋酸钠晶体,加硫酸酸化,溶液变为紫红色,证明待测液中存在Mn2+。但某同学在较浓的MnSO4溶液中加入铋酸钠晶体,加硫酸酸化,结果没有紫红色出现,但观察到黑色固体(MnO2)生成。产生此现象的离子反应方程式为
Ⅲ.产品纯度的测定
(7)取上述NaBiO3产品wg,加入足量稀硫酸和MnSO4稀溶液使其完全反应,再用cmol·L-1的H2C2O4标准溶液滴定生成的MnO
 (已知:H2C2O4+MnO
(已知:H2C2O4+MnO ——CO2+Mn2++H2O,未配平),当溶液紫红色恰好褪去时,消耗vmL标准溶液。该产品的纯度为
——CO2+Mn2++H2O,未配平),当溶液紫红色恰好褪去时,消耗vmL标准溶液。该产品的纯度为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】以废镍(含NiO,杂质为少量Fe2O3)生产Ni2O3的一种工艺流程如下:
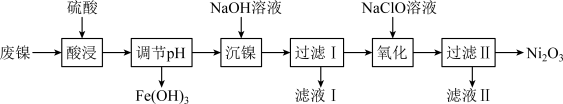
(1)“调节pH”后检验溶液中不再存在Fe3+的方法是______ 。
(2)“沉镍”的目的是将溶液中的Ni2+转化为Ni(OH)2沉淀,确认Ni2+已经完全沉淀的实验方法是______ 。
(3)“滤液Ⅱ”所含阴离子主要为Cl-,写出“氧化”时反应的离子方程式:______ 。
(4)若“氧化”反应不充分,所制Ni2O3样品中会混有Ni(OH)2。为测定样品中Ni2O3的质量分数,进行实验:称取5.000 g样品,加入足量硫酸后再加入100 mL 1.0 mol·L-1的Fe2+标准溶液,充分反应,加水定容至200 mL。取出20.00 mL,用0.040 mol·L-1 KMnO4标准溶液滴定,用去KMnO4标准溶液20.00 mL,试通过计算确定Ni2O3的质量分数。测定过程中涉及反应如下:Ni2O3+Fe2++H+=Ni2++Fe3++H2O(未配平);Fe2++MnO4-+H+=Fe3++Mn2++H2O(未配平)______

(1)“调节pH”后检验溶液中不再存在Fe3+的方法是
(2)“沉镍”的目的是将溶液中的Ni2+转化为Ni(OH)2沉淀,确认Ni2+已经完全沉淀的实验方法是
(3)“滤液Ⅱ”所含阴离子主要为Cl-,写出“氧化”时反应的离子方程式:
(4)若“氧化”反应不充分,所制Ni2O3样品中会混有Ni(OH)2。为测定样品中Ni2O3的质量分数,进行实验:称取5.000 g样品,加入足量硫酸后再加入100 mL 1.0 mol·L-1的Fe2+标准溶液,充分反应,加水定容至200 mL。取出20.00 mL,用0.040 mol·L-1 KMnO4标准溶液滴定,用去KMnO4标准溶液20.00 mL,试通过计算确定Ni2O3的质量分数。测定过程中涉及反应如下:Ni2O3+Fe2++H+=Ni2++Fe3++H2O(未配平);Fe2++MnO4-+H+=Fe3++Mn2++H2O(未配平)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】H2C2O4·2H2O是一种无色晶体,在实验室常用作络合剂、掩蔽剂、沉淀剂、还原剂以及用于校准高锰酸钾标准溶液等。
回答下列问题:
(1)实验室需配制0.1 mol·L-1的H2C2O4溶液250 mL。若用H2C2O4·2H2O配制,需用托盘天平称量H2C2O4·2H2O质量为_______ g;若用H2C2O4溶液稀释配制,需量取2 mol·L-1的H2C2O4溶液的体积为_________ mL。
(2)用H2C2O4·2H2O配制时,涉及称量、溶解、溶液转移、定容等操作。
①下列图示对应的操作规范的是___________ (填字母,下同)。
A.称量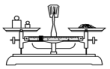 B.溶解
B.溶解 C.转移溶液
C.转移溶液 D.定容
D.定容 
②下列操作会导致配得的溶液浓度偏高的是___________ 。
A.所用的H2C2O4·2H2O晶体中含有少量无水的H2C2O4
B.溶解时,洗涤烧杯及玻璃棒的溶液未转移到容量瓶中
C.定容时,视线如图所示:
D.摇匀后发现液面低于刻度线,用胶头滴管滴加水到刻度线处
(3)利用反应5H2C2O4+3H2SO4+2KMnO4=K2SO4+2MnSO4+8H2O+10CO2↑可校准KMnO4标准溶液。精确称取0.7875 g H2C2O4·2H2O,加入适量稀硫酸,然后向其中滴入KMnO4溶液,消耗KMnO4溶液50.00 mL,则KMnO4溶液的物质的量浓度为___________ 。
回答下列问题:
(1)实验室需配制0.1 mol·L-1的H2C2O4溶液250 mL。若用H2C2O4·2H2O配制,需用托盘天平称量H2C2O4·2H2O质量为
(2)用H2C2O4·2H2O配制时,涉及称量、溶解、溶液转移、定容等操作。
①下列图示对应的操作规范的是
A.称量
 B.溶解
B.溶解 C.转移溶液
C.转移溶液 D.定容
D.定容 
②下列操作会导致配得的溶液浓度偏高的是
A.所用的H2C2O4·2H2O晶体中含有少量无水的H2C2O4
B.溶解时,洗涤烧杯及玻璃棒的溶液未转移到容量瓶中
C.定容时,视线如图所示:

D.摇匀后发现液面低于刻度线,用胶头滴管滴加水到刻度线处
(3)利用反应5H2C2O4+3H2SO4+2KMnO4=K2SO4+2MnSO4+8H2O+10CO2↑可校准KMnO4标准溶液。精确称取0.7875 g H2C2O4·2H2O,加入适量稀硫酸,然后向其中滴入KMnO4溶液,消耗KMnO4溶液50.00 mL,则KMnO4溶液的物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】研究人员从处理废旧线路板后的固体残渣(含SnO2、PbO2等)中进一步回收金属锡(Sn),一种回收流程如下。
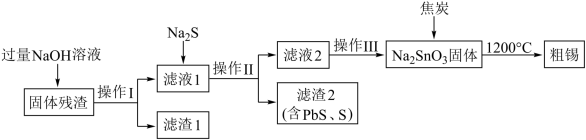
已知:i.50Sn、82Pb为IVA族元素; ii.SnO2、PbO2与强碱反应生成盐和水。
(1)SnO2与NaOH反应的化学方程式为____________ 。
(2)滤液1中加入Na2S的目的是除铅,将相关方程式补充完整:____________
Na2PbO3+ Na2S+
Na2S+ = PbS↓+S↓+_____
= PbS↓+S↓+_____
(3)不同溶剂中Na2SnO3的溶解度随温度变化如图。
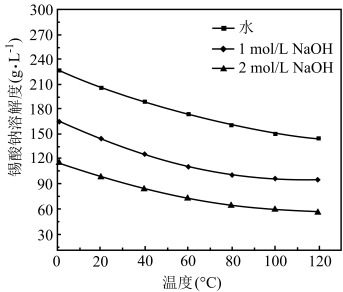
① 相同温度下,Na2SnO3的溶解度随NaOH浓度增大而减小,结合平衡移动原理解释原因:__________________ 。
② 操作III的具体方法为__________________________ 。
(4)测定粗锡中Sn的纯度:在强酸性环境中将a g粗锡样品溶解(此时Sn全部转化成Sn2+),迅速加入过量NH4Fe (SO4)2溶液,以二苯胺磺酸钠为指示剂,用c mol·L−1 K2Cr2O7标准溶液滴定至终点。平行测定三次,消耗K2Cr2O7溶液的体积平均为v mL,计算Sn的纯度。(Sn的摩尔质量为119 g·mol-1)
已知:Sn2+ + 2Fe3+ = Sn4+ + 2Fe2+
Cr2O + 6Fe2++14H+ =2Cr3+ + 6Fe3+ + 7H2O
+ 6Fe2++14H+ =2Cr3+ + 6Fe3+ + 7H2O
①溶解粗锡时不宜选用浓盐酸,理由是__________ 。
②粗锡样品中Sn的纯度为_________ (用质量分数表示)。

已知:i.50Sn、82Pb为IVA族元素; ii.SnO2、PbO2与强碱反应生成盐和水。
(1)SnO2与NaOH反应的化学方程式为
(2)滤液1中加入Na2S的目的是除铅,将相关方程式补充完整:
Na2PbO3+
 Na2S+
Na2S+ = PbS↓+S↓+_____
= PbS↓+S↓+_____
(3)不同溶剂中Na2SnO3的溶解度随温度变化如图。

① 相同温度下,Na2SnO3的溶解度随NaOH浓度增大而减小,结合平衡移动原理解释原因:
② 操作III的具体方法为
(4)测定粗锡中Sn的纯度:在强酸性环境中将a g粗锡样品溶解(此时Sn全部转化成Sn2+),迅速加入过量NH4Fe (SO4)2溶液,以二苯胺磺酸钠为指示剂,用c mol·L−1 K2Cr2O7标准溶液滴定至终点。平行测定三次,消耗K2Cr2O7溶液的体积平均为v mL,计算Sn的纯度。(Sn的摩尔质量为119 g·mol-1)
已知:Sn2+ + 2Fe3+ = Sn4+ + 2Fe2+
Cr2O
 + 6Fe2++14H+ =2Cr3+ + 6Fe3+ + 7H2O
+ 6Fe2++14H+ =2Cr3+ + 6Fe3+ + 7H2O①溶解粗锡时不宜选用浓盐酸,理由是
②粗锡样品中Sn的纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】学习小组在实验室中利用如图所示装置制备SO2并进行相关性质的探究。回答下列问题:
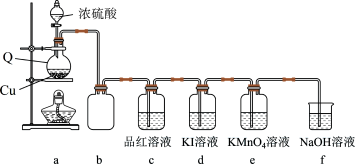
(1)仪器Q的名称为______ ;装置c中品红溶液褪色,可证明SO2具有______ 性,装置b的作用是______ 。
(2)向分液漏斗中滴加浓硫酸之前,需先通入一段时间N2,此操作的目的是______ 。
(3)装置a中反应的化学方程式为_____ 。
(4)探究:探究SO2在KI溶液体系中的反应产物
实验开始后,发现装置d中的溶液迅速变黄,继续通入SO2,装置d中出现乳黄色浑浊。该小组同学查阅资料得知,存在反应:SO2+4I-+4H+=S↓+2I2+2H2O。但有同学提出上述反应生成的I2可与SO2发生反应:SO2+I2+2H2O=SO +2I-+4H+。为进一步探究体系中的产物,完成下列实验方案。
+2I-+4H+。为进一步探究体系中的产物,完成下列实验方案。
①取适量装置d中浊液,向其中滴加几滴______ 溶液(填试剂名称),振荡,无明显变化,浊液中无I2。
②将装置d中浊液进行分离,得淡黄色固体和澄清溶液;取适量分离后的澄清溶液于试管中,______ ,出现白色沉淀,产物溶液中存在SO 。综上可知,SO2在KI溶液中发生了反应。
。综上可知,SO2在KI溶液中发生了反应。

(1)仪器Q的名称为
(2)向分液漏斗中滴加浓硫酸之前,需先通入一段时间N2,此操作的目的是
(3)装置a中反应的化学方程式为
(4)探究:探究SO2在KI溶液体系中的反应产物
实验开始后,发现装置d中的溶液迅速变黄,继续通入SO2,装置d中出现乳黄色浑浊。该小组同学查阅资料得知,存在反应:SO2+4I-+4H+=S↓+2I2+2H2O。但有同学提出上述反应生成的I2可与SO2发生反应:SO2+I2+2H2O=SO
 +2I-+4H+。为进一步探究体系中的产物,完成下列实验方案。
+2I-+4H+。为进一步探究体系中的产物,完成下列实验方案。①取适量装置d中浊液,向其中滴加几滴
②将装置d中浊液进行分离,得淡黄色固体和澄清溶液;取适量分离后的澄清溶液于试管中,
 。综上可知,SO2在KI溶液中发生了反应。
。综上可知,SO2在KI溶液中发生了反应。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】以锌锰废电池中的碳包(含碳粉、Fe、Cu、Ag和MnO2等物质)为原料回收MnO2的工艺流程如下:
I.将碳包中物质烘干,用足量稀HNO3溶解金属单质,过滤,得滤渣a;
II.将滤渣a在空气中灼烧除去碳粉,得到粗MnO2;
III.向粗MnO2中加入酸性H2O2溶液,MnO2溶解生成Mn2+,有气体生成;
IV.向III所得溶液(pH约为6)中缓慢滴加0.50mol•L-1Na2CO3溶液(pH约为12),过滤,得滤渣b,其主要成分为MnCO3;
V.滤渣b经洗涤、干燥、灼烧,制得较纯的MnO2。
(1)Ι中Ag与足量稀HNO3反应生成NO的化学方程式为___________ 。
(2)已知II的灼烧过程中同时发生反应:
MnO2(s)+C(s)=MnO(s)+CO(g) △H=+24.4kJ•mol-1
MnO2(s)+CO(g)=MnO(s)+CO2(g) △H=-148.1kJ•mol-1
写出MnO2和C反应生成MnO和CO2的热化学方程式:___________ 。
(3)H2O2的电子式为_______ ,分子中含有的化学键类型为_______ 、_______ 。
(4)III中MnO2溶解的离子方程式为_______ ,溶解一定量的MnO2,H2O2的实际消耗量比理论值高,用化学方程式解释原因:______ 。
(5)IV中,若改为“向0.50mol•L-1Na2CO3溶液中缓慢滴加III所得溶液”,滤渣b中会混有较多_____ 杂质。
(6)V中MnCO3在空气中灼烧的化学方程式为_______ 。
I.将碳包中物质烘干,用足量稀HNO3溶解金属单质,过滤,得滤渣a;
II.将滤渣a在空气中灼烧除去碳粉,得到粗MnO2;
III.向粗MnO2中加入酸性H2O2溶液,MnO2溶解生成Mn2+,有气体生成;
IV.向III所得溶液(pH约为6)中缓慢滴加0.50mol•L-1Na2CO3溶液(pH约为12),过滤,得滤渣b,其主要成分为MnCO3;
V.滤渣b经洗涤、干燥、灼烧,制得较纯的MnO2。
(1)Ι中Ag与足量稀HNO3反应生成NO的化学方程式为
(2)已知II的灼烧过程中同时发生反应:
MnO2(s)+C(s)=MnO(s)+CO(g) △H=+24.4kJ•mol-1
MnO2(s)+CO(g)=MnO(s)+CO2(g) △H=-148.1kJ•mol-1
写出MnO2和C反应生成MnO和CO2的热化学方程式:
(3)H2O2的电子式为
(4)III中MnO2溶解的离子方程式为
(5)IV中,若改为“向0.50mol•L-1Na2CO3溶液中缓慢滴加III所得溶液”,滤渣b中会混有较多
(6)V中MnCO3在空气中灼烧的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】为保护环境,节约资源,某研究性学习小组探究用易拽罐制取明矾[KAl(SO4)2·12H2O]。
查阅资料得知:明矾溶于水,不溶于乙醇:易拉罐主要成分为铝,另含有镁、铁等。
实验步骤如下:
步骤1、将易拉罐剪开,裁成铝片。用砂纸磨去表面的油漆,颜料及透明塑胶内衬:
步骤2、制备NaAlO2
称量1 g上述处理过的铝片,切碎,分数次放入盛有40mL5% NaOH溶液的烧杯中:将烧杯置于热水浴中加热。反应完毕后,溶液呈灰黑色浑浊,趁热过滤。
步骤3、氢氧化铝的生成和洗涤
在所得滤液中滴加3mol·L-1H2SO4溶液,用pH试纸检验,调节pH至8~9为止:此时溶液中生成大量的白色氢氧化铝沉淀,过滤,并用热蒸馏水多次洗涤沉淀
步骤4、明矾的制备
将过滤后所得氢氧化铝沉淀转入蒸发皿中,加10 mL 9mol/L H2SO4,再加15 mL水,小火加热使其溶解,加入4g硫酸钾继续加热至溶解,将所得溶液在空气中自然冷却,待结晶完全后,过滤,用无水酒精洗涤晶体两次;将晶体用滤纸吸干,制得明矾。
回答以下问题:
(1)步骤2中铝片溶于烧碱的反应建议在通风橱中进行,用热水浴加热,避免明火,原因是______ ;过滤后,滤渣的主要成分是__________ 。
(2)步骤3中,若调节pH过低,导致的结果是____________ ;洗涤氢氧化铝沉淀的方法是________ 。
(3)步骤4中用到的主要仪器是:铁架台(带铁圈),蒸发皿、量筒、漏斗、烧杯、酒精灯和__ ;加入硫酸钾后制取明矾的化学反应方程式是_______________ 。
(4)不用水而用无水酒精洗涤明矾晶体的原因是_________________ 。
(5)实验验证明矾晶体中含有SO42—离子的方法是_____________ 。
(6)该实验制得明矾15.8 g,则称取的1 g铝片中铝元素含量不低于_______________ %。
查阅资料得知:明矾溶于水,不溶于乙醇:易拉罐主要成分为铝,另含有镁、铁等。
实验步骤如下:
步骤1、将易拉罐剪开,裁成铝片。用砂纸磨去表面的油漆,颜料及透明塑胶内衬:
步骤2、制备NaAlO2
称量1 g上述处理过的铝片,切碎,分数次放入盛有40mL5% NaOH溶液的烧杯中:将烧杯置于热水浴中加热。反应完毕后,溶液呈灰黑色浑浊,趁热过滤。
步骤3、氢氧化铝的生成和洗涤
在所得滤液中滴加3mol·L-1H2SO4溶液,用pH试纸检验,调节pH至8~9为止:此时溶液中生成大量的白色氢氧化铝沉淀,过滤,并用热蒸馏水多次洗涤沉淀
步骤4、明矾的制备
将过滤后所得氢氧化铝沉淀转入蒸发皿中,加10 mL 9mol/L H2SO4,再加15 mL水,小火加热使其溶解,加入4g硫酸钾继续加热至溶解,将所得溶液在空气中自然冷却,待结晶完全后,过滤,用无水酒精洗涤晶体两次;将晶体用滤纸吸干,制得明矾。
回答以下问题:
(1)步骤2中铝片溶于烧碱的反应建议在通风橱中进行,用热水浴加热,避免明火,原因是
(2)步骤3中,若调节pH过低,导致的结果是
(3)步骤4中用到的主要仪器是:铁架台(带铁圈),蒸发皿、量筒、漏斗、烧杯、酒精灯和
(4)不用水而用无水酒精洗涤明矾晶体的原因是
(5)实验验证明矾晶体中含有SO42—离子的方法是
(6)该实验制得明矾15.8 g,则称取的1 g铝片中铝元素含量不低于
您最近一年使用:0次



